INTRODUCCION
La mayoría de los episodios de pancreatitis aguda (80-90%) son leves, se controlan solos, y remiten espontáneamente a los 3 o 4 días. Lo normal es que estos pacientes no necesiten cuidados intensivos ni cirugía, con un tratamiento clásico en una sala normal la tasa de mortalidad es inferior al 1%1.
En pacientes con enfermedad grave, caracterizada por la presencia del fallo del órgano y/o necrosis de más del 30%2 el tratamiento de apoyo en la unidad de cuidados intensivos tiene una importancia capital. La detección temprana de aquellos pacientes que posteriormente desarrollan pancreatitis necrosante permite comenzar este tratamiento antes de que se produzca el fallo del órgano o éste se desarrolle completamente. El tratamiento clásico en la unidad de cuidados intensivos, que incluye hoy día la administración intravenosa de antibióticos, se puede considerar el patrón oro3.
El episodio de pancreatitis aguda grave en su curso natural progresa en dos fases: los primeros 14 días están caracterizados por un síndrome de respuesta inflamatoria sistémica (SRIS) que se controla con la dosificación de diversos antiinflamatorios4-7. La insuficiencia pulmonar y el síndrome de distrés respiratorio del adulto son comunes en estos pacientes, y no se pueden distinguir clínica ni histológicamente del síndrome de distrés respiratorio del adulto que se asocia con la sepsis. En la pancreatitis necrosante, el síndrome de respuesta inflamatoria sistémica se produce a menudo en ausencia de infección. Además del mal funcionamiento del órgano se producen generalmente los siguientes trastornos: hipovolemia, estado hiperdinámico, pérdida de fluido del espacio intravascular y aumento de la permeabilidad capilar. La segunda fase, que comienza unas 2 semanas después de la presentación de la enfermedad está dominada por la morbilidad relacionada con la sepsis, debido a la necrosis pancreática infectada8,9. Se asocian aquí múltiples complicaciones sistémicas, como fallo pulmonar, renal y cardiovascular. De hecho, el 80% de pacientes fallece a causa de complicaciones sépticas de otros órganos10-11.
La necesidad y el momento de una intervención quirúrgica en un paciente con pancreatitis aguda depende de varios factores, como la etiología, el curso y la gravedad de la enfermedad y la presentación de complicaciones locales. Hay que plantearse dos preguntas si se está considerando la posibilidad de la cirugía: a) ¿en qué paciente? y b) ¿cuándo se llevará a cabo?
TERAPIA QUIRURGICA EN LA PANCREATITIS NECROSANTE
Aspectos técnicos
La decisión de operar a un paciente con pancreatitis aguda grave a menudo es difícil de tomar y exige un criterio clínico maduro. El tratamiento de la pancreatitis necrosante ha evolucionado considerablemente en los últimos 30 años12. Debido a la alta incidencia de complicaciones prematuras, entre las que se encuentran la alta mortalidad y el mal resultado a largo plazo en los pacientes que sobrevivían, la resección temprana del páncreas fue abandonada13,14. Aultman et al revisaron los resultados con la pancreatitis necrosante, y durante el período de 1980 a 1989 se trató a los pacientes con múltiples operaciones de desbridación y necrosectomía; la tasa de mortalidad fue del 86%. Entonces adoptaron una estrategia que, en principio, no era quirúrgica, con lo que la tasa de mortalidad descendió al 10,5%15. En un estudio sobre 45 pacientes, Paajanen et al informaron de los resultados tras distintos protocolos de tratamiento en pacientes con pancreatitis aguda. Cuando la estrategia fue resección temprana (n = 13) la tasa de mortalidad fue del 54%. Por otro lado la práctica temprana, de la laparotomía y el lavado abdominal (n = 15) seguía estando acompañada de una mortalidad del 40% y cuando finalmente cambiaron el protocolo de tratamiento a la necrosectomía tardía (n = 17) la tasa de mortalidad descendió al 24%16. La resección del páncreas permite una completa desbridación, pero se incumple el objetivo de la conservación del tejido pancreático viable. Desde un punto de vista macromorfológico, el proceso necrosante afecta en gran medida al tejido graso que rodea al páncreas, mientras que la glándula en sí misma sólo se halla necrótica en la superficie, y el tejido pancreático que rodea el conducto sigue siendo viable. El aspecto macroscópico de la extensión de la necrosis no se corresponde bien con su histología13,17, y en consecuencia, la necrosis del páncreas suele ser sobrestimada por el cirujano. Por tanto, la resección como tratamiento de la necrosis pancreática en la inmensa mayoría de los casos supone un tratamiento excesivo y debe abandonarse. Además, la resección en la pancreatitis aguda incrementa la morbilidad tardía debida a insuficiencia endocrina y exocrina. En un estudio reciente se ha demostrado que el desarrollo de diabetes a largo plazo depende de la cantidad de parénquima pancreático extirpado: de 34 pacientes examinados 3 años después de una pancreatitis necrosante, el 47% desarrolló diabetes (todos ellos habían sufrido resección) mientras que no se produjo diabetes en aquellos que sólo habían sido tratados con necrosectomía18. La tendencia actual a reducir al mínimo las técnicas invasivas favorece el uso de técnicas percutáneas no quirúrgicas. Freeny et al avalaron la seguridad y la eficacia del drenado con catéter percutáneo para el tratamiento inicial de la necrosis pancreática con infección. Un total de 34 pacientes con necrosis pancreática fueron tratados de la sepsis con drenado con catéter percutáneo; 18 de éstos estaban críticamente enfermos con fallos multiorgánicos, y 16 (47%) de los 34 pacientes se curaron sólo con el drenado con catéter percutáneo. La sepsis fue controlada en el 74% de los pacientes, lo que permitió reservar la cirugía selectiva para el tratamiento de la fístula pancreática. En 8 pacientes no se observó una mejoría clínica tras el drenado y fue necesaria la necrosectomía. Ningún paciente sufrió complicaciones relacionadas con el catéter y la tasa de mortalidad en toda la serie fue del 12% (4/34)19. A pesar de que estos resultados son estimulantes, es probable que la oclusión recurrente del catéter debida al tejido necrótico impida la completa desbridación de este tejido. De hecho ha habido otros autores que han presentado resultados menos favorables20: Rattner et al descubrieron que si sus pacientes con necrosis pancreática eran tratados con un drenaje percutáneo guiado radiológicamente como modalidad terapéutica inicial, se producía de forma inevitable sepsis recurrente que exigía el drenaje quirúrgico21. Hoy día, el método mejor documentado es un tratamiento de conservación del órgano que combina necrosectomía con un tratamiento postoperatorio de evacuación de residuos y exudados retroperitoneales. Existen tres técnicas comparables: la necrosectomía puede estar combinada con open packing22,23, con una relaparotomía planificada en etapas24 o con lavado interno de la bolsa omental25. Se ha demostrado que los tres protocolos realizados por manos expertas conducen a resultados aceptables. En 72 pacientes tratados con necrosectomía repetida por medio de una técnica de cremallera entre 1983 y 1995, la morbilidad y la mortalidad hospitalarias fueron del 56 y el 25%, respectivamente. Los autores llegaron a la conclusión de que el método de cremallera mejoraba la eficacia de la necrosectomía y disminuía la incidencia de infección intraabdominal recurrente. Sin embargo, hubo problemas de hemorragia postoperatoria, lo que supuso un resultado peor26. Así, preferimos un método más conservador que combine la necrosectomía con el lavado interno de la bolsa epiploica reduciendo, así, el riesgo de hemorragia postoperatoria27.
El momento
Los pacientes con pancreatitis necrosante que fallecen en los primeros 7 días sufren complicaciones cardiovasculares, pulmonares y renales que determinan el curso clínico, y gracias al tratamiento temprano en la UCI la inestabilidad hemodinámica inicial se puede tratar de forma eficaz. Por tanto, ya no se observan apenas aquellos casos de fallecimiento y prácticamente ninguno de nuestros pacientes es operado durante esta fase inicial11. Sólo operamos inmediatamente en el caso de que se demuestre necrosis infectada temprana o en el raro caso de complicaciones del tipo hemorragia grave o perforación del intestino.
En la segunda fase del curso natural de la enfermedad (sin tratamiento antibiótico), la infección del tejido necrótico representa el mayor factor de riesgo para un mal desenlace. El número de pacientes con necrosis infectada aumenta con el tiempo y alcanza casi el 70% en la tercera semana de la enfermedad9. Además, 2 semanas o más después de la aparición de la enfermedad es más fácil la delimitación entre tejido viable y necrótico que en las etapas anteriores del proceso. Sin embargo, el proceso de delimitación aún no se puede evaluar de forma objetiva. Por tanto, el aplazamiento de la intervención quirúrgica hasta 2 o 3 semanas tras la aparición del episodio permite unas condiciones quirúrgicas óptimas.
El papel de la infección
Ha habido una tendencia en todo el mundo a ser más restrictivo en el uso de la cirugía. En la tabla 1 se exponen las indicaciones actuales para la cirugía comparándolas con las del pasado. La infección de la necrosis pancreática es el factor más importante de mortalidad en la pancreatitis aguda grave, y es generalmente aceptado que debe ser tratada de forma quirúrgica. Si se exceptúa una minoría de fallecimientos prematuros debidos a la llamada pancreatitis aguda fulminante, la mayoría de las muertes se producen, hoy día, tras los primeros 7 o 10 días, debido a complicaciones infecciosas, principalmente la necrosis infectada, hasta el punto de que la infección pancreática está considerada como el principal factor de mortalidad en la pancreatitis aguda. De hecho, el 80% de los pacientes con pancreatitis aguda grave muere a causa de la infección de la necrosis pancreática. Por tanto, la prevención de este factor de riesgo supone un gran paso adelante en el tratamiento de la pancreatitis necrosante, lo que está respaldado por los datos obtenidos en varios ensayos clínicos aleatorios restringidos a pacientes con diagnóstico de pancreatitis aguda grave. Los resultados de estos estudios han sido revisados y sujetos a metaanálisis, y se ha demostrado una mejora en los resultados asociada con el tratamiento con antibióticos28,29. Por ello, un gran número de médicos con la responsabilidad de tratar la pancreatitis aguda utiliza profilaxis antibiótica en el tratamiento inicial de pacientes con diagnóstico de enfermedad grave. Como la necrosis se desarrolla en las primeras etapas, es necesario que se inicie el tratamiento con antibióticos tan pronto como se sospeche o se demuestre un curso grave, de acuerdo con los valores de proteína CAP, o con los resultados de la tomografía axial computarizada (TAC). En el curso natural de la pancreatitis aguda, los cultivos de la necrosis pancreática infectada producen una flora monomicrobiana en el 60-87% de los casos, mientras que los cultivos polimicrobianos sólo se confirman en un 13-40%. Generalmente hay un predominio de bacterias aerobias gramnegativas (E. coli, Pseudomonas spp.; Proteus, Klebsilla spp.), lo que hace pensar en un origen entérico, aunque también se han encontrado bacterias grampositivas, anaerobias, y alguna vez hongos. La incidencia de la infección por hongos y organismos grampositivos puede aumentar a largo plazo, especialmente tras un tratamiento prolongado con antibióticos; sin embargo, si se trata de forma adecuada, la infección micótica del páncreas no está asociada con un desenlace fatal8. Además, se ha demostrado que hay una "barrera" en el páncreas que es responsable de la entrada selectiva de los antibióticos. La evaluación de la concentración de las distintas clases de antibióticos ha demostrado que las quinolonas (ciprofloxacino, ofloxacino), así como el carbapenem y el imipenem son las sustancias que alcanzan los valores más altos en el tejido pancreático y, además, tienen la mayor acción bactericida contra la mayoría de los organismos presentes en la infección pancreática30. Por ello, estas sustancias antibióticas están consideradas como antibióticos de primera elección para los pacientes con pancreatitis necrosante. En cambio, los aminoglucósidos, a pesar de su eficacia contra los microorganismos gramnegativos, son incapaces de penetrar en el páncreas humano en concentraciones bactericidas y finalmente han demostrado que son ineficaces en la pancreatitis necrosante.
La mayoría de los datos disponibles acerca del papel de los antibióticos se refiere a la administración intravenosa de sustancias antibióticas. La eliminación o la reducción de las bacterias intestinales puede proporcionar un posible mecanismo para reducir o eliminar la infección en la necrosis pancreática. En un ensayo aleatorio controlado que investigaba la descontaminación selectiva del intestino en pacientes con pancreatitis aguda grave definida por una puntuación Imrie ≥ 3 y/o un grado Baltasar D o E, la descontaminación selectiva redujo el número de infecciones por bacterias gramnegativas. Sin embargo, en este estudio también se suministró cefuroxima por vía intravenosa; además, el resultado positivo de la descontaminación selectiva puede haberse visto acentuado por los antibióticos intravenosos prescritos de forma rutinaria31. De forma más reciente se han publicado datos sobre la perfusión continua de antibióticos en la arteria regional, que parece inhibir la infección de la necrosis pancreática tanto en perros como en seres humanos con pancreatitis grave necrosante. Sin embargo, el estudio en humanos32 no se hizo de forma controlada ni aleatoria, por lo que son necesarios más estudios para evaluar esta terapia. Además, la administración intraarterial regional es mucho más difícil técnicamente que poner una sencilla línea intravenosa.
El papel de la necrosis
La pancreatitis aguda grave está definida por la presencia de fallo de órganos o complicaciones locales, especialmente la necrosis pancreática2. En otras palabras, la necrosis sirve más para confirmar que para predecir el curso grave de la enfermedad. Sin embargo, la medida de los indicadores de necrosis en suero y plasma son útiles para la valoración temprana de la gravedad de la enfermedad, y se ha descubierto que, dentro de las 48 h que siguen a la presentación de la enfermedad la proteína reactiva C (el parámetro mejor estudiado) ayuda a discriminar entre pancreatitis edematosa y necrosante con una precisión del 90 al 95%. En pacientes con curso grave de la enfermedad la necrosis se desarrolla de forma temprana, es decir, dentro de los primeros 4 días tras la aparición de los síntomas. La necrosis se puede presentar únicamente como pancreática o como pancreática y peripancreática. Se desconocen las razones por las que algunos pacientes padecen la forma necrosante de la enfermedad y también cuáles son los factores que influyen en la extensión de la necrosis. Hoy día no se conoce ningún tratamiento eficaz para evitar su formación o reducir su extensión en un paciente concreto.
Por otro lado, sigue habiendo controversia sobre si la necrosis en sí misma (es decir, la necrosis estéril) es un factor de riesgo para que existan complicaciones y también sobre cómo tratarla3,21,33,34.
Beger et al descubrieron que la extensión de la necrosis pancreática influía en la tasa de mortalidad. Cuando más del 30% de la glándula estaba necrótica el 7% de los pacientes fallecía, y cuando la necrosis cubría toda la glándula, la tasa de mortalidad era del 50%. Además, la posibilidad de una contaminación bacteriana estaba directamente relacionada con el grado de necrosis pancreática. En pacientes con necrosis extendidas (es decir, de más del 50% del páncreas) la tasa de infección llegaba al 71%35. A partir de estos datos se llegó a la conclusión de que los pacientes con necrosis estéril extendida generalmente necesitaban tratamiento quirúrgico.
Otros cirujanos han intentado evitar la cirugía en pacientes con necrosis estéril, con independencia de su extensión, por varias razones: la operación se puede posponer hasta que sobrevenga la infección, dado que las técnicas para comprobar su existencia son seguras y fiables. Además, la operación del tejido necrótico (previamente) estéril puede conducir a la infección, empeorando así el pronóstico. Aparte de esto, muchos pacientes se recuperan sin cirugía incluso si la necrosis estéril está muy extendida. En pruebas recientes se ha descubierto que el tratamiento conservador de la necrosis estéril es seguro y efectivo. La tasa de mortalidad en 56 pacientes con necrosis estéril con tratamiento no quirúrgico fue del 1,8% (1/56)3. Sin embargo, algunos pacientes con necrosis estéril no mejoran a pesar del tratamiento con cuidados intensivos máximos. En estos casos, que representan sólo una pequeña minoría de pacientes con necrosis estéril, la cirugía puede hacerse necesaria incluso en ausencia de infección. Para reducir al mínimo el riesgo de hemorragia durante la operación y evitar la pérdida innecesaria de tejido pancreático viable se debe aplazar la cirugía hasta después de la tercera semana de la aparición de la enfermedad.
En un informe reciente se demostró que en pacientes con necrosis estéril existía relación entre la amplitud de la necrosis y la frecuencia de fallo de órganos; mientras que la necrosis infectada estaba asociada con el fallo de órganos de forma independiente de la extensión de la necrosis, lo que apoya la hipótesis de que la infección es el mayor determinante del desenlace36.
La etiología
Se ha supuesto que existen diferencias con respecto al curso clínico, el tratamiento terapéutico y el desenlace en función del factor etiológico subyacente en la pancreatitis aguda. Fung et al, de la Mayo Clinic descubrieron que la pancreatitis aguda es más grave cuando está inducida por colangiopancreatografía retrógrada endoscópica (CPRE). Es importante conocer que el grupo post-CPRE tuvo una tasa más alta de necrosis pancreática infectada, lo que puede explicar en parte esta gravedad37. En otro estudio realizado sobre 190 pacientes, fuera cual fuese la gravedad de su enfermedad, se analizaron las enzimas del suero, los indicadores de necrosis, las complicaciones sistémicas y la mortalidad en función de la etiología. Se demostró claramente que una vez que los mecanismos patógenos han iniciado la pancreatitis aguda, el curso y desenlace de la enfermedad no se veían influidos por el factor etiológico subyacente38. Sin embargo, la etiología sí afecta a la indicación de una intervención quirúrgica que no se centre en la pancreatitis en sí, sino en el factor que la provoca. Si se descubre que se debe a un páncreas divisum, normalmente se resuelve el problema con una papilotomía de la papila menor. Si hay un tumor obstruyendo la ampolla de Vater o en la cabeza del páncreas y que se espera que produzca un ataque de pancreatitis aguda, el tratamiento siguiente será una CPRE. Más tarde, tan pronto como la pancreatitis mejore, el tratamiento que se debe seguir es una resección según los estándares quirúrgicos oncológicos.
Si la pancreatitis está relacionada con un cálculo biliar, el tratamiento puede seguir una o dos direcciones que dependen del curso clínico. En casi todos los pacientes con enfermedad de leve a moderada el tratamiento será el rutinario en las pancreatitis, ya que en la mayoría de los casos el paciente responde a este régimen de tratamiento en las primeras 24 a 48 h: el dolor comienza a calmarse, y los signos vitales y las alteraciones de las enzimas del suero vuelven a la normalidad; esto sucede generalmente en la primera semana de hospitalización. En este punto, en nuestro grupo solemos realizar un examen de CPRE y una desobstrucción preoperatoria del conducto biliar seguida de una colecistectomía laparoscópica, que ha demostrado ser segura y bien tolerada en estas circunstancias39,40. Si no se consigue la desobstrucción del conducto biliar es imprescindible llevar a cabo una colangiografía para asegurarse de que no quedan cálculos en el conducto. Si hubiera alguno, se debe retirar con el procedimiento con el que esté más familiarizado el cirujano. Entre estos procedimientos puede estar una exploración laparoscópica del conducto común, incluso una colecistectomía abierta y exploración del conducto común según la técnica usual o una colangiografía endoscópica postoperatoria inmediata con esfinterotomía y extracción de la piedra39,41. Al practicarse la colecistectomía durante la misma estancia en el hospital se evita la alta probabilidad de pancreatitis recurrente por cálculos biliares que acompañaba la práctica de la denominada "colecistectomía a intervalos". La extirpación de la vesícula biliar se puede realizar de forma segura durante la misma estancia hospitalaria, con lo que el coste económico para la sociedad por la pérdida de horas de trabajo y hospitalización repetida es menor41. En los pacientes cuya condición empeora a pesar del tratamiento, en los que padecen colangitis o colestasis y en los que ingresaron con pancreatitis grave, se debe considerar la posibilidad de que un cálculo biliar se haya encajado en la ampolla de Vater. Estos pacientes deben ser tratados en la UCI con apoyo cardiovascular y respiratorio óptimos, y se deben dispensar antibióticos de amplio espectro por vía intravenosa. Tan pronto como sea posible, especialmente en pacientes con colangitis concomitante, se debe estabilizar su condición para que puedan soportar una colangiografía endoscópica. En este momento, se puede confirmar la presencia de un cálculo biliar encajado, y la piedra puede ser extraída o desalojada, aliviando la obstrucción42-45. A menudo se realiza una esfinterotomía en este momento y se limpia de cálculos el conducto. No se debe insertar ningún espiral por el riesgo inherente de infección. El paciente regresa entonces a la UCI, y se sigue su tratamiento médico, con la esperanza de que mejore su situación. Cuando el examen endoscópico no demuestra evidencia de obstrucción del conducto, se debe continuar con el tratamiento médico. La cirugía por cualquier causa durante los primeros días en pacientes con pancreatitis grave no está indicada casi nunca3,39,41,46. Sin embargo, si la obstrucción del conducto no puede ser eliminada con la endoscopia, se debe realizar una operación con toda urgencia. En este momento, se debe explorar el conducto biliar común y se deben retirar todos los cálculos para garantizar el libre flujo de bilis y jugo pancreático al duodeno. Casi nunca es necesario abrir el duodeno para realizar esto. Es más, nosotros nos mostraríamos extremadamente remisos a realizar una duodenotomía ante una inflamación aguda, por el temor de que se produjera una fuga duodenal. Se debe realizar una colecistectomía y colocar un tubo T largo dentro del conducto biliar común. Hay que estar alerta, especialmente con este grupo de pacientes que han sido explorados, ante el desarrollo de necrosis pancreática infectada que exigiría de nuevo un tratamiento quirúrgico.
Resultados en Berna
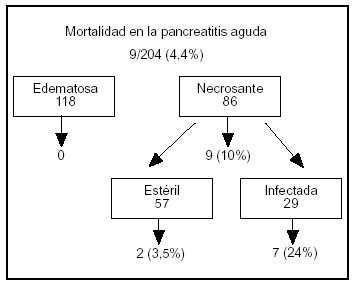
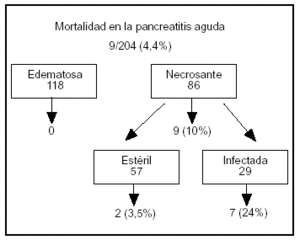
Aplicamos el protocolo "tratamiento según el estatus de la infección" a un total de 86 pacientes con pancreatitis necrosante demostrada con CT aumentado con contraste3. Todos ellos recibieron terapia con imipenem/cilastatina por vía intravenosa con una dosis de 3 x 0,5 g/día durante un mínimo de 14 días. En caso de presentación de síntomas clínicos de sepsis se practicó a los pacientes una aspiración con aguja fina con tinción de Gram y cultivo. Todos los pacientes con pancreatitis necrosante fueron tratados en la UCI con las máximas medidas de terapia conservadora. En 29 pacientes (34%) se descubrió necrosis pancreática infectada con el análisis por aspiración con aguja fina tras un promedio de 21 días desde la aparición de la enfermedad, lo que condujo a la intervención quirúrgica de dichos pacientes. Tras la necrosectomía, los pacientes fueron tratados con continuos lavados retroperitoneales durante un promedio de 38 días (entre 10 y 124). En el período postoperatorio 6 pacientes necesitaron una laparatomía. La duración media de la estancia de los pacientes con necrosis pancreática estéril e infectada fue de respectivamente 23,5 días (entre 11 y 85) y 85 días (entre 22 y 209). Nueve pacientes murieron, la mayoría de ellos debido a fallo orgánico generalizado de origen séptico (fig. 1).
Figura 1. Resumen de la mortalidad en 204 pacientes con pancreatitis aguda tratados en el Hospital Universitario de Berna3.