INTRODUCCIÓN
El shock séptico es un estado de hipoperfusión tisular grave desencadenado por la respuesta inflamatoria sistémica de origen infeccioso. La conferencia consenso de ACCP/SCCM en 19921 definió el shock séptico como el estado de hipotensión inducido por la sepsis, a pesar de un adecuado aporte de líquidos, junto con alteraciones en la perfusión tisular. La hipotensión se definió como una presión arterial sistólica < 90 mmHg o el descenso de ≥ 40 mmHg de la presión sistólica normal. Los trastornos de perfusión se definieron como el aumento del ácido láctico > 2 mEq/l, oliguria < 30 ml/hora, y trastornos mentales agudos, como agitación, obnubilación o confusión. En cuanto a los pacientes que, a pesar de estar tratados con fármacos vasoactivos y/o inotropos y estar normotensos, mantienen un trastorno de perfusión o fallo de algún órgano, se consideraron en situación de shock séptico.
Un estudio epidemiológico reciente mostró un aumento en EE.UU. del 8,5% en la incidencia anual de shock séptico2. Este aumento parece estar condicionado por la mayor edad de los pacientes, el aumento de la invasión e instrumentación médica, la inmunosupresión de la quimioterapia, trasplantes, alta incidencia de sida y el incremento de resistencias a los antimicrobianos. A pesar de la incorporación de nuevos tratamientos, la mortalidad permanece alta, alrededor del 50%-60%.
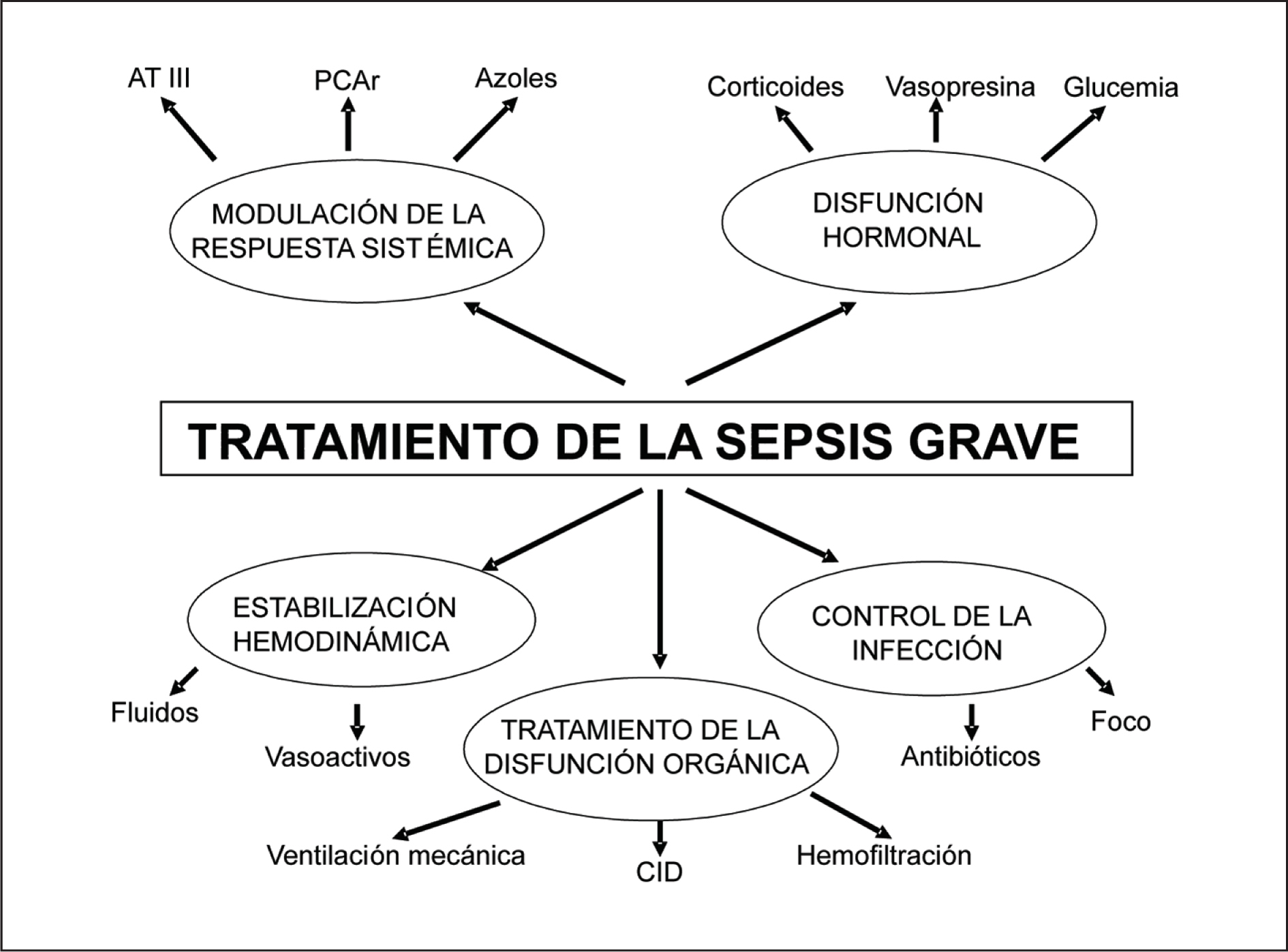
Actualmente, el tratamiento de la sepsis grave y del shock séptico lo podemos dividir en control de la infección, estabilización hemodinámica, tratamiento específico de la disfunción orgánica, modulación de la respuesta inflamatoria y tratamiento de la disfunción hormonal. A pesar de ser la estabilización hemodinámica, tras el control de la infección, la parte más habitual del tratamiento de la sepsis grave y que más reuniones de expertos y artículos de revisión ha generado3-5, algunos aspectos fundamentales como los objetivos terapéuticos, modos de monitorización y el inicio y/o cantidad de volumen y fármacos vasoactivos, se encuentran en debate permanente (fig. 1).
Figura 1. Esquema de tratamiento de la sepsis grave. AT III: antitrombina III; PCA: proteína C activada.
OBJETIVOS TERAPÉUTICOS
A finales de los años ochenta se preconizó maximizar algunos parámetros hemodinámicos y metabólicos, como el transporte de oxígeno (TO2) y el consumo de oxígeno (VO2), con el objetivo de mejorar la supervivencia de distintos grupos de pacientes críticos, incluidos los sépticos. Shoemaker et al6 propusieron valores de índice cardíaco > 4,5 l/min/m2, índice de TO2 > 600 ml/min/m2, e índice de VO2 > 170 ml/min/m2, encontrando mayor supervivencia en aquellos pacientes críticos en los que se conseguía alcanzar estas metas. Hayes et al7 estudiaron la supervivencia en un grupo de pacientes críticos cuyo tratamiento estaba enfocado a maximizar los indicadores metabólicos, encontrando mayor supervivencia en el grupo control. En sus conclusiones estos autores sugirieron que el empleo de dosis elevadas de fármacos inotrópicos puede tener efectos deletéreos, a pesar de mantener valores normales o supranormales de TO2. Gattinoni et al8 valoraron la mortalidad, morbilidad y días de estancia en una Unidad de Cuidados Intensivos (UCI) en 762 pacientes críticos distribuidos aleatoriamente en tres grupos según el objetivo terapéutico: uno para conseguir un índice cardíaco (IC) normal (2,5-3,5 l/min/m2) (grupo control), el segundo dirigido a maximizar el IC (> 4,5 l/min/m2) y el tercero a optimizar la saturación venosa mixta de oxígeno (SvmO2) (> 70%). No encontraron diferencia significativa de supervivencia en los pacientes en los que se consiguieron niveles supranormales de IC o de SvmO2.
Recientemente, Rivers et al9 compararon en pacientes con shock séptico la eficacia de optimizar precozmente valores hemodinámicos y metabólicos con un tratamiento estándar. Los pacientes ingresaron en la UCI tras 6 horas en Urgencias en las que en el grupo de tratamiento se debía de alcanzar los siguientes objetivos: presión venosa central (PVC) entre 8 y 12 mmHg, mediante un aporte de volumen, vasopresores hasta conseguir presión arterial media (PAM) superior a 65 mmHg, vasodilatadores si la PAM era superior a 90 mmHg, corrección del hematocrito hasta alcanzar un 30% y, si la saturación venosa central de oxígeno (SvcO2, medida en la aurícula derecha) era inferior al 70%, se utilizaba dobutamina hasta conseguir los niveles de SvcO2 deseados. Con esta estrategia, el 99% de los pacientes con tratamiento optimizado consiguieron los mencionados objetivos y presentaron una mortalidad hospitalaria del 30,5%, significativamente menor que los tratados de forma estándar, que fue del 46,5%. Algunas críticas vertidas sobre este estudio han señalado diferencias en la mortalidad del grupo placebo comparadas con las publicadas en otros estudios similares, en la reposición de volumen, en el tiempo de estancia en el área de urgencias entre los grupos, y en la utilización de transfusiones de hematíes, factor con impacto negativo en el pronóstico de pacientes sépticos según otros estudios publicados con anterioridad. Pero es importante reseñar la asociación en las series estudiadas entre inicio tardío del tratamiento y fracaso del tratamiento7,8,10,11 o, por el contrario, efectos beneficiosos del tratamiento si se aplica de forma precoz6,9,12. Sólo dos estudios9,10 incluyen pacientes exclusivamente sépticos, otros tres pacientes críticos mixtos7,8,11 y dos estudios pacientes quirúrgicos. De los dos estudios en pacientes sépticos uno no encuentra diferencia en cuanto a supervivencia y otro sí.
Básicamente, el primer objetivo debe ser lograr una presión arterial normal. De forma arbitraria, basándose en estudios experimentales, se ha considerado que la presión de perfusión es adecuada a partir de una presión arterial sistólica de 90 mmHg o una PAM de 60 mmHg. La PAM valora mejor la presión de perfusión, por lo que es preferible a la presión arterial sistólica. Una PAM por encima de 60 mmHg asegura habitualmente la perfusión tisular. La perfusión tisular es igual de adecuada con PAM entre 60 mmHg y 85 mmHg4.
Inicialmente se debe asegurar una precarga "adecuada", con el objeto de mejorar el gasto cardíaco. La medición de presiones de llenado (presiones en la aurícula derecha, PVC) o presiones de enclavamiento en la arteria pulmonar (PAPo) proporciona, además de una referencia de la precarga y de la volemia eficaz, un límite de seguridad en el aporte de líquidos en la resucitación.
Se ha considerado en la práctica diaria la PAPo como indicador de la precarga del ventrículo izquierdo. Sin embargo, entre la PAPo, la presión en la aurícula izquierda (PAI) y la presión telediastólica del ventrículo izquierdo (PTDVI) puede haber obstáculos y/o alteraciones que impidan esta equivalencia. Así, circunstancias como la colocación de la punta del catéter de arteria pulmonar en zona I o II de West, aumento de áreas con zona I o II por hipovolemia, presión positiva al final de la espiración (PEEP) elevada (o auto-PEEP), lesiones como la obstrucción de las venas pulmonares, la afectación mitral y aórtica, y el aumento de la presión torácica o intraabdominal, provocan mediciones de precarga erróneas.
La PAPo se utiliza como presión límite de seguridad al considerarse una aproximación a la presión hidrostática capilar pulmonar (PCP), factor decisivo en la producción del edema pulmonar. La PAPo es la medida de la presión en las venas pulmonares que, con frecuencia, puede corresponder con la PAI y, en condiciones normales, se corresponde con la PTDVI13. La PAPo es una estimación a la baja de la PCP, de tal forma que ambas presiones sólo son superponibles cuando las resistencias venosas pulmonares son, prácticamente, nulas. Al contrario de lo que ocurre en la circulación sistémica, las resistencias venosas contribuyen en un 40% a las resistencias totales pulmonares y esta proporción aumenta en situaciones de sepsis e hipoxia, que cursan con intensa venoconstricción pulmonar. Garr et al determinaron en 1967 la siguiente ecuación que relaciona la PAPo con la PCP: PCP = PAPo + 0,4 (PAP media-PAPo). Esta relación entre PCP y PAPo, que en individuos sanos no representa una diferencia superior a 2-3 mmHg, en pacientes graves con síndrome de distrés respiratorio agudo (SDRA) secundario a sepsis puede llegar a ser ≥ 10 mmHg, ya que el componente venoso puede llegar a representar más del 60% del valor total de las resistencias vasculares pulmonares14.
La utilización de las presiones como guía de seguridad en el aporte de líquidos y como valoración de los parámetros de función cardíaca necesitan de un gran conocimiento de la técnica para saber interpretar los datos obtenidos, destreza en la realización de la misma cumpliendo un riguroso protocolo de medidas (calibración, calidad de trazados, ausencia de artefactos y posición correcta del catéter), y conocer los factores externos que pueden influir sobre el cero de referencia o presión transmural, como son el aumento de las presiones tanto en el tórax como en el abdomen, haciendo las correcciones pertinentes.
Al comienzo del aporte de volumen, la monitorización debe realizarse a través de la PVC. Aunque esta medición representa únicamente la presión de aurícula derecha y, normalmente, la presión telediastólica del ventrículo derecho, la interrelación de ambos ventrículos, sobre todo en los casos de disfunción cardiovascular, justifica su uso. La curva de función del ventrículo derecho alcanza su plateau con presiones entre 8 y 12 mmHg, los intentos de aumentar el gasto cardíaco sobrepasando este nivel son inútiles ya que el corazón izquierdo sólo es capaz de bombear lo que recibe del ventrículo derecho, y además el exceso de líquido suele producir efectos indeseables15. Por otra parte, un aumento de presiones conlleva una dilatación de las cámaras derechas y una reducción de la compliancia del ventrículo izquierdo por el fenómeno de interdependencia. Así se limita de forma importante la necesidad de utilizar el catéter de arteria pulmonar. Cuando no se alcanzan los objetivos es conveniente insertar un catéter de Swan-Ganz, porque cualquier patología del ventrículo derecho modifica su curva de función ventricular.
En la actualidad se están desarrollando otros métodos de monitorización de la precarga y la volemia, distintos a la determinación de presiones de llenado, que se pueden considerar complementarios. Los avances en ecocardiografía doppler, sobre todo con sonda transesofágica (ECO-TE) y el cálculo de volúmenes mediante la técnica de termodilución transpulmonar simple (PiCOO), se están demostrando útiles.
La ecocardiografía doppler (ECO) facilita no sólo imágenes estructurales del corazón y grandes vasos, sino también información funcional, derivada de cálculos de las dimensiones (áreas) de las cavidades cardíacas en distintos momentos del ciclo cardíaco, del análisis del flujo transvalvular y de los diámetros de los grandes vasos. Con la ECO no podemos medir presiones directamente, pero se han descrito varias fórmulas producidas del análisis de la regresión lineal múltiple entre los parámetros derivados de los flujos transmitral y venoso pulmonar, obtenidos por doppler, y las distintas presiones de llenado medidas con catéter de arteria pulmonar. Varios estudios de metodología diversa han sido publicados con la intención de ofrecer una forma fácil y fiable de calcular las distintas presiones de llenado, obteniendo elevadas correlaciones (0,85-0,95), tanto con ecocardiografía transtorácica (ECO-TT) como con ECO-TE. Estudios realizados en pacientes sépticos han demostrado la eficacia de la ECO en su manejo hemodinámico, tanto en la valoración de la precarga, de la contractilidad y de la compliancia del ventrículo izquierdo, así como la respuesta al aporte de volumen mediante exploraciones repetidas16.
La utilización de PiCCO permite monitorizar de forma continua el gasto cardíaco, la variabilidad de la presión de pulso y del volumen sistólico. Así mismo, estima de forma intermitente la gravedad del edema pulmonar, el volumen intratorácico intravascular y el de las cavidades cardíacas, dos medidas relacionadas con la precarga ventricular.
La determinación sucesiva del edema pulmonar (ELW: extravascular lung water) durante la administración de fluidos en el enfermo crítico fue utilizada hace más de una década por Mitchel et al17. Estos investigadores demostraron el efecto beneficioso de su utilización disminuyendo la duración de la ventilación mecánica y de la estancia en UCI en un grupo de enfermos críticos.
Las dos medidas volumétricas que se pueden medir con el PiCCO, el volumen torácico intravascular y el volumen cardíaco telediastólico (global end-diastolic volume) han mostrado más fiabilidad para estimar la precarga ventricular que las medidas de presión habitualmente utilizadas en la clínica (PVC y PAPo). Recientemente, Michard et al18 han investigado la utilidad del volumen cardíaco telediastólico para estimar la precarga ventricular comparándola con la PVC en un grupo de enfermos con shock séptico. Estos investigadores concluyen que en los enfermos en shock séptico, y al contrario de lo que sucede con la PVC, el volumen cardíaco telediastólico es un indicador fiable de la precarga ventricular.
La monitorización con el PiCCO nos permite conocer de forma continua dos medidas, la variabilidad de la presión de pulso y la variabilidad del volumen sistólico, que pueden ser especialmente útiles para detectar aquellos enfermos en los que se puede esperar un aumento del gasto cardíaco en respuesta a la administración de fluidos intravenosos, lo que algunos autores denominan estado "precarga-dependiente". La utilidad de estas medidas ha sido únicamente investigada en enfermos en ventilación mecánica controlada.
En los pacientes sépticos el gasto cardíaco se encuentra aumentado normalmente, pero al inicio del cuadro, y tardíamente se puede encontrar disminuido. El objetivo del aporte de volumen es aumentar el gasto cardíaco y la mayoría de las veces es suficiente. Los valores de 2,5-3 l/min/m2 de índice cardíaco se consideran suficientes, ya que en estudios clínicos se ha demostrado la ineficacia de forzar el tratamiento para la consecución de índices cardíacos superiores8.
Es conveniente que la monitorización del gasto cardíaco sea continua y para ello se ha utilizado un catéter de arteria pulmonar con termodilución. Si está canalizada una arteria sistémica se puede calcular el gasto cardíaco continuo mediante el análisis del contorno de la presión de pulso19. Si el enfermo está en ventilación mecánica, es posible la determinación del gasto cardíaco continuo mediante técnica de reinhalación parcial del CO2 basada en el principio indirecto de Fick (NICO®)19, o mediante la medida del volumen latido por sonda eco-doppler esofágica (HEMOSONIC®).
La sonda de ecografía-doppler esofágica (HEMOSONIC®) permite una monitorización hemodinámica mínimamente invasiva mediante la medición continua del diámetro y del flujo aórtico. La obtención continua del volumen sistólico (VS), del gasto cardíaco y de una serie de parámetros derivados de la morfología de la onda de flujo aórtico permiten, teóricamente, tener una idea de la situación hemodinámica del paciente (precarga, contractilidad y resistencias vasculares sistémicas), facilitando de este modo la detección inmediata de cambios hemodinámicos, el tratamiento precoz y la evaluación en tiempo real de la respuesta al mismo. Las mediciones de gasto cardíaco obtenidas mediante esta sonda se correlacionan aceptablemente con otras técnicas de monitorización y su empleo intraoperatorio en pacientes quirúrgicos conlleva un aumento en la supervivencia20.
Las principales limitaciones de este sistema de monitorización son fundamentalmente las arritmias cardíacas y las malformaciones o dificultades que impidan la inserción de la sonda a través del esófago. Asimismo, se requiere un período mínimo de aprendizaje para que las mediciones obtenidas sean fiables, aunque este período de entrenamiento no es mucho mayor que el de otras técnicas convencionales de monitorización. Queda aún por determinar la utilidad práctica de esta técnica en los pacientes de UCI y concretamente en los sépticos graves.
PERFUSIÓN/OXIGENACIÓN TISULAR
La obtención de los objetivos hemodinámicos antes citados, aunque imprescindible, no asegura una adecuada perfusión y oxigenación tisular. De forma indirecta y fácil podemos valorar en la clínica el estado de perfusión mediante la diuresis horaria, el relleno capilar, la temperatura de la piel, la existencia de livideces o el estado mental del paciente. La utilidad de la SvmO2 como índice de perfusión global no ha sido demostrada, siendo más bien un índice de los cambios del gasto cardíaco.
Determinación de ácido láctico
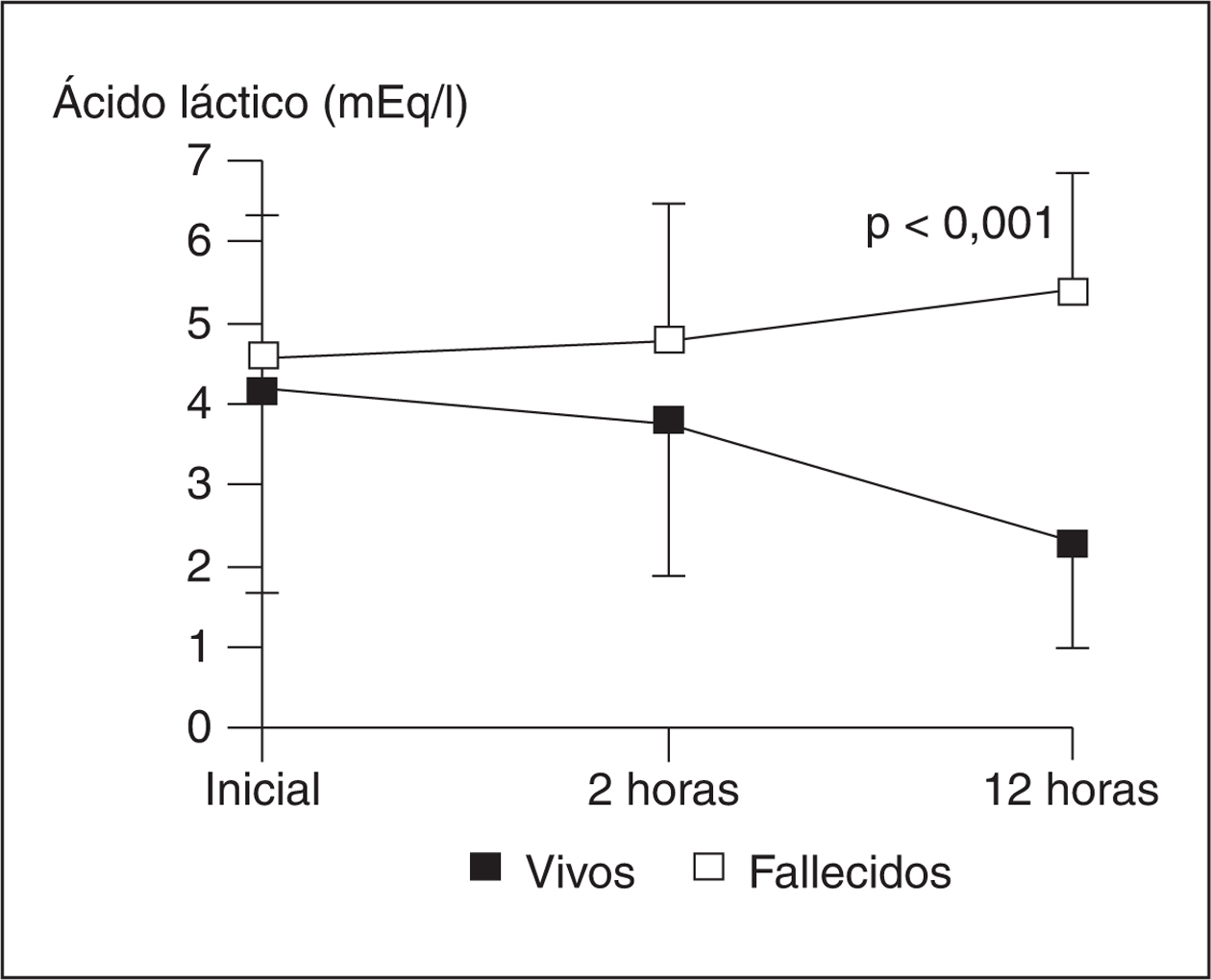
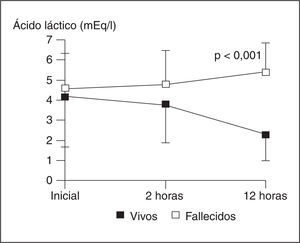
Los niveles de ácido láctico están aumentados con frecuencia en los pacientes sépticos y, sin embargo, este hallazgo se considera inespecífico. Además de aumentar como consecuencia de la hipoxia celular y metabolismo anaerobio, otros factores como el hipermetabolismo, el déficit de piruvato deshidrogenasa y la disminución del aclaramiento hepático, pueden aumentarlo, y todos ellos se pueden dar en la sepsis grave. El cociente láctico/pirúvico mayor de 15 es más adecuado que la determinación aislada de ácido láctico para diferenciar la hiperlactacidemia por hipoxia, del aumento de la glucólisis aeróbica en situaciones de gran estrés metabólico, como es la sepsis grave. A pesar de su inespecificidad, la persistencia de niveles altos de lactato ha sido descrito como un buen marcador pronóstico metabólico21 (fig. 2).
Figura 2. Evolución de los niveles de ácido láctico en 62 pacientes con sepsis grave. Se comparan los grupos de supervivencia y se observa diferencia significativa de los niveles de ácido láctico a las 12 horas. Med Intensiva 1997;21S:22.
Monitorización regional de oxígeno
La inexistencia de un trastorno en la perfusión global no descarta la presencia de alteraciones regionales (disoxia regional), por lo que su conocimiento sería de gran ayuda para prevenir la disfunción orgánica. La monitorización de la perfusión esplácnica ha sido el objetivo de la monitorización regional de O2 por ser la mucosa intestinal, debido a su característica vascularización, muy sensible a la inestabilidad hemodinámica y propensa al desequilibrio entre la oferta y la demanda de O2. Por otra parte, su alta actividad metabólica, la importante actividad inmunológica y su función "barrera" se ha relacionado con el origen del fallo multiórgano.
La hipercapnia tisular es un fenómeno universal de los tejidos hipóxicos por hipoperfusión durante los estados de shock. La tonometría gástrica consiste en la monitorización del pH de la pared gástrica mediante su determinación a través de la ecuación de Henderson-Hasselbalch. Su utilización como indicador temprano de disoxia regional y predictor de mortalidad ha sido referenciado en la bibliografía, pero sin embargo no se ha demostrado su utilidad como guía de tratamiento en el shock séptico22.
Capnografía sublingual
Recientemente se ha determinado que el descenso de flujo sanguíneo a nivel sublingual es paralelo al observado en el territorio mesentérico en situación de shock, y que la determinación de PCO2 sublingual (PSLCO2) se correlaciona significativamente con la PCO2 de la mucosa gástrica. La facilidad de abordaje y determinación hace que sea una técnica no invasiva, y ha despertado gran atención como técnica de monitorización de la disoxia regional. Se ha mostrado como un buen indicador pronóstico, sobre todo la diferencia entre la PCO2 sublingual y la PCO2 arterial medidas simultáneamente (PSLCO2-PaCO2). Su utilización como objetivo terapéutico, al igual que la tonometría gástrica, en los pacientes con shock séptico no ha sido demostrada en estudios clínicos amplios, pero la facilidad de utilización y la ausencia de algunas de las limitaciones de la tonometría gástrica aumentan sus expectativas23.
TRATAMIENTO
Las guías de tratamiento coinciden en que el primer paso debe ser una administración de volumen precoz e intensa. Posteriormente, si no se consigue normalizar la presión arterial, se debe administrar un fármaco vasoconstrictor.
Volumen
Analizando el estudio de Rivers et al9 se observa que la administración de líquidos fue superior en el grupo optimizado (+ 1,5 l de media). Por tanto, una rápida e intensa administración de volumen contribuye a la disminución de mortalidad.
La primera incógnita es determinar qué tipo de líquidos se debe utilizar, cristaloides o coloides. Desgraciadamente en el trabajo de Rivers el tipo de líquido se dejó a criterio del investigador. Ambos tipos de soluciones son utilizadas en la actualidad, no existiendo diferencia significativa a favor de ninguno de los dos tipos en los trabajos publicados3-5. Aunque no se han comunicado diferencias en los resultados entre coloides y cristaloides, la administración de los primeros necesita de 2 a 4 veces menos volumen que los segundos, con el consiguiente ahorro de tiempo de infusión4. En cuanto al suero salino hipertónico no existen pruebas por ahora que justifiquen su utilización en el shock séptico.
En los pacientes en shock séptico se aconseja mantener niveles de hemoglobina entre 8-10 g/dl (28%-30% de hematocrito), no aconsejando transfundir hasta los 7 g/dl si no existen problemas en el TO23-5. Por encima de esta cifra no se han demostrado ventajas y sí complicaciones derivadas del aumento de la viscosidad e inmunodepresión. Durante la administración de líquidos se espera un descenso de la hemoglobina de entre 1 y 3 g/dl4.
Los volúmenes deben administrarse de forma rápida, en forma de "carga" cada 15-30 minutos. Para los cristaloides el volumen de las cargas se recomienda de 500 ml, de los que sólo permanecen el 10%-20% en el compartimento intravascular a partir de la primera hora. Por otra parte, los coloides se administrarán mediante cargas de 250 ml. Un litro de coloide aumenta el volumen plasmático de 700 a 1.000 ml, de los que el 40% se mantienen intravascularmente a las 24 horas. Durante las 24 primeras horas las necesidades de aporte de volumen pueden oscilar entre 6 y 10 litros, de los cuales una gran parte se alojará en el intersticio, sobre todo si lo que se ha administrado son cristaloides3-5.
Tras cada carga debe monitorizarse el objetivo terapéutico (PAM, signos de hipoperfusión, SvcO2, gasto cardíaco) y el nivel alcanzado en las presiones límites de seguridad (PVC, PAPo). La infusión de líquidos tiene como objetivo restaurar la presión de flujo normal, lo que se debe conseguir con una PAM entre 65-75 mmHg. La PVC como guía de la administración de líquidos debe llevarse hasta un valor límite de 12 mmHg en ventilación espontánea y en pacientes ventilados mecánicamente hasta 15 mmHg, por la supraestimación derivada del aumento de presión transmural. La PAPo hasta 18 mm Hg4. Es interesante tener en cuenta que muchos pacientes tendrán una patología abdominal, quirúrgica o no, que aumente la presión intraabdominal (PIA). Es obligatorio ante esta situación medir la PIA mediante una sencilla técnica a través de la sonda vesical, porque si está aumentada, parte de esa presión se transmite al tórax disminuyendo el retorno venoso, la precarga, el gasto cardíaco y la PAM, y supraestimando la precarga y el gradiente hidrostático transcapilar por las cifras de PVC y PAPo, ya que eleva la presión cero de referencia24. Por tanto tendremos que tener en cuenta esta supraestimación y aumentar el nivel de seguridad de la presión de llenado e incluir otros parámetros complementarios como el índice de volumen telediastólico global, medido mediante la técnica de termodilución transpulmonar17.
Vasopresores
Tras la adecuada repleción de volumen, y si no se ha conseguido el objetivo de perfusión deseado, el siguiente escalón debe ser la utilización de fármacos con efecto vasoconstrictor, siendo aconsejable realizar la monitorización de la presión arterial de forma invasiva5. La utilización de un fármaco vasoconstrictor induce a pensar en su potencial efecto deletéreo sobre la distribución de flujo, concretamente a nivel mesentérico y renal. Así, a pie de cama manejamos el principio de utilizar ampliamente el volumen y la menor dosis de noradrenalina que nos permita conseguir una PAM > 65 mmHg. Sin embargo, se han publicado estudios no controlados que no encuentran efectos desfavorables con el tratamiento de noradrenalina en pacientes sépticos graves4,5.
La noradrenalina es una catecolamina natural con un potente efecto β-adrenérgico y un pronunciado efecto ß-adrenérgico. Por tanto, es un potente vasoconstrictor que eleva la presión arterial y la poscarga cardíaca, y aumenta la contractilidad cardíaca sin importantes variaciones de la frecuencia cardíaca. Es un fármaco de probada eficacia, solo o acompañado de otros vasoactivos3-5. Las dosis son muy variables, desde 0,01 µg kg-1min-1 a 3,3 µg kg-1min-1, aunque las dosis medias oscilan entre 0,2 y 1,3 µg kg-1min-1. La noradrenalina aumenta las resistencias vasculares periféricas y la PAM, con pequeños cambios sobre la frecuencia cardíaca y el gasto cardíaco. El efecto sobre el gasto cardíaco en los pacientes puede ser variable, dependiendo de que predomine el aumento de la poscarga o el efecto inotropo positivo.
Al contrario que en otros tipos de shock, en los que la noradrenalina tiene un marcado efecto vasoconstrictor renal en detrimento de la perfusión renal, en la sepsis grave, al normalizar la resistencia vascular, mejora el flujo renal y el nivel de filtración4,5. En pacientes en shock séptico en los que la noradrenalina corrige la hipotensión, no se han encontrado efectos perjudiciales sobre la perfusión y oxigenación intestinal, mejorando los parámetros si se asocia a dobutamina4,5. De esta forma se considera a la noradrenalina como un fármaco vasoconstrictor seguro en los pacientes sépticos debidamente replecionados de volumen.
La adrenalina no se debe utilizar a no ser que fracasen otros agentes vasoconstrictores5. La dopamina es el precursor natural de la noradrenalina, tiene múltiples efectos clínicos dosis-dependientes, según los receptores sobre los que actúe. Se ha descrito alteración de la circulación esplácnica. También tiene efectos sobre la prolactina y las hormonas tiroideas, que pueden tener repercusión sobre la respuesta sistémica a la agresión4. Por estas razones, y sobre todo porque la noradrenalina posee mayor efecto terapéutico3-5, la primera elección de vasoconstrictor en la sepsis debe ser la noradrenalina.
En los últimos años ha tomado relevancia la utilización de vasopresina como vasopresor. Es un fármaco utilizado ampliamente en otras indicaciones, como la diabetes insípida y las varices esofágicas, siendo etiquetado de fármaco seguro. No tiene efectos metabólicos directos, pero por la relación con el eje hipotalámico-hipofisario-adrenal, es secretagogo de hormona adrenocorticotrópica (ACTH) y aumenta finalmente los niveles de cortisol.
Los estudios sobre la efectividad de la vasopresina en el shock séptico son escasos y se limitan a estudios observacionales, en los que se emplea la vasopresina como tratamiento de rescate en pacientes catecolamin-dependientes, consiguiendo mejoría de la presión arterial e incremento de la diuresis. Las cifras de mortalidad en estos pacientes oscilan entre el 44% y el 85%, difícil de comparar pues se trata de estadios de shock muy tardíos. Sólo existen tres estudios aleatorios y controlados con un total de 44 casos. Dos de ellos compararon la vasopresina con la noradrenalina y en el tercero se sustituyó la noradrenalina por vasopresina a dosis altas, sin encontrar beneficio en la mortalidad25. También se han publicado series de casos de pacientes en shock séptico en estadios avanzados tratados con derivados sintéticos de la vasopresina, como la terlipresina o la desmopresina con resultados prometedores. Por otra parte, se han descrito con el tratamiento conjunto de noradrenalina y vasopresina frecuentes lesiones isquémicas de la piel, principalmente en los dedos, el tronco y en la mucosa de la lengua.
Hasta que no se realice un estudio bien diseñado y con adecuada muestra de pacientes, no sabremos cuál es el lugar de la vasopresina en el tratamiento del shock séptico. Mientras tanto, dado su papel en la fisiopatología del shock séptico y los indicios favorables actualmente disponibles como tratamiento, se podría utilizar en pacientes dependientes de altas dosis de noradrenalina como medida de rescate y en perfusión continua a dosis de 0,01-0,04 unidades/ min, para evitar efectos secundarios.
Inotropos
La función cardíaca suele estar afectada en la sepsis grave, pero el gasto cardíaco se mantiene en valores normales o altos por mecanismos de compensación como la dilatación ventricular y la disminución de la poscarga. Habitualmente, la reposición de líquidos es suficiente para normalizar el gasto cardíaco y el tratamiento con noradrenalina no lo modifica sustancialmente. Sin embargo, en el caso de encontrar valores bajos de gasto cardíaco (< 2,5 l/min) se recomienda añadir al tratamiento fármacos inotropos.
La dobutamina, el fármaco inotrópico más utilizado, es una amina simpaticomimética que actúa, principalmente, aumentando la contractilidad cardiaca mediante la estimulación ß-adrenérgica. Periféricamente tiene efectos ß2 y α1, que son contrapuestos, resultando ligeramente vasodilatadora. Puede inducir taquicardia y arritmias. Numerosos estudios han demostrado la eficacia de la dobutamina en el shock séptico al conseguir aumentar el gasto cardíaco5. También se ha descrito su efecto beneficioso a nivel del lecho esplácnico, sola o en combinación con la noradrenalina. La dosis de administración varía entre 2 y 28 µg kg-1min-1.
Corticoides
Los corticoides tienen un importante papel en la contractilidad cardíaca y en la regulación del tono vascular normal, ya que intervienen en la síntesis de catecolaminas endógenas, en la síntesis y función de los receptores adrenérgicos y en el bloqueo de los receptores de la óxido nítrico sintetasa. Los síntomas de su déficit, la insuficiencia suprarrenal, son inespecíficos, particularmente en pacientes graves y así, el cuadro hemodinámico de la insuficiencia suprarrenal puede ser superponible al shock séptico. Los pacientes sépticos con insuficiencia suprarrenal no responden adecuadamente a la administración de líquidos y son dependientes de vasopresores. En nuestra UCI se realizó un estudio en el que se revisaron 34 autopsias de fallecidos por shock séptico encontrándose alteraciones de las glándulas suprarrenales en 22 pacientes (67%), siendo la necrosis suprarrenal la lesión más frecuente. Annane et al han señalado una importante incidencia de disfunción suprarrenal (76%) en su estudio sobre 300 pacientes en shock séptico. Por esta razón, es preciso asegurar una función suprarrenal adecuada capaz de satisfacer las necesidades de cortisol y, de lo contrario, iniciar un tratamiento sustitutivo26.
El shock séptico es un estado de hipoperfusión grave de etiología infecciosa que se define por la presencia de hipotensión arterial. El patrón hemodinámico es normalmente hiperdinámico, aunque en su evolución puede presentarse como hipodinámico.
Para guiar el tratamiento se establecen unos objetivos de perfusión global hemodinámicos y metabólicos de los que se consideran especialmente útiles la presión arterial, el gasto cardíaco, el ácido láctico y la diuresis. Actualmente, no disponemos del método idóneo de monitorización de la disoxia regional con validez clínica práctica. La monitorización de las presiones de llenado, la PVC y la PAPo, nos facilita la consecución de los objetivos, proporcionando unos valores de presión límites de seguridad para evitar el edema pulmonar. Otros parámetros como los volúmenes, junto con las presiones de llenado, nos informan verazmente del estado de precarga.
Se han descrito la utilidad de las variaciones de determinados parámetros (volumen ventricular, presión de pulso y volumen sistólico), en relación con el ciclo respiratorio, con el objeto de identificar a los "no respondedores" a la administración de volumen e iniciar en ellos los vasoactivos precozmente.
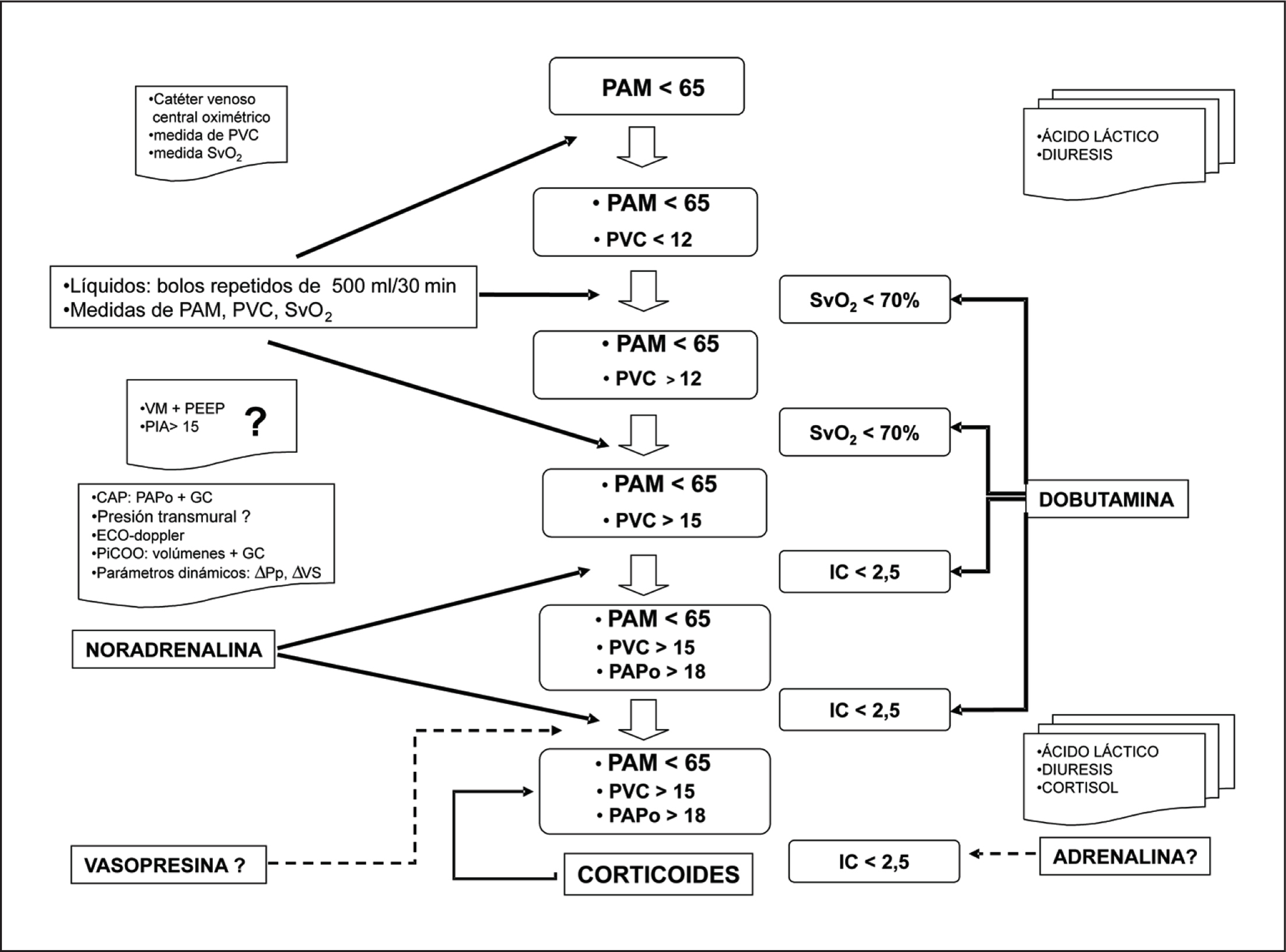
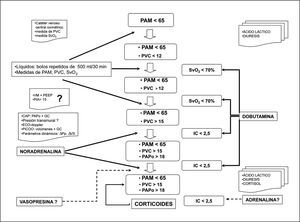
El tratamiento hemodinámico se inicia con aporte de líquidos de forma intensa y precoz hasta conseguir una PAM que "garantice" la perfusión tisular. Posteriormente, si no se obtiene este objetivo, se inician los vasopresores, preferentemente la noradrenalina. Es conveniente la monitorización continua del gasto cardíaco con cualquiera de las técnicas disponibles a fin de detectar precozmente su descenso e iniciar el tratamiento con dobutamina (fig. 3).
Figura 3. Criterios de shock séptico. PVC: presión venosa central; SvO2: saturación venosa de oxígeno; PAM: presión arterial media; PEEP: presión positiva al final de la espiración; PIA: presión intraabdominal; PAPo: presiones de enclavamiento en la arteria pulmonar; GC: gasto cardíaco; ECO: ecocardiografía; PiCOO: termodilución transpulmonar simple; VS: volumen sistólico; IC: índice cardíaco; VM: ventilación mecánica; CAP: catéter de arteria pulmonar.
La insuficiencia suprarrenal es muy frecuente en estos pacientes y su implicación en la función cardiovascular obliga a diagnosticarla y tratarla.