El síndrome de Takotsubo es un tipo de miocardiopatía caracterizada por disfunción ventricular izquierda transitoria, asociada a cambios electrocardiográficos similares a los del infarto agudo de miocardio, sin evidencia de enfermedad coronaria y con escasa movilización de enzimas miocárdicas. Es también conocido como disfunción apical transitoria, «apical ballooning» o miocardiopatía inducida por el estrés, ya que afecta generalmente a mujeres posmenopáusicas después de un evento estresante. Los criterios establecidos para su diagnóstico son: anormalidades electrocardiográficas agudas como elevación del segmento ST o inversión de ondas T, ausencia de enfermedad coronaria obstructiva, aquinesia o disquinesia transitoria del ventrículo izquierdo y ausencia de traumatismo craneoencefálico, hemorragia intracraneal, feocromocitoma, miocarditis o miocardiopatía hipertrófica1. La incidencia y prevalencia de este síndrome se desconocen, y son pocos los casos descritos en pacientes sometidos a cirugía cardiovascular. Presentamos el caso de una paciente intervenida de un mixoma auricular, que en el postoperatorio sufre shock cardiogénico secundario a un síndrome de Takotsubo.
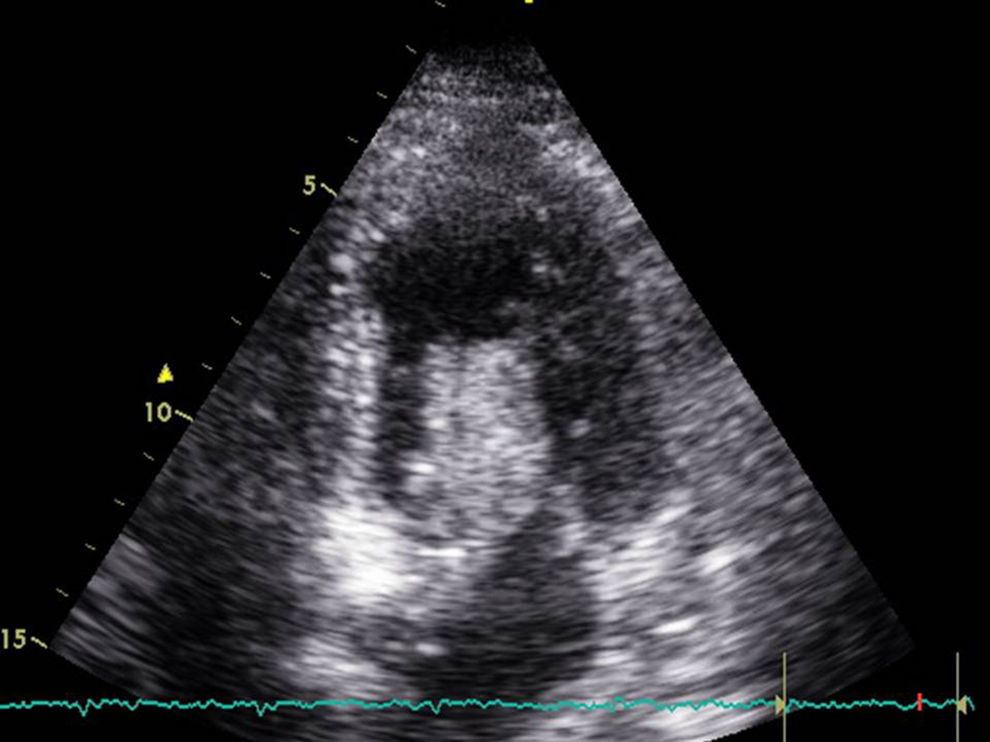
Se trata de una mujer de 68 años, con antecedentes personales de hipertensión arterial y diabetes no insulinodependiente, que acude a urgencias por clínica de insuficiencia cardiaca de 2 semanas de evolución. A su llegada presentaba disnea de reposo y sensación de palpitaciones, detectándose fibrilación auricular rápida que requirió cardioversión farmacológica. Se realizó una ecocardiografía (fig. 1) en la que se observaba una gran masa auricular izquierda (1,8×7cm), que protruía hacia VI ocasionando estenosis mitral secundaria, dilatación auricular y una fracción de eyección de ventrículo izquierdo (FEVI) conservada. La coronariografía preoperatoria no mostró lesiones.
La paciente fue intervenida quirúrgicamente 4 días más tarde, realizándose exéresis del mixoma por vía transeptal, sin incidencias destacables salvo una tendencia a la hipoxemia. Tiempos de clampaje y circulación extracorpórea de 52 y 83min, respectivamente. Se realizó ecocardiografía intraoperatoria que mostró ausencia de restos del mixoma y una FEVI normal. La paciente permaneció estable, conectada a ventilación mecánica durante las primeras horas de estancia en la UCI debido a la hipoxemia, con una FiO2=0,6 y PEEP=10-12cmH2O. A las 8h de la cirugía, se produjo de forma súbita una crisis hipertensiva (TA sistólica >220mmHg) seguida de hipotensión y parada cardiaca en disociación electromecánica, recuperando pulso con medidas de reanimación en pocos minutos. La paciente se encontraba en shock cardiogénico, refractario a dosis altas de fármacos vasoactivos (adrenalina, dobutamina, noradrenalina), por lo que finalmente se decide soporte con membrana de oxigenación extracorpórea veno-arterial (ECMO V-A).
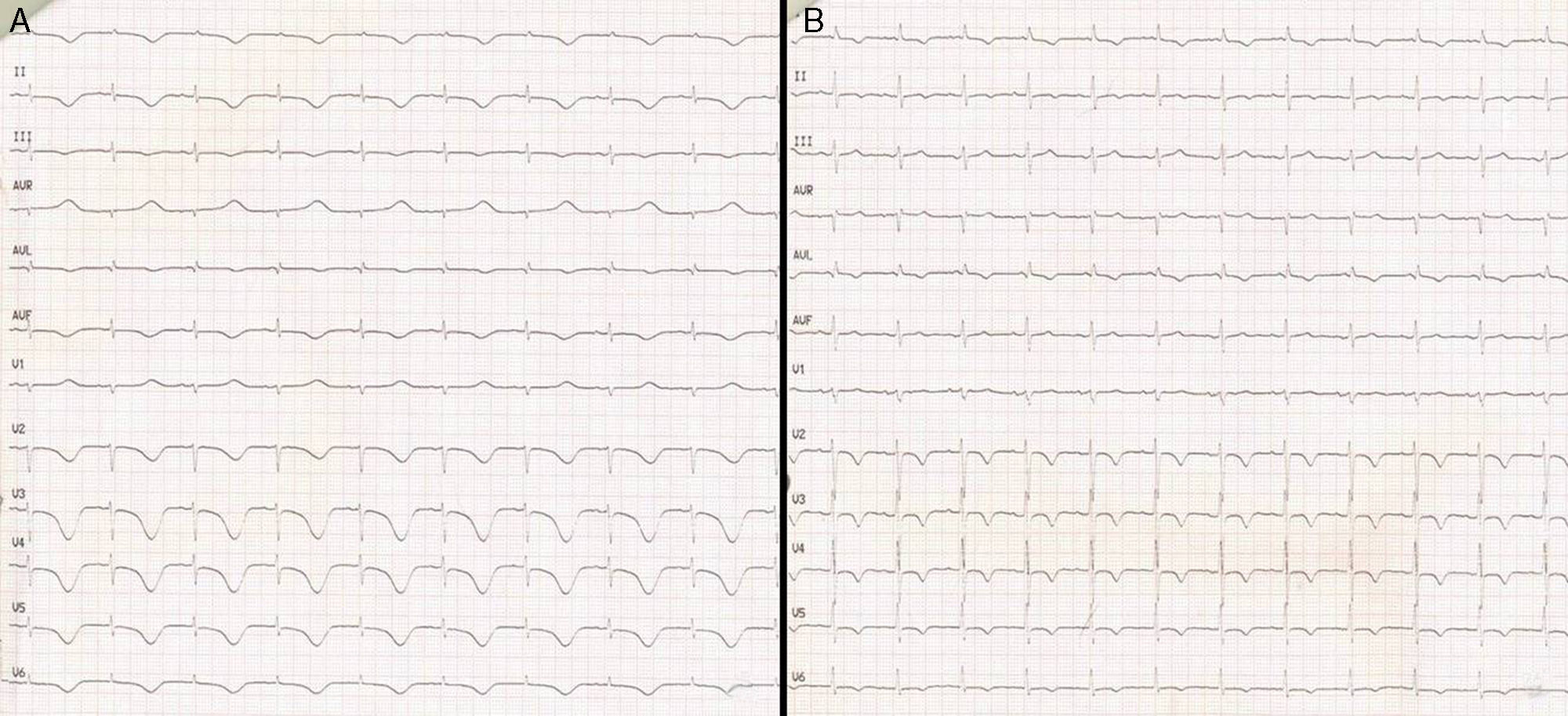
Se realizó ecocardiografía transtorácica que mostraba disfunción ventricular izquierda severa (FEVI<20%), hiperdinamia de los segmentos basales y aquinesia de los segmentos medios y apicales, hallazgos típicos del síndrome de Takotsubo. Las enzimas cardiacas no se elevaron de forma significativa en los días posteriores, teniendo en cuenta la cirugía, con cifra máxima de troponina I ultrasensible de 4.000pg/ml (normal entre 2-15,6pg/ml). En el ECG sí aparecieron cambios significativos respecto a los registros previos, con un QTc largo (680ms) y desarrollo de ondas T invertidas en precordiales durante varios días (fig. 2). Los electrolitos y el resto de parámetros analíticos estaban en rango normal.
La terapia con ECMO V-A se mantuvo durante 4 días, permitiendo la retirada del apoyo vasoactivo y una evolución clínica posterior favorable. Los estudios ecocardiográficos mostraron progresiva mejoría de la función ventricular. La paciente pudo ser extubada al cabo de pocos días y trasladada a planta, donde permaneció hasta ser dada de alta en buena situación funcional. En la última ecocardiografía realizada se observaba ligera hipoquinesia en septo anterior y territorio inferior, con función sistólica global conservada.
En este caso, el diagnóstico de síndrome de Takotsubo se estableció en función de las características de la ecocardiografía, la ausencia de lesiones coronarias previas, el escaso movimiento de enzimas cardiacas, a pesar de la disfunción ventricular y la cirugía, y los cambios electrocardiográficos en derivaciones precordiales (ondas T invertidas y un síndrome de QT largo, con electrolitos normales). En los últimos años se ha observado un incremento en el diagnóstico de esta enfermedad2, también en pacientes sometidos a cirugía cardiovascular3–5, aunque ninguno reportado en el postoperatorio de resección de un mixoma auricular.
La etiología y fisiopatología no han sido bien determinadas, pero se han propuesto varios mecanismos, como el vasoespasmo coronario, las anormalidades en la función microvascular coronaria y el más importante, la cardiotoxicidad mediada por catecolaminas. Probablemente por esto, el principal factor de riesgo es el estrés, tanto físico como psíquico, presente en diversas pruebas diagnósticas e intervenciones quirúrgicas, especialmente emergentes o urgentes6. La cirugía cardiaca y la circulación extracorpórea, elementos que generan importante estrés, pueden justificar por sí mismas la aparición de este síndrome, especialmente si el perfil epidemiológico del paciente y los datos ecocardiográficos y electrocardiográficos se ajustan a los criterios diagnósticos, como ocurre en nuestro caso. En el diagnóstico diferencial debemos considerar el embolismo coronario o una mala protección miocárdica. Los hallazgos ecocardiográficos típicos, con escasa movilización enzimática, una cirugía corta y sin incidencias, y un periodo de estabilidad hemodinámica previa con un primer ECG normal descartan razonablemente ambos problemas perioperatorios. En los últimos años, hay evidencia de que la resonancia magnética puede ser útil en el diagnóstico diferencial con otras entidades como la miocarditis o el embolismo coronario7, aunque no pudo realizarse en el caso descrito.
Hay que destacar la aparición del QT largo en el ECG. La asociación entre miocardiopatía de Takotsubo y prolongación transitoria del intervalo QT, ha sido bien documentada8,9, observándose una mayor frecuencia en pacientes con algún tipo de cardiopatía, síndrome de QT largo previo o alteraciones genéticas. En el síndrome de Takotsubo, la normalización electrocardiográfica ocurre aproximadamente tras 2 meses del episodio. Aunque las arritmias ventriculares malignas, muerte súbita y bloqueo cardiaco son infrecuentes también se han reportado casos, identificándose la mayor prolongación del intervalo QT como factor de riesgo para el desarrollo de estas complicaciones (QTc>500ms), por lo que es necesaria la estrecha monitorización del ritmo cardiaco, la prevención o tratamiento de las arritmias y la implantación de marcapasos si fuera necesario.
En conclusión, el síndrome de Takotsubo es una causa infrecuente de shock cardiogénico en el postoperatorio de cirugía cardiaca, pero que hay que considerarlo en pacientes con cirugía aparentemente no complicada, coronarias normales y ecocardiografía compatible, porque conlleva en general buen pronóstico con el tratamiento de soporte adecuado.
FinanciaciónEste trabajo no ha recibido ningún tipo de financiación.