La limitación de tratamientos de soporte vital (LTSV) es una práctica recomendada en determinadas circunstancias. Las formas de limitación son variadas y su aplicación es diferente entre unos centros y otros. Conocer la situación actual de la LTSV en pacientes que presentan un ingreso prolongado en UCI y que sufren un empeoramiento es el objetivo de este trabajo.
DiseñoCohorte, observacional, prospectivo.
ÁmbitoUn total de 75 UCI españolas.
PacientesSe estudia a 589 pacientes que presentan 777 complicaciones o eventos adversos con repercusión orgánica a partir del séptimo día de ingreso, reclutados durante 3 meses.
Variables de interés principalesEstudiamos el momento en que se propone la limitación, el actor que la propone, el grado de acuerdo dentro del equipo, la influencia de este hecho en la relación médico-paciente-familia y sus formas de aplicación.
ResultadosSe plantea alguna limitación al tratamiento en el 34,3% de los pacientes con estancia prolongada en UCI que sufren complicaciones graves. La incidencia es mayor en pacientes con neumopatía moderada o grave, enfermedad oncológica, tratamientos inmunosupresores y en pacientes dependientes. En el 97% de los casos en los que se propone realizar la LTSV, finalmente se acuerda la misma. La decisión dentro del equipo médico fue unánime en el 87,9% de casos. Habitualmente la relación médico-paciente-familia no cambia o incluso mejora ante esta situación.
ConclusiónLa LTSV en las UCI es una práctica que se suele llevar a cabo con la decisión unánime del equipo médico, se realiza con más frecuencia en pacientes con comorbilidad grave y no suele deteriorar la relación con pacientes y familiares.
Limitation of life-sustaining treatment (LLST) is a recommended practice in certain circumstances. Limitation practices are varied, and their application differs from one center to another. The present study evaluates the current situation of LLST practices in patients with prolonged admission to the ICU who suffer worsening of their condition.
DesignA prospective, observational cohort study was carried out.
SettingSeventy-five Spanish ICUs.
PatientsA total of 589 patients suffering 777 complications or adverse events with organ function impairment after day 7 of admission, during a three-month recruitment period.
Main variables of interestThe timing of limitation, the subject proposing LLST, the degree of agreement within the team, the influence of LLST upon the doctor-patient-family relationship, and the way in which LLST is implemented.
ResultsLLST was proposed in 34.3% of the patients presenting prolonged admission to the ICU with severe complications. The incidence was higher in patients with moderate to severe lung disease, cancer, immunosuppressive treatment or dependence for basic activities of daily living. LLST was finally implemented in 97% of the cases in which it was proposed. The decision within the medical team was unanimous in 87.9% of the cases. The doctor-patient-family relationship usually does not change or even improves in this situation.
ConclusionLLST in ICUs is usually carried out under unanimous decision of the medical team, is performed more frequently in patients with severe comorbidity, and usually does not have a negative impact upon the relationship with the patients and their families.
Las unidades de cuidados intensivos (UCI) y las medidas de soporte vital con sustitución de funciones orgánicas han supuesto un aumento en la supervivencia de gran número de enfermedades, pero también han dado lugar a una prolongación inútil del proceso de morir con una carga emocional y económica difícil de calcular1,2. En 1983, Bedell et al.3 describieron que, aunque el 44% de los pacientes hospitalizados responden inicialmente a la reanimación cardiopulmonar (RCP), solo el 14% sobrevive en el momento del alta hospitalaria, con un porcentaje mucho menor en pacientes con determinadas enfermedades como neumonía o fracaso renal. Los mismos autores no encontraron ningún paciente hospitalizado con cáncer metastásico, accidente cerebrovascular agudo, sepsis o neumonía que sobreviviera tras el ingreso hospitalario por una parada cardiorrespiratoria4. Esto llevó a Symmers5 a preguntarse si la nueva tecnología conseguía realmente mantener la vida o simplemente interfería con el proceso de morir, y a Blackhall6 a proponer que los médicos la aplicaran de manera selectiva, como se sigue recomendando7. Hace 35 años la mayoría de los pacientes que fallecían en las UCI eran tratados con RCP8; conocida la escasa utilidad del empleo indiscriminado de estas medidas, su empleo masivo ha dejado paso a la limitación del esfuerzo terapéutico o limitación de tratamientos de soporte vital (LTSV)9.
En un documento conjunto entre intensivistas y paliativistas10 se pone de manifiesto que el punto de partida de estas discusiones está en el reconocimiento de que en el paciente incurable o en fase final no debe prolongarse la vida de forma innecesaria. Para ello podemos apoyarnos en escalas de gravedad o predictores de mortalidad11. No obstante, ¿es posible predecir el futuro con una seguridad tal como para no correr el riesgo de privar a una persona de una potencial curación?
El Código de Deontología Médica del Consejo General de Colegios Oficiales de Médicos de España12 en su artículo 12 reconoce el derecho del paciente a rechazar un tratamiento y dispensa al médico de aplicar un tratamiento que considere inadecuado o inaceptable y, en el artículo 36, obliga al médico a aplicar las medidas adecuadas para conseguir el bienestar del enfermo cuando la curación o mejoría de este ya no sea posible. La Sociedad Española de Medicina Intensiva, Crítica y Unidades Coronarias (SEMICYUC) publicó en 2002 unas recomendaciones sobre la LTSV13 que pretenden dar orientaciones para fomentar la discusión bioética. La LTSV se aplica de muy diversas formas y ha evolucionado a lo largo de los últimos años. Para conocer la situación actual sobre esta cuestión se analiza la parte de los resultados del estudio multicéntrico «Evolución y pronóstico de los pacientes con ingreso prolongado en UCI que sufren un empeoramiento» (EPIPUSE) relacionada con el objetivo de «conocer la frecuencia con la que se plantea la LTSV en pacientes con estancias prolongadas en UCI, el actor que las propone, el consenso que se alcanza antes de ejecutarlas y la proporción de ellas que son finalmente llevadas a la práctica».
Pacientes y métodosEl estudio EPIPUSE es un estudio de cohortes observacional, prospectivo y multicéntrico de pacientes con estancia prolongada en UCI. En una fase inicial se contactó con los jefes de servicio de 152 UCI españolas. Fueron 75 UCI las que se incorporaron de forma efectiva a la fase de reclutamiento. La relación de los investigadores de cada centro aparece en el anexo A. El proyecto fue aprobado por el Comité Ético de Investigación Clínica del Hospital Universitario Fundación Alcorcón (Alcorcón, Madrid) y posteriormente remitido a los centros participantes. Asimismo, se solicitó el aval científico de la SEMICYUC, que fue concedido.
El periodo de reclutamiento de pacientes duró 3 meses y posteriormente hubo un periodo de seguimiento de 4 meses más. El criterio para incluir a un paciente fue: pacientes mayores de 18 años con estancia en la UCI durante 7 días o más y que presentaran una complicación o evento adverso con repercusión orgánica (aumento del SOFA en un punto o más).
Consideramos complicación o evento adverso con repercusión orgánica a un evento clínico que deteriore alguna función orgánica y repercuta en el SOFA, de causa conocida o no, debida o no a un problema de seguridad. Queda excluido el empeoramiento progresivo de una entidad clínica previamente diagnosticada.
La LTSV se lleva a cabo según los protocolos de las unidades participantes, sin que este proceso esté influido por el presente estudio. Sobre LTSV consideramos 3 momentos: 1) cuando se plantea la posibilidad de realizar LTSV; 2) cuando se decide formalmente realizar algún tipo de LTSV tras la deliberación del equipo médico y se registra esta decisión en la historia clínica y 3) cuando se lleva a cabo la LTSV.
Elaboramos una base de datos en la que se recoge información demográfica de los pacientes, así como antecedentes personales que pueden influir en la evolución y en la posibilidad de recuperación y aparición de complicaciones. Valoramos la evolución a través de los datos de supervivencia y tiempo de estancia tanto en la UCI como en el hospital. Las causas de las complicaciones se recogen de forma descriptiva y tabulada. Registramos si se dispone de documentos de instrucciones previas y la validez de estas instrucciones en los casos concretos. Respecto a la LTSV registramos los momentos definidos previamente, el actor que propone la limitación (paciente, familiares, profesionales), el grado de acuerdo dentro del equipo médico (expresado como porcentaje de médicos de acuerdo en llevar a cabo la LTSV sobre el total de médicos presentes en la sesión), el impacto que este hecho tiene en la relación médico-paciente-familiares mediante un campo tabulado y finalmente los tratamientos aplicados o retirados. Al finalizar el periodo de seguimiento de los pacientes, los investigadores de los diferentes centros enviaron sus bases de datos anónimas y encriptadas al promotor del estudio para su integración centralizada. Las variables cuantitativas se describen con medidas de centralización y de dispersión (media y desviación estándar, mediana y rango intercuartílico, Q1-Q3). Las variables cualitativas se describen mediante frecuencias absolutas (N) y relativas (%).
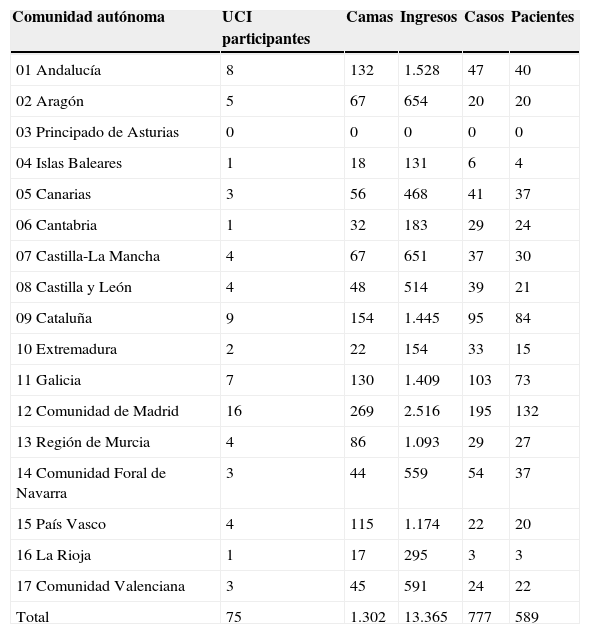
Durante los 3 meses que duró el periodo de reclutamiento ingresaron 13.456 pacientes en las 75 UCI participantes en el estudio, que suponen un total de 1.302 camas. De ellos, 2.594 pacientes presentaron una estancia de 7 días o más. Durante ese tiempo se registraron 777 complicaciones o eventos adversos con repercusión orgánica a partir del 7.° día de ingreso en 589 pacientes. La distribución por comunidades autónomas aparece en la tabla 1.
Distribución de UCI, casos y pacientes por comunidades autónomas
| Comunidad autónoma | UCI participantes | Camas | Ingresos | Casos | Pacientes |
|---|---|---|---|---|---|
| 01 Andalucía | 8 | 132 | 1.528 | 47 | 40 |
| 02 Aragón | 5 | 67 | 654 | 20 | 20 |
| 03 Principado de Asturias | 0 | 0 | 0 | 0 | 0 |
| 04 Islas Baleares | 1 | 18 | 131 | 6 | 4 |
| 05 Canarias | 3 | 56 | 468 | 41 | 37 |
| 06 Cantabria | 1 | 32 | 183 | 29 | 24 |
| 07 Castilla-La Mancha | 4 | 67 | 651 | 37 | 30 |
| 08 Castilla y León | 4 | 48 | 514 | 39 | 21 |
| 09 Cataluña | 9 | 154 | 1.445 | 95 | 84 |
| 10 Extremadura | 2 | 22 | 154 | 33 | 15 |
| 11 Galicia | 7 | 130 | 1.409 | 103 | 73 |
| 12 Comunidad de Madrid | 16 | 269 | 2.516 | 195 | 132 |
| 13 Región de Murcia | 4 | 86 | 1.093 | 29 | 27 |
| 14 Comunidad Foral de Navarra | 3 | 44 | 559 | 54 | 37 |
| 15 País Vasco | 4 | 115 | 1.174 | 22 | 20 |
| 16 La Rioja | 1 | 17 | 295 | 3 | 3 |
| 17 Comunidad Valenciana | 3 | 45 | 591 | 24 | 22 |
| Total | 75 | 1.302 | 13.365 | 777 | 589 |
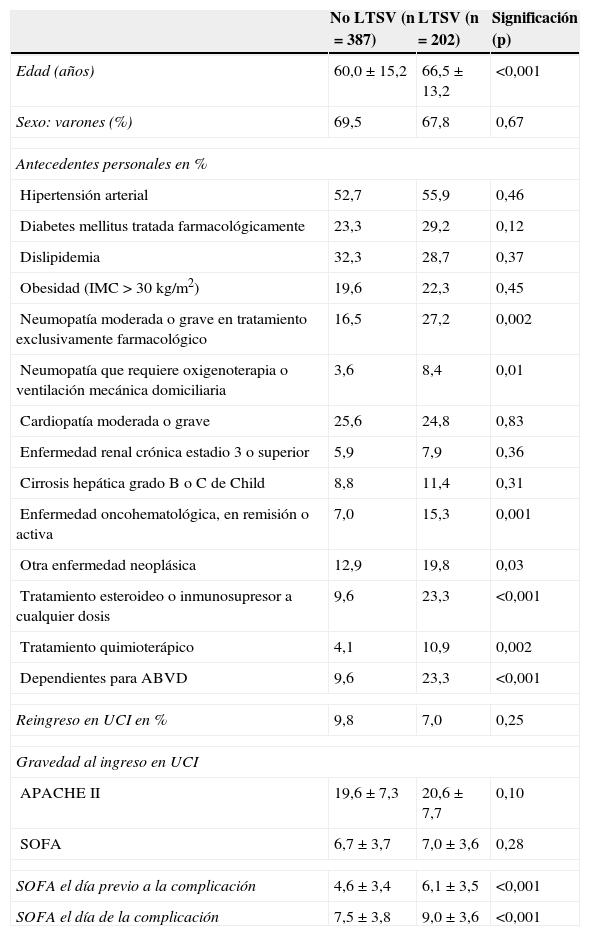
La edad de los pacientes incluidos en el estudio EPIPUSE presenta un rango de 18 a 94 años. Se propuso LTSV en 202 de los 589 pacientes incluidos en el estudio (34,3%). En la tabla 2 aparecen las características basales y los datos relativos al ingreso de los casos incluidos en función de si se planteó algún tipo de LTSV o no.
Características basales y evolución durante el ingreso
| No LTSV (n=387) | LTSV (n=202) | Significación (p) | |
|---|---|---|---|
| Edad (años) | 60,0±15,2 | 66,5±13,2 | <0,001 |
| Sexo: varones (%) | 69,5 | 67,8 | 0,67 |
| Antecedentes personales en % | |||
| Hipertensión arterial | 52,7 | 55,9 | 0,46 |
| Diabetes mellitus tratada farmacológicamente | 23,3 | 29,2 | 0,12 |
| Dislipidemia | 32,3 | 28,7 | 0,37 |
| Obesidad (IMC>30 kg/m2) | 19,6 | 22,3 | 0,45 |
| Neumopatía moderada o grave en tratamiento exclusivamente farmacológico | 16,5 | 27,2 | 0,002 |
| Neumopatía que requiere oxigenoterapia o ventilación mecánica domiciliaria | 3,6 | 8,4 | 0,01 |
| Cardiopatía moderada o grave | 25,6 | 24,8 | 0,83 |
| Enfermedad renal crónica estadio 3 o superior | 5,9 | 7,9 | 0,36 |
| Cirrosis hepática grado B o C de Child | 8,8 | 11,4 | 0,31 |
| Enfermedad oncohematológica, en remisión o activa | 7,0 | 15,3 | 0,001 |
| Otra enfermedad neoplásica | 12,9 | 19,8 | 0,03 |
| Tratamiento esteroideo o inmunosupresor a cualquier dosis | 9,6 | 23,3 | <0,001 |
| Tratamiento quimioterápico | 4,1 | 10,9 | 0,002 |
| Dependientes para ABVD | 9,6 | 23,3 | <0,001 |
| Reingreso en UCI en % | 9,8 | 7,0 | 0,25 |
| Gravedad al ingreso en UCI | |||
| APACHE II | 19,6±7,3 | 20,6±7,7 | 0,10 |
| SOFA | 6,7±3,7 | 7,0±3,6 | 0,28 |
| SOFA el día previo a la complicación | 4,6±3,4 | 6,1±3,5 | <0,001 |
| SOFA el día de la complicación | 7,5±3,8 | 9,0±3,6 | <0,001 |
Los motivos de ingreso en UCI de los pacientes son muy variados: el 14,4% ingresaron por neumonía, el 13,9% por sepsis de otra localización; por insuficiencia respiratoria de otro origen ingresaron el 12,9%; el 7,9% fueron casos cardiológicos además de un 5,9% de paradas cardiorrespiratorias recuperadas; 9,9% fueron por motivos neurológicos. El 35,1% restante fueron enfermedades con menor representación: postoperatorios, traumas, digestivos, etc.
Respecto a la complicación o evento adverso que motivó su inclusión en el estudio destacan un 19,3% de neumonías, otras infecciones en un 17,8%, 14,9% lo fueron por insuficiencia respiratoria de otro origen y un 8,9% por complicaciones neurológicas.
La mortalidad en UCI fue del 21,6% en los casos en los que no se planteó LTSV y del 82,7% en los que se planteó este curso de acción (p<0,001). Asimismo, la mortalidad hospitalaria para ambas situaciones fue del 28,7 y 93%, respectivamente (p<0,001).
También encontramos diferencias en la estancia en UCI y la estancia hospitalaria: en UCI fue de 35,6±29,6 días en los pacientes en los que no se planteó LTSV y de 27,3±22,1 en los que sí se planteó (p<0,001); la estancia hospitalaria fue, respectivamente, de 58,8±38,7 y 38,3±31,1 días (p<0,001).
Al finalizar el periodo de seguimiento, 9 pacientes permanecían aún ingresados en UCI y otros 14 más en planta de hospitalización. Respecto a la existencia de instrucciones previas entre los pacientes incluidos, ninguno de ellos había redactado este documento. Un total de 16 pacientes (un 2,7%) ingresaron en la UCI con la decisión previa de no aplicar algún tipo de tratamiento (ej., no intubar).
Comparando las características de los pacientes en los que se planteó LTSV con las de aquellos en los que no se planteó, no observamos diferencias estadísticamente significativas en los datos demográficos, salvo en la edad.
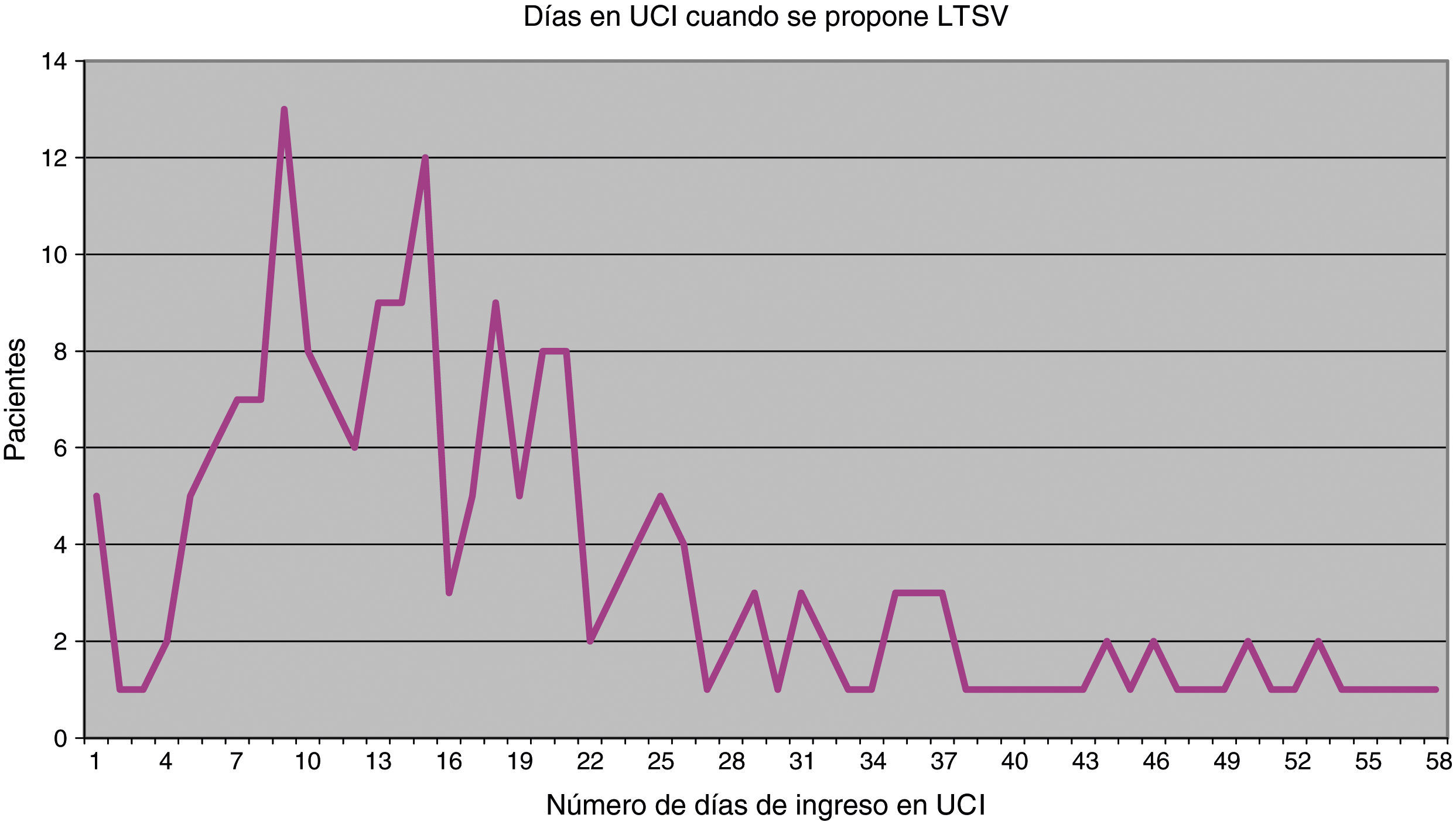
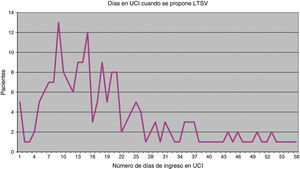
De las 202 ocasiones en las que se planteó limitar algún tipo de tratamiento, se decidió hacerlo en 196 (97%) y finalmente se llevó a la práctica en 183 (90,6%). El momento en que se realiza por primera vez el planteamiento de LTSV es muy variable (fig. 1). Como media este se produce en el 23.° día de ingreso en UCI, pero la desviación estándar es amplia, de 20 días. La mediana se sitúa en el 13.° día y el rango intercuartílico es 11-27. El tiempo que transcurre desde que se propone LTSV hasta que se acuerda esta decisión también es variable, si bien en 118 casos (60,2%) la decisión se tomó el mismo día en que fue propuesto, en 34 casos (17,3%) la decisión se tomó al día siguiente y en otros 33 casos (16,8%) la decisión se tomó a lo largo de la semana siguiente. En 11 casos la decisión fue adoptada más tarde. En cuanto al tiempo desde que se decide realizar la LTSV hasta que finalmente es llevada a la práctica, lo más habitual es que todo ello ocurra en el mismo día (150 casos, 82%), mientras que en 17 casos (9,3%) se realizó al día siguiente, en 13 (7,1%) se realizó a lo largo de esa semana y hubo 3 casos en que se realizó con posterioridad.
Los tratamientos limitados o actitudes tomadas en 195 de los 196 casos del estudio aparecen en la tabla 3.
Tratamientos de soporte limitados y otras actuaciones
| • No RCP si parada cardiorrespiratoria: 172 casos de 195 registros (88,2%) |
| • No iniciar ventilación mecánica: 67 casos |
| • Retirar ventilación mecánica: 20 casos |
| • No proceder a intubación traqueal: 46 casos |
| • No transfundir hemoderivados: 129 casos |
| • No iniciar diálisis: 139 casos |
| • No iniciar tratamiento con fármacos vasoactivos: 121 casos |
| • Retirada de tratamientos farmacológicos: |
| 1. En 6 casos se retiraron todos los tratamientos |
| 2. En 99 casos se retiraron todos los tratamientos salvo aquellos destinados a sedación, alivio sintomático o que buscaran la comodidad del paciente |
| 3. En 22 ocasiones se redujeron parámetros de ventilación mecánica |
| 4. En 25 casos se redujo o suspendió el tratamiento con fármacos vasoactivos |
| • Extubación terminal: 21 casos |
| • Sedación terminal o paliativa: 126 casos |
De los 183 casos en los que finalmente se llevó a cabo algún tipo de LTSV la mortalidad fue del 97,8%. La relación temporal entre el momento de LTSV y el fallecimiento es la siguiente: 94 pacientes (51,4%) fallecieron en el mismo día de la LTSV, 42 más (23%) lo hicieron al día siguiente y 30 (16,4%) fallecieron en el curso de la misma semana. Los 13 pacientes fallecidos restantes lo fueron en el curso del mes, salvo uno que falleció a los 51 días.
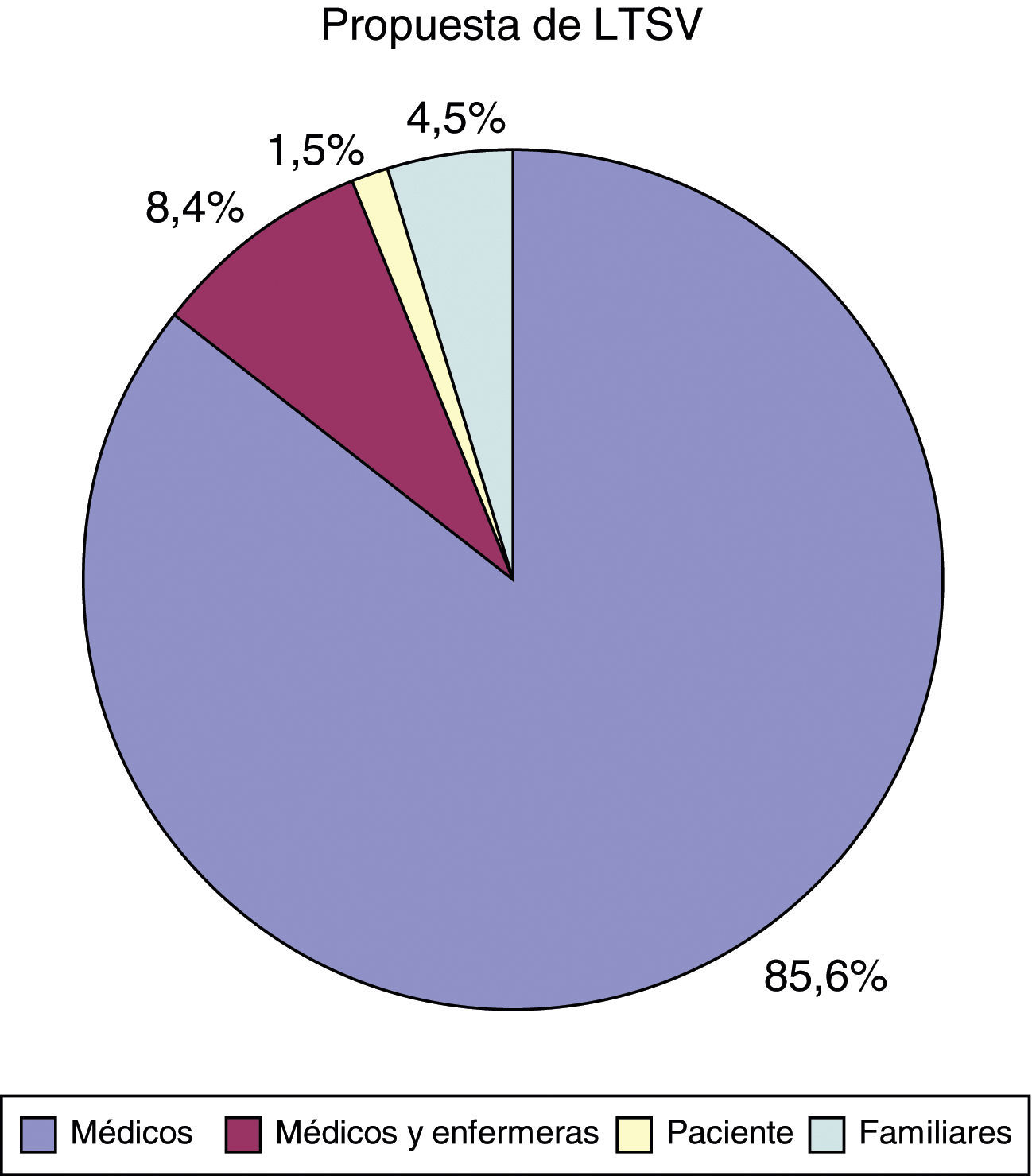
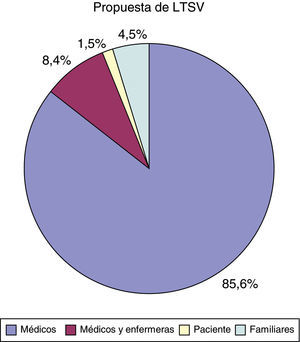
La propuesta de LTSV surge del personal sanitario que atiende al paciente en 190 casos (fig. 2). Sobre la participación del paciente en la decisión: en 3 casos fue el propio paciente el que la propuso; en 172 casos (85,1%) el paciente no pudo participar por encontrarse en coma o por ser considerado incapaz; hubo 3 casos (1,5%) en los que el paciente no participó de la decisión pero fue informado de ella y en los otros 24 casos restantes (11,9%) se decidió ni consultar ni informar de la decisión de LTSV.
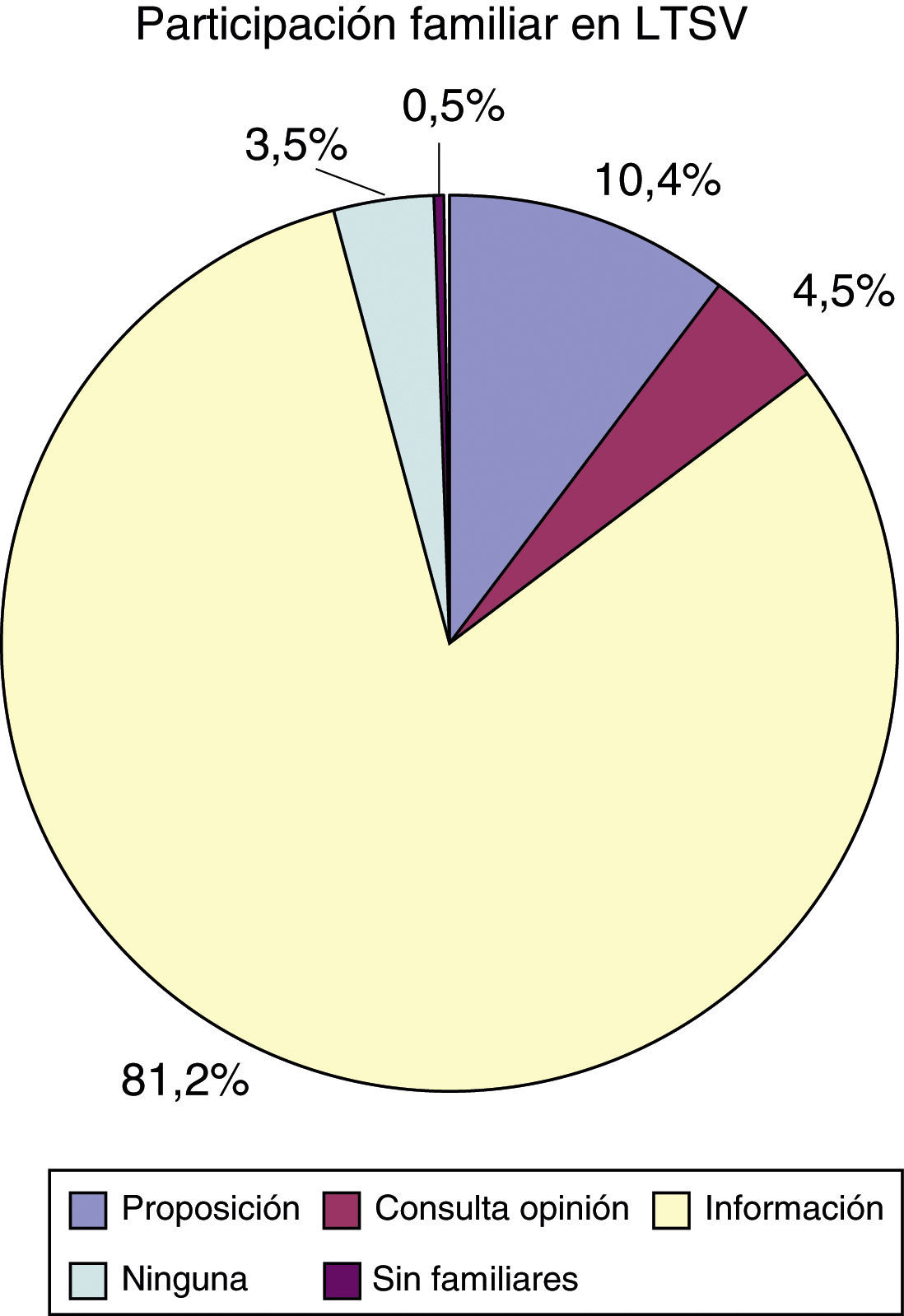
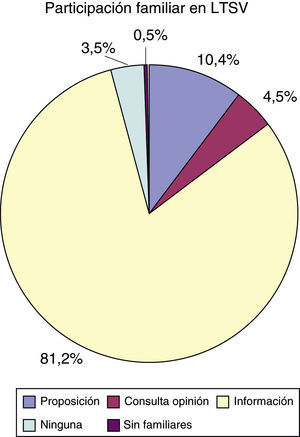
Respecto a la participación de los familiares en las decisiones de LTSV, 21 familias (10,4%) propusieron la limitación, y en 9 casos (4,5%) se pidió opinión a los familiares. En 164 ocasiones (81,2%) se les informó de la decisión una vez tomada y, finalmente, en 7 casos (3,5%) el equipo médico no informó a los familiares de la decisión de LTSV. En ninguna ocasión el paciente solicitó que los familiares no fueran informados (fig. 3).
En cuanto al grado de acuerdo dentro del equipo médico en el momento final de la decisión de LTSV, en 172 casos (87,8%) el acuerdo fue unánime, hubo 13 casos (6,6%) en los que la decisión fue respaldada por el 60-90% de los integrantes y en 3 casos (1,5%) la decisión solo contó con el acuerdo del 40-50% del equipo presente.
Finalmente, respondiendo a la pregunta «Consecuencias de la proposición/decisión de LTSV en la relación médico-paciente-familiares», los investigadores consideraron que mejora la relación con el paciente, los familiares o ambos en 73 casos, empeora la relación con los familiares en 12 casos y no se apreció ningún cambio significativo en la relación médico-paciente-familia en 110.
DiscusiónLas formas de LTSV en el entorno de la UCI pueden ser muy diversas. Se puede rechazar el ingreso del paciente en la UCI, o bien realizar el ingreso habiendo preestablecido ciertas limitaciones en las medidas de soporte vital a aplicar. Otra opción consiste en no iniciar o en retirar todas o algunas de estas medidas, como la RCP, ventilación mecánica, oxigenoterapia, tratamientos de depuración extrarrenal o soporte vasoactivo, etc. Sobre el paciente ya en la UCI, aunque no hay consenso, se han propuesto protocolos una vez que los médicos reconocen que el paciente probablemente fallecerá y el tratamiento intensivo no está justificado14,15. De hecho, hay importantes diferencias de actitud entre equipos e incluso entre miembros de un mismo equipo16–22. Sin duda, la formación en cuestiones éticas influye en la toma de decisiones23,24.
A lo largo de los últimos años se ha publicado un gran número de artículos describiendo los tipos y frecuencia de aplicación de LTSV en las UCI. Por su amplitud y cercanía describimos los resultados del registro inglés de los años 1995-200125: al 9,9% de los pacientes ingresados en las UCI se les retiró todo tratamiento activo, con una mortalidad del 99% pero con gran variabilidad entre las distintas unidades, lo que sugiere una aplicación de estas decisiones no uniforme. La mortalidad de los pacientes con LTSV en las UCI supuso aproximadamente un tercio de las muertes al alta hospitalaria. Después de aplicar diferentes modelos de ajuste aparecen, como factores asociados a la decisión de retirar todo tratamiento activo, la edad, enfermedades graves preexistentes, la cirugía de urgencia o el ingreso urgente en UCI, la realización de RCP en las 24 h anteriores al ingreso y la necesidad de ventilación o sedación/bloqueo neuromuscular en las primeras 24 h de ingreso, con pocos cambios a lo largo del tiempo de estudio. Similares factores de riesgo fueron descritos por Meissner et al.26 en una UCI posquirúrgica.
De una manera similar pero en un estudio internacional, los datos de las UCI que participaron en la elaboración del índice SAPS 3 son los siguientes27: se practicó algún tipo de LTSV al 8,6% de los pacientes ingresados en UCI (aproximadamente la mitad de los casos fue no iniciar un tratamiento y la otra mitad fue retirarlo). Se confirmó que un tercio de las muertes al alta hospitalaria siguieron a una LTSV, con una mortalidad hospitalaria en los pacientes tras la LTSV del 80-95%. El tiempo desde el ingreso hasta la toma de la decisión fue de 2-4 días. Es interesante ver qué factores se asocian a la decisión de LTSV, pues hay causas clínicas (la mayoría de las variables que implican gravedad recogidas en el SAPS 3) y otras de índole estructural u organizativa, a saber: fueron más comunes las LTSV en hospitales sin servicios de Urgencias, en UCI pequeñas y con una ratio enfermera/paciente menor, un mayor número de médicos por cama de UCI, en las que se realizan reuniones multidisciplinarias y en las que enfermeras e intensivistas pasan visita juntos, y menos frecuentes en las UCI donde había un intensivista de forma continuada.
En los años 1999 y 2000 se llevó a cabo el mayor estudio sobre LTSV en UCI de Europa, el End-of-Life Practices in European Intensive Care Units (ETHICUS)28, con datos de UCI de 17 países, en el que se pusieron de manifiesto importantes diferencias en la forma de tomar la decisión de limitar el esfuerzo terapéutico en las diferentes naciones. En el subanálisis sobre las razones dadas por los médicos para tomar la decisión de LTSV la más frecuente fue la enfermedad principal del paciente (79%), especialmente el hecho de que no respondiera al tratamiento (46%), mientras que las enfermedades crónicas (12%), la calidad de vida (4%), la edad (2%) y la petición del paciente o la familia (2%) fueron argumentos poco frecuentes.
Sobre la frecuencia con la que se toman decisiones de LTSV en las UCI, aunque los resultados son dispares entre las diferentes series, podemos concluir que entre el 40% y el 90% de los fallecimientos ocurridos en las UCI fueron precedidos por algún tipo de LTSV29–36. La frecuencia con la que se toman estas decisiones no es bien conocida y probablemente está infravalorada37. A modo de ejemplo, en un reciente estudio en la región de Murcia (España) los autores ponen de manifiesto la escasa frecuencia con la que se pregunta a los pacientes por sus deseos al final de la vida38.
En nuestro estudio, de los 589 pacientes que presentaron una complicación más allá del 7.° día de ingreso en UCI, se planteó LTSV en 202, lo que supone el 34,3% de los pacientes, porcentaje similar al de otras series.
En numerosos estudios publicados sobre factores asociados a LTSV la edad se menciona como un criterio menor. En nuestro estudio, la media de edad de los pacientes con algún tipo de LTSV fue de 66,5 años, con diferencias significativas en la edad entre los pacientes a los que se les aplica LTSV y a los que no. Sin embargo, esa edad media no hace pensar que este dato haya sido un factor destacado. En cualquier caso, el diseño no iba dirigido a conocer el motivo por el que se propone LTSV sino sencillamente a una descripción de la misma.
En general podemos decir que el perfil de paciente en el que se plantea la LTSV es equiparable al resto de pacientes de la muestra, pero hay algunas diferencias significativas: de entre los pacientes con algún tipo de LTSV es más frecuente la presencia de neumopatía moderada o grave, de enfermedad oncológica y de tratamiento esteroideo o inmunosupresor. Asimismo, entre el grupo de pacientes que acaban recibiendo alguna LTSV hay una mayor proporción de pacientes dependientes. Por lo tanto, y de acuerdo con diversos estudios descriptivos25,27, los antecedentes personales de los pacientes influyen en la decisión de plantear alguna LTSV.
La mayor parte de las propuestas de LTSV surgen del equipo médico, como ya había sido descrito por Esteban et al.39. Asimismo, apreciamos que suele haber acuerdo en realizar LTSV una vez propuesta. De hecho, en el 97% de los casos en los que se plantea la LTSV se decide llevarla a cabo. Son posibles diferentes explicaciones para este hecho: puede considerarse que existe una gran prudencia entre pacientes, familiares y profesionales a la hora de proponer una LTSV, considerando las consecuencias que tiene esta decisión. Sin embargo, por todos es conocida la dificultad a la hora de tomar decisiones en Medicina y los diversos cursos de acción propuestos para un mismo paciente por los diferentes médicos participantes en su asistencia; si esto es así con cualquier decisión clínica, cabría pensar que también sería así en el caso de la LTSV, lo que no se ve reflejado en ese dato. Otra explicación podría ser la confianza depositada en el médico que trata al paciente (dado que es el actor que con más frecuencia propone la LTSV) por el resto de facultativos, así como por pacientes y familiares, que nos hace llevar a tomar la decisión en la inmensa mayoría de los casos en los que esta es propuesta. Independientemente de la realidad que lleve a estos datos, hay que considerar que esta muestra se limita a pacientes que presentan una complicación grave en el seno de un ingreso prolongado en UCI, por lo que estos mismos datos no son directamente extrapolables a decisiones de LTSV en otras situaciones. En consonancia con esto podemos apreciar que el planteamiento de LTSV se produce en torno al 13.° día de ingreso, lo que probablemente refleja el hecho de que, en un número elevado de casos, la LTSV se propone tras haberse comprobado la inutilidad del tratamiento en UCI para resolver los problemas orgánicos del paciente.
El hecho de que la LTSV se lleve a cabo en la mayor parte de los casos en que es propuesta está relacionado también con el acuerdo habitualmente unánime dentro del equipo médico a la hora de decidir LTSV (en nuestra muestra fue así en el 87,8% de casos), como recomienda la SEMICYUC12. Sin embargo, este hecho pone de manifiesto nuevamente un importante punto de mejora, pues no deja de sorprender que en el 12,2% de los casos hubiera miembros del equipo que no estaban de acuerdo con la LTSV pero que se llevara a cabo a pesar de ello. Estos datos son similares a los publicados por Iribarren-Diarasarri et al.40.
Nuestro trabajo refleja un bajo porcentaje de casos en los que la propuesta de limitar el tratamiento surge del personal de enfermería. Probablemente esto se deba a que en muchas unidades las enfermeras no participan en la sesión clínica y, por ello, cabe la posibilidad de que comentarios realizados de forma personal no hayan quedado reflejados en los datos recogidos41,42.
Numerosos estudios han valorado la relación del triángulo médico-paciente-familiares en el contexto de las decisiones de LTSV43–45. De forma coincidente, nuestros datos demuestran una buena relación entre los profesionales y los pacientes y familiares. Aunque es cierto que la valoración recogida en este estudio es una apreciación subjetiva por parte del médico sobre la calidad de la relación con pacientes y familiares, el volumen de respuestas que muestran una mejoría en esa relación indica que el hecho es cierto. Es frecuente que, con el curso de los días, las visitas y la información recibida, los familiares de los pacientes que están teniendo una mala evolución van comprendiendo la escasa probabilidad de supervivencia; si a esto añadimos el estrecho conocimiento que tienen de sus allegados, en muchos casos esto los lleva a la valoración subjetiva de que no será capaz de sobrevivir. Cuando en esa situación el médico confirma sus «sospechas» suele generarse ansiedad ante la posibilidad de una «mala muerte» (distanasia), y la propuesta de modificar el enfoque terapéutico mediante la LTSV suele ser bien acogida.
Como medida de tratamiento en la situación más extrema, el tipo de LTSV que se plantea con mayor frecuencia es no realizar RCP cuando se presenta una parada cardiorrespiratoria. Una de las dificultades con las que cuenta el presente estudio es la posibilidad de infranotificación de decisiones en las que se plantea la acción a tomar en un futuro (especialmente en lo que se refiere a no aplicar algún tratamiento). Si bien la más habitual de estas decisiones sobre tratamientos futuros es el hecho de no realizar RCP si el paciente presentase una parada cardiaca, es posible que no se hayan reflejado todas las decisiones referentes a no intubar, ventilar, dializar, transfundir, etc. Nos lleva a realizar esta reflexión el hecho de que solo se registre la intención de no intubar a los pacientes en el 23,6% de los casos, si bien es cierto que este resultado también puede deberse a una elevada proporción de pacientes ya intubados en el momento de tomar esta decisión. Otros tratamientos que muestran una frecuencia similar en las decisiones de no llevar a cabo tratamientos futuros son las técnicas de reemplazo renal (71,3%), la transfusión de hemoderivados (66,2%) y el empleo de fármacos vasoactivos (62,1%).
Respecto a acciones a aplicar en el mismo momento de la decisión, destacan una frecuencia de sedación terminal o paliativa del 64,6%, así como un 10,8% de extubaciones terminales.
Otro aspecto relevante es el manejo que reciben los tratamientos farmacológicos en el momento de LTSV. Lo más frecuente es la retirada de todos los tratamientos salvo aquellos dirigidos a mantener una situación de comodidad o analgesia, si bien apreciamos algún caso en el que se retiran absolutamente todos los tratamientos farmacológicos, lo que sin duda es un punto de mejora posible. Asimismo, como forma más gradual de realizar la LTSV, en el 11,3% de los casos se optó por reducir los parámetros de ventilación mecánica y en otros 12,8% se realizó una disminución o retirada de los fármacos vasoactivos sin retirar otros tratamientos. Los datos registrados en esos casos no son suficientes para explicar o justificar esta actitud, que debe ser revisada. En el 12,3% de los casos la decisión de LTSV consiste en no aumentar el nivel de tratamiento; esto puede justificar una mortalidad inferior al 100%.
Consideramos que este estudio tiene algunas fortalezas que es necesario mencionar. Fundamentalmente, la amplia muestra sobre la que está realizado, más de 2.500 pacientes con ingresos prolongados en UCI durante 3 meses. También es significativo el alto número y distribución de los centros participantes, de la práctica totalidad del territorio español, lo que hace que la muestra sea representativa de la situación actual en nuestras UCI. Esta heterogeneidad, también manifiesta por el gran abanico de enfermedades representadas, permite que los resultados sean extrapolables a otros centros.
Nuestro estudio también tiene una serie de limitaciones que deben ser tenidas en consideración. De acuerdo con el diseño del estudio EPIPUSE, se requiere como criterio de inclusión la aparición de complicaciones a partir de la segunda semana de ingreso, por lo que solo se recogen pacientes que presentan complicaciones con repercusión orgánica durante ingresos prolongados; esto hace que los resultados obtenidos solo sean extrapolables a esta subpoblación de pacientes. Dado el periodo de reclutamiento de nuestro estudio (3 meses), no podemos descartar que diferencias estacionales pudieran afectar a los resultados.
ConclusionesSe aplica algún tipo de limitación en los tratamientos de soporte vital en un tercio de los pacientes que presentan complicaciones o eventos adversos con repercusión orgánica ocurridos a partir de la segunda semana de ingreso en UCI. Estas decisiones son más frecuentes en pacientes con neumopatía, enfermedad oncológica o en situación de dependencia para ABVD. En general esta decisión surge del equipo médico y se lleva a cabo con el acuerdo de todo el equipo, así como de los familiares y, en menor medida, de los pacientes que están en condiciones de participar en esta decisión. En la práctica clínica en nuestro medio, los documentos de instrucciones previas no suelen ser un recurso disponible a la hora de tomar decisiones.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
A D.ª Elia Pérez, de la Unidad de Investigación del Hospital Universitario Fundación Alcorcón, por su trabajo en el campo de la metodología y la estadística.
ANDALUCÍA: Francisco José Saldaña González (Clínica Santa Isabel), José Manuel Galván Martín (Hospital Costa del Sol), Rocío Monterroso (Hospital Jerez de la Frontera), José Rubio Quiñones (Hospital Puerta del Mar), Ramón Díaz Alersi (Hospital Puerto Real), Dolores María Mayor García e Isabel Rodríguez Higueras (Hospital Torrecárdenas), Mercedes Barranco Ruiz (Hospital Universitario Virgen de las Nieves), José Antonio Sánchez Román (Hospital Universitario Virgen de Valme). ARAGÓN: Miguel Ángel Suárez Pinilla y Carlos López Núñez (Hospital Clínico Universitario Lozano Blesa), Juan Carlos García Ronquillo (Hospital de Barbastro), Mónica Zamora Elson (Hospital General San Jorge), José Carlos Torralba Allué (Hospital Obispo Polanco), Gabriel Tirado Anglés (Hospital Royo Villanova). ISLAS BALEARES: Rosa Poyo-Guerrero Lahoz y Catalina Forteza Cañelas (Hospital Son Llàtzer). CANARIAS: Ruth Santacreu (Complejo Hospital Universitario de Canarias), Montserrat Sisón Heredia (Hospital Doctor José Molina Orosa), Dácil Parrilla Toribio y Sergio Tomás Rodríguez Ramos (Hospital Universitario Nuestra Señora de la Candelaria). CANTABRIA: Mónica Cordero Vallejo y Álvaro Castellanos Ortega (Hospital Universitario Marqués de Valdecilla). CASTILLA-LA MANCHA: Ana Bueno González (Hospital General Universitario de Ciudad Real), Jerusalén Villegas del Ojo (Hospital Santa Bárbara), Carmen Benito Puncel (Hospital Universitario de Guadalajara), Pilar Sánchez Rodríguez (Hospital Virgen de la Salud). CASTILLA Y LEÓN: Christian J. Sala Scarbay (Complejo Asistencial de Soria - Hospital de Santa Bárbara), Teresita Loreto Álvarez Pérez y F. Concepción Tarancón Maján (Complejo Asistencial de Zamora - Hospital Virgen de la Concha), Myriam González (Complejo Asistencial Universitario de León - Hospital de León), Ramón Cicuéndez Ávila (Hospital Clínico Universitario de Valladolid). CATALUÑA: Joaquín Amador Amérigo (Consorci Sanitari de Terrassa - Hospital de Terrassa), Glòria Miró Andreu (Consorci Sanitari del Maresme - Hospital de Mataró), Antoni Mas y Aníbal Silva (Corporació Sanitària Clínic - Hospital Universitari Clínic de Barcelona IDIBAPS - UCI de Enfermedades Digestivas), Elisabeth Zavala (Corporació Sanitària Clínic - Hospital Universitari Clínic de Barcelona IDIBAPS - UCI Quirúrgica), Olga Rubio Sanchiz (Fundació Althaia - Hospital Sant Joan de Déu de Manresa), Marta Basas (Hospital del Mar), Miguel León Vallés y Silvia Iglesias Moles (Hospital Universitari Arnau de Vilanova de Lleida), Marcos Ibáñez (Hospital Universitari Joan XXIII), Isabel Cherta (Hospital Universitari Mútua Terrassa). EXTREMADURA: María José García Ramos y Federico Minaya González (Complejo Hospitalario de Cáceres - Hospital San Pedro de Alcántara), Noemí Mara Gil Pérez (Complejo Hospitalario del Área de Salud de Mérida - Hospital de Mérida). GALICIA: María Sandra Gómez Canosa (Complejo Hospitalario Arquitecto Marcide-Novoa Santos - Hospital Arquitecto Marcide), Santiago Freita Ramos (Complejo Hospitalario de Pontevedra), Iván Astola Hidalgo y Mónica Mourelo Fariña (Complejo Hospitalario Universitario de A Coruña - Hospital A Coruña), Eva Saborido Paz (Complejo Hospitalario Universitario de Santiago - Hospital Clínico Universitario), Miguel Ángel Pereira Loureiro (Complejo Hospitalario Universitario de Vigo - Hospital Meixoeiro - UCP), Mélida García Martul y María José Rodríguez Fernández (Complejo Hospitalario Universitario de Vigo - Hospital Xeral Cies), José Vicente Bravo Doviso (Complejo Hospitalario Xeral-Calde de Lugo - Hospital Universitario Lucus Augusti). COMUNIDAD DE MADRID: María Cruz Martín Delgado (Hospital Universitario de Torrejón), María Belén Estébanez Montiel (Hospital del Tajo), José Manuel Gómez García (Hospital General Universitario Gregorio Marañón), Eduardo Arias Sarmiento (Hospital Universitario 12 de Octubre), Ricardo Andino Ruiz, Marta García Costas y Ana Leal Micharet (Hospital Universitario de La Princesa), Teresa Honrubia Fernández (Hospital Universitario de Móstoles), María Victoria Enciso Calderón (Hospital Universitario del Henares), Alberto Hernández-Tejedor (Hospital Universitario Fundación Alcorcón), Domingo Díaz Díaz (Hospital Universitario Infanta Leonor), Gonzalo Hernández (Hospital Universitario Infanta Sofía), Abelardo García de Lorenzo (Hospital Universitario La Paz – UCI Quemados), José Alberto Gallardo Álvarez y Ángel Luis Córdoba Sánchez (Hospital Universitario Madrid Norte Sanchinarro), José Andrés Cambronero Galache (Hospital Universitario Príncipe de Asturias), Inmaculada Fernández Simón y Miguel Valdivia de la Fuente (Hospital Universitario Puerta de Hierro Majadahonda), Félix Lacoma (Hospital Universitario Quirón Madrid), Isidro Prieto del Portillo (Hospital Universitario Ramón y Cajal). REGIÓN DE MURCIA: Antonia López Martínez (Hospital General Universitario Morales Meseguer), Luis Herrera Para y Salvador Moreno Aliaga (Hospital General Universitario Santa Lucía), Carmen M. Susarte Juliá (Hospital Universitario Reina Sofía de Murcia), María Martínez Martínez (Hospital Universitario Virgen de la Arrixaca). COMUNIDAD FORAL DE NAVARRA: Pablo Monedero (Clínica Universidad de Navarra), María Barber Ansón (Complejo Hospitalario de Navarra - UCI-A - Hospital de Navarra), Eva Regidor Sanz y Laura Macaya Redín (Complejo Hospitalario de Navarra - UCI-B - Hospital Virgen del Camino). PAÍS VASCO: Mónica Domezain del Campo (Hospital Universitario Cruces), Alberto Manzano Ramírez y Yolanda Poveda Hernández (Hospital Universitario de Araba - Sede Santiago), Juan Fernando Castedo González (Hospital Universitario de Araba – Sede Txagorritxu), Itziar Mintegui Malcorra y Itxaso Elosegui Plaza (Hospital Universitario Donostia). LA RIOJA: José Luis Monzón Marín y Lidia Martínez Camarero (Hospital San Pedro), COMUNIDAD VALENCIANA: Manuel Palomo Navarro (Hospital de Sagunt), Ana Llamas Álvarez (Hospital General Universitario de Elche), Pedro Kot (Hospital Universitario y Politécnico La Fe de Valencia).