Analizar el perfil, la incidencia de limitación de tratamiento de soporte vital (LTSV) y la potencialidad de donación de órganos en pacientes neurocríticos.
DiseñoMulticéntrico prospectivo.
ÁmbitoNueve centros autorizados para extracción de órganos para trasplante.
PacientesTodos los pacientes ingresados en el hospital con GCS < 8 durante 6 meses fueron seguidos hasta su alta o hasta 30 días de estancia hospitalaria.
Variables de interésDatos demográficos, causa del coma, situación clínica al ingreso y evolución. Incidencia de LTSV, muerte encefálica (ME) y donación de órganos.
ResultadosSe incluyó a 549 pacientes. Edad media 59,0 ± 14,5. El 27,0% de los comas fueron por hemorragias cerebrales.
Se aplicó LTSV en 176 pacientes (32,1%). En 78 casos consistió en no ingreso en la UCI. La edad, presencia de contraindicaciones y determinadas causas del coma se asociaron a LTSV.
Fallecieron 319 pacientes (58,1%); 133 fueron ME (24,2%) y el 56,4% de ellos fueron donantes de órganos (n=75). Edema y desviación de la línea media en la TAC y la evaluación previa por el coordinador de trasplantes se asociaron a ME. La LTSV se asoció a no evolución a ME. Nueve pacientes de menos de 80 años, sin contraindicaciones para donación y con un GCS ≤ 4 fueron limitados en los 4 primeros días y fallecieron en asistolia.
ConclusionesLa aplicación de LTSV es frecuente en el paciente neurocrítico. Casi la mitad de LTSV consistió en el no ingreso en unidades de críticos y, en ocasiones, sin evaluar su potencialidad como donante por la coordinación de trasplantes.
To analyze the profile, incidence of life support therapy limitation (LSTL) and donation potential in neurocritical patients.
Study designA multicenter prospective study was carried out.
SettingNine hospitals authorized for organ harvesting for transplantation.
PatientsAll patients consecutively admitted to the hospital with GCS < 8 during a 6-month period were followed-up until discharge or day 30 of hospital stay.
Study variablesDemographic data, cause of coma, clinical status upon admission and outcome were analyzed. LSTL, brain death (BD) and organ donation incidence were recorded.
ResultsA total of 549 patients were included, with a mean age of 59.0 ± 14.5 years. The cause of coma was cerebral hemorrhage in 27.0% of the cases.LSTL was applied in 176 patients (32.1%). In 78 cases LSTL consisted of avoiding ICU admission. Age, the presence of contraindications, and specific causes of coma were associated to LSTL.
A total of 58.1% of the patients died (n=319). One-hundred and thirty-three developed BD (24.2%), and 56.4% of these became organ donors (n=75). The presence of edema and mid-line shift on the CT scan, and transplant coordinator evaluation were associated to BD. LSTL was associated to a no-BD outcome. Early LSTL (first 4 days) was applied in 9 patients under 80 years of age, with no medical contraindications for donation and a GCS ≤ 4 who finally died in asystole.
ConclusionsLSTL is a frequent practice in neurocritical patients. In almost one-half of the cases, LSTL consisted of avoiding admission to the ICU, and on several occasions the donation potential was not evaluated by the transplant coordinator.
En un firme intento de homogeneizar los programas de donación en el mundo, se desarrolló en Madrid la 3rd World Health Organization (WHO) Global Consultation on Organ Donation and Transplantation1, con un llamamiento a los gobiernos para avanzar hacia el concepto de autosuficiencia en el trasplante y, por lo tanto, cubrir las necesidades de sus pacientes utilizando todos los recursos dentro de sus posibilidades para aumentar la disponibilidad de órganos. A pesar de las muchas iniciativas dirigidas a aumentar el número de donantes de órganos, se requiere seguir avanzando en esta área, ya que persiste una necesidad constante y creciente de órganos para trasplante. Aunque el número absoluto de donantes cadavéricos de órganos sólidos en España fue 1.655 en 2013, un número estable respecto a años previos2, la lista de pacientes en espera para trasplante de un órgano se mantiene estable o aumenta en los últimos años.
Hasta ahora, en España, la mayoría de donantes de órganos proviene de pacientes que fallecen en los hospitales en situación de muerte encefálica (ME)3. La proporción de ME se ha estimado del 2,3% de muertes hospitalarias o del 12,4% de muertes en unidades de críticos4. Estos indicadores, aunque están basados en análisis retrospectivos de las muertes acontecidas en las áreas de críticos, sirven de referencia para el cálculo de potencialidad de donación en nuestros centros. El programa de garantía de calidad de la ONT, cuyo objetivo es conocer la potencialidad de donación de las unidades de críticos (basado en auditorías internas y externas, que evalúa las circunstancias últimas en los pacientes que fallecen en las unidades de críticos), identifica de forma retrospectiva las «pérdidas» de potenciales donantes no identificados por los propios coordinadores de trasplante en tiempo real, y permite establecer áreas de mejora en los hospitales auditados. Dichas auditorías revelan que el número de donantes podría ser un 21,6% superior si se identificasen todos los donantes potenciales (paciente cuya condición clínica hace sospechar que cumple criterios de ME)5 y se evitaran todas las posibles pérdidas.
Para estimar la potencialidad de donación en ME, otros autores han considerado más apropiado analizar el número de pacientes ingresados en coma en la Unidad de Cuidados Intensivos (UCI)6, incluso en el hospital7, ya que determinadas decisiones en cuanto al diagnóstico y tratamiento, a lo largo del proceso de atención al paciente neurocrítico, podrían influir en el número final de posibles donantes. Así, el impacto que pueden tener las decisiones en los cuidados al final de la vida en la potencialidad de donación ha sido poco estudiado hasta el momento. El estudio Ethicus8 ponía de manifiesto que la limitación del tratamiento de soporte vital (LTSV) es una práctica habitual en las UCI europeas (10% de pacientes ingresados y 73% de pacientes que fallecen en las UCI). Aunque existe menos conocimiento en cuanto a la incidencia de LTSV en otras áreas del hospital, trabajos publicados en la última década ponen de manifiesto que la proporción de pacientes a los que se aplica LTSV en los servicios de urgencias no es despreciable, sobre todo en pacientes añosos y con múltiples comorbilidades9,10.
El perfil cambiante de los potenciales donantes en nuestro país y la nueva realidad de nuestra red sanitaria con recursos más limitados hace necesario optimizar la detección de potenciales donantes dentro y fuera de las UCI11. Por ello, el objetivo del presente estudio es analizar el perfil de pacientes con enfermedad neurológica crítica ingresados no solo en la UCI sino en cualquier otra área del hospital, la incidencia de LTSV en este grupo de pacientes y la potencialidad de donación de órganos en ME.
Material y métodosDiseño, inclusión de datos y centros participantesNueve centros (7 de ellos con servicio de neurocirugía y 3 con programa de trasplante), de un total de 26 autorizados para extracción de órganos en Cataluña participaron en el proyecto. El estudio fue aprobado por el Comité de Ética e Investigación Clínica de cada centro participante.
Durante 6 meses (del 1 de octubre del 2009 al 31 de marzo del 2010), todos los pacientes ingresados en el hospital con coma, definido como Glasgow Coma Score (GCS) inferior a 8, en cualquier momento de su evolución fueron registrados por un investigador de cada centro participante. Se excluyeron aquellos casos cuya causa del coma imposibilitaba el diagnóstico de ME.
Los pacientes incluidos fueron seguidos hasta el alta hospitalaria (incluidos los pacientes que fallecieron), o una estancia de 30 días. La información relativa a la LTSV se obtenía mediante revisión de la historia clínica y entrevista con el médico responsable del paciente.
Todos los formularios de los casos incluidos de acuerdo a los criterios establecidos se registraron en una base de datos web coordinada desde la Organización Catalana de Trasplantes (OCATT). Los coordinadores del estudio validaron los datos incluidos en el registro para asegurar su consistencia.
Definición de las variablesDe cada paciente incluido en el estudio se registraron variables clínicas al ingreso y durante su evolución. Se incluyeron: fecha de ingreso y alta, edad, sexo, comorbilidades, servicio donde ingresaba inicialmente y causa del coma. Se registraron el GCS y los hallazgos en la TAC al ingreso hospitalario. Durante su estancia hospitalaria se registraba el servicio en el que se hallaba ingresado cuando el GCS disminuía (GCS < 8) y se incluía en el estudio; hallazgos en la TAC, terapias de soporte vital recibidas, ingreso en UCI (o servicio que dispone de la monitorización y terapias de soporte vital para un adecuado mantenimiento del donante de forma continuada); LTSV durante el ingreso. Se definía LTSV tanto el no inicio como la retirada de un tratamiento de soporte vital y, se consideraba como tal en el estudio si se hallaba registrado en la historia clínica o lo manifestaba el médico responsable del paciente. De acuerdo a las recomendaciones de la SEMICYUC12, se entiende que la resucitación cardiopulmonar, la ventilación mecánica, los sistemas de depuración extrarrenal, los fármacos vasoactivos, la nutrición artificial, y los hemoderivados son tratamientos de soporte vital. Aunque no ingresar a un paciente en UCI puede considerarse una forma de no inicio de tratamiento, se detalla como un tipo específico de LTSV.
Se incluía si había sido valorado en algún momento de su evolución por el equipo de coordinación de trasplantes, así como la evolución final; evolución a ME, donación de órganos, y causa de no donación. En los supervivientes, el estado funcional al alta o a los 30 días, según la escala GOS (Glasgow Outcome Scale)13.
El diagnóstico de ME se realizó de acuerdo a la legislación española vigente durante el periodo de estudio14. Se consideró contraindicación la evidencia de tumor maligno, la infección aguda no controlada o la disfunción multiorgánica. La edad por sí misma no se consideró una contraindicación.
La efectividad del proceso de donación se calculó, de acuerdo a su definición en los indicadores de calidad de la SEMICYUC, como la proporción de donantes reales entre el total de ME15. Definiéndose donante real como el donante en ME que llega a quirófano y del que al menos se extrae un órgano para trasplante4,5,16. Se definió la potencialidad de ME como la proporción de casos diagnosticados como ME entre el total de pacientes ingresados en el hospital con coma GCS inferior a 8.
Análisis estadísticoLas frecuencias absolutas y relativas se utilizaron como descriptores clásicos para variables categóricas. Para variables continuas normales según el test de Kolmogorov-Smirnov se utilizaron la media y desviación estándar. Para variables continuas no normales, la mediana y el rango intercuartil. La asociación entre 2 variables categóricas se estudió mediante la prueba de Chi-cuadrado o la prueba de Fisher, según se precisara.
Para comparar una variable continua normal entre 2 grupos independientes se aplicó la t de Student para muestras independientes. Para comparar una variable continua no normal entre 2 grupos independientes se aplicó una prueba de Mann-Whitney. El análisis multivariante para evaluar el efecto de variables independientes sobre una dependiente (sobre LTSV y sobre evolución a ME) se realizó mediante regresión logística. En el análisis multivariante se incluyeron las variables asociadas a LTSV o a evolución a ME en el análisis univariado. En todos los casos se consideró significación estadística cuando p < 0,05. Se utilizó el programa estadístico SPSS v18.
ResultadosPoblación de estudioDurante el periodo de estudio se identificaron 605 pacientes con coma GCS < 8. Se excluyeron 24 casos con el diagnóstico de intoxicación aguda, 17 encefalopatías metabólicas y 15 estatus epilépticos, por la imposibilidad de realizar el diagnóstico de ME en estas situaciones. Así, finalmente se incluyó un total de 549 pacientes en el análisis. De ellos, 400 de hospitales con programa de trasplantes. La edad media de la población de estudio fue de 59,0 ± 14,5, 345 varones(62,8%).
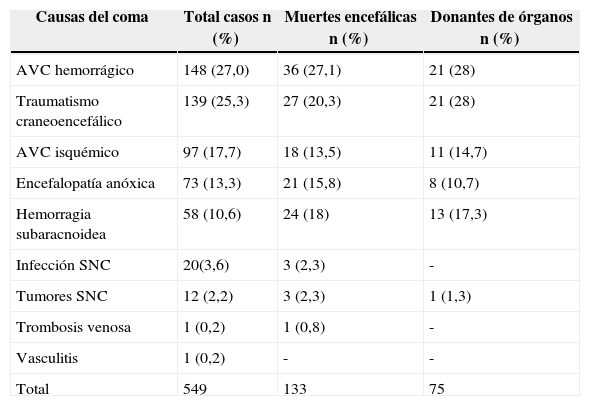
La causa del coma de los pacientes incluidos en el estudio se detalla en la tabla 1. La causa más frecuente de coma fue el accidente vascular cerebral (AVC) hemorrágico (n=148, 27,0%), seguido del traumatismo craneoencefálico (n=139, 25,3%) y el AVC isquémico (n=97, 17,7%).
Causas del coma
| Causas del coma | Total casos n (%) | Muertes encefálicas n (%) | Donantes de órganos n (%) |
|---|---|---|---|
| AVC hemorrágico | 148 (27,0) | 36 (27,1) | 21 (28) |
| Traumatismo craneoencefálico | 139 (25,3) | 27 (20,3) | 21 (28) |
| AVC isquémico | 97 (17,7) | 18 (13,5) | 11 (14,7) |
| Encefalopatía anóxica | 73 (13,3) | 21 (15,8) | 8 (10,7) |
| Hemorragia subaracnoidea | 58 (10,6) | 24 (18) | 13 (17,3) |
| Infección SNC | 20(3,6) | 3 (2,3) | - |
| Tumores SNC | 12 (2,2) | 3 (2,3) | 1 (1,3) |
| Trombosis venosa | 1 (0,2) | 1 (0,8) | - |
| Vasculitis | 1 (0,2) | - | - |
| Total | 549 | 133 | 75 |
AVC: accidente vascular cerebral; SNC: sistema nervioso central.
El 55,4% de los pacientes (n=304) presentaban el estado de coma al ingreso hospitalario. En 245 casos el GCS descendió por debajo de 8 durante su estancia en el hospital (44,6%). La mayoría (n=481; 87,6%) fueron incluidos en el estudio en los 3 primeros días de estancia en el hospital. La mediana de GCS en el momento de la detección e inclusión en el estudio fue de 5 (RIQ25-75 3-6).
El coordinador de trasplantes había evaluado el caso como posible donante en 433 ocasiones (78,9%) en algún momento de su evolución. En 141 de los pacientes (24,2%) incluidos en el estudio existían contraindicaciones médicas para la donación de órganos.
El 68,7% de los pacientes (377) ingresaron en UCI durante su estancia hospitalaria, 448 recibieron ventilación mecánica (81,6%) y 304 fármacos vasoactivos (55,4%).
Limitación del tratamiento de soporte vitalSe aplicó LTSV en 176 pacientes (32,1%). La LTSV fue a los 3 días (mediana, RIQ25-75 1-9) de su ingreso. En 78 casos la LTSV consistió en no ingreso (n=73) o no reingreso (n=5) en la UCI.
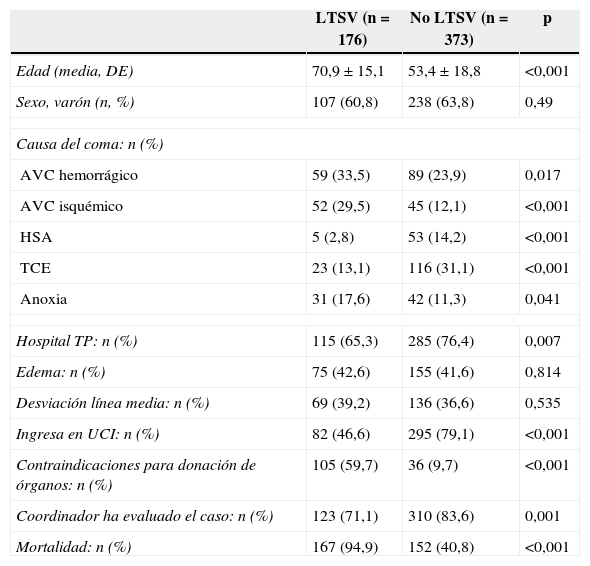
La tabla 2 muestra las características de los pacientes a los que se aplicó algún tipo de LTSV frente a lo que no se les aplicó en ningún momento de su evolución. El grupo de pacientes a los que se aplicó LTSV eran 17 años mayores que el grupo en el que no se aplicó LTSV. La causa del coma influyó en la incidencia de LTSV, siendo mayor en los pacientes con AVC hemorrágico, isquémico, y en la encefalopatía anóxica. Entre el grupo de pacientes a los que no se aplicó ningún tipo de LTSV, 78 no ingresaron en la UCI; 39 porque fallecieron antes del ingreso y el resto porque mejoraron su nivel de conciencia.
Análisis univariado de factores asociados a LTSV
| LTSV (n=176) | No LTSV (n=373) | p | |
|---|---|---|---|
| Edad (media, DE) | 70,9 ± 15,1 | 53,4 ± 18,8 | <0,001 |
| Sexo, varón (n, %) | 107 (60,8) | 238 (63,8) | 0,49 |
| Causa del coma: n (%) | |||
| AVC hemorrágico | 59 (33,5) | 89 (23,9) | 0,017 |
| AVC isquémico | 52 (29,5) | 45 (12,1) | <0,001 |
| HSA | 5 (2,8) | 53 (14,2) | <0,001 |
| TCE | 23 (13,1) | 116 (31,1) | <0,001 |
| Anoxia | 31 (17,6) | 42 (11,3) | 0,041 |
| Hospital TP: n (%) | 115 (65,3) | 285 (76,4) | 0,007 |
| Edema: n (%) | 75 (42,6) | 155 (41,6) | 0,814 |
| Desviación línea media: n (%) | 69 (39,2) | 136 (36,6) | 0,535 |
| Ingresa en UCI: n (%) | 82 (46,6) | 295 (79,1) | <0,001 |
| Contraindicaciones para donación de órganos: n (%) | 105 (59,7) | 36 (9,7) | <0,001 |
| Coordinador ha evaluado el caso: n (%) | 123 (71,1) | 310 (83,6) | 0,001 |
| Mortalidad: n (%) | 167 (94,9) | 152 (40,8) | <0,001 |
AVC: accidente vascular cerebral; Hospital TP: hospital con programa de trasplantes; HSA: hemorragia subaracnoidea; LTSV: limitación del tratamiento de soporte vital; TCE: traumatismo craneoencefálico; UCI: unidad de cuidados intensivos.
Existió una mayor proporción de pacientes ingresados en UCI y evaluados por el coordinador de trasplantes dentro de su proceso asistencial en el subgrupo de pacientes sin LTSV. No se observaron diferencias significativas en los hallazgos en la TAC tales como la desviación de línea media y la presencia de edema cerebral entre ambos subgrupos. Sin embargo, existía una mayor proporción de pacientes con contraindicaciones médicas para la donación en el grupo de pacientes con LTSV.
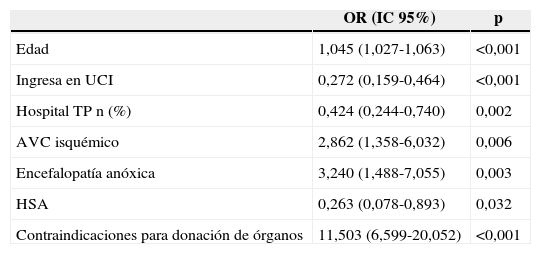
El análisis multivariado puso de manifiesto que la edad, la presencia de contraindicaciones médicas para la donación, y determinadas causas del coma (mayor LTSV en AVC isquémico y encefalopatía anóxica) se asociaron a la LTSV. Sin embargo la HSA como causa del coma se asoció de forma negativa a LTSV. Obviamente el ingreso en UCI se asoció a una menor LTSV. El ingreso en hospital trasplantador se constituye como factor «protector» de LTSV (tabla 3).
Regresión logística. Factores asociados con LTSV
| OR (IC 95%) | p | |
|---|---|---|
| Edad | 1,045 (1,027-1,063) | <0,001 |
| Ingresa en UCI | 0,272 (0,159-0,464) | <0,001 |
| Hospital TP n (%) | 0,424 (0,244-0,740) | 0,002 |
| AVC isquémico | 2,862 (1,358-6,032) | 0,006 |
| Encefalopatía anóxica | 3,240 (1,488-7,055) | 0,003 |
| HSA | 0,263 (0,078-0,893) | 0,032 |
| Contraindicaciones para donación de órganos | 11,503 (6,599-20,052) | <0,001 |
AVC: accidente vascular cerebral; Hospital TP: hospital con programa de trasplantes; HSA: hemorragia subaracnoidea; UCI: unidad de cuidados intensivos.
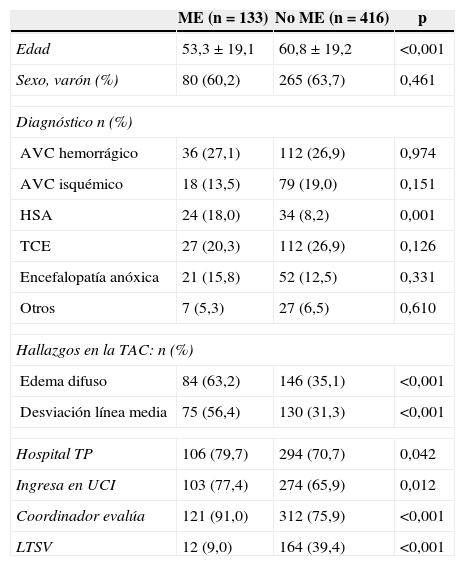
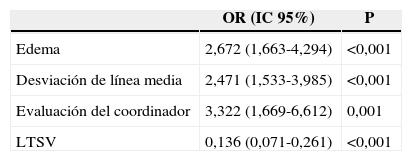
De un total de 319 pacientes fallecidos (58,1% de la población estudiada), 133 lo hicieron en ME (24,2%). La ME aconteció a los 2 días (mediana, RIQ25-75 1-6) del ingreso. La tabla 4 muestra las diferentes características de los pacientes que fallecieron en ME respecto al resto de pacientes incluidos en el estudio. En el análisis multivariado (tabla 5), la presencia de edema y desviación de la línea media en la TAC y la existencia de una valoración previa por el coordinador de trasplantes, durante el proceso asistencial, se asociaron a la evolución a ME, mientras que la aplicación de LTSV se asoció a no evolución a ME.
Factores asociados a evolución a ME. Análisis univariado
| ME (n=133) | No ME (n = 416) | p | |
|---|---|---|---|
| Edad | 53,3 ± 19,1 | 60,8 ± 19,2 | <0,001 |
| Sexo, varón (%) | 80 (60,2) | 265 (63,7) | 0,461 |
| Diagnóstico n (%) | |||
| AVC hemorrágico | 36 (27,1) | 112 (26,9) | 0,974 |
| AVC isquémico | 18 (13,5) | 79 (19,0) | 0,151 |
| HSA | 24 (18,0) | 34 (8,2) | 0,001 |
| TCE | 27 (20,3) | 112 (26,9) | 0,126 |
| Encefalopatía anóxica | 21 (15,8) | 52 (12,5) | 0,331 |
| Otros | 7 (5,3) | 27 (6,5) | 0,610 |
| Hallazgos en la TAC: n (%) | |||
| Edema difuso | 84 (63,2) | 146 (35,1) | <0,001 |
| Desviación línea media | 75 (56,4) | 130 (31,3) | <0,001 |
| Hospital TP | 106 (79,7) | 294 (70,7) | 0,042 |
| Ingresa en UCI | 103 (77,4) | 274 (65,9) | 0,012 |
| Coordinador evalúa | 121 (91,0) | 312 (75,9) | <0,001 |
| LTSV | 12 (9,0) | 164 (39,4) | <0,001 |
AVC: accidente vascular cerebral; Hospital TP: hospital con programa de trasplantes; HSA: hemorragia subaracnoidea; ME: muerte encefálica; REA: reanimación; TCE: traumatismo craneoencefálico; UCI: unidad de cuidados intensivos.
Regresión logística. Factores asociados con ME
| OR (IC 95%) | P | |
|---|---|---|
| Edema | 2,672 (1,663-4,294) | <0,001 |
| Desviación de línea media | 2,471 (1,533-3,985) | <0,001 |
| Evaluación del coordinador | 3,322 (1,669-6,612) | 0,001 |
| LTSV | 0,136 (0,071-0,261) | <0,001 |
LTSV: limitación del tratamiento de soporte vital; ME: muerte encefálica.
El 56,4% de los pacientes (n=75) que fallecieron en ME fueron donantes de órganos. La causa del coma en los pacientes que fallecieron en ME y en los que fueron finalmente donantes se muestran en las columnas 2.ª y 3.ª de la tabla 1. Los motivos de no donación en el resto de casos de ME (n=58) fueron: contraindicaciones médicas absolutas 15,8% del total de ME (n=21), otras contraindicaciones 5,3% (n=7), negativas familiares 18,1% (n=24), y problemas en el mantenimiento 2,3% (n=3). Además hubo un caso de negativa judicial y en 2 casos no se consiguió completar el diagnóstico legal (no llegó a realizarse el diagnóstico clínico por un tercer médico o presentó asistolia a la espera de la realización de prueba complementaria confirmatoria).
En el 30,6% de los pacientes fallecidos (n=57) por parada cardiaca se había aplicado algún tipo de LTSV y no presentaban contraindicaciones médicas para la donación de órganos. Solo en 35 de ellos (61,4%) el coordinador había evaluado el caso. El periodo de tiempo transcurrido entre el ingreso y la LTSV en estos pacientes fue de 3 días (mediana, RIQ25-75 1-7). Nueve de estos pacientes eran menores de 80 años, tenían un GCS ≤ 4 al ingreso y se aplicó LTSV en los primeros 4 días de ingreso.
Evolución de los pacientes que sobrevivieronDe los pacientes que no fallecieron durante el periodo de estudio (n=230), 114 fueron dados de alta dentro de los primeros 30 días tras su ingreso y 116 permanecían ingresados a los 30 días (en 5 de ellos se había aplicado LTSV). De los pacientes dados de alta del hospital, 13 (11,4%) fueron dados de alta en estado vegetativo, 19 (16,7%) con una invalidez grave, 39 (34,2%) con una invalidez moderada y 43 (37,7%) con una buena recuperación, según la escala GOS. Entre los 114 pacientes dados de alta, únicamente en 4 se había aplicado algún tipo de LTSV (los 4 fueron dados de alta en estado vegetativo).
DiscusiónEste es el primer estudio que evalúa de forma prospectiva la potencialidad de ME y la efectividad del proceso de donación de órganos entre los pacientes ingresados en el hospital con coma definido como GCS inferior a 8. El principal hallazgo del estudio es que la potencialidad de fallecer en ME entre estos pacientes fue del 24,2%. Otro hallazgo relevante en el presente estudio fue que en el 32,1% de los pacientes se aplicó LTSV y que en el 44,3% dicha LTSV consistió en no ingreso en la UCI. Además, la LTSV se asoció con la no evolución a ME.
En la década de los 90 los esfuerzos por aumentar el número de órganos susceptibles de ser trasplantados se centraron en optimizar el proceso de donación en ME. Sin embargo estas medidas no fueron suficientes para adecuar la oferta de órganos con la creciente demanda en gran medida por la disminución en la incidencia de ME (disminución de accidentes de tránsito, prevención de enfermedad vascular cerebral). En la pasada década, en España, desde la Organización Nacional de Trasplantes se promocionó el proyecto conocido como Plan 4011,17, cuyo objetivo era elevar la tasa de donación hasta 40 por millón de población (pmp) en el territorio nacional. Dicho proyecto, además de incluir como objetivo la optimización del proceso de donación en ME, implicaba aumentar la detección de posibles donantes fuera de las áreas de críticos, ampliar la utilización de todos los posibles donantes cadavéricos, incluyendo la donación en asistolia (controlada y no controlada), y la implementación de la donación de vivo como un complemento a la donación de cadáver.
El presente trabajo muestra la potencialidad y efectividad de donación en ME de 9 centros españoles, incluyendo a los pacientes neurocríticos con GCS inferior a 8 ingresados tanto en las UCI como en otras áreas del hospital. Uno de cada 5 pacientes (24,2%) ingresados en estos centros evolucionaron a ME, siendo algo más de la mitad de ellos finalmente donantes de órganos (56,4%).
El cálculo de potencialidad y efectividad de donación de estos centros se realizó, a diferencia de otros trabajos, de forma prospectiva. La mayor parte de estudios realizados previamente con el objetivo de evaluar la potencialidad de donación se ha realizado mediante análisis retrospectivos (a partir de revisión de historias clínicas) de casos de pacientes fallecidos en las unidades de críticos o de pacientes fallecidos en otras áreas del hospital7. Senouci et al.6 realizaron un ejercicio de predicción prospectiva similar, pero incluyeron únicamente a los pacientes ingresados en UCI. Hallaron que los pacientes con criterios clínicos de ME representaban el 15,1% de pacientes que ingresaban en UCI con GCS inferior a 8. El hecho de que la proporción de pacientes con GCS inferior a 8 admitidos en el hospital que fallece en ME en nuestra serie sea superior al grupo de Senouci et al. hace pensar que existe una proporción de pacientes que pueden no llegar a ingresar en las unidades de críticos por diferentes motivos y que presumiblemente podrían evolucionar a ME. En el presente estudio, la proporción de pacientes neurocríticos ingresados en UCI fue inferior al 70%, lo que deja una proporción nada desdeñable de pacientes que podrían ser posibles donantes en otras áreas del hospital que no es la UCI.
Le Conte et al.9 hallaron que en el 78,8% de los pacientes fallecidos en urgencias se había realizado algún tipo de LTSV, sobre todo en pacientes de más de 80 años, con antecedentes de cáncer con metástasis o con limitaciones funcionales previas. En un análisis posterior realizado por el mismo grupo18 se puso de manifiesto que el 7% de pacientes ancianos que fallecen en los servicios de urgencias con enfermedad neurológica podrían haber sido seleccionados y evaluados como potenciales donantes de órganos. Si bien en dicho estudio no se incluyó la información en cuanto al diagnóstico completo de ME.
Es bien conocido que entre los pacientes ingresados por una enfermedad aguda, el paciente neurológico agudo es en el que más frecuentemente se aplica algún tipo de LTSV en UCI8. A pesar de que disponemos de herramientas para predecir una evolución fatal en las enfermedades que con mayor frecuencia provocan daño neurológico (hemorragia cerebral mediante el ICH score19, datos clínicos y electrofisiológicos en la encefalopatía anóxica20,21, por ejemplo), la decisión temprana de aplicar LTSV en las diferentes enfermedades ha sido ampliamente debatida22,23, ya que la LTSV se ha asociado a una mayor mortalidad. Es evidente que en las decisiones al final de la vida no pueden ser considerados únicamente los datos de gravedad al ingreso del paciente neurocrítico, sino que es necesario considerar la evolución durante los primeros días, datos de la neuromonitorización24 y de respuesta al tratamiento25 y, sobre todo, los deseos del paciente (a través de él mismo o de sus familiares) en cuanto a los cuidados recibidos26.
En el presente estudio se pone de manifiesto que la LTSV se aplica en uno de cada 3 pacientes admitidos en el hospital por enfermedad neurológica crítica (GCS inferior a 8), y en casi la mitad de los casos se trata de pacientes que no llegan a ingresar en UCI. La mediana de tiempo desde el ingreso hasta que se procede a la LTSV es de 3 días. De los 176 pacientes en que se decidió la LTSV, en 71 (40,3%) no existían contraindicaciones para la donación. La LTSV se asoció en el presente trabajo con menor evolución a ME, y, en concreto, en 9 pacientes de menos de 80 años y sin contraindicaciones para la donación de órganos, con un GCS ≤ 4, la LTSV se realizó dentro de los primeros 4 días de ingreso hospitalario, lo que supone un 12% de potenciales pérdidas. La cuestión es si hubiesen podido ser evaluados como posibles donantes en caso de no haberse aplicado una LTSV.
A la luz de los trabajos publicados sobre el impacto que la LTSV precoz puede tener en la evolución fatal de la enfermedad neurocrítica y en la potencialidad de donación, se requieren estudios más extensos para evaluar el impacto de un cambio en la actitud inicial en este tipo de pacientes.
Otro aspecto importante es la participación del coordinador de trasplantes en el proceso de decisiones en el entorno de cuidados al final de la vida del paciente neurocrítico. En el grupo de nuestro estudio, haber sido valorado a lo largo de su evolución hospitalaria por el coordinador de trasplantes se asociaba a menor incidencia de LTSV únicamente en el análisis univariado. Pero es importante señalar que en 53 casos en que se procedió a LTSV, el coordinador no había evaluado en ningún momento el caso. No se habían investigado, por ello, los deseos del paciente a través de sus allegados en cuanto a la donación de órganos ni tejidos.
Sigue existiendo dilema ético27–29 en cuanto a la instauración de tratamientos y terapias de soporte vital no en beneficio del propio paciente sino a la espera de la ME en pacientes neurocríticos con una muerte inminente inevitable, y en los que las medidas encaminadas al tratamiento de la enfermedad no estarían indicadas. Aunque la instauración de dichas medidas no sea con el objetivo de curar o mejorar al propio paciente, sí existe en nuestro entorno consenso en que están justificadas si se realizan de acuerdo a los deseos del paciente en cuanto a donar sus órganos. Por ello es necesario realizar una entrevista con sus seres queridos en la que la información sea clara y trasparente, e incluya todas las posibles opciones en cuanto a los cuidados al final de la vida dependiendo de la evolución en los primeros días. Así se asegurará tomar una decisión al respecto consensuada con el equipo médico y con la propia familia.
El presente estudio no incluía como objetivo el análisis de la potencialidad de donación en asistolia controlada (Maastricht III). No se analizó el tipo de terapia de soporte vital limitada ni el momento del fallecimiento tras la LTSV. Este tipo de donantes, aunque ha mostrado una menor rentabilidad en cuanto a órganos extraídos respecto a los donantes en ME, son una opción válida en casos concretos. Nos referimos a aquellos pacientes que ingresan en las unidades de críticos con GCS < 8, con mal pronóstico, que tras un trial de tratamiento, su pronóstico es fatal, el tratamiento es fútil, y al no evolucionar a ME, se decide LTSV. Evidentemente, de acuerdo a la legislación vigente30 y a las recomendaciones de buena práctica en el proceso de donación en asistolia31, el proceso de donación es independiente de la decisión de LTSV. La donación siempre será de acuerdo con los deseos del fallecido (deseos expresados previamente por el propio paciente o por la familia en la entrevista familiar de donación) y en ausencia de contraindicaciones.
Existen limitaciones en el presente estudio. El grupo de hospitales y de causas del coma es heterogéneo y, por ello, los hallazgos no pueden generalizarse a todas las enfermedades neurológicas y todos los entornos. Pero el gran número de casos incluidos permite extraer datos importantes en cuanto a la potencialidad de donación y la incidencia de LTSV. Aunque los casos se han incluido de forma prospectiva, no se detallan los factores últimos que motivaron la decisión, el momento de LTSV, ni el tratamiento de soporte vital concreto que se limitó (no inicio o retirada) en cada caso. Pero sí se evidencia que siendo la LTSV frecuente en este grupo de pacientes, es menos frecuente en los primeros días, aunque no en una proporción despreciable.
En conclusión, este estudio evidencia la potencialidad real de donación de órganos en ME y la elevada incidencia de LTSV en los pacientes neurocríticos en nuestros hospitales. Pone de manifiesto que la aplicación de la LTSV aunque se realiza con mayor frecuencia en pacientes con contraindicaciones para la donación de órganos, se asocia con la no evolución a ME, existiendo casos que son limitados a los primeros días aun sin contraindicaciones para la donación de órganos. De ahí la importancia de que los profesionales sanitarios implicados en la atención al paciente con daño cerebral severo, tanto de las unidades de críticos como de otras áreas del hospital, sobre todo de los servicios de urgencias, reciban una adecuada formación y sepan reconocer a los pacientes con ME inminente y la posibilidad de considerarlos donantes de órganos. El principio fundamental es facilitar unos cuidados al final de la vida de calidad, de acuerdo a las recomendaciones actuales. La participación del coordinador de trasplantes es importante en cuanto a procurar incluir la opción de donar los órganos de acuerdo a los deseos del paciente dentro de estos cuidados, y siempre facilitando una información sensata, clara y trasparente a los familiares.
Conflicto de interesesLos autores no tienen conflictos de interés.
A la Dra. Roser Deulofeu y a la Organización Catalana de Trasplantes (OCATT) por su respaldo y su colaboración en el diseño inicial del estudio y en la elaboración de la plataforma digital.