INTRODUCCIÓN
El síndrome de Lemierre, también conocido como "sepsis postangina", es una entidad rara en la actualidad. Aunque ya existían referencias a principio de siglo, fue Lemierre el primero en darlo a conocer en 19361. Se trata de un proceso infeccioso, frecuentemente mortal en la era preantibiótica, que afecta principalmente a adolescentes y adultos jóvenes previamente sanos, aunque tiene un segundo pico de incidencia en ancianos.
Clínicamente se considera una sepsis secundaria a infecciones de la cavidad oral y vías respiratorias altas. Posteriormente aparece una tromboflebitis de la vena yugular interna (VYI) desde donde se originan embolias sépticas que pueden extenderse a diversos órganos.
El diagnóstico se realiza mediante la identificación del microorganismo en el hemocultivo, pero esto no siempre es tan sencillo debido al crecimiento más rápido de otras bacterias aerobias.
El tratamiento antibiótico óptimo no está totalmente claro debido a la existencia de cepas productoras de beta-lactamasas.
CASO CLINICO
Niña de 13 años trasladada a la Unidad de Cuidados Intensivos Pediátricos (UCIP) por presentar, desde 11 días antes, una neumonía con mala evolución clinicorradiológica a pesar del tratamiento antibiótico con cefotaxima.
En los días previos a su ingreso en el hospital de origen presentó un cuadro de faringoamigdalitis aguda que cursó con fiebre alta, decaimiento y adenopatías submandibulares múltiples.
La exploración mostraba mediano estado general, palidez de piel y mucosas, temperatura axilar de 38,5º C y faringe normal. No se palpaban adenopatías cervicales. Cardiocirculatorio: tonos rítmicos a 100 lpm y presión arterial de 96/55 mmHg. Respiratorio: hipoventilación en campo medio e inferior izquierdo, con una frecuencia respiratoria de 28 rpm y SaO2 del 100% respirando aire ambiental. Abdomen: blando, sin masas ni megalias. Neurológico: sensorio libre; signos meníngeos negativos; pares craneales normales.
Entre los exámenes complementarios destacaba una leucocitosis de 14.900 células/µl, con importante neutrofilia (87%), anemia normocítica normocrómica (hemoglobina 7,1 g/dl) y trombocitosis reactiva (625.000 plaquetas/µl). Velocidad de sedimentación globular (VSG), 106 mm/h. Proteína C reactiva (PCR): 12 mg/dl.
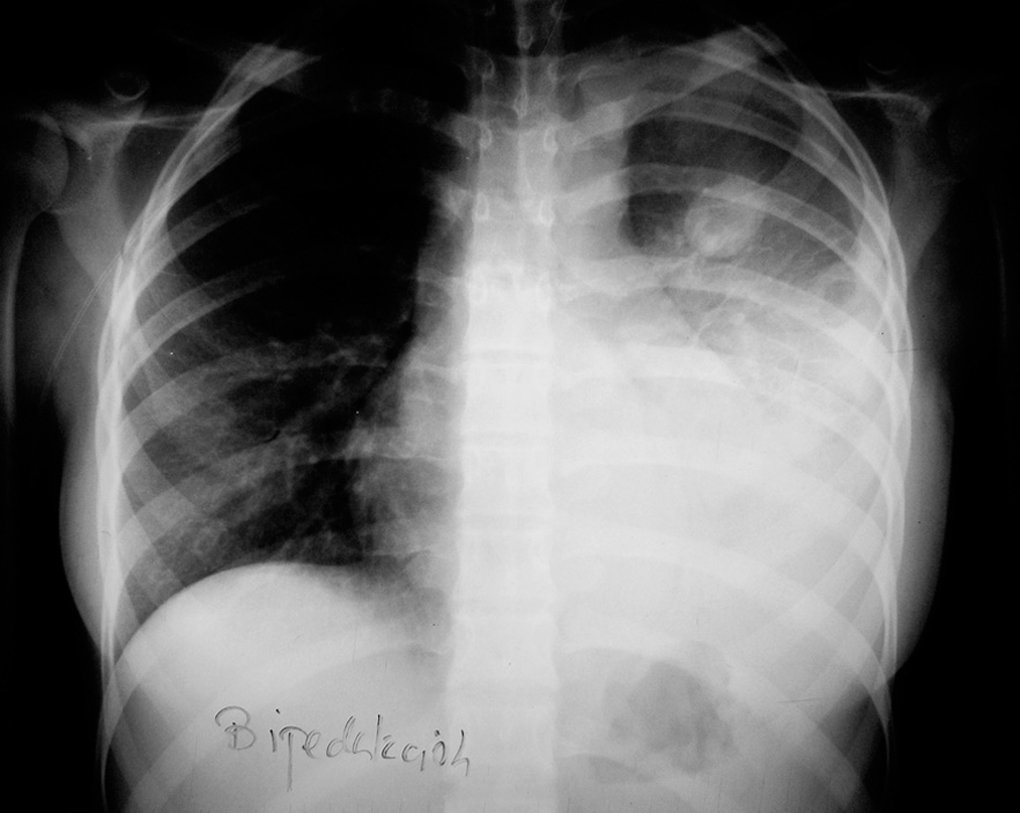
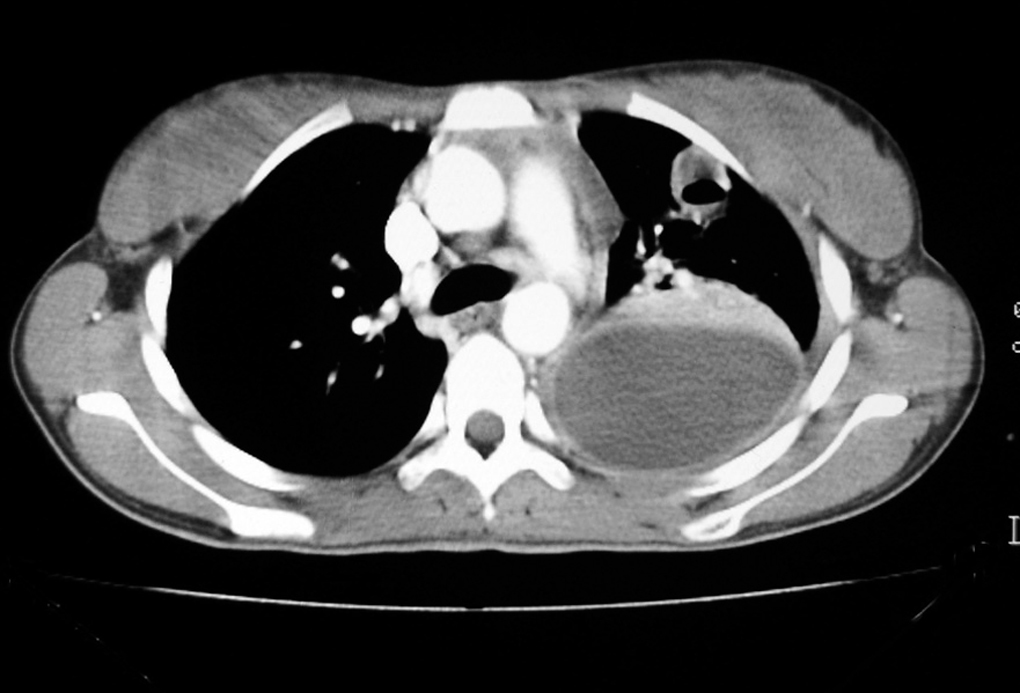
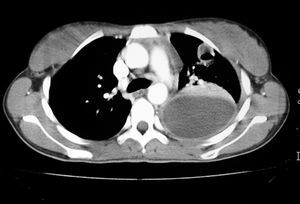
En la radiografía y tomografía axial computarizada (TAC) de tórax (figs. 1 y 2) se apreciaba una imagen redondeada y cavitada en lóbulo superior izquierdo, con un extenso derrame pleural del mismo lado.
Figura 1. Radiografía de tórax: se observa colección pleural izquierda asociada a condensación con broncograma aéreo en lóbulo inferior izquierdo. Nódulo cavitado en lóbulo superior izquierdo.
Figura 2. Tomografía axial computarizada (TAC) pulmonar: se observa colección pleural izquierda con engrosamiento pleural difuso que ocasiona atelectasia del parénquima pulmonar adyacente. Nódulo cavitado con pequeño nivel hidroaéreo en lóbulo superior izquierdo.
A su ingreso en nuestra UCIP se inició tratamiento antibiótico con imipenem y teicoplanina ante la sospecha de neumonía estafilocócica o por anaerobios, y se colocó un drenaje torácico para evacuar el derrame. Al segundo día del ingreso se recibieron dos hemocultivos positivos para F. necroforum, sustituyéndose la teicoplanina por metronidazol, que se mantuvo durante 4 semanas.
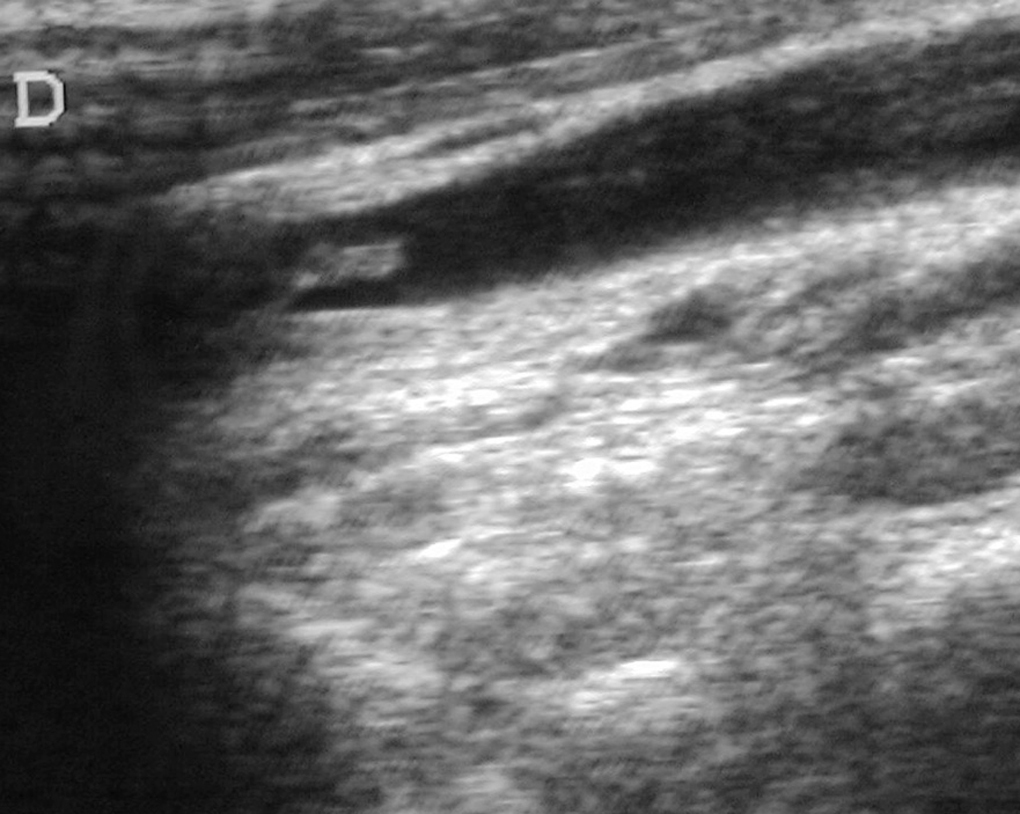
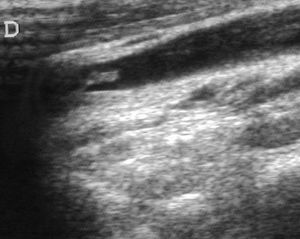
Ante la sospecha de síndrome de Lemierre, se realizó ecografía doppler cervical que evidenció una trombosis de la VYI derecha (fig. 3), confirmándose el diagnóstico y añadiéndose al tratamiento heparina de bajo peso molecular.
Figura 3. Ecografía cervical: sección longitudinal laterocervical derecha mostrando vena yugular interna derecha ocupada por formación ecogénica con extremo libre flotante.
El resto de estudios, incluyendo ecocardiografía, ecografía abdominal, TAC craneal, Mantoux, radiografía de senos y estudio inmunológico, fueron normales. El cultivo y la baciloscopia de líquido pleural fueron asimismo negativos.
Se dio de alta hospitalaria a los 30 días, completando tratamiento ambulatorio con metronidazol durante un mes más. En la actualidad se encuentra asintomática y sin secuelas.
DISCUSION
El síndrome de Lemierre fue en el pasado una entidad mucho más común y con frecuencia fatal, sin embargo, el uso generalizado de antibióticos en las infecciones amigdalares la han convertido en una enfermedad rara y poco conocida, por lo que algunos autores la han denominado "la enfermedad olvidada"2-5.
El agente causal en la mayor parte de los casos es el Fusobacterium necrophorum, microorganismo anaerobio gramnegativo, aunque se han descrito otros gérmenes capaces de provocar esta enfermedad (F. nucleatum, F. prausnitzii, Bacteroides sp., Streptococus sp., Eikenella corrodens). Con menor frecuencia la enfermedad es causada por más de un microorganismo, en forma de una coinfección por bacterias aerobias y anaerobias6,7.
El F. necrophorum ha demostrado ser sensible in vitro a antibióticos de amplio espectro incluyendo penicilina, cloramfenicol, clindamicina y metronidazol; es resistente a los aminoglucósidos, aztreonam y trimetropin sulfametoxazol, y presenta una sensibilidad variable a cefalosporinas, eritromicina y tetraciclina8.
La patogenia no está bien definida. El Fusobacterium forma parte de la flora normal de la cavidad oral, gastrointestinal y del aparato genital femenino; la alteración de las barreras mucosas facilita la proliferación del microorganismo, que puede alcanzar el torrente sanguíneo y provocar embolismos sépticos.
Aunque existen pocos datos epidemiológicos, en un estudio prospectivo danés, realizado entre los años 1990-19959, la incidencia del síndrome de Lemierre causado por el F. necrophorum fue de 0,8/ 1.000.000 de habitantes por año, observándose el doble de casos en los últimos tres años del estudio. El aumento de la incidencia podría deberse al uso más restrictivo de los antibióticos, a un cambio en la sensibilidad del microorganismo o a un incremento en el uso de fármacos como los macrólidos o algunas cefalosporinas de segunda y tercera generación, que carecen o tienen una actividad variable frente a este germen10,11.
El cuadro clínico viene precedido típicamente por una faringitis, amigdalitis o absceso periamigdalino con fiebre elevada, que se sigue de una trombosis de la VYI. El paciente suele presentar dolor alrededor del ángulo de la mandíbula o paralelo al músculo esternocleidomastoideo. Los émbolos sépticos desde la VYI facilitan la diseminación metastásica de la enfermedad y la formación de abscesos en pulmón, hígado y articulaciones. Los abscesos pulmonares pueden llevar a insuficiencia respiratoria aguda, que en ocasiones precisa soporte ventilatorio12.
Su diagnóstico se confirma con el aislamiento del F. necrophorum; no obstante, ante un cuadro clínico compatible el tratamiento se debe iniciar de forma precoz ya que la demora del mismo ensombrece mucho el pronóstico. La tabla 1 muestra los criterios diagnósticos12,13. La radiología de tórax suele mostrar múltiples opacidades mal definidas, que en ocasiones se cavitan y que reflejan la llegada de émbolos sépticos. Aunque el derrame pleural es común, el empiema es infrecuente. La TAC pulmonar con contraste muestra las cavitaciones precozmente así como su relación con los vasos pulmonares distales. La TAC cervical es también muy sensible para demostrar las trombosis de la VYI, venas periamigdalares, parafaríngeas e intratorácicas; aunque con menor rendimiento diagnóstico, la ecografía supone una buena alternativa debido a su accesibilidad y bajo coste. La resonancia magnética nuclear puede utilizarse en casos de alergia a contrastes iodados y cuando la ecografía no ha sido de utilidad para detectar trombosis, con la ventaja añadida de no irradiar al paciente14.
El tratamiento antibiótico óptimo no está claro ya que, aunque el F. necrophorum suele ser sensible a penicilina, clindamicina o metronidazol, se han comunicado fallos en el tratamiento con penicilina probablemente debidos a la producción de beta-lactamasas. Las recomendaciones recientes incluyen la combinación de un agente resistente a beta-lactamasas y metronidazol o monoterapia con ticarcilina-clavulánico o imipenem10.
El tratamiento debe mantenerse al menos 6 semanas a dosis altas, no recomendándose cambios prematuros de antibióticos10,15. El papel de la anticoagulación es controvertido ya que no se han realizado estudios controlados que confirmen su eficacia. La ligadura de la VYI puede ser considerada en pacientes con sepsis incontrolada o fallo respiratorio severo causado por émbolos pulmonares repetidos.
La mortalidad se ha reducido del 90% en la era preantibiótica a un 4%-18% en la actualidad, estando en relación con la sepsis y el compromiso pulmonar10,12.
Queremos llamar la atención sobre una patología grave que por su baja incidencia puede tardar en ser diagnosticada. La presentación clínica típica caracterizada por émbolos sépticos pulmonares con o sin otras infecciones metastásicas, tras un episodio de faringoamigdalitis aguda, debe hacernos pensar en esta enfermedad, especialmente si se asocia a tromboflebitis de la VYI. La utilización de penicilina o amoxicilina en casos de sospecha de faringoamigdalitis bacteriana, en lugar de nuevos antibióticos con actividad variable frente a F. necrophorum, puede disminuir la incidencia de esta grave enfermedad.
Conflicto de intereses. Los autores no hemos recibido ayuda económica alguna para la realización de este trabajo. Tampoco hemos firmado ningún acuerdo por el que vayamos a recibir beneficios u honorarios por parte de alguna entidad comercial. Por otra parte, ninguna entidad comercial ha pagado a fundaciones, instituciones educativas u otras organizaciones sin ánimo de lucro a las que estemos afiliados.