Se atribuye a Platón la frase «si bien buscas, encontrarás», y es aplicable al diagnóstico de la aspergilosis pulmonar en la unidad de cuidados intensivos (UCI). Resulta arriesgado emitir aseveraciones prudentes sobre su incidencia sin preguntarnos antes sobre los métodos diagnósticos aplicados. Por un lado, si no realizamos una búsqueda activa corremos el riesgo de infradiagnosticar esta enfermedad. Por otro, si la búsqueda es dirigida podemos marrar diagnosticando colonizaciones como infecciones.
La mayoría de estudios sobre incidencia de aspergilosis se han realizado analizando bases de datos retrospectivas cuyo objetivo primario no era la búsqueda de esta etiología. A pesar de que hay autores que documentan una baja incidencia de aspergilosis en el paciente crítico1,2, esta conclusión puede resultar errónea si asumimos que dichos estudios se han basado exclusivamente en el aislamiento en una muestra respiratoria de especies de Aspergillus. En un reciente estudio multicéntrico europeo en pacientes intubados con neumonía causada por Influenza documentan una incidencia superior al análisis realizado por Claveria L et al.3 que puede estar en parte explicado porque analizaron pacientes con más de 48h de ventilación mecánica4, y no en las primeras 24h de ingreso en la UCI.
En el otro extremo observamos como los estudios que han realizado una búsqueda activa de aspergilosis la incidencia documentada puede ser hasta 20 veces superior5, el diagnóstico microbiológico no quedó exclusivamente circunscrito al aislamiento del hongo en el cultivo añadiendo la determinación de biomarcadores como galactomanano en la muestra de lavado broncoalveolar y en suero.
El diagnóstico de aspergilosis pulmonar en el paciente crítico es actualmente un desafío no resuelto para el clínico. En primer lugar, porque los criterios clínicos y radiológicos pueden remedar a otras etiologías. Es fundamental tener una sospecha previa de la enfermedad y apoyarnos en una estrategia de diagnóstico microbiológico dirigida.
Reducir los criterios al aislamiento del hongo en la muestra respiratoria conduce sin duda al riesgo de infradiagnosticar la aspergilosis. Se consideran el método de diagnóstico microbiológico de referencia, y suponen el criterio de entrada contemplado en los criterios ASPICU propuestos por Blot SI et al.6. Estos criterios se propusieron para identificar mejor al paciente crítico que los recomendados por la European Organization for Research and Treatment of Cancer/Mycosis Study Group (EORTC/MSG)7. Sin embargo, sabemos que el crecimiento del hongo en los cultivos es lento, y pueden suponer un retraso en el inicio de tratamiento hasta resultar positivos, tienen una baja sensibilidad que es menor del 65%, puede alterarse por contaminaciones, y además resultar falsos negativos si está recibiendo tratamiento antifúngico. La principal ventaja de los cultivos sería la de poder realizar antifungograma para conocer la sensibilidad in vitro a antifúngicos.
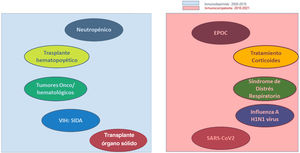
Además, hemos de destacar la importancia que tiene la calidad de la muestra respiratoria, en los estudios anteriormente citados que demuestran tan baja incidencia de aspergilosis el aspirado traqueal fue la muestra respiratoria mayoritariamente utilizada. Esto sin duda es un factor clave, ya que contribuye a una estrategia de búsqueda de menor calidad, la toma de muestras respiratoria no invasiva tiene la limitación de no abarcar al área de parénquima pulmonar afectado, siendo actualmente el lavado broncoalveolar broncoscópico la muestra de mayor calidad indicada tras la biopsia pulmonar cuya indicación en pacientes críticos suele ser anecdótica. La realización de fibrobroncoscopia diagnóstica en enfermos en ventilación mecánica es una técnica segura con apenas complicaciones cuando es realizada por personal experimentado8. Claverias L et al.3 concluyen en su estudio que en pacientes de riesgo debería implementarse una estrategia de búsqueda activa de aspergilosis pulmonar. En la figura 1 detallamos el perfil clínico de pacientes que ingresan en la UCI que podemos considerarlos de riesgo, en apenas una década han aparecido perfiles diferentes al clásico que suponía el paciente neutropénico y/o inmunodeprimido. Es importante recalcar que tener esta condición no es exclusiva para presentar una aspergilosis pulmonar, y por tanto la sospecha ha de ser independiente del estado inmunitario del paciente crítico.
Por tanto, hemos de contemplar estos nuevos perfiles de pacientes sin inmunodepresión, y considerar que en ausencia de neutropenia la expresividad clínica y radiológica de la enfermedad varían al igual que los métodos de diagnóstico microbiológico como la determinación de galactomanano en suero, que es menos útil9.
Si aspiramos a lo óptimo, y optamos a realizar una búsqueda activa de la aspergilosis en la UCI hemos de recomendar contemplar los perfiles de riesgo demostrados, indicar la realización de una muestra respiratoria con rentabilidad diagnóstica, que en orden decreciente de calidad serían lavado broncoalveolar broncoscópico que permite la toma de una muestra de tracto respiratorio inferior dirigida, mini-lavado broncoalveolar, cuya mayor ventaja es que no precisa de personal experimentado para su realización, aunque con el inconveniente de ser una técnica ciega no dirigida, y el aspirado traqueal cuya sensibilidad diagnóstica ha mostrado ser inferior al proceder de vías respiratorias altas. Por último, no restringirse al cultivo microbiológico, siendo necesario ampliar el estudio añadiendo la determinación de biomarcadores como la determinación de galactomanano en lavado broncoalveolar en la muestra respiratoria10.
Ampliando estos criterios de búsqueda, utilizando todos los recursos disponibles en cada centro: tinción de la muestra en fresco, cultivo, determinación de biomarcadores, ensayo de flujo lateral y determinación de PCR, podremos iniciar tratamiento precozmente11.
La situación clínica ha de determinar si iniciar o no un tratamiento antifúngico, pero en enfermos críticos con necesidad de soporte ventilatorio invasivo y alteración del intercambio gaseoso e hipoxemia hemos de plantear tratar para combatir de esta forma la alta mortalidad descrita actualmente. El resultado positivo en alguna de las pruebas microbiológicas recomendadas en un enfermo sin hipoxemia, con favorable evolución clínica y en vías de desconexión del respirador puede conducirnos a plantear que se trata de una colonización y evitar la administración de antifúngicos.
Será interesante conocer si implementando estas estrategias de búsqueda activa de la aspergilosis pulmonar en la UCI se producirá un cambio o no en la incidencia de esta grave complicación infecciosa. La variabilidad en la incidencia descrita en la literatura nos obliga a asumir que la investigación se compone de errores metodológicos que han de marcar el camino hacia el conocimiento. Para conocer la incidencia real han de diseñarse estudios de seguimiento descriptivos longitudinales y prospectivos que contemplen todo el arsenal diagnóstico disponible.
FinanciaciónEstudio no financiado.