La sepsis es una entidad sindrómica de elevada prevalencia y mortalidad. Su manejo está estandarizado y tiene una eficacia dependiente del tiempo. Sin embargo, el manejo de los pacientes con sepsis es complejo. La heterogeneidad de las formas de presentación puede dificultar su detección y manejo, así como las diferencias en formación, competencias o disponibilidad de recursos sanitarios. La Comisión Asesora para la Atención al PAciente con Sepsis (CAAPAS), formada por 7 sociedades científicas, el Sistema de Emergencias Médicas (SEM) y el Servei Català de la Salut (CatSalut), han desarrollado en Catalunya el Código Sepsis Interhospitalario (CSI). El objetivo general del CSI es facilitar la detección precoz, la atención inicial y la coordinación interhospitalaria para optimizar el tratamiento de los pacientes con sepsis o shock séptico en formato código de riesgo vital, de forma homogénea a lo largo de todo el territorio catalán.
Sepsis is a syndromic entity with high prevalence and mortality. The management of sepsis is standardized and exhibits time-dependent efficiency. However, the management of patients with sepsis is complex. The heterogeneity of the forms of presentation can make it difficult to detect and manage such cases, in the same way as differences in training, professional competences or the availability of health resources. The Advisory Commission for Patient Care with Sepsis (CAAPAS), comprising 7 scientific societies, the Emergency Medical System (SEM) and the Catalan Health Service (CatSalut), have developed the Interhospital Sepsis Code (CSI) in Catalonia (Spain). The general objective of the CSI is to increase awareness, promote early detection and facilitate initial care and interhospital coordination to attend septic patients in a homogeneous manner throughout Catalonia.
La sepsis es un síndrome inducido por un proceso infeccioso que provoca una disregulación de la respuesta inflamatoria con resultado de disfunción orgánica aguda o agudizada. Las sepsis que cursan con hipotensión que no responde a la reposición de volumen, lactacidemia o que requieren fármacos vasoactivos para mantener la perfusión tisular se denominan shock séptico. Su detección se basa en la exploración física basada en la valoración de la repercusión sistémica de la infección. Su severidad es estratificable en base al número y/o grado de afectación de los órganos afectados. La escala SOFA se recomienda como elemento descriptivo del grado de severidad1.
La incidencia de sepsis aumenta progresivamente en los países industrializados y se podría situar entre 200 y 400 casos por 100.000 habitantes y año2-4. El coste asociado al manejo de la sepsis grave depende de diversos factores, aumentando de forma exponencial con el número de órganos que fracasan5. Su letalidad está alrededor del 20-30%, y está afectada por factores no modificables (características del paciente, foco de infección, microorganismo responsable) y por factores modificables, siendo los más importantes el tiempo en restaurar la perfusión tisular y la adecuación en el manejo del foco séptico (tiempo hasta el inicio del tratamiento antibiótico, adecuación de la cobertura empírica y drenaje, si precisa, del foco séptico)6-8.
Sin embargo, la existencia de protocolos para la optimización del manejo de cualquier patología es una condición necesaria, pero no suficiente9, siendo precisa en el caso de patologías de diagnóstico o manejo complejo, o ante la necesidad de coordinar diferentes recursos asistenciales, diseñar estrategias de implementación para favorecer su aplicación en la práctica clínica habitual. Debido a la elevada incidencia y morbimortalidad asociada a la sepsis, a la existencia de guías estandarizadas en cuanto al diagnóstico y manejo de la sepsis10, y a la relación entre la precocidad en el tratamiento y el pronóstico funcional y vital11-16, debemos acordar que el manejo de la sepsis cumple criterios de «código de riesgo vital». Además, en el caso del manejo de los pacientes sépticos, los recursos (humanos, competenciales o tecnológicos) necesarios para el diagnóstico, manejo del foco séptico y soporte avanzado del fracaso de órganos (especialmente el hemodinámico, la ventilación mecánica y la hemofiltración) pueden no estar disponibles en todos los centros que atienden a pacientes agudos, por lo que existe la necesidad de coordinación entre diferentes niveles asistenciales. La necesidad de mantener el concepto de tiempo-dependencia en el manejo del fracaso multiorgánico de los pacientes con sepsis hace imprescindible implementar también estrategias para la coordinación interhospitalaria.
La sepsis en Catalunya. Comisión Asesora para la Atención al PAciente con Sepsis (CAAPAS). Objetivos del Código SepsisCatalunya tiene una población aproximada de 7,5 millones de habitantes. En Catalunya, la sepsis afectó entre el año 2008 y el 2012 prácticamente a 80.000 pacientes, con un promedio de más de 16.000 pacientes/año, mostrando un incremento anual continuo5. De estos, se estima que hasta un 25% pueden requerir atención en Unidades de Medicina Intensiva (UCI). Según Almirall et al., en un estudio prospectivo de base poblacional, la sepsis de adquisición comunitaria provoca 47 ingresos en UCI/100.000 habitantes/año y en relación con su estancia hospitalaria supone una ocupación de 2 camas/día/100.000 habitantes17.
El modelo sanitario catalán tiene algunas diferencias respecto a otros modelos del estado español. Una de estas diferencias es que un número importante de camas de hospitalización se hallan ubicadas en hospitales comarcales, con un volumen de atención en urgencias muy elevado, y por lo tanto con una gran capacidad de detección de casos. Sin embargo, no disponen de todos los recursos humanos o tecnológicos para el manejo de los estados más evolucionados o graves de la sepsis. Un 40% de los hospitales catalanes no disponen de UCI para pacientes adultos, mientras que solo existen 5 UCI pediátricas en todo el territorio.
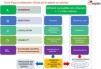
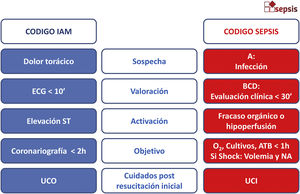
Durante la primera década del siglo XXI, el Servei Català de la Salut (CatSalut) había implementado 3 códigos de riesgo vital: el código infarto, el código politrauma y el código ictus. En sepsis, diferentes hospitales y algunos grupos de investigación estaban trabajando en Catalunya circuitos asistenciales y recursos docentes para mejorar la atención al paciente con sepsis grave18-20. A raíz de estas iniciativas, y por mediación de la Societat Catalana de Medicina Intensiva i Crítica (SOCMIC), se inician los contactos para generar un «Código Sepsis Interhospitalario», al uso de los códigos de riesgo vital ya existentes (fig. 1), que proporcione una cobertura homogénea a todos los pacientes del Sistema Sanitario independientemente del lugar donde se produzca la primera atención. Se crea el Grupo de Trabajo de Sepsis por parte de la SOCMIC en el año 2012, que evoluciona hasta la formación de la Comisión Asesora para la Atención al PAciente con Sepsis (CAAPAS) en el año 2014. Esta Comisión estaba conformada por 7 sociedades científicas catalanas representativas de los ámbitos de Intensivos (SOCMIC), Urgencias (Sociedad Catalana de Medicina de Urgencias y Emergencias [SOCMUE]), Medicina Interna (Sociedad Catalanobalear de Medicina Interna [SCMI]), Cirugía (Sociedad Catalana de Cirugía), Infecciosas (Sociedad Catalana de Enfermedades Infecciosas y Microbiología Clínica [SCMIiMC]), Medicina Familiar (Sociedad Catalana de Medicina Familiar y Comunitaria [CAMFIC]) y Pediatría (Sociedad Catalana de Pediatría), avaladas por sus juntas de gobierno con la colaboración del SEM (Servicio de Emergencias Médicas, encargado de la atención extrahospitalaria emergente y el traslado interhospitalario de los pacientes críticos), y con representación del CatSalut, el sistema de salud catalán.
Posteriormente, el Parlament de Catalunya, sensible con el impacto social que genera la sepsis, emite el día 19 de junio de 2015 la resolución 1069/X reconociendo la sepsis como una entidad de riesgo vital e insta al Gobierno de la Generalitat a, textualmente, «definir y coordinar las medidas necesarias para la aplicación del Código Sepsis Grave durante el año 2015 como un nuevo código de emergencias médicas»21. Las recomendaciones de la CAAPAS han sido asumidas por CatSalut para estructurar el CÓDIGO SEPSIS («Codi Sèpsia»), publicado como instrucción operativa para todos los hospitales del sistema público catalán (Instrucción 11/2015 de 8 de octubre de 2015)22.
Objetivos del «Codi Sèpsia» de CatalunyaEn el ámbito del paciente con un proceso infeccioso, podríamos diferenciar 3 escenarios clínicos diferentes que, por lo tanto, configuran un contexto asistencial diferente: «infección», «sepsis» y «shock séptico». La reciente revisión de la definición de sepsis recomienda valorar de forma objetiva el grado de disfunción multiorgánica mediante la escala de valoración SOFA23, y se recomienda su uso como elemento descriptivo de la repercusión sistémica. Definimos «sepsis» como aquel subgrupo de infecciones que provocan al menos una insuficiencia orgánica aguda (SOFA≥2) o agudizada (incremento del SOFA basal ≥2). Definimos «shock séptico» como aquella infección que a pesar de una adecuada reanimación con sueros requiere fármacos vasoactivos para revertir una situación de hipoperfusión tisular, hipotensión o lactacidemia. Definimos como fracaso multiorgánico aquel escenario en que al menos dos categorías SOFA tienen una puntuación de 2 o superior.
El objetivo general del «Codi Sèpsia» (CS) es facilitar la detección precoz, la atención inicial y la coordinación interhospitalaria para optimizar el tratamiento de los pacientes con sepsis o shock séptico en formato código de riesgo vital. El CS propone un manejo secuencial tiempo-dependiente con coordinación interhospitalaria para los pacientes sépticos (tabla 1).
Diferencias entre sistemáticas propuestas para la valoración de la repercusión sistémica de las infecciones en adultos
| Código Sepsis | qSOFA28 | NEWS30 | SIRS29 | |
|---|---|---|---|---|
| A: Anamnesis | Sd. Infeccioso | |||
| B: Breathing/Respiratorio | Taquipnea (sospecha) | Taquipnea | Taquipnea | Taquipnea |
| Hipoxia (activación) | Hipoxia | |||
| Aporte de oxígeno | ||||
| C: Circulation/Circulatorio | Taquicardia (sospecha) | Taquicardia | Taquicardia | |
| Hipotensión (activación) | Hipotensión | Hipotensión | ||
| D: Disability/Neurológico | Alteración nivel conciencia (sospecha) | Alteración nivel conciencia | Alteración nivel conciencia | |
| Meningismo (activación) | ||||
| E: Elevación biomarcadores | Lactato | Leucocitosis | ||
| Otros | Temperatura | Temperatura |
Los objetivos específicos con:
- -
Sensibilizar y formar al personal asistencial en la importancia de la detección y el manejo precoz de la sepsis grave.
- -
Consensuar criterios para la detección y la atención precoz a los pacientes con sepsis grave.
- -
Estandarizar el manejo inicial (reanimación), identificando criterios de severidad y mala evolución.
- -
Validar los criterios y circuitos que estructuren la coordinación interhospitalaria con la finalidad de ubicar el paciente en el nivel asistencial adecuado.
- -
Hacer seguimiento, análisis y feedback de los indicadores epidemiológicos, de actividad, proceso y resultado.
En el manejo de la sepsis identificamos 4 fases a aplicar tras la detección de un paciente séptico:
- -
Activación del código.
- -
Control del foco-reanimación.
- -
Soporte órgano-específico.
- -
Resolución del episodio.
Tiene como objetivo facilitar la identificación precoz por parte del personal sanitario de los signos sugestivos de disfunción de órganos en aquellos pacientes con una historia clínica compatible con infección. Requiere un soporte tecnológico mínimo y puede iniciarse en el lugar donde se encuentra el paciente, sea en el ámbito hospitalario o extrahospitalario.
En todos los pacientes con un proceso infeccioso se debería evaluar clínicamente la repercusión sistémica. Dada la controversia actual sobre las formas de optimizar la valoración de la presencia o riesgo de sepsis en una infección24-27, de la necesidad de UCI o del riesgo de mortalidad, y a fin de respetar la idiosincrasia de cada centro, la CAAPAS propuso en su día una valoración de la repercusión sistémica de la infección en formato A+BCD+E (tanto para la valoración del adulto como del paciente pediátrico) y que es compatible tanto con la valoración clínica del SOFA, qSOFA28, SIRS29 o EWS30 (fig. 1). El diagnóstico de sepsis debería ser eminentemente clínico. No debe esperarse a los resultados de la analítica sanguínea para la activación del CS, dado que pueden retrasar innecesariamente el inicio de las maniobras. La propuesta es que se valore si existe o no repercusión sistémica en cada paciente que presenta una anamnesis compatible con infección, primero clínicamente, y solo si es necesario, posteriormente mediante biomarcadores de riesgo.
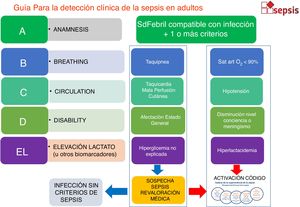
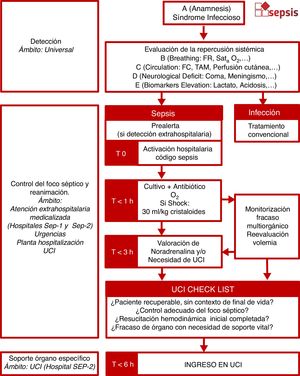
Se propone (fig. 2):
Algoritmo de detección del paciente séptico adulto. Detección clínica basada en la valoración cardiovascular, respiratoria y neurológica. Se consideran la taquicardia y la taquipnea respuesta adaptativa que puede preceder a la aparición de fallo orgánico. Se han suprimido en lo posible los valores numéricos dado que no hay consenso sobre cuáles son los niveles de corte en las diferentes escalas que podrían utilizar los diferentes centros. Ante la evidencia de fallo orgánico permite activar el código sepsis. En caso de detección extrahospitalaria se sugiere prealertar a los responsables del cribado en la puerta de urgencias (prealerta de sepsis).
A. Anamnesis: historia clínica y/o exploración física compatible con una infección.
+
B. Breathing/Respiratorio: valoración de la disfunción respiratoria.
C. Circulation/Circulatorio: valoración de la disfunción circulatoria.
D. Dissability/Focalidad neurológica: valoración de meningismo o alteraciones del nivel de consciencia.
+/−
E. Evaluación bioquímica: lactato/otros biomarcadores de hipoperfusión tisular o fallo orgánico (en entornos hospitalarios).
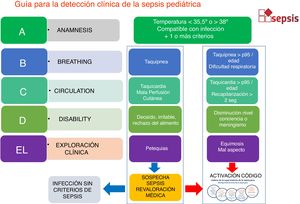
En el paciente pediátrico (fig. 3) se enfatizan algunas especificidades, como los signos de mal estado general, la aparición de petequias o la mala perfusión cutánea.
Algoritmo de detección del paciente séptico pediátrico. Detección clínica basada en la valoración cardiovascular, respiratoria y neurológica. Ante la evidencia de fallo orgánico permite activar el código sepsis. En caso de detección extrahospitalaria se sugiere prealertar a los responsables del cribado en la puerta de urgencias (prealerta de sepsis).
Se procede a la activación del CS ante un paciente con sepsis o shock séptico (anamnesis compatible con un síndrome infeccioso más al menos una disfunción de órgano [B, C o D] y/o hiperlactacidemia inicial), atendido en entorno hospitalario, que no está en la fase final de la vida y en el que no se plantea limitaciones para la utilización de las técnicas de soporte vital. Se debe individualizar el tratamiento de la sepsis y la decisión de atender en formato código a aquellos pacientes que disponen de voluntades anticipadas contrarias a recibir los tratamientos de control de foco o soporte vital inherentes al manejo del paciente séptico, pacientes con deterioro cognitivo severo o pacientes en fase terminal de su vida o enfermedad, sin que eso vaya en detrimento de las medidas de atención básicas a todos los pacientes (administración de oxígeno, reposición de la volemia, administración de antibióticos, etc.).
Aunque la activación administrativa del código es hospitalaria, existe la prealerta extrahospitalaria de sepsis, que se emitirá desde Equipos de Atención Primaria, dispositivos de atención continuada y/o urgente extrahospitalarios, Unidades de Atención Básica, Intermedia o Avanzada del SEM, etc., que atiendan a pacientes con infección y cumplan los criterios consensuados. En la medida de lo posible se iniciarán las medidas de reanimación. En este caso, el SEM trasladará a los pacientes tributarios de ser un CS con la prioridad ajustada a la gravedad al hospital de proximidad que pueda confirmar el diagnóstico clínico, la correspondiente activación del CS, el diagnóstico de laboratorio y las actividades de la fase de reanimación (control de foco, administración de volumen, monitorización, etc.). El SEM podrá trasladar a los pacientes a un centro de nivel asistencial superior cuando la evolución clínica del paciente permita identificar la necesidad de la atención inmediata en UCI, siguiendo criterios de riesgo vital.
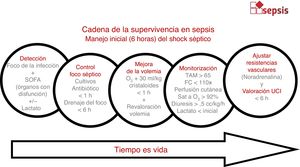
Fase 2. Control del foco y recuperación hemodinámicaEl control del foco y la recuperación inicial se basan en un paquete de 5 pasos (fig. 4):
- -
Paciente ya identificado como susceptible de ser tratado en formato código.
- -
Administración precoz de antibiótico empírico eficaz para la reducción de la carga bacteriana (conjuntamente con el drenaje del foco si es necesario).
- -
La recuperación de la perfusión tisular de oxígeno mediante la recuperación de la volemia y la administración de oxígeno.
- -
La monitorización de la respuesta del paciente a las medidas iniciales.
- -
La valoración (clínica y analítica) de las disfunciones orgánicas y la valoración de la necesidad de un estadio asistencial superior (UCI).
Cadena de manejo en la sepsis. Paquete de acciones a implementar tras la detección de un paciente con una sepsis: administración inmediata de oxígeno, toma de hemocultivos, analítica sanguínea y administración de antibiótico. Si signos de hipoperfusión, administrar 30ml de cristaloides por kg de peso en 1h y monitorizar el estado de volemia en caso de no respuesta. Valorar la administración de noradrenalina en pacientes con signos de hipoperfusión profunda o que no responden a las cargas de volumen iniciales. Valorar el traslado a UCI ante la falta de respuesta a las maniobras iniciales.
El elemento fundamental del CS es la identificación del caso, la administración de antibioterapia empírica y el inicio de las maniobras para restablecer la perfusión tisular. Por ello todos los centros han de disponer de un protocolo de tratamiento antibiótico empírico específico para CS, validado en la comisión de infecciones del centro correspondiente, y un protocolo de manejo hemodinámico acorde a los recursos y habilidades de cada centro, basado en las recomendaciones actualizadas de la Surviving Sepsis Campaign. El ingreso de los pacientes en UCI (desde el centro donde el paciente está ingresado) no es más que una parte del proceso asistencial, que implica el fracaso de las maniobras de reanimación o una severidad que condiciona el uso de técnicas de soporte vital.
La reanimación y el control del foco se deben adecuar al estado clínico del paciente. En caso de shock séptico se ha de considerar una emergencia vital, por lo que tiene como objetivos durante la primera hora de atención restaurar la correcta perfusión tisular de oxígeno, completar el diagnóstico sindrómico, la extracción de las muestras sanguíneas para cultivos y la administración de la antibioterapia empírica precoz, preferentemente durante la primera hora de atención31. La colocación de accesos vasculares venosos centrales o la realización de las pruebas de imagen pertinentes no deben demorar las maniobras de reanimación y control del foco32. Recomendamos la monitorización del paciente séptico con controles durante al menos las 6 primeras horas, tanto desde un punto de vista clínico (cardiovascular, respiratorio y neurológico) como analítico. Es mandatorio el control analítico del lactato si el inicial ha sido patológico.
Aunque el acceso venoso óptimo para la administración de fármacos vasoactivos es la luz de una vía central usada en exclusividad para este fin, como en cualquier paciente en shock, no es conveniente demorar el inicio de la noradrenalina hasta la obtención de una vía central, dado que el proceso puede retrasar de forma significativa la recuperación hemodinámica. En este caso sugerimos la utilización de un catéter periférico único insertado en una vena del mayor calibre posible, en la extremidad superior donde no se esté monitorizando la presión arterial de forma no invasiva, limitando en lo posible la movilidad del brazo. Una vez iniciada la noradrenalina, es recomendable no mantenerla por vía periférica por más de 6h dado que aumenta el riesgo de complicaciones33,34.
En el caso de que el control del foco de infección requiera manejo quirúrgico, este se ha de intentar realizar en las primeras 6h si el paciente está en shock séptico. En el paciente séptico sin shock, la decisión quirúrgica debe individualizarse, pero no debería demorarse más de 12h.
En el caso de respuesta parcial o de persistencia de las disfunciones de órganos a pesar de la adecuada reanimación inicial, si el paciente requiere un incremento en la monitorización y/o la aplicación por parte de profesionales entrenados (personal de enfermería y médico) de técnicas diagnósticas y terapéuticas específicas para el manejo de las diferentes disfunciones de órganos y/o inicio de técnicas de soporte órgano-específico (fármacos vasoactivos, ventilación mecánica, técnica substitutiva renal) deberá comentarse el caso a la UCI de referencia (entendida como una unidad acreditada para ofrecer asistencia multidisciplinar continuada a pacientes críticos en un ámbito específico en el que se dispone de los medios funcionales, estructurales y organizativos suficientes) para su ingreso si procede.
Fase 3. Soporte órgano-específico. Traslado a UCIA diferencia del código infarto agudo de miocardio en Catalunya y, a similitud del código ictus, los pacientes no son tributarios de traslado directo a UCI, sino que se deberán comentar con el intensivista de referencia a través del SEM (fig. 5). La derivación del paciente a otro centro de mayor nivel asistencial con UCI se coordinará a través de la Central de Coordinación Sanitaria del SEM con la finalidad de ubicar al paciente en el hospital con el nivel asistencial adecuado. Con el objetivo de optimizar el manejo del paciente, es necesario comunicar y compartir la información necesaria entre el médico responsable del centro emisor y el intensivista de referencia del centro receptor de forma objetiva (que incluye de forma explícita: foco y repercusión sistémica, ausencia de limitaciones del tratamiento de soporte vital, reanimación adecuada, grado de fracaso multiorgánico, necesidad de soporte órgano-específico requerido, etc.) y consensuar las acciones futuras. En caso de indicación, el traslado del paciente se realizará usando una Unidad de Soporte Vital (USVA/USVI) con un nivel de priorización ajustado al estado del paciente, hasta 3h en el de sepsis (fallo de un órgano sin inestabilidad hemodinámica), prioridad cero en el caso del shock séptico o fracaso multiorgánico.
Algoritmo para la coordinación interhospitalaria. La prealerta extrahospitalaria permite avisar al sistema de cribado de urgencias del hospital para preparar el manejo emergente de los pacientes en código sepsis que así lo requieran. El check list de comprobación sugiere 4 de 4 respuestas afirmativas para consensuar el traslado entre los servicios emisores y receptores.
Una vez iniciadas las maniobras de reanimación y control de foco, se consideran criterios para valorar la derivación a UCI:
- 1.
La ausencia de mejora clínica a las 3-6 primeras horas una vez iniciadas las medidas de reanimación en pacientes adultos.
- 2.
La necesidad de soporte órgano-específico de mayor complejidad (ventilación mecánica invasiva, manejo de la inestabilidad hemodinámica, soporte vasoactivo y monitorización cardiovascular avanzada, técnicas de depuración renal, ECMO, etc.).
- 3.
Así mismo, se considera la derivación a un centro de mayor complejidad la falta de recursos para el correcto diagnóstico o el correcto drenaje de foco (drenaje percutáneo, cirugías complejas, etc.) sin que este supuesto pueda significar retraso en el inicio de las maniobras de reanimación hemodinámica.
La resolución del episodio comporta la derivación del paciente al centro hospitalario pertinente, preferentemente el centro emisor, en función de sus requerimientos terapéuticos.
Coordinación interhospitalaria. Niveles asistenciales y flujo de pacientesLa atención adecuada se debe proporcionar en el nivel asistencial que corresponda a las necesidades del paciente y en el tiempo adecuado en función de la severidad del estado clínico. La sectorización del territorio en forma de clústeres o grupos de hospitales coordinados entre ellos facilita la creación de grupos de trabajo y la ordenación de los flujos adecuando los criterios de severidad del paciente con el nivel asistencial que precisa (tabla 2).
Ejemplo de distribución hospitalaria: Clúster hospitalario área Barcelonès Nord/Maresme en el paciente adulto
| Área | Nivel | SEP-2a Referencia | SEP-2b Referencia |
|---|---|---|---|
| Hospital de Calella | SEP-1 | Hospital de Mataró | H. Germans Trias i Pujol |
| Hospital Esperit Sant | SEP-1 | H. Germans Trias i Pujol | H. Germans Trias i Pujol |
| Hospital Municipal de Badalona | SEP-1 | H. Germans Trias i Pujol | H. Germans Trias i Pujol |
| Hospital de Mataró | SEP-2a | Hospital de Mataró | H. Germans Trias i Pujol |
| Hospital Germans Trias i Pujol | SEP-2b | H. Germans Trias i Pujol | H. Germans Trias i Pujol |
SEP-1: hospitales que pueden implementar la fase de detección, activación y reanimación-control de foco. SEP-2: hospitales que pueden implementar la fase de soporte órgano-específico (disponen de UCI), pero que no disponen de logística 24h al día/7 días a la semana para el manejo quirúrgico de determinados focos sépticos. SEP-2b: hospitales SEP-2 (UCI) con dotación para el manejo quirúrgico de todos los focos sépticos 24h al día/7 días a la semana. Todos los niveles incluyen los previos.
Los hospitales de agudos para pacientes adultos se han clasificado en 3 niveles según sus capacidades funcionales:
- -
Los hospitales que disponen de recursos para la fase de reanimación y control de foco se catalogan como SEP-1.
- -
Los hospitales con UCI (fase soporte órgano-específico) se catalogan como SEP-2.
- -
Los centros SEP-2 se consideran SEP-2b si son referencia para el control de foco en condiciones especiales, y son capaces de realizar control quirúrgico de los focos sépticos diferentes al abdominal y partes blandas las 24h del día los 7 días de la semana (control de foco urinario obstructivo, control de foco torácico, neuroquirúrgico, etc.).
- -
Todos los centros SEP-1 y SEP-2 tienen asignados un centro SEP-2b de referencia donde derivar sus pacientes en caso de necesitarlo.
- -
Todos los hospitales engloban su nivel asistencial inferior.
El modelo pediátrico es solapable con algún matiz. Los hospitales de agudos para pacientes pediátricos también se catalogan en 3 niveles:
- -
Los hospitales que disponen de recursos para la fase de reanimación y control de foco se catalogan como SEP-1.
- -
Los hospitales con UCI pediátrica se catalogan como SEP-2a.
- -
Los hospitales SEP-2 se catalogan como 2b si pueden ofrecer tratamiento de soporte con ECMO.
- -
Todos los hospitales engloban su nivel asistencial inferior.
El objetivo del registro es la evaluación de las actuaciones que permitan hacer propuestas de mejora en cada centro y en el conjunto del sistema sanitario para alcanzar los objetivos del proyecto en la implantación del CS. Se proponen dos registros en paralelo:
- -
Registro Automatizado de Datos Administrativos Relacionados con Sepsis (RADAR-Sepsis), a partir de datos obtenidos de la codificación al alta hospitalaria y de la base de datos de comorbilidad del CatSalut. Tiene como objetivo generar un panel para el análisis comparativo de la epidemiología, resultado y consumo de recursos asociado. Permite el feedback de los episodios agregados por áreas sanitarias y hospitales5,34-37.
- -
Registre de Sèpsia i Xoc Sèptic (RSiXS): registro prospectivo alojado en el «Portal de Aplicaciones» del Departament de Salut de la Generalitat de Cataluña desde octubre del 201833. Recoge de forma prospectiva indicadores epidemiológicos, de episodio, proceso, consumo y resultado, para el análisis de la mortalidad evitable en los pacientes sépticos que requieren ingreso en UCI. Se consideran como indicadores claves de proceso los recomendados por la SEMICYUC38, aunque adaptados a las nuevas recomendaciones32:
- ∘
Inicio precoz de la antibioticoterapia en el paciente con sepsis y/o shock séptico en la primera hora.
- ∘
Tratamiento antibiótico empírico adecuado.
- ∘
Reanimación precoz del shock séptico en la primera hora posdetección:
- •
Reposición de 30ml/kg peso.
- •
Administración de noradrenalina si hipotensión refractaria a volemia.
- •
Tiempo de detección a presión arterial media >65mmHg.
El «Codi Sèpsia Interhospitalari» (CSI) propone un modelo organizativo territorial, que permite por un lado respetar la autonomía de cada centro a la hora de gestionar su propio código sepsis, pero que aporta ordenación territorial para facilitar el flujo de pacientes, así como metodologías y criterios consensuados para una más ágil coordinación entre los diferentes actores asistenciales implicados.
FinanciaciónProyecto parcialmente financiado por la Fundació Marató de TV3 (Sepsis Training, Audit and Feedback (STAF) Project; Codi Projecte 201836).
Conflicto de interesesTodos los autores declaran no tener ningún conflicto de interés en el desarrollo del proyecto.
A Emma Bosch por el desarrollo y cesión de los logos del «Código Sepsis».