La disección coronaria espontánea (DCE) es una rara causa de síndrome coronario agudo (SCA). Desde su descripción inicial hace ya 88 años la información disponible sobre esta enfermedad ha sido siempre muy limitada, basada en datos dispersos de una miríada de anecdóticos casos clínicos y de pequeñas series retrospectivas de pacientes. Sin embargo, durante la última década se han producido importantes avances en nuestro conocimiento sobre esta interesante entidad1–3. Actualmente disponemos de nueva información proporcionada por algunas series prospectivas relativamente amplias y por registros bien diseñados organizados a nivel nacional en diferentes países1–5. No obstante, la evidencia científica sobre esta enfermedad todavía sigue siendo muy limitada en comparación con la disponible sobre otras patologías cardiovasculares más frecuentes, y todavía está lejos de poder sustentar una guía de práctica clínica convencional. Sin embargo, el año pasado se publicaron, coordinadamente desde ambos lados del Atlántico, dos importantes documentos de consenso de expertos sobre DCE1,2. Sin duda, estamos ante el inicio de una nueva fase en cuanto al conocimiento de esta entidad que nos debe ayudar a su mejor diagnóstico y tratamiento. Pero ¿qué hemos aprendido en los últimos años sobre la DCE?
La DCE se define como una separación de las capas de la pared arterial coronaria con formación de dos luces1,2. Estas luces pueden estar comunicadas entre sí (luz verdadera y luz falsa) o no (hematoma intramural). Las disecciones coronarias asociadas a una complicación de placa aterosclerótica o iatrogenia vascular no se incluyen en la definición actual de DCE1–5.
En primer lugar, seguimos sin conocer la etiología ni la patofisiología de esta entidad. De hecho, las dos hipótesis clásicas siguen plenamente vigentes: 1) rotura intimal que por aumento de presión condiciona la formación de una luz falsa por extensión y 2) sangrado intraparietal (por rotura de vasa vasorum) con formación de un hematoma intramural, que posteriormente puede evolucionar o no con rotura intimal y comunicación con la luz verdadera1–5. Algunas evidencias recientes podrían apoyar más esta segunda hipótesis (de fuera a dentro). En cualquier caso, el compromiso de la luz verdadera condiciona las manifestaciones isquémicas.
En segundo lugar, sabemos que el perfil clínico más clásico, mujer muy joven, sin factores de riesgo coronario que presenta un infarto agudo de miocardio en relación con un parto, es excepcional. Hemos aprendido que la DCE se presenta fundamentalmente en mujeres de mediana edad (4-5.a décadas) con algún factor de riesgo coronario que sufren un SCA1–5. En la mitad de los pacientes un estrés físico o emocional puede encontrarse como causa precipitante. Desgraciadamente la presentación clínica es indistinguible del SCA secundario a aterosclerosis coronaria aunque el enfoque terapéutico sea muy diferente. La forma periparto es excepcional (<3%) y esta situación parece implicar un peor pronóstico. Por otro lado, las múltiples enfermedades clásicamente asociadas a la DCE (enfermedades inflamatorias sistémicas, colagenosis, etc.) parecen afectar a un número muy reducido (<5%) de pacientes en las series más importantes. Sin embargo, su asociación con la displasia fibromuscular (DFM) ha quedado bien establecida y confirmada en múltiples series independientes, con una prevalencia variable (25-85%) según la exhaustividad y el método diagnóstico empleado en el cribado1,2,6. La DFM también es una enfermedad de causa desconocida, no aterosclerótica ni inflamatoria, que afecta fundamentalmente a las grandes arterias (iliacas, renales, carótidas). Aunque esta asociación no implica causalidad es tentador especular sobre un sustrato subyacente común de vulnerabilidad o fragilidad vascular6. También se ha sugerido que la DFM podría afectar al árbol coronario, aunque la evidencia que lo apoya ha sido muy cuestionada. Finalmente, la asociación de casos familiares es anecdótica. No obstante, en pacientes con DCE recientemente se ha descrito afectación del locus PHACTR1/EDN1 (genotipo rs9349379) que, curiosamente, también ha sido implicado en la DFM7. Aunque estos nuevos datos todavía deben considerarse como preliminares, el estudio de una posible base genética de la enfermedad ha despertado un enorme interés.
En tercer lugar, hemos aprendido que la prevalencia de la DCE en pacientes con SCA es mucho mayor de la reportada clásicamente8. La mayor sospecha clínica ha sido fundamental para mejorar nuestra capacidad diagnóstica. Así, la utilización sistemática de troponina ultrasensible y de coronariografía muy precoz en mujeres que presentan un SCA ha conseguido diagnosticar muchos casos que antes pasaban desapercibidos1–5,8. Ahora sabemos que la imagen clásica de disección angiográfica (imagen característica de doble luz o de flap intimal) en realidad solo se ve en 1/3 de los pacientes. En la mayoría de los casos angiográficamente se aprecian lesiones difusas, algunas bastante características, o bien estenosis focales (que imitan a lesiones ateroscleróticas) (fig. 1A). También es frecuente la presencia de una tortuosidad coronaria importante1–5,8. Una alta sospecha clínica permite realizar el diagnóstico en estos casos. Así, se ha sugerido que la DCE podría ser la causa de hasta 1/3 de los SCA en mujeres ≤50 años4. Por otro lado, las técnicas de diagnóstico intracoronario (ultrasonidos coronarios y, más recientemente, la tomografía de coherencia óptica [con una impresionante resolución espacial: 15micras]) han permitido confirmar el diagnóstico en casos angiográficamente dudosos9. Pero es que además, estas técnicas tomográficas permiten analizar con gran detalle la verdadera extensión y severidad de la afectación coronaria, proporcionando imágenes espectaculares de la luz verdadera y falsa y de la puerta de entrada (o del hematoma intramural comprimiendo la luz coronaria)9 (fig. 1B,C). En la mayoría de los casos se demuestra que la separación no es a nivel intimal sino que se sitúa entre el tercio externo de la media y la adventicia, generando una membrana «íntimo-medial» relativamente gruesa como siempre habían destacado los hallazgos necrópsicos. Además, estas nuevas técnicas diagnósticas han sido también de gran utilidad para demostrar como en la mayoría de los pacientes durante el seguimiento se produce, espontáneamente, una reparación vascular completa (restitutio ad integrum) recuperando una arquitectura parietal (íntima, media y adventicia) completamente normal9.
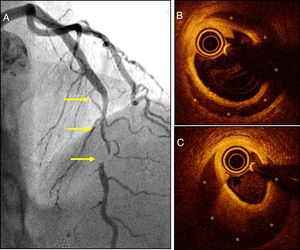
A) Paciente con síndrome coronario agudo (SCA) con una lesión angiográficamente severa y larga (sin doble luz) pero típica de disección coronaria espontánea (DCE), en el segmento medio de la arteria coronaria descendente anterior (flechas). B y C) Imágenes de tomografía de coherencia óptica que demuestran la presencia de una membrana íntimo-medial y un amplio hematoma intramural (asteriscos amarillos) que compromete la luz verdadera. El asterisco blanco señala la sombra causada por la guía; la imagen circular en la luz verdadera corresponde al catéter de imagen intracoronaria.
En cuarto lugar, también hemos aprendido mucho sobre el manejo de estos pacientes1–5. A diferencia del SCA por aterosclerosis, donde la intervención percutánea con implantación de stents farmacoactivos representa el tratamiento de elección, en los pacientes con DCE lo mejor es intentar inicialmente un manejo conservador1–5,10,11 (fig. 2). En la mayoría de los casos el cuadro clínico se estabiliza con tratamiento médico, la evolución posterior es favorable y, finalmente, la arteria se repara por completo. Además, los resultados del intervencionismo coronario frecuentemente son subóptimos (lesiones residuales, disecciones distales no resueltas) y conllevan un riesgo mucho mayor de complicaciones (fundamentalmente por extensión de la disección o del hematoma intramural)10,11. Desafortunadamente los resultados de la revascularización quirúrgica tampoco son buenos debido a la friabilidad de la pared arterial disecada. Por eso la mayoría de los expertos recomiendan reservar la revascularización para casos de fracaso del tratamiento médico (isquemia persistente o recurrente)10,11. Los stents farmacoactivos, utilizados de forma relativamente conservadora en cuanto a la longitud del segmento tratado, representan el tratamiento de elección10,11 (fig. 2). Las técnicas de fenestración vascular (para comunicar con la luz verdadera y descomprimir la luz falsa) y los dispositivos vasculares completamente biorreabsorbibles son estrategias muy atractivas para casos seleccionados, pero la experiencia es bastante limitada.
Algoritmo de diagnóstico y tratamiento de los pacientes con disección coronaria espontánea (DCE). Ante la sospecha clínica la angiografía es la mejor herramienta diagnóstica pero, en algunos casos, las técnicas de diagnóstico intracoronario (tomografía de coherencia óptica [OCT]; ecografía intravascular [IVUS]) pueden ser necesarias para un diagnóstico definitivo. Estas técnicas son especialmente útiles en pacientes que precisan revascularización. También pueden usarse (línea discontinua) en casos seleccionados para un mejor diagnóstico anatómico o con fines de investigación. En los pacientes con isquemia persistente o recurrente está indicada la revascularización (*). Idealmente deben emplearse stents farmacoactivos (aunque la fenestración y otras técnicas también pueden ser útiles) dentro de una estrategia de intervención conservadora, ya que generalmente no es necesario tratar todo el segmento afecto. Sin embargo, en la mayoría de los pacientes los síntomas se estabilizan y la estrategia inicial debe ser un manejo médico conservador (**). Durante el seguimiento las técnicas de imagen no invasivas (tomografía axial computarizada [TAC], resonancia magnética cardiaca [RMC])(***) son de utilidad para descartar la presencia de arteriopatía no coronaria, en especial la displasia fibromuscular. La TAC también puede utilizarse para el seguimiento no invasivo de las alteraciones coronarias. La realización rutinaria de otros procedimientos invasivos en el seguimiento en principio no estaría justificada excepto dentro de protocolos de investigación (línea discontinua).
Fuente: Modificado de Alfonso et al.10.
Finalmente, en cuanto al tratamiento médico, hemos aprendido que el uso de anticoagulantes no está justificado (la fibrinólisis estaría contraindicada) y el tratamiento antiagregante no debe ser tan agresivo como en el SCA por aterosclerosis, ni en la fase aguda ni a muy largo plazo donde no disponemos de evidencia que lo avale1–5. Sin embargo, el uso de betabloqueantes es muy atractivo desde el punto de vista fisiopatológico y algunos datos apuntan a que podría reducir la tasa de recurrencias1–5. Las estatinas y los IECA estarían recomendados en pacientes con alteraciones en los lípidos plasmáticos o con disfunción ventricular, respectivamente. En pacientes con DCE en segmentos coronarios proximales la tomografía computarizada puede facilitar un adecuado seguimiento no invasivo. Hay que vigilar la posibilidad de recurrencias (∼10% en 3 años) y planificar seguimientos clínicos1–5. Por último, en estos pacientes los programas de rehabilitación cardiaca y los clubs online o presenciales de afectados han mostrado una gran aceptación.
Hemos resumido aquí lo que hemos aprendido durante esta última década sobre la DCE. Desgraciadamente, en comparación con otras enfermedades cardiovasculares, es evidente que nuestro conocimiento sobre DCE sigue siendo muy limitado. Generar la adecuada evidencia científica, en base a estrategias o tratamientos controlados comparados de forma aleatorizada, es un reto especialmente difícil en esta patología infrecuente3. Por consiguiente, es fundamental seguir fomentando la investigación desde registros prospectivos multicéntricos bien organizados, a nivel nacional o internacional1–3.
Conflicto de interesesNo existen conflictos de interés.







![Algoritmo de diagnóstico y tratamiento de los pacientes con disección coronaria espontánea (DCE). Ante la sospecha clínica la angiografía es la mejor herramienta diagnóstica pero, en algunos casos, las técnicas de diagnóstico intracoronario (tomografía de coherencia óptica [OCT]; ecografía intravascular [IVUS]) pueden ser necesarias para un diagnóstico definitivo. Estas técnicas son especialmente útiles en pacientes que precisan revascularización. También pueden usarse (línea discontinua) en casos seleccionados para un mejor diagnóstico anatómico o con fines de investigación. En los pacientes con isquemia persistente o recurrente está indicada la revascularización (*). Idealmente deben emplearse stents farmacoactivos (aunque la fenestración y otras técnicas también pueden ser útiles) dentro de una estrategia de intervención conservadora, ya que generalmente no es necesario tratar todo el segmento afecto. Sin embargo, en la mayoría de los pacientes los síntomas se estabilizan y la estrategia inicial debe ser un manejo médico conservador (**). Durante el seguimiento las técnicas de imagen no invasivas (tomografía axial computarizada [TAC], resonancia magnética cardiaca [RMC])(***) son de utilidad para descartar la presencia de arteriopatía no coronaria, en especial la displasia fibromuscular. La TAC también puede utilizarse para el seguimiento no invasivo de las alteraciones coronarias. La realización rutinaria de otros procedimientos invasivos en el seguimiento en principio no estaría justificada excepto dentro de protocolos de investigación (línea discontinua). Fuente: Modificado de Alfonso et al.10.](https://static.elsevier.es/multimedia/02105691/0000004500000006/v1_202107200632/S0210569119302360/v1_202107200632/es/main.assets/thumbnail/gr2.jpeg?xkr=1dZuESKpnCAWr3yCSGZ24A==)


