Diseñar un indicador de mortalidad del síndrome coronario agudo (SCA) en el servicio de medicina intensiva (SMI).
DiseñoEstudio descriptivo observacional multicéntrico.
ParticipantesPacientes con SCA ingresados en SMI incluidos en el registro ARIAM- SEMICYUC entre enero del 2013 y abril del 2019.
IntervencionesNinguna.
Variables de interés principalesLas variables analizadas fueron demográficas, tiempo de acceso al sistema sanitario y estado clínico. Se analizó la terapia de revascularización, los fármacos y la mortalidad. Se realizó un análisis de regresión logística de COX y posteriormente se diseñó una red neuronal. Se elaboró una curva ROC para calcula la potencia del nuevo score. Finalmente, la utilidad clínica o relevancia del indicador ARIAM se evaluará mediante un gráfico de Fagan.
ResultadosSe incluyó a 17.258 pacientes, con una mortalidad al alta del SMI del 3,5% (605). Las variables analizadas con significación estadística (p<0,001) fueron introducidas en el modelo predictivo supervisado, una red neuronal artificial. El nuevo indicador ARIAM mostro una media de 0,0257 (IC del 95%, 0,0245-0,0267) en los pacientes dados de alta de UCI y de 0,27085 (IC del 95%, 0,2533-0,2886) en los que fallecieron, p <0,001. El área ROC del modelo conseguido fue de 0,918 (IC del 95%, 0,907-0,930). En el test de Fagan se demostró que el indicador ARIAM muestra que la probabilidad de fallecimiento es del 19% (IC del 95%, 18-20%) cuando es positivo y del 0,9% (IC del 95%, 0,8-1,01%) cuando es negativo.
ConclusionesEs posible crear un nuevo indicador de mortalidad del SCA en el SMI que sea más exacto, reproducible y actualizable periódicamente.
To design a mortality indicator for acute coronary syndrome (ACS) in the intensive care unit (ICU).
DesignMulticenter observational descriptive study.
ParticipantsACS patients admitted to SMI included in the ARIAM-SEMICYUC registry between January 2013 and April 2019.
InterventionsNone.
Main variables of interestVariables analyzed were demographic, time of access to the health system, and clinical condition. Revascularization therapy, drugs, and mortality were analyzed. A COX regression analysis was performed and subsequently a neural network was designed. An ROC curve was developed to calculate the power of the new score. Finally, the clinical utility or relevance of the ARIAM's indicator will be evaluated using a Fagan test.
Results17,258 patients were included, with a 3.5% (605) mortality at discharge from the ICU. The variables analyzed with statistical significance (p<0.001) were entered into the supervised predictive model, an artificial neural network. The new ARIAM's indicator showed a mean of 0.0257 (95% CI: 0.0245–0.0267) in patients discharged from the ICU and 0.27085 (95% CI: 0.2533–0.2886) in those who died, p<0.001. The ROC area of the model achieved was 0.918 (95% CI: 0.907–0.930). The Fagan test showed that the ARIAM's Indicator shows that the probability of death is 19% (95% CI: 18%–20%) when it is positive and 0.9% (95% CI: 0.8%–1.01%) when it is negative.
ConclusionsIt is possible to create a new mortality indicator for ACS in the ICU that is more accurate, reproducible, and periodically updated.
Desde la antigüedad, uno de los principales objetivos de la medicina ha sido conocer el pronóstico de los pacientes en cualquiera de sus ámbitos. La estratificación de este riesgo se remonta a los inicios de los servicios de medicina intensiva (SMI), donde se usan diferentes escalas o scores pronósticos específicos y validados para cada patología. Los más utilizados son el APACHE, SOFA, o en relación con las unidades coronarias el The Global Registry of Acute Coronary Events (GRACE) o Thrombolysis in Myocardial Infarction (TIMI)1.
El síndrome coronario agudo (SCA) es una enfermedad frecuente en el SMI y se prevé que en 2049 la incidencia del SCA aumente debido al envejecimiento de la población, superando los 175.000 casos/año2,3.
En las últimas décadas, uno de los principales objetivos de los expertos de Medicina Intensiva ha sido el desarrollo y posterior validación de estos modelos de predicción. Con ello, se pretende adaptar el tratamiento al riesgo individual, evitar costes innecesarios y planificar la estrategia de prevención secundaria1.
Por desgracia, las escalas de estratificación en los pacientes coronarios distan mucho de la perfección1. En la actualidad todos ellos cuentan con bastantes limitaciones que ponen de manifiesto la necesidad de crear un indicador o algoritmo capaz de adecuarse a la población contemporánea, de forma individualizada y eficaz.
Tradicionalmente, los scores de referencia en el SCA han sido GRACE y TIMI, que han demostrado gran utilidad y buena discriminación de la mortalidad, con áreas bajo la curva ROC cercanas a 1. Sin embargo, tienen limitaciones importantes, como, por ejemplo, no hacen referencia a la mortalidad al ingreso en el SMI, han sido desarrollados a partir de una población muy seleccionada y que a día de hoy no es representativa de la población actual y tampoco se ajustan a los avances terapéuticos hasta la fecha (tabla 1)1,4.
Diferencias entre población ARIAM contemporánea vs. TIMI y GRACE
| Población ARIAM vs. TIMI y GRACE | ||||
|---|---|---|---|---|
| ARIAM | TIMI | GRACE | ||
| SCACEST | SCASEST | SCACEST | SCAC/SEST | |
| Localizador alteraciones ECG | ||||
| Anterior | 43% | 42,7% | 33,0% | |
| Inferior | 49% | 56,9% | 27,7% | |
| Killip al ingreso | ||||
| Killip IV | 5,9% | 1,2% | 0% | 0,4-1% |
| Estrategias | ||||
| ICP primaria | 81,6% | 0% | 18% | |
| Fibrinólisis | 6,3% | 100% | 16,5% | |
| ICP tardía | 5,8% | 26,6% | ||
| Tratamientos antitrombóticos | ||||
| 2,° antiagregante | 98,5% | 98,7% | 14% | 31,8% |
| Clopidogrel | 35,2% | 50,8% | ||
| Prasugrel | 8,0% | 2,3% | ||
| Ticagrelor | 55,3% | 45,6% | ||
| Antagonistas IIb/IIIa | 5,7% | 1,3% | 3,0% | 18% |
| Evolución clínica | ||||
| Killip máximo | 12,6% | 6,5% | ||
| I | 73,9% | 75,7% | 1,3% | |
| II | 11,1% | 11,2% | ||
| III | 4,1% | 8,6% | ||
| IV | 10,9% | 4,4% | ||
| Infarto o reinfarto | 2,3% | 2,4% | 5,2% | 28,6%a |
| Cirugía cardiaca | 1,3% | 2,9% | 5,5% | 5% |
| Estancia y mortalidad hospitalaria | ||||
| Estancia (días) | ||||
| Media | 6,4 | 8,2 | 10,5 | |
| Mediana | 4,52 | 5,76 | 6-8 | |
| Mortalidad hospitalaria | 8,0% | 4,0% | 6,0%b | 4,6% |
El registro ARIAM es un registro observacional y multicéntrico (nacional) de participación voluntaria (anexo 1) y de corte anual (3 meses), creado por la Sociedad Española de Medicina Intensiva, Crítica y Unidades Coronarias (SEMICYUC). Se creó en 1994 y desde el 2010 pasó a denominarse ARIAM-SEMICYUC. Está integrado en el grupo de trabajo de Cuidados Intensivos Cardiológicos y reanimación cardiopulmonar de la sociedad de Medicina Intensiva, Crítica y Unidades Coronarias. Su labor es mejorar la calidad asistencial en el ámbito de la cardiopatía isquémica, siendo en el momento actual el registro español más amplio en esta materia con una media de 2.335 registros/anuales y un total de 23.357 registros5,6.
Se desconoce a día de hoy cuál es el método óptimo para el diseño de scores adecuados. En el artículo publicado en Medicina Intensiva por Nuñez et al. inciden en que la Medicina Intensiva es un campo ideal para el empleo de técnicas conocidas como Big Data Analysis (BDA) y Machine Learning (ML), que pueden permitir en el futuro mejorar nuestra capacidad de investigación clínica y dirigir de manera más precisa las terapias que proporcionamos a nuestros pacientes, y las redes neuronales artificiales son un claro ejemplo de ello7-12.
El objetivo de este trabajo es diseñar un Indicador de Mortalidad para todas las formas del SCA en UCI (ARIAM) a partir de las variables que puedan estar presentes en momento del ingreso en UCI, con los datos del Registro ARIAM y empleando un modelo predictivo supervisado (red neuronal).
Material y métodosÁmbitoLa base ARIAM-SEMICYUC cumple con la legislación española de estudios postautorización observacionales (Orden SAS/3470/2009, de 16 de diciembre) y la normativa de la Ley de Protección de Datos. En mayo del 2012 fue reconocido como un registro de interés para el Sistema Nacional de Salud por el Ministerio de Sanidad, Consumo y Bienestar Social y, por lo tanto, no es necesaria la autorización expresa y cumplimentación de documento de consentimiento informado por parte de los pacientes.
En la introducción de datos, siempre se garantiza la anonimidad de los pacientes siendo imposible su identificación y se realiza mediante una aplicación informática disponible en: https://ariam.investigacion-intensivos.org/. Los datos los introducen aquellos investigadores que previamente han solicitado su participación en el registro y cuentan con un usuario/contraseña de acceso.
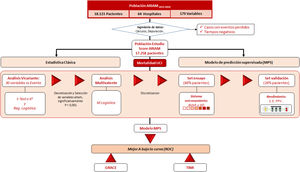
Pacientes y participantesSe realizó un estudio observacional basándonos el registro ARIAM («base ARIAM») (fig. 1). Se incluyó a los pacientes ingresados con el diagnóstico de SCA (de menos de 48h de evolución desde el inicio de los síntomas) entre enero de 2013 y abril de 2019 en las unidades de Cuidados Intensivos españolas colaboradoras con el registro.
Análisis estadístico convencionalEn primer lugar, se realizó el procesamiento de los datos de la Base ARIAM, también conocido como ingeniería de datos. Este proceso incluye depuración de casos, recodificación de atributos tanto continuos como categóricos, creación de atributos sintéticos (agrupamiento, operadores, combinación, cálculos y recodificación de tiempos). Se incluyeron variables con datos socio-demográficos, signos vitales, determinaciones de laboratorio, tratamientos y técnicas realizadas y lugar de atención médica. Además, se recogieron datos de diagnóstico al ingreso y la mortalidad. Los tiempos se calcularon en función de las fechas y horas registradas. Se eliminaron todos aquellos pacientes en los cuales faltaba algún dato.
Se definió el evento objeto de estudio como mortalidad en el servicio de Medicina Intensiva por cualquier causa. Se llevó a cabo un estudio estadístico convencional, descriptivo e inferencial (uni y multivariante) de los datos, tanto globales como respecto del evento. Las variables continuas se expresaron en medias con desviación estándar y se compararon mediante la prueba t de Student o la prueba no paramétrica de Mann-Whitney. Las variables categóricas se describieron por valores absolutos y porcentajes y se compararon mediante la prueba χ2. Posteriormente, las variables significativas en el análisis univariante se utilizaron para un análisis multivariante mediante regresión logística de COX. Con las mismas variables que resultaron significativas en el análisis multivariante, se diseñó una Red Neuronal Artificial (RNA) (anexos 2 y 3).
Red neuronal e indicador ARIAMEl modelo predictivo supervisado (MPS) utilizado fue el multilayer perceptron (MLP) de propagación hacia atrás. En el modelo, los datos se dividieron aleatoriamente en una muestra de aprendizaje (training set) (80%) y una muestra de validación (validation set) (20%). Se utilizaron las funciones de transferencia tangente hiperbólica en las capas ocultas y softmáx en la de salida. El gradiente de pendiente se utilizó para estimar los pesos y sesgos sinápticos. La tasa de aprendizaje inicial fue de 0,4 y el impulso (momentum) fue de 0,9. El indicador/score ARIAM (ARIAM) se considerará el valor de la neurona de la capa de salida que determina fallecimiento.
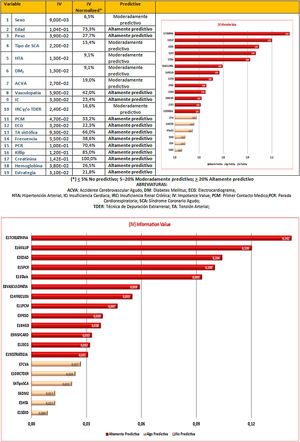
Mediante un análisis de sensibilidad de las variables incluidas en la red, se determina el parámetro importancia de la variable (IV) en relación con la predicción del evento y su valor normalizado (IVn).
Métricas de rendimientoLa potencia del MPS para predecir la supervivencia del paciente se evaluó mediante métricas de rendimiento (sensibilidad, especificidad, precisión, valores predictivos, razones de probabilidad) y el cálculo del área bajo la curva en un análisis de receiver operating characteristic (ROC). El nuevo indicador obtenido (ARIAM) se comparó con el GRACE y TIMI mediante el área ROC. La utilidad clínica o relevancia del indicador se evaluó mediante un gráfico de Fagan. El gráfico de Fagan permite estimar la probabilidad posterior a la prueba de la condición objetivo en un paciente individual basándose en una probabilidad de prueba previa seleccionada.
Para el tratamiento de datos se empleó el paquete estadístico IBM® SPSS® Statistics versión 22.0. (©Copyright IBM Corporation 1989 to 2013, Chicago, IL, EE. UU.) y para el diseño y validación de la red neuronal artificial se usó el programa IBM® Neural Network versión 25.0. Un p valor de p <0,05 se consideró significativo.
ResultadosSe incluyó a un total de 18.123 pacientes con SCA que ingresaron en el SMI, de los cuales 865 fueron eliminados debido a la falta de alguna variable o errores en la recogida de los datos. Estos pacientes pertenecen a 64 hospitales españoles, de todos los niveles y repartidos por toda la geografía. La mortalidad global de los pacientes incluidos fue de 3,5% (603 pacientes).
De las 30 variables analizadas (tabla 2) donde se incluían datos socio-demográficos, constantes vitales al ingreso, determinaciones analíticas, tratamientos y técnicas realizadas y lugar de atención médica, etc. La prevalencia de algunas de estas características en los pacientes que fallecieron fueron: 4,6% de sexo femenino, una media de edad de 73,5±11 años frente a los 64,8 años de los pacientes que fueron dados de alta, antecedentes médicos de HTA (4,1%), dislipidemia (3,6%), alteración electrocardiográfica tipo SCACEST (4,3%), situación clínica de Killip IV (36%), PA sistólica (110,9±35mmHg), FC (87±27 lpm), cifras de creatinina (1,62±1,3mg/dl) o hemoglobina (12,6±2,3g/dl). El tipo estrategia terapéutica, ICP primaria (3,5%) o fibrinólisis (6,1%).
Variables incluidas en el estudio
| Variable | Definición y notas aclaratorias | Categorías (límites) |
|---|---|---|
| Datos sociodemográficos | ||
| Edad | Variable calculada a partir de las fechas de ingreso y de nacimiento | Entre (18-110 años) |
| Sexo | Sexo del paciente al nacimiento | Hombre/mujer |
| Peso | Peso estimado en kg | Entre 25 y 250 kg |
| Talla | Talla estimada en cm | Entre 60 y 230 cm |
| Antecedentes y factores de riesgo coronario | ||
| Historia familiar | Antecedentes de coronariopatía precoz en familiares de primer grado o hermanos (< 55 años en varones o <65 años en mujeres): angina, infarto de miocardio, muerte súbita de causa des conocida, cirugía de bypass aorto-coronario o ICP | Desconocido/dudosoSíNo |
| Tabaquismo | No fumador (nunca ha fumado o es abstinente más de 20 años)Fumador actual (paciente que ha fumado algún cigarrillo en los últimos 30 días) | DesconocidoNo FumadorFumador actual (último mes)Exfumador (< 1 año)Exfumador (> 1 año) |
| Hipertensión | Cualquiera de las siguientes1. Antecedente de hipertensión arterial en la historia del paciente o bien sigue tratamiento con fármacos, dieta o ejercicio para controlar la PA2. Documentación previa de PA sistólica ≥ 140mmHg o PA diastólica ≥ 90mmHg en pacientes sin diabetes o insuficiencia renal crónica o PA sistólica ≥ 130 mmHg o PA diastólica ≥ 80mmHg en al menos 2 ocasiones para pacientes con diabetes o insuficiencia renal crónica.3. Tratamiento actual de la HTA | Desconocido/dudosoSíNo |
| Dislipidemia | Antecedente de dislipidemia consignada en la historia, tratamiento previo o actual con hipocolesterolemiantes o documentación de niveles de colesterol> 200 mg/dl o LDL ≥ 130 mg/dl o HDL <40 mg/dl en varones y <50 mg/ dl en mujeres | Desconocido/dudosoSíNo |
| Diabetes | Historia de diabetes diagnosticada o tratada. Criterios de la American Diabetes Association:1. Hemoglobina A1c ≥ 6,5%; o 2. Glucosa en ayunas ≥ 126 mg/dl; o 3. Glucosa 2-h ≥ 200 mg/dl en la prueba de tolerancia a la glucosa; o 4. En pacientes con síntomas clásicos de hiperglucemia, crisis hiperglucémica, una glucosa aleatoria ≥200 mg/dlDiabetes tipo I: antecedente de diabetes tipo I en la historia clínica o el paciente cumpla criterios de la OMSDiabetes tipo II: antecedente de diabetes tipo II en la historia clínica o el paciente cumpla criterios de la OMS | Desconocido/dudosoDiabetes tipo 1Diabetes tipo 2 |
| Cocaína | Consumo reciente (7 días) de cocaína o positividad del testen orina | Desconocido/dudosoSíNo |
| Enfermedad pulmonarobstructiva crónica | Diagnóstico (confirmado o de sospecha) de asma o EPOC consignado en la historia clínica | Desconocido/dudosoSíNo |
| ACVA | Antecedente de ictus consignado en la historia clínica | Sí, isquémicoSí, hemorrágicoSí, sin especificarNoDesconocido/dudoso |
| Arteriopatía periférica | Historia de arteriopatía obstructiva aorto-femoral o clínica de claudicación intermitente no estudiada | Desconocido/dudosoSíNo |
| Cardiopatía isquémica previa | Evidencia o conocimiento de síntomas, IAM u otro equivalente sugestivo de isquemia cardiaca antes del evento agudo | Desconocido/dudosoSíNo |
| Variable | Definición y notas aclaratorias | Categorías (límites) |
|---|---|---|
| Insuficiencia cardiaca | Diagnóstico clínico consignado como tal en la historia clínica, o síntomas sugestivos como disnea a pequeños esfuerzos, ortopnea recurrente, retención de líquidos o descripción de crepitantes, ingurgitación yugular o edema pulmonar radiológicoLa evidencia de fracción de eyección deprimida sin signos clínicos de insuficiencia cardiaca no es suficiente para el diagnóstico de insuficiencia cardiaca | Desconocido/dudosoSíNo |
| Insuficiencia renal crónica o diálisis | Diagnóstico consignado en la historia clínica o niveles de creatina previos al ingreso de> 1,4 mg/dl | Desconocido/dudosoSíNo |
| ICP o cirugía de revascularización | Intervención coronaria percutánea (angioplastia, stento trombo-aspiración) o cirugía de revascularización cardiaca previa | Desconocido/dudosoSíNo |
| Acceso al sistema y tiempos | ||
| Primer contacto médico | Lugar del primer contacto sanitario | MédicoCentro de Salud061-112Urgencias hospitalariaPlanta HospitalizaciónOtrosDesconocido/dudoso |
| Procedencia | Ubicación inmediatamente anterior al ingreso en UCI | Otro hospitalIngreso directoHemodinámicaUrgenciasConsultas externasPlantaQuirófanoOtros |
| T. dolor/UCI | Tiempo desde el inicio de los síntomas hasta su ingreso en UCI, variable calculada a partir de las horas de inicio de síntomas e ingreso en la Unidad de Cuidados Intensivos | Min |
| Electrocardiograma | ||
| Tipo de SCA | SCASEST: síndrome coronario agudo sin elevación persistente de ST. SCACEST: síndrome coronario agudo con elevación persistente de ST o BCRIHH presumiblemente agudo | SCASESTSCACEST |
| Tipo de alteración | Alteraciones observadas en ECG | ST elevado más de 2 mm o más de 2 derivacionesST elevado menos de 2mm o menos de 2 derivacionesPatrón de tronco/multivasoDescenso de ST≥0,5 mmDescenso ST<0,5 mmElevación transitoria ST (< 20 min) |
| Situación clínica, analítica y estrategia al ingreso | ||
| Parada cardiorrespiratoria | SíNo | |
| Killip inicial | Consignar la primera determinación en UCI | IIIIIIIV |
| PA sistólica/diastólica iniciales mmHg) | Consignar la primera determinación en UCI | Entre 20 y 250mmHg la sistólica y entre 20 y 150 la diastólica |
| Frecuencia cardiaca inicial | Consignar la primera determinación en UCI | Entre 0-350 lpm |
| Hemoglobina al ingreso | g/l | Entre 1-20 |
| Creatinina al ingreso | mg/dl | Entre 0,1 y 20 |
| Estrategia de reperfusión | Estrategia de reperfusión/tratamiento | ICP primariaFibrinólisisNinnguna |
En relación con el evento, 19 variables presentaron diferencias estadísticamente muy significativas (p <0,001) (tabla 3). El tipo estrategia terapéutica, ICP primaria o fibrinólisis, también fue significativo (p <0,001).
Estadísticos convencionales: análisis bivariante y multivariante
| Test | S Logistic | M logistic | |||||||
|---|---|---|---|---|---|---|---|---|---|
| AltaN=16.655(96,5%) | FallecimientoN=603(3,5%) | Valor p | RR | IC del 95% | p | RR | IC del 95% | p | |
| Datos demográficos | |||||||||
| Sexo | |||||||||
| Hombre | 12.452 (96,9) | 402 (3,1) | 20.076 | 1 | 1 | ||||
| Mujer | 4.203 (95,4) | 201 (4,6) | <0,001 | 1,481 | 1246-1761 | <0,001 | 1022 | 0,81-1,289 | 0,858 |
| Edad | 64,8+13,0 | 73,5+11,0 | –16.070 <0,001 | 1,005 | 1,003-1,006 | <0,001 | 1,058 | 1,048-1,069 | <0,001 |
| Peso | 79,1+15,9 | 76,6+14,3 | 3,874 <0,001 | 0,989 | 0,983-0,994 | <0,001 | 1,002 | 0,995-1,009 | 0,542 |
| Talla | 167,2+11,5 | 165,9+9,3 | 2.476 0,00133 | 0,992 | 0,987-0,998 | 0,0133 | |||
| IMC | 29,8+23,6 | 28,2+10,5 | 1.692 0,0906 | 0,994 | 0,987-1,001 | 0,1110 | |||
| Antecedentes | |||||||||
| H.ª familiar | 13.132 (96,6) | 1.643 | |||||||
| No | 2.002 (96,4) | 486 (3,4) | 0,4400 | 1 | |||||
| Sí | 1.521 (96,0) | 32 (3,6) | 0,842 | 0,645-1,099 | 0,2050 | ||||
| D/D | 85 (4,0) | 0,878 | 0,625-1,236 | 0,4570 | |||||
| Tabaco | |||||||||
| No | 4.539 (95,7) | 204 (4,3) | 2.386 | 1 | |||||
| Sí u otros | 12.116 (96,8) | 399 (3,2) | 0,0523 | 0,982 | 0,980-0,998 | 0,0133 | |||
| Hipertensión | 0,769-1,224 | 0,799 | |||||||
| No | 6.598 (97,3) | 182(2,7) | 24.851 | 1 | 1 | ||||
| Sí | 9.949 (95,9) | 420 (4,1) | <0,001 | 1,530 | 1,283-1,826 | <0,001 | 0,970 | ||
| D/D | 108 (99,1) | 1 (0,9) | 0,336 | 0,047-2,418 | 0,3360 | 1 | |||
| Hiperlipidemia | |||||||||
| No | 7.721 (96,5) | 277 (3,5) | 0,170 | 1 | |||||
| Sí | 8.741 (96,4) | 318 (3,6) | 0,9184 | 1,014 | 0,861-1,195 | 0,8675 | |||
| D/D | 193 (96,1) | 8 (3,9) | 1,155 | 0,564- 2,367 | 0,6931 | ||||
| Diabetes | |||||||||
| No | 11.547 (97,1) | 340 (2,9) | 47.504 | 1 | 0,597-2,296 | 0,6460 | 1 | 0,850-1,304 | 0,638 |
| DM1 | 261 (96,7) | 9 (3,3) | <0,001 | 1,171 | 1,509-2,109 | <0,001 | 1 | ||
| DM2 | 4.711 (94,9) | 248 (5,1) | 1,784 | 0,708-3,694 | 0,2540 | 1,053 | |||
| D/D | 136 (95,8) | 6 (4,2) | 1,617 | 1 | |||||
| Cocaína | |||||||||
| No | 12.365 (96,4) | 456 (3,6) | 0,580 | 1 | |||||
| Sí | 4.290 (96,7) | 147 (3,3) | 0,4462 | 0,929 | 0,769-1,123 | 0,4463 | |||
| C. isquémica | |||||||||
| No | 10.884 (96,7) | 377 (3,3) | 2.054 | 1 | |||||
| Sí | 5.771 (96,2) | 226 (3,8) | 0,1518 | 1,131 | 0,956-1,337 | 0,1520 | |||
| ICP o CABG | |||||||||
| No | 1.3687 (96,6) | 481 (3,4) | 4.470 | 1 | |||||
| Sí | 2.903 (96,1) | 117 (3,9) | 0,1070 | 1,147 | 0,933-1,409 | 0,1923 | |||
| D/D | 65 (92,9) | 5 (7,1) | 2,189 | 0,877- 5,461 | 0,0930 | ||||
| EPOC | |||||||||
| No | 15.298 (96,6) | 540 (3,4) | 6.637 | 1 | |||||
| Sí | 1.318 (95,6) | 60 (4,4) | 0,0362 | 1,290 | 0,982-1,694 | 0,0674 | |||
| D/D | 29 (90,6) | 3 (9,4) | 2,931 | 0,890- 9,651 | 0,0770 | ||||
| ACVA | 0,803-1,649 | 0,444 | |||||||
| No | 15.662 (95,7) | 537 (3,3) | 38.495 | 1 | 1 | ||||
| Isquémico | 715 (92,6) | 57 (7,4) | <0,001 | 2,325 | 1,752-3,086 | <0,001 | 1,151 | ||
| Hemorrágico | 60 (100) | 0 (0,0) | |||||||
| D/D | 218 (96,1) | 9 (3,9) | 1,204 | 0,615-2,358 | 0,5881 | 1 | |||
| Vasculopatía | 110.847 | ||||||||
| No | 15.530 (96,9) | 497 (3,1) | <0,001 | 1 | 1 | 1,359-2,410 | <0,001 | ||
| Sí | 1.090 (91,1) | 106 (8,9) | 3,039 | 2,442-3,781 | <0,001 | 1,810 | |||
| D/D | 35 (100) | 0 (0) | |||||||
| Insf, cardiaca | 15.962 (96,9) | 514 (3,1) | 154,002 | 1,278-2,364 | <0,001 | ||||
| No | 665 (88,4) | 87 (11,6) | <0,001 | 1 | 1 | ||||
| Sí | 31 (93,9) | 2 (6,1) | 4,081 | 3,210-5,189 | <0,001 | 1,738 | |||
| D/D | 2,004 | 0,478-8,395 | 0,3487 | 1 | |||||
| IRC/TDER | 15.505 (96,7) | 521 (3,3) | 41.599 | 1,119-2,214 | 0,009 | ||||
| No | 1.133 (93,3) | 82 (6,7) | <0,001 | 1 | <0,001 | 1 | |||
| Sí | 17 (100) | 0 (0) | 2,154 | 1693-2,740 | 1,574 | ||||
| D/D | 1 | ||||||||
| Acceso al sistema sanitario y tiempos | |||||||||
| PCM | 0,958-1,553 | 0,108 | |||||||
| C, Salud | 1.992 (98,0) | 102 (2,0) | 20,076 | 1 | 1 | 0,628-1,104 | 0,202 | ||
| 061 | 3.146 (94,1) | 199 (5,9) | <0,001 | 3,096 | 2,428-3,947 | <0,001 | 1,220 | 1,146-2,842 | 0,011 |
| Otros | 290 (94,2) | 18 (5,8) | 3,038 | 1,815-5,084 | <0,001 | 0,832 | 0,853-1,861 | 0,245 | |
| Médico | 516 (94,0) | 33 (6,0) | 3,130 | 2,092-4,683 | <0,001 | 1,804 | |||
| Hospitaliz, | 600 (91,9) | 53 (8,1) | 4,323 | 3,069-6,089 | <0,001 | 1,260 | |||
| Urgencias | 7.061 (97,3) | 197 (2,7) | 1,365 | 1,072-1,739 | 0,0116 | 1 | |||
| D/D | 50 (98,0) | 1 (2,0) | 0,979 | 0,134-7,156 | 0,9832 | 1 | |||
| Procedencia | 77 (97,5) | ||||||||
| C. externas | 231 (95,9) | 2 (2,5) | 61,256 | 1 | |||||
| Otras | 4.252 (96,7) | 10 (4,1) | 0,0542 | 1,667 | 0,357-7,775 | 0,5156 | |||
| Hemodin, | 32 (97,0) | 147 (3,3) | 1,331 | 0,324-5,471 | 0,6917 | ||||
| Quirófano | 592 (92,2) | 1 (3,0) | 1,203 | 0,105-13,74 | 0,8817 | ||||
| Planta | 9.022 (97,0) | 50 (7,8) | 3,252 | 0,776-13,63 | 0,1068 | ||||
| Urgencias | 896 (93,9) | 280 (3,0) | 1,195 | 0,292-4,889 | 0,8044 | ||||
| SEM | 1.503 (96,5) | 58 (6,1) | 2,492 | 10,59-10,40 | 0,2103 | ||||
| D/D | 24 (3,5) | 1,383 | 0,331-5,780 | 0,6565 | |||||
| T. dolor/UCI | 842+1362 | 900,7+1.695 | –1.0160,3098 | ||||||
| Electrocardiograma | |||||||||
| Tipo SCA | |||||||||
| SCASEST | 7.960 (97,4) | 211 (2,6) | 38.256 | 1 | 1 | ||||
| SCACEST | 8.695 (95,7) | 392 (4,3) | <0,001 | 1,701 | 1,435-2,01 | <0,001 | 0,554 | 0,086-3,560 | 0,534 |
| Alteración | 1.178 (99,1) | 11 (0,9) | 0,057 | ||||||
| Normal | 168 (86,2) | 27 (13,8) | 165,756 | 1 | 1 | <0,001 | |||
| BRI | 6.839 (95,7) | 306 (4,3) | <0,001 | 17,211 | 8,381-35,34 | <0,001 | 1,849 | 0,981-3,484 | <0,001 |
| Est máx | 1.562 (96,5) | 56 (3,5) | 4,792 | 2,617-8,772 | <0,001 | 2,347 | 1,757-3,134 | <0,001 | |
| Est mín | 1.696 (95,4) | 94 (4,6) | 3,839 | 2,003-7,361 | <0,001 | 2,530 | 1,696-3,774 | ||
| DEST máx | 1.188 (98,0) | 24 (2,0) | 5,113 | 2,726-9,588 | <0,001 | 2,042 | 1,466-2,843 | ||
| DEST mín | 316 (97,8) | 7 (2,2) | 2,163 | 1,055-4,437 | 0,035 | 1 | |||
| D/D | 590 (99,0) | 6 (1,0) | 2,372 | 0,912-6,170 | 0,076 | 1 | 1308-4,294 | ||
| EST transi | 1.476 (99,0) | 15 (1,0) | 1,089 | 0,401-2,960 | 0,867 | 1 | |||
| T negativas | 1.134 (96,8) | 38 (3,2) | 1,088 | 0,498-2,379 | 0,832 | 1 | |||
| Otros | 235 (92,5) | 19 (7,5) | 3,589 | 0,985-7,056 | 0,539 | 1 | |||
| Tronco | 8,658 | 4,07-18,43 | <0,001 | 2,370 | |||||
| Situación clínica, analítica y estrategia al ingreso | |||||||||
| PCR previa | |||||||||
| No | 16.083 (97,4) | 424 (2,6) | 963,429 | 1 | 1 | ||||
| Sí | 572 (76,2) | 179 (23,8) | <0,001 | 11,87 | 9,781-14,40 | <0,001 | 5,735 | 4,370-7,526 | <0,001 |
| Killip | |||||||||
| I | 13.480 (98,9) | 150 (1,1) | 2.333,35 | 1 | 3,879-6,447 | 1 | |||
| II | 1.887 (97,4) | 105 (5,3) | <0,001 | 5,001 | 11,14-17,91 | <0,001 | 2,282 | 1,714-3,038 | <0,001 |
| III | 929 (86,4) | 146 (13,6) | 14,123 | 39,94-64,01 | <0,001 | 5,555 | 4,168-7,405 | <0,001 | |
| IV | 359 (64,0) | 202 (36) | 50,566 | <0,001 | 9,343 | 6,863-12,72 | <0,001 | ||
| PA sistólica (mmHg) | 135,9+28,1 | 110,9+35.5 | 21,240 | 0,969 | 0,966-0,972 | <0,001 | 0,986 | 0,982-0,989 | <0,01 |
| <0,001 | |||||||||
| FC (lpm) | 78,2+19,5 | 87,4+27,0 | –11,273 | 1,019 | 1,016-1,022 | <0,001 | 1,010 | 1,006-1,014 | <0,01 |
| <0,001 | |||||||||
| Hemoglobina (g/dL) | 13,9+1,9 | 12,6+2,3 | 14,111<0,001 | 0,772 | 0,744-0,801 | <0,001 | 0,944 | 0,900-0,991 | 0,021 |
| Creatinina (mg/dL) | 1,05+0,7 | 1,62+1,3 | –18,034<0,001 | 1,444 | 1,369-1,522 | <0,001 | 1,307 | 1,194-1,431 | <0,01 |
| Estrategia | |||||||||
| Ninguna | 8.148 (96,8) | 267 (3,2) | 22,892<0,001 | 1 | 1 | ||||
| ICP previa | 7.531 (96,5) | 275 (3,5) | 1,12 | 0,94-1,33 | 0,1973 | 1 | 1,136-2,345 | 0,008 | |
| Fibrinólisis | 940 (93,9) | 61 (6,1) | 1,99 | 1,49-2,65 | <0,001 | 1,632 | |||
Test: chi al cuadrado (cualitativas) o t-test (cuantitativas).
ACVA: accidente cardiovascular agudo; BRI: bloqueo rama izquierda; C. externas: consultas externas; C. isquémica: cardiopatía isquémica; DEST máx: descenso ST> de 2mm; DEST mín: descenso ST <2mm; EPOC: enfermedad pulmonar obstructiva crónica; EST máx: elevación ST> de 2mm; EST min: elevación ST <2mm; EST transi: elevación ST transitoria; ICP o CABG: intervención coronaria percutánea o coronary artery bypass grafting; IMC: índice masa corporal; IRC/ TDER: insuficiencia renal crónica/terapia de depuración extrarrenal; M Logistic: Multilogistic regression analysis; S Logistic: Simple logistic regression analysis; PCM: primer contacto médico; PCR previa: parada cardiorrespiratoria; SEM: servicio médico extrahospitalario.
El nuevo indicador ARIAM mostró una media de 0,0257 (IC del 95%, 0,0245-0,0267) en los pacientes dados de alta de UCI y de 0,27085 (IC del 95%, 0,2533-0,2886) en los que fallecieron, con una p <0,001. Este indicador derivado de la función softmáx de la capa de salida puede ser interpretado fácilmente como una probabilidad de fallecer: así, un valor 0,0835 indica que la probabilidad de fallecer será del 8,35%.
En el modelo conseguido todas las variables introducidas mostraron un cierto valor predictivo, siendo muy alto (IVn> 20%) para: la creatinina, Killip, edad, parada cardiorrespiratoria, PA sistólica, vasculopatía, frecuencia cardiaca, primer contacto médico, peso, hemoglobina, insuficiencia cardiaca, ECG y estrategia inicial (fig. 2).
Métricas de rendimientoRespecto de las métricas de rendimiento para toda la serie (con un punto de corte del indicador> 0,04), merecen destacarse los siguientes datos: especificidad 88,19% y valor predictivo negativo 99,19% (anexo 5).
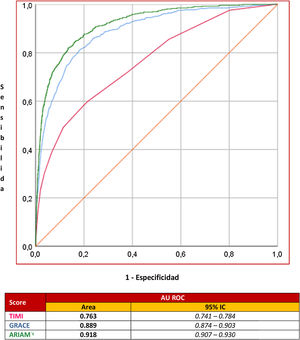
El área ROC del modelo conseguido fue de 0,918 (IC del 95%, 0,907-0,930); este estadístico «c» comparado con otros 2 indicadores (GRACE, TIMI) como predictores de mortalidad del SCA en el SMI fue: ARIAM 0,918 (IC del 95%, 0,907-0,930) vs. GRACE 0,889 (IC del 95%, 0,874-0,903; p <0,05) y vs. TIMI 0,763 (IC del 95%, 0,741-0,784, p <0,01) (fig. 3).
Se realizó el test de Fagan para conocer la relevancia clínica del score. El resultado positivo del indicador ARIAM indica que la probabilidad de muerte aumenta al 19% (IC del 95%, 18-20%), mientras que, en caso negativo, la probabilidad disminuye al 0,9% (IC del 95%, 0,8-1,01%) (anexo 6).
DiscusiónA nivel mundial, la enfermedad cardiovascular es la causa más frecuente de muerte, morbilidad y coste sanitario en España, y su frecuencia está en aumento a consecuencia del envejecimiento de la población. Actualmente causa casi 1,8 millones de muertes al año en Europa, lo que corresponde al 20% de todas las muertes, con grandes variaciones entre países1,13,14. La asistencia sanitaria del SCA consume una gran cantidad de recursos en España por lo que una correcta estratificación del riesgo puede ser primordial a día de hoy3.
Se espera de un score pronóstico, que además de establecer un criterio de diagnóstico, de manejo o como su nombre lo indica de pronóstico, sean fáciles de utilizar y midan un resultado con la suficiente entidad clínica15. Tanto en las actuales guías de práctica clínica, como en los indicadores de calidad de la SEMICYUC, se recomienda una valoración precoz del riesgo a todo paciente con SCA mediante la escala GRACE13,16.
Las escalas pronósticas deben ser empleadas para la población para la que se diseñaron; así, un indicador creado para población general no será válido para el SMI y viceversa15. En este sentido, las herramientas hasta la fecha (GRACE y TIMI) presentan limitaciones importantes ya que ninguno de ellos se relaciona específicamente con la mortalidad al ingreso en el SMI, sino a los 6 meses o a los 14 días, respectivamente17-21. TIMI, además, cuenta con diferencias en cuanto a las características clínicas de los pacientes incluidos: No incluye pacientes con shock cardiogénico (Killip IV) y, además, dado que se diseñó basándose en un estudio de tratamientos fibrinolíticos, no incluye a pacientes tratados mediante revascularización percutánea primaria, que a día de hoy es la terapia más frecuente en este tipo de pacientes17-22.
Para que un score sea práctico en la clínica es necesario que incluya las variables que han demostrado ser más relevantes a la hora de predecir el evento. Además, debe ser un score novedoso, reproducible y fácilmente actualizable. El ARIAM utiliza 19 variables al ingreso donde se incluyen datos socio-demográficos, analíticos y constantes clínicas14,16. Este nuevo score ha demostrado buena discriminación de la mortalidad al ingreso, superando a otras escalas anteriormente utilizadas.
Los pacientes con un score ARIAM positivo tendrán una probabilidad de fallecer del 19% a causa del SCA. El modelo diseñado tuvo una exactitud/precisión (diagnostic accuracy) del 96,81% en el conjunto de aprendizaje y del 96,79% en el de validación. La probabilidad de mortalidad aumentará a más del 19% cuando el ARIAM es positivo y será <1% cuando es negativo, por tanto, mostró muy buena discriminación para el evento objeto del estudio e implicará priorización en la estrategia de tratamiento. Al contrario, un ARIAM negativo identificará los pacientes de riesgo bajo y permitirá orientar el cribado y las estrategias de prevención.
El área bajo la curva ROC de nuestro indicador es incluso superior al área ROC de GRACE, por lo que permite discriminar la mortalidad de forma más precisa18.
Posiblemente el diseño de nuevas variables sintéticas creadas a partir de los tiempos registrados en el ARIAM pueda aumentar la rentabilidad del modelo. Un ejemplo de ello es el análisis del tiempo inicio del dolor torácico-llegada a la UCI, que, aunque no se ha demostrado como predictor independiente de mortalidad en UCI (al existir gran dispersión en los datos de la muestra), sí que muestra diferencias interesantes que convendría analizar con más detalle en futuros trabajos16.
Este nuevo modelo mejora las limitaciones potenciales de los scores actuales ya que permite la estratificación del riesgo de forma temprana. En los últimos años, se han desarrollo nuevos scores, como el M-CARS, ante la necesidad de actualización de los existentes, pero a pesar de ello, cuenta con importantes desventajas frente al modelo que proponemos: no ser específico de pacientes con SCA y haber sido diseñado mediante un estudio unicéntrico, por lo que la generalización del M-CARS a otras poblaciones puede suponer una importante limitación23.
Nuestro trabajo presenta 2limitaciones. La primera, común a cualquier score de riesgo, pese a discriminar bien los grupos de riesgo, no necesariamente predice correctamente el riesgo individual. La segunda inherente a los métodos de aprendizaje automático, que pueden funcionar muy bien en nuestros conjuntos de aprendizaje y validación (validez interna), pero es necesario desplegar el modelo a nuevas series de datos o registros web (validez externa o prospectiva) para así validar el nuevo score en poblaciones futuras.
ConclusiónEl indicador ARIAM, creado a partir de una RNA, es un score asistencial clínico más adecuado a la población actual, más exacto, reproducible y actualizable de forma periódica y que supone una herramienta muy útil en los SMI a la hora de valoraciones clínicas o servir de referencia en estudios de calidad. Este nuevo score puede ser de utilidad a la hora de elaborar comparaciones con otros scores predictivos previos que fomenten nuevas investigaciones.
Contribución de autoresLos autores de este trabajo son los investigadores principales de sus hospitales y han contribuido con un mayor número de casos en los cortes del Registro ARIAM incluidos en el estudio.
El diseño y la redacción del estudio han sido realizados por JJAB, ARG y HLG y corregida por el resto de los autores, que están de acuerdo con su contenido.
FinanciaciónEl registro ARIAM-SEMICYUC está financiado al 100% por la Sociedad Española de Medicina Intensiva, Crítica y Unidades Coronarias.
Conflicto de interesesLos autores declaran no tener conflicto de intereses, ni haber recibido ningún tipo de apoyo financiero para la realización del estudio.
Los nombres de los componentes del registro ARIAM-SEMICYUC están relacionados en el anexo 1 del material adicional.