La administración de fluconazol intravenoso (100 mg/día) no previene las infecciones graves causadas por Candida sp. en los enfermos críticos con un tiempo de ventilación mecánica mayor de 5 días.
Artículo: Garbino J, Lew DP, Romand JA, Hugonnet S, Auckenthaler R, Pittet D. Prevention of severe Candida infections in nonneutropenic, high-risk, critically ill patients: a randomized, double-blind, placebo-controlled trial in patients treated by selective digestive decontamination. Intensive Care Med 2002;28:1708-17.
Antecedentes: las infecciones por Candida sp. son habitualmente endógenas. Es decir, el aparato digestivo de los pacientes que desarrollan una infección por Candida sp. se coloniza antes de desarrollar la infección. Menos del 40% de los sujetos sanos es portador de Candida sp. Sin embargo, los enfermos ingresados en la unidad de cuidados intensivos (UCI) adquieren ese microorganismo en proporciones que oscilan entre un 59 y un 80%.
Los factores de riesgo asociados con la aparición de infecciones graves por Candida sp. no son habitualmente modificables en la práctica (p. ej., administración previa de antibióticos, enfermedad quirúrgica digestiva, nutrición parenteral), salvo las bacteriemias asociadas a catéteres intravasculares. Por ello, se han propuesto diferentes medidas preventivas tales como la administración digestiva1 o sistémica2 de antifúngicos.
Objetivo: evaluar la eficacia de la administración de fluconazol en dosis bajas para la profilaxis de las infecciones causadas por Candida sp. en pacientes críticos ventilados mecánicamente.
Diseño: ensayo clínico con asignación aleatoria.
Lugar: 2 unidades de cuidados intensivos (Suiza).
Período de estudio: se refiere un período de 30 meses, pero no se especifican fechas.
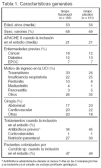
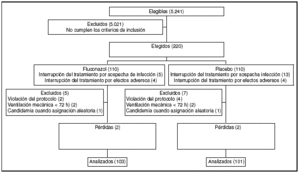
Pacientes (tabla 1 y fig. 1)
Figura 1.
Criterios de inclusión: 1. Edad > 18 años.
2. Ventilación mecánica > 48 h y duración esperada de la ventilación mecánica ≥ 72 h más.
3. Tratamiento con solución antibiótica orofaríngea en el momento de la asignación aleatoria.
Criterios de exclusión: 1. Expectativa de vida < 7 días.
2. Historia de infección sistémica por hongos.
3. Alergia a los compuestos azoles.
4. Tratamiento con un fármaco antifúngico en los 7 días previos a la asignación aleatoria.
5. Síndrome de inmunodeficiencia adquirida.
6. Bacteremia por Candida sp. en el momento de inclusión en el estudio.
7. Tiempo de protrombina < 50% tras 24 h de tratamiento con vitamina K (20 mg).
8. Neutropenia.
9. Embarazo.
10. Rechazo a otorgar el consentimiento informado.
Intervenciones que se comparan:
Grupo fluconazol: 100 mg de fluconazol intravenoso en una sola dosis diaria.
Grupo control: placebo.
El tratamiento asignado se mantuvo hasta que se diagnosticó una infección por Candida sp., hasta la retirada de la ventilación mecánica o hasta la aparición de un efecto adverso grave.
Todos los pacientes fueron tratados con una solución faríngea compuesta por 150 mg de polimixina B, 1.000 mg de neomicina y 1.000 mg de vancomicina, disueltas en 60 ml y administrada en 4 dosis diarias de 15 ml.
Asignación aleatoria: sí. Se refiere que se mantuvo oculta.
Enmascaramiento: se refiere el estudio como doble ciego.
Desenlaces principales: desarrollo de una infección grave por Candida sp. El período de seguimiento fue la estancia hospitalaria.
En el término infección grave se incluyeron: candidemia, peritonitis y neumonía. Las definiciones de todas ellas están claramente expresadas en el artículo.
Análisis por intención de tratar: aunque los autores refieren que el análisis se hizo por intención de tratar, se excluyó del análisis a 6 enfermos por violación del protocolo (2 en el grupo fluconazol y 4 en el grupo placebo) y no se refieren sus desenlaces (fig. 1).
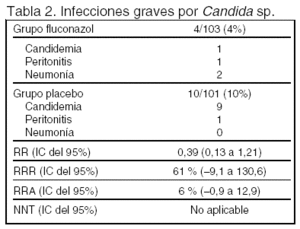
Resultados principales: los resultados del desenlace principal se expresan en la tabla 2 y los de los efectos adversos en la tabla 3. No hubo diferencias en la incidencia de efectos adversos.
La incidencia de bacteriemias fue 62,9 por 1.000 pacientes/días en el grupo fluconazol y 60,6 en el grupo placebo; la incidencia de neumonía asociada a la ventilación mecánica fue de 9,9 por 1.000 días y 11,4 de ventilación mecánica, respectivamente. La mortalidad fue del 40 y el 41%, respectivamente.
Información sobre costes: no consta.
Financiación del estudio: Pfizer, Inc.
Conclusiones de los autores: el uso profiláctico de fluconazol intravenoso en un grupo seleccionado de pacientes ventilados mecánicamente reduce la incidencia de infecciones por Candida sp., sobre todo la candidemia.
Conclusiones de los revisores: las conclusiones deben ser tomadas con precaución. Los resultados del desenlace principal (p = 0,09) no alcanzan el nivel de significación estadística predefinida por los autores, aun excluyendo a los enfermos en los que se produjo una violación del protocolo tras la asignación aleatoria.
La aplicabilidad de este estudio puede tener ciertas limitaciones debido a que la población incluida en el ensayo clínico es un grupo muy seleccionado de pacientes (tiempo de ventilación mecánica > 5 días) con una incidencia muy alta de colonización por hongos (en el momento de ingresar en el estudio casi la mitad de los pacientes tuvo algún cultivo positivo para hongos y durante el estudio se diagnosticó colonización en la mitad de los pacientes no colonizados del grupo tratamiento y en las dos terceras partes del grupo control), así como una tasa de bacteriemia nosocomial (47%) y de candidemia (un 10% en el grupo placebo) muy superior a lo referido en pacientes críticos y más teniendo en cuenta que ningún episodio de candidemia fue secundario a la colonización de catéteres.
Dada la baja incidencia de infecciones graves por Candida sp. en los enfermos críticos, a pesar de la alta incidencia de colonización digestiva y la ausencia de efecto sobre la mortalidad de las estrategias basadas en la administración profiláctica de fluconazol, no existe suficiente soporte para realizar profilaxis de las infecciones por Candida sp. en los enfermos críticos. Por otro lado, en el caso de que se identificara un subgrupo con riesgo alto de infección grave está por dilucidar si es más eficaz o coste/efectiva la administración de antifúngicos sistémicos o no absorbibles por vía digestiva.
Glosario
RR (riesgo relativo): Es el cociente entre el riesgo de que ocurra un suceso en el grupo tratado dividido por el riesgo de que ocurra el suceso en el grupo control (habitualmente placebo).
RRR (reducción relativa del riesgo): Es la reducción proporcional en el riesgo de que ocurra un hecho adverso (p. ej., muerte) expresada en porcentaje. Se calcula (1 RR) ×100%.
RAR (reducción absoluta del riesgo): Es la diferencia entre el riesgo de que ocurra un hecho adverso en el grupo control menos el riesgo en el grupo tratado expresada en porcentaje. Se calcula (Rc Rt) ×100.
IRR (incremento relativo del riesgo): Es el incremento proporcional en el riesgo de que ocurra un suceso (p. ej., mortalidad) expresada en porcentaje. Se calcula (1 RR) ×100%.
IAR (incremento absoluto del riesgo): Es la diferencia entre el riesgo de que ocurra un suceso en el grupo control menos el riesgo en el grupo tratado expresada en porcentaje. Se calcula (Rc Rt) ×100.
NNT (número necesario para tratar): Es el número de pacientes que hay que tratar para prevenir un efecto adverso (100/RAR) o para que ocurra un efecto beneficioso (100/IAB). Se calcula.