En los enfermos críticos quirúrgicos la descontaminación digestiva selectiva reduce la incidencia absoluta de infección un 22,5%, sin efectos adversos.
Selective digestive decontamination reduces the infection rate by 22.5% in critically ill surgical patients without any arm effect.
Artículo: Krueger WA, Lenhart FP, Neeser G, Ruckdeschel G, Schreckhase H, Eissner HJ et al. Influence of combined intravenous and topical antibiotic prophylaxis on the incidence of infections, organ dysfunctions, and mortality in critically ill surgical patients: a prospective, stratified, randomized, double-blind, placebo-controlled clinical trial. Am J Respir Crit Care Med 2002;166: 1029-37.
Antecedentes: la mayoría (60 a 90%) de las infecciones que presentan los pacientes ingresados en las unidades de cuidados intensivos (UCI) están producidas por microorganismos que colonizan la orofaringe y el intestino de los pacientes antes de causar una infección (infecciones endógenas). Cuando la infección está causada por microorganismos que porta el enfermo al ingreso en la UCI se considera que es primaria endógena. Cuando la infección está causada por la flora que coloniza el aparato digestivo del enfermo tras su ingreso en la UCI se considera secundaria endógena.
La descontaminación digestiva selectiva (DDS) es una estrategia para la profilaxis de la infección que consiste en la administración de: 1. un antibiótico de amplio espectro por vía parenteral durante los primeros 4 días (habitualmente cefotaxima), para prevenir las infecciones primarias endógenas; 2. antimicrobianos tópicos no absorbibles (habitualmente colistina, tobramicina y anfotericina B) en la orofaringe y en el resto del tubo digestivo como profilaxis de las infecciones secundarias endógenas, mediante la prevención o erradicación de la colonización de la orofaringe, estómago e intestino por microorganismos potencialmente patógenos. Estos antimicrobianos no absorbibles preservan la flora endógena anaeróbica sin cambios.
Cincuenta y tres ensayos clínicos han demostrado el efecto de la DDS sobre la disminución de las infecciones adquiridas en la UCI, particularmente la neumonía asociada a ventilación mecánica. Un metaanálisis demostró una reducción relativa global de la mortalidad hospitalaria del 20% (NNT = 23) y de la infección respiratoria del 65% (NNT = 5) con el empleo de la DDS1. El efecto de la DDS sobre enfermos con diferentes categorías de gravedad o con diferentes enfermedades muestra resultados variables1,2.
Objetivo: estimar el efecto de la DDS en la incidencia de infección en una población de enfermos quirúrgicos y traumatizados.
Diseño: ensayo clínico con asignación aleatoria.
Lugar: 2 UCI predominantemente quirúrgicas de 2 hospitales.
Período de estudio: abril de 1989 a marzo de 1991.
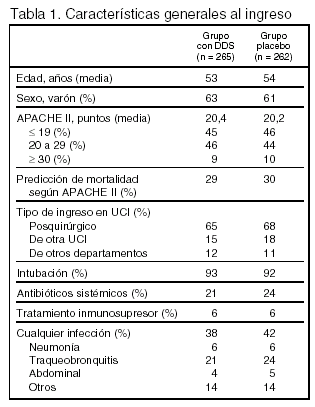
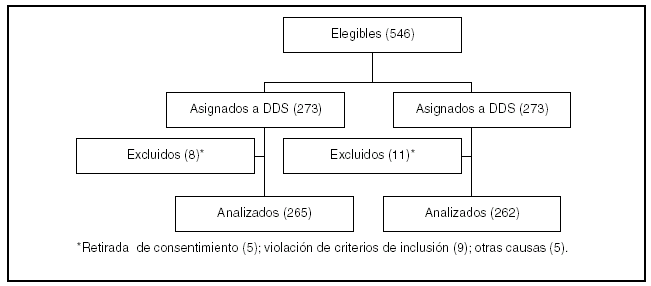
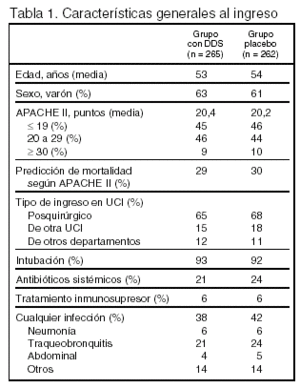
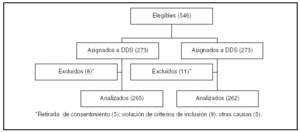
Pacientes (tabla 1, figura 1)
Figura 1.
Criterios de inclusión: 1. Edad > 18 años. 2. Estancia prevista > 48 h. 3. Al menos 1 de los siguientes: a) intubación esperada > 24 h; b) PaO2 < 55 mmHg respirando aire; c) cirugía torácica o abdominal en las 24 h precedentes, d) disfunción grave de órganos en el momento del ingreso; e) riesgo de aspiración por trastornos de la deglución; f) enfermedad pulmonar obstructiva crónica; g) edad > 70 años, y h) tratamiento inmunosupresor.
Criterios de exclusión: 1. Muerte esperada en las primeras 48 horas. 2. Sin asignación aleatoria en las primeras 12 h tras el ingreso en la UCI. 3. Embarazo. 4. Intolerancia a la medicación. 5. Hemorragia digestiva alta en las 4 semanas precedentes.
Intervenciones que se comparan:
Grupo DDS: Se administró: 1: Ciprofloxacino 400 mg/12 h durante 4 días. 2. Solución de gentamicina (80 mg), polimixina B (50 mg)/6 h aplicada en los orificios nasales, en la cavidad oral y en el estómago.
Cuando los enfermos eran tratados con antibióticos sistémicos no se administró el ciprofloxacino.
En los enfermos con síndrome de distrés respiratorio del adulto o inmunosuprimidos se añadió a la solución digestiva 125 mg de vancomicina.
En los enfermos colonizados (cultivos positivos repetidos) por Candida sp. se administró anfotericina B 250 mg/6 h en la solución digestiva.
Grupo placebo: placebo de similares características.
Al ingreso y 2 o 3 veces por semana se obtuvieron muestras rectales, orofaríngeas, gástricas y de aspirado traqueal para cultivo.
Asignación aleatoria: estratificada por valor de APACHE II al ingreso: ≤ 19; 20 a 29; ≥ 30. La asignación aleatoria se mantuvo oculta.
Enmascaramiento: sí.
Desenlaces principales: incidencia de infección.
El diagnóstico de neumonía fue clínico, sin tener en cuenta los datos microbiológicos.
Análisis por intención de tratar: sí.
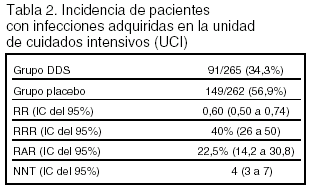
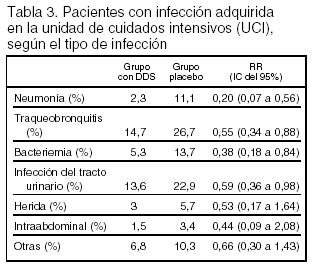
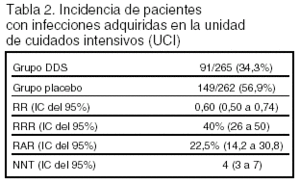
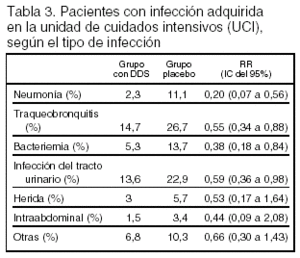
Resultados principales: están expresados en las tablas 2 y 3.
La mortalidad fue 19,6% en el grupo tratado con DDS y 28,6% en el grupo placebo.
No se encontraron efectos adversos relacionados con la DDS.
Información sobre costes: los costes por la administración de antibióticos fueron 48,2 A por paciente día en el grupo DDS y 32,3 Aen el grupo placebo.
La media de la suma de la puntuación TISS desde el día 0 al 14 fue 333 en el grupo DDS y 374 en el grupo placebo.
Financiación del estudio: Bayer Vital GMBH. Merck.
Esta sección está financiada con la ayuda ISCIII-FIS 02/8115.
Conclusiones de los autores: la administración de DDS reduce la incidencia de infección en los enfermos críticos, y no se observa la aparición de resistencia a los antibióticos. La reducción de la mortalidad sólo se observó en el estrato con valores de APACHE II entre 20 y 30 puntos.
Conclusiones de los revisores: las conclusiones de los autores están en consonancia con los resultados. Los resultados de este estudio sobre la mortalidad ya fueron incluidos en un metaanálisis1 por lo que no añaden nueva información sobre ese desenlace. No obstante, la publicación de este ensayo permite valorar el efecto de la DDS en la incidencia de infección en una población preferentemente quirúrgica con una baja incidencia de neumonía. Se observa una disminución importante en la incidencia de todas las infecciones. Otro aspecto relevante que comunican los autores es la ausencia de aparición de resistencia antimicrobiana durante el período de estudio (24 meses).