Describir las prácticas relacionadas a ventilación mecánica (VM) en Argentina y explorar los factores asociados a la mortalidad en UCI en esta población.
DiseñoSe realizó un estudio observacional, prospectivo, multicéntrico.
ÁmbitoUnidad de Cuidados Intensivos.
PacientesIncluimos pacientes mayores de 18 años ingresados en las UCI participantes que requirieron VM invasiva durante al menos 12 horas desde el ingreso a la institución de salud.
IntervencionesNinguna.
VariablesTodas las variables se clasificaron en tres categorías: variables relacionadas con factores demográficos y clínicos antes de la VM, factores relacionados con el primer día de VM, y factores relacionados con los eventos ocurridos durante la VM (complicaciones y destete de la VM). El destete de la ventilación mecánica y la mortalidad se clasificaron según WIND (Weaning according to a New Definition).
ResultadosEl análisis primario incluyó a 950 pacientes. La principal indicación de VM fue insuficiencia respiratoria aguda (58% de los pacientes). El modo de ventilación inicial fue ventilación mandatoria continua con control de volumen en el 75% de los casos. La mortalidad en UCI y hospitalaria fue del 44,6% y 47,9%, respectivamente. Las variables identificadas como predictoras independientes de mortalidad en UCI fueron edad (OR 3,48 IC 95%, 1,22-11,66; p=0,028), fracaso en la implementación de ventilación mecánica no invasiva (VNI) antes de VM (OR 2,76, IC 95%, 1,02-7,10; p=0,038), diagnóstico de sepsis (OR 2,46, IC 95%, 1,09-5,47; p=0,027) y fracaso de la extubación (OR 4,50, IC 95%, 2,05-9,90; p<0,001).
ConclusionesEl presente estudio permitió describir las características y evolución clínica de los pacientes que recibieron ventilación mecánica en Argentina, encontrando como principal resultado que la mortalidad fue mayor a la reportada en estudios internacionales.
To describe mechanical ventilation (MV) practices in Argentina, and to explore factors associated with ICU mortality in this population.
DesignA prospective, multicenter, observational study was carried out.
SettingIntensive Care.
PatientsWe enrolled patients above 18 years old admitted to any of the participating ICUs requiring invasive MV for at least 12hours since the admission to the healthcare institution, including MV initiation in emergency department, operating room or other hospitals.
InterventionsNone.
VariablesAll variables were classified into three categories: variables related to demographic and clinical factors before the MV, factors related to the first day on MV, and factors related to events happening during the MV (complications and weaning from MV). Mechanical ventilation weaning and mortality were classified according to WIND.
ResultsThe primary analysis included 950 patients. The main indication for MV was acute respiratory failure (58% of patients). Initial ventilation mode was volume control-continuous mandatory ventilation in 75% of cases. ICU and hospital mortality were 44.6% and 47.9% respectively. The variables identified as independent predictors of mortality in ICU were age (OR3.48 IC95% 1.22-11.66; p=0.028), failure to implement NIV before MV (OR 2.76, IC 95%, 1.02-7.10; p=0.038), diagnosis of sepsis (OR 2.46, IC 95%, 1.09-5.47; p=0.027) and extubation failure (OR 4.50, IC 95%, 2.05-9.90; p<0.001).
ConclusionsThe present study allowed us to describe the characteristics and clinical course of the patients who received mechanical ventilation in Argentina, finding as the main result that mortality was higher than that reported in international studies.
La ventilación mecánica (VM) invasiva representa una herramienta fundamental en el manejo de los pacientes con insuficiencia respiratoria aguda (IRA). La evidencia actual muestra que varias intervenciones destinadas a prevenir la lesión pulmonar inducida por el ventilador y optimizar las estrategias de destete tienen un gran impacto en la duración de la ventilación mecánica y en la mortalidad1–5. Varios estudios epidemiológicos han investigado las diferentes tendencias de implementación de la ventilación mecánica en todo el mundo6–8. Además, estos estudios han compartido información útil que ha llevado a actualizar el punto de vista de la práctica clínica habitual de los pacientes en VM.
En América Latina, los datos epidemiológicos sobre los patrones de implementación de VM son escasos. Hasta donde sabemos, no existen estudios publicados sobre datos epidemiológicos en una población general de pacientes con ventilación mecánica invasiva en Argentina9,10. Para abordar este tema, buscamos describir las prácticas de ventilación mecánica en Argentina y explorar los factores asociados con la mortalidad en la Unidad de Cuidados Intensivos (UCI) en esta población.
Material y métodosRealizamos un estudio prospectivo, multicéntrico y observacional entre el 1 de septiembre de 2019 y el 31 de diciembre de 2019, en Unidades de Cuidados Intensivos de Argentina. El protocolo del estudio original fue aprobado por el Comité de Ética de la Sociedad Argentina de Terapia Intensiva con el número N.° 1 2019 y registrado en clinicaltrials.gov (número NCT04107467). Cada centro de salud participante obtuvo la correspondiente aprobación por parte de su propio comité de ética. El estudio se realizó siguiendo las directrices de Strengthening the Reporting of Observational Studies in Epidemiology (STROBE) para estudios de cohortes observacionales11.
Se incluyeron pacientes mayores de 18 años ingresados en cualquiera de las UCI participantes que requirieran VM invasiva durante al menos 12 horas desde el ingreso a la institución participante; pacientes que hayan iniciado la ventilación mecánica fuera de la UCI en un servicio diferente (áreas de emergencias o quirófano), o que hayan ingresado desde otra institución y fueran trasladados a la UCI de una unidad participante. Se excluyeron los sujetos ingresados a las UCI pediátricas, Salas de Reanimación o Recuperación de Anestesia o Unidades de Cuidados Coronarios. Los pacientes solo se incluyeron en su primer ingreso a la UCI. No se incluyeron en el análisis los pacientes con más del 10% de datos faltantes sobre variables clave utilizadas para construir el modelo de predicción.
Recolección de los datos y procesamientoLos datos fueron recolectados diariamente entre las 8:00 am y las 11:00 am por el co-investigador del estudio asignado para cada unidad participante, o por cualquier miembro del equipo designado para el estudio, utilizando formularios de reporte de casos (CRF) especialmente diseñados. La información recopilada se almacenó en un CRF en línea utilizando el software REDCap (Research Electronic Data Capture, Vanderbilt University, Tennessee, EE. UU.) instalado en los servidores del Centro del Parque, Buenos Aires, Argentina, para garantizar la protección y confidencialidad de los datos de acuerdo con la Declaración de Helsinki12,13. Todos los responsables de los centros participantes tuvieron acceso a la página web en la que se dispuso de toda la documentación relativa al estudio, incluyendo la definición operativa de las variables, el manual de operaciones y los enlaces correspondientes para facilitar el cálculo de puntuaciones relacionadas con la gravedad de la condición del paciente.
Para minimizar la falta de datos, se habilitó una aplicación móvil para la carga de datos fuera de línea. Los pacientes fueron seguidos hasta el día 28 desde la inscripción o hasta el alta hospitalaria o la muerte, lo que ocurriera primero.
Todos los investigadores principales del estudio (GAP, EG, MA, EN y JHD) brindaron apoyo y retroalimentación vía correo electrónico a los coinvestigadores locales de los centros participantes y también se puso a disposición una línea telefónica para responder consultas y brindar apoyo inmediato.
Los coinvestigadores locales fueron responsables de capacitar a su equipo en la recopilación de datos y el control de calidad. La consistencia de los datos fue evaluada diariamente (datos faltantes, valores atípicos, errores de carga) por uno de los investigadores principales (EN). Siempre que se requirió más información sobre los datos, los demás miembros del equipo de investigación (GAP, EG, MA, EN y JHD) se pusieron en contacto con los investigadores de los centros participantes.
Análisis estadísticoEl resultado primario fue la mortalidad en la UCI. Todas las variables se clasificaron en tres categorías: variables relacionadas con factores demográficos y clínicos antes de la VM, factores relacionados con el primer día de VM y factores relacionados con los eventos ocurridos durante la VM (complicaciones y destete de la VM). El destete de la ventilación mecánica y la mortalidad se clasificaron según la definición del estudio WIND14. Los datos continuos se informaron como media y desvío estándar (DE) o como mediana y rango intercuartílico [IQR 25-75], según corresponda. El análisis de normalidad se realizó mediante la prueba de Shapiro-Wilk. Los datos categóricos se expresaron como valores absolutos y porcentajes. Se realizó la prueba t de Student o la prueba U de Mann-Whitney para comparar variables continuas según fuera apropiado. Se utilizó la prueba de chi-cuadrado o la prueba exacta de Fisher para comparar variables categóricas. Para identificar los predictores de mortalidad, ajustamos un modelo de regresión logística con predictores clave como variables independientes y mortalidad en UCI como variable dependiente. La relación entre el resultado y la exposición se determinó inicialmente mediante análisis univariado. Las variables seleccionadas para el análisis multivariado fueron aquellas consideradas como relevantes por los autores y/o que tuvieron un valor de p<0,1 en el análisis anterior. Se evaluó la linealidad entre las covariables numéricas y la variable dependiente15. En ausencia de linealidad, se estratificaron de manera similar a lo reportado previamente en la bibliografía6,9,10. Para las variables categóricas multinivel, el nivel de referencia se seleccionó de acuerdo con la menor probabilidad relacionada con la variable dependiente. Se realizaron análisis de sensibilidad utilizando diferentes criterios para seleccionar el modelo final (best-subset, backward, Recursive feature Elimination)15,16. Se seleccionó el modelo con menor valor de criterio de información de Akaike. Todas las variables seleccionadas se informaron con su correspondiente odds ratio (OR) y su respectivo intervalo de confianza (IC) del 95%. La bondad de ajuste del modelo final se analizó mediante la prueba de Hosmer-Lemeshow, y la capacidad de discriminación del mismo se evaluó mediante la AUC (area under the curve) y su IC 95%. Finalmente, el poder predictivo del modelo se evaluó mediante K-fold cross-validation (10-folds)16. Como se trata de un estudio observacional, decidimos incluir tantos pacientes como fuera posible, sin un tamaño de muestra predeterminado. Los datos se analizaron con el software R versión 3.6.217.
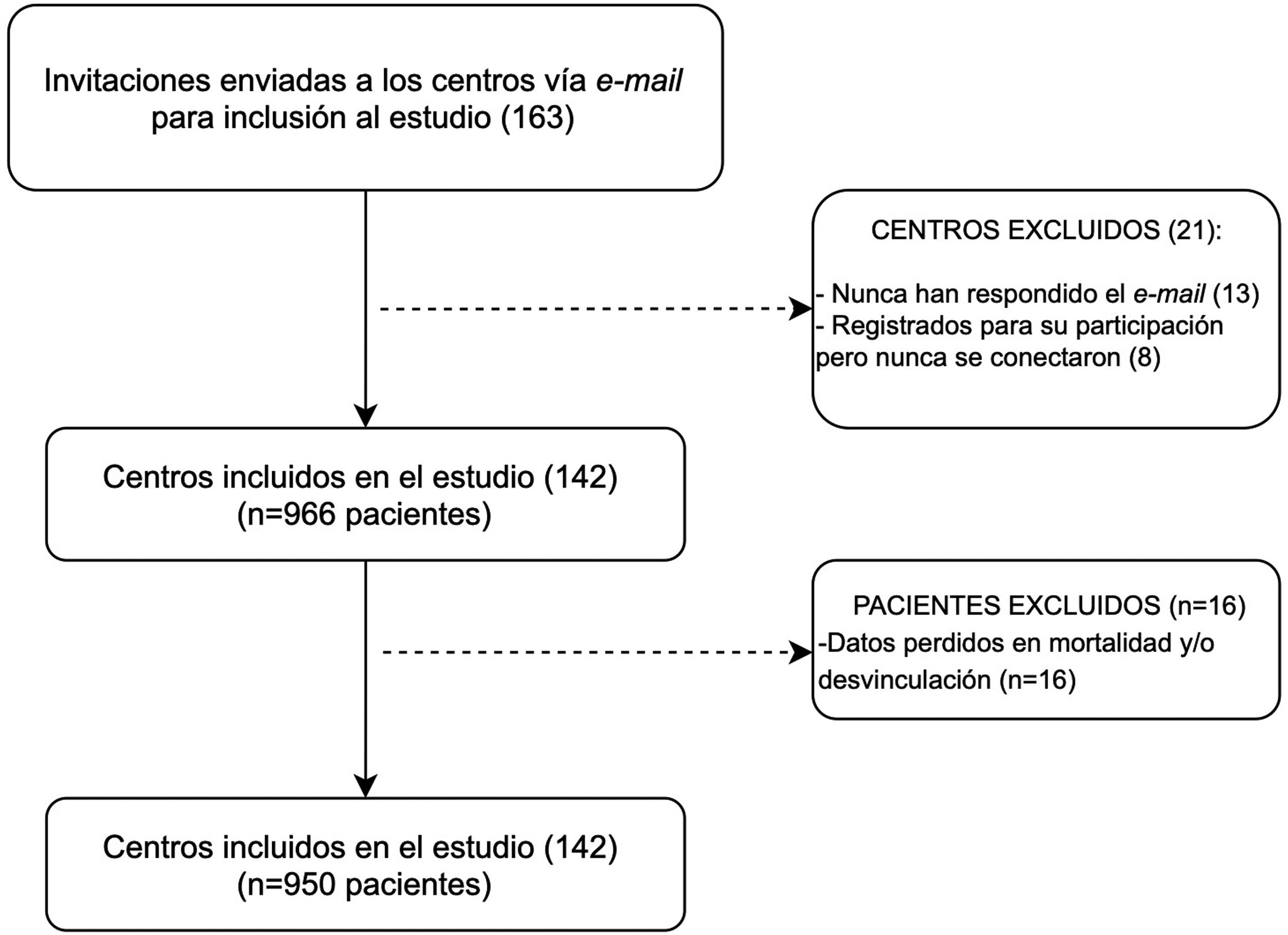
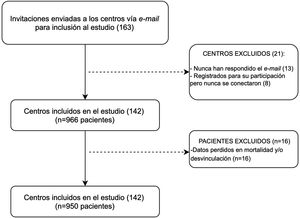
ResultadosUnidades participantes y pacientes incluidosParticiparon un total de 142 unidades (de 22 provincias y la Ciudad Autónoma de Buenos Aires, fig. 1) que representan el 14% del total de UCIs argentinas, el 48,5% de ellas en hospitales públicos (n=461) y el 51,5% en instituciones privadas (n=489)18. El análisis primario incluyó a 950 pacientes, 41,1% (n=390) de género femenino, con una edad media de 58,1 (18,5) años y SAPS II 46,8 (16,7). La principal indicación de VM fue la insuficiencia respiratoria aguda (58% [n=555] pacientes). Las características basales se describen en la tabla 1.
Características de pacientes admitidos a UCI. Variables demográficas y de inicio de ventilación mecánica
| Variables | Total (n=950) | Vivos (n=526) | Muertos (n=424) | OR (CI 95%) | p-valor | Datos perdidosn (%) |
|---|---|---|---|---|---|---|
| Género femenino, n (%) | 390 (41,1) | 221 (42,0) | 169 (39,9) | 0,91 (0,70-1,19) | 0,502 | 0 (0) |
| Edad, media (ds) | 58,1 (18,5) | 55,0 (19,3) | 62,1 (16,6) | 1,02 (1,01-1,03) | <0,001 | 0 (0) |
| IMC, media (ds), kg | 27,8 (6,8) | 27,9 (6,9) | 27,7 (6,6) | 1,00 (0,97-1,02) | 0,681 | 0 (0) |
| Índice de Charlson, mediana [RIQ] (n=892) | 4 [1-6] | 3 [1-5] | 4 [2-6] | 1,19 (1,13-1,25) | <0,001 | 58 (6,1) |
| SAPS II, media (ds) (n=879) | 46,8 (16,7) | 44 (17,2) | 50 (17,6) | 1,02 (1,01-1,03) | <0,001 | 71 (7,5) |
| Región geográfica* | - | - | - | - | - | |
| CABA, n (%) | 268 (28,2) | 167 (31,7) | 101 (23,8) | 1 | N/A | |
| PBA, n (%) | 289 (30,4) | 150 (28,5) | 139 (32,8) | 1,53 (1,09-2,15) | 0,013 | |
| Centro, n (%) | 186 (19,6) | 93 (17,7) | 93(21,9) | 1,65 (1,13-2,42) | 0,009 | 0 (0) |
| Cuyo, n (%) | 57 (6,0) | 37 (7,0) | 20 (4,7) | 0,89 (0,48-1,61) | 0,713 | |
| Norte, n (%) | 105 (11,1) | 57 (10,8) | 48 (11,3) | 1,39 (0,88-2,20) | 0,155 | |
| Patagonia, n (%) | 45 (4,7) | 22 (4,2) | 23 (5,4) | 1,73 (0,91-3,28) | 0,091 | |
| Tipo de institución | - | - | - | - | - | |
| Pública | 461 (48,5) | 254 (54,7) | 210 (45,3) | 1 | N/A | 0 (0) |
| Privada | 489 (51,5) | 273 (55,8) | 216 (44,2) | 0,96 (0,74-0,24) | 0,769 | |
| Tiempo de admisión a la UCI desde el ingreso al hospital, días, mediana [RIQ] | 0 [0-2] | 0 [0-1] | 0 [0-3] | 1,04 (1,02-1,07) | <0,001 | 0(0) |
| Falla de VNI antes de la VM, n (%) | 102 (10,7) | 43 (8,2) | 59 (13,9) | 1,82 (1,20-2,77) | 0,005 | 0 (0) |
| Causas de VM, n (%) | - | - | - | - | - | |
| IRA | 555 (58,4) | 296 (31,1) | 260 (27,3) | 1 | NA | 0 (0) |
| IRA en EPC | 79 (8,3) | 39 (4,1) | 41 (4,3) | 1,17 (0,73-1,88) | 0,509 | |
| Coma | 301 (1,7) | 182 (19,1) | 120 (12,6) | 0,76 (0,57-1,01) | 0,056 | |
| ENM | 15 (1,6) | 10 (1) | 5 (0,5) | 0,57 (0,18-1,63) | 0,313 | |
| PaO2/FIO2 previo a VM, media (ds) (n=312) | 236,7 (136,0) | 265,0 (142,0) | 208,0 (123,6) | 0,99 (0,98-0,99) | <0,001 | 638 (67,1) |
IMC: índice de masa corporal; SAPS II: Simplified Acute Physiology Score; UCI: unidad de cuidados intensivos; VNI: ventilación mecánica no invasiva; VM: ventilación mecánica; IRA: insuficiencia respiratoria aguda; EPC: enfermedad pulmonar crónica; ENM: enfermedad neuromuscular.
Regiones geográficas: CABA: ciudad autónoma de Buenos Aires; PBA: provincia de Buenos Aires; Centro: Córdoba, Santa Fe y Entre Río; Cuyo: Mendoza, San Luis y San Juan; Norte: Tucumán, Salta, Misiones, Chaco, Corrientes, Santiago del Estero, Jujuy, Formosa, Catamarca y La Rioja; Patagonia: Río Negro, Neuquén, Chubut, La Pampa, Santa Cruz y Tierra del Fuego.
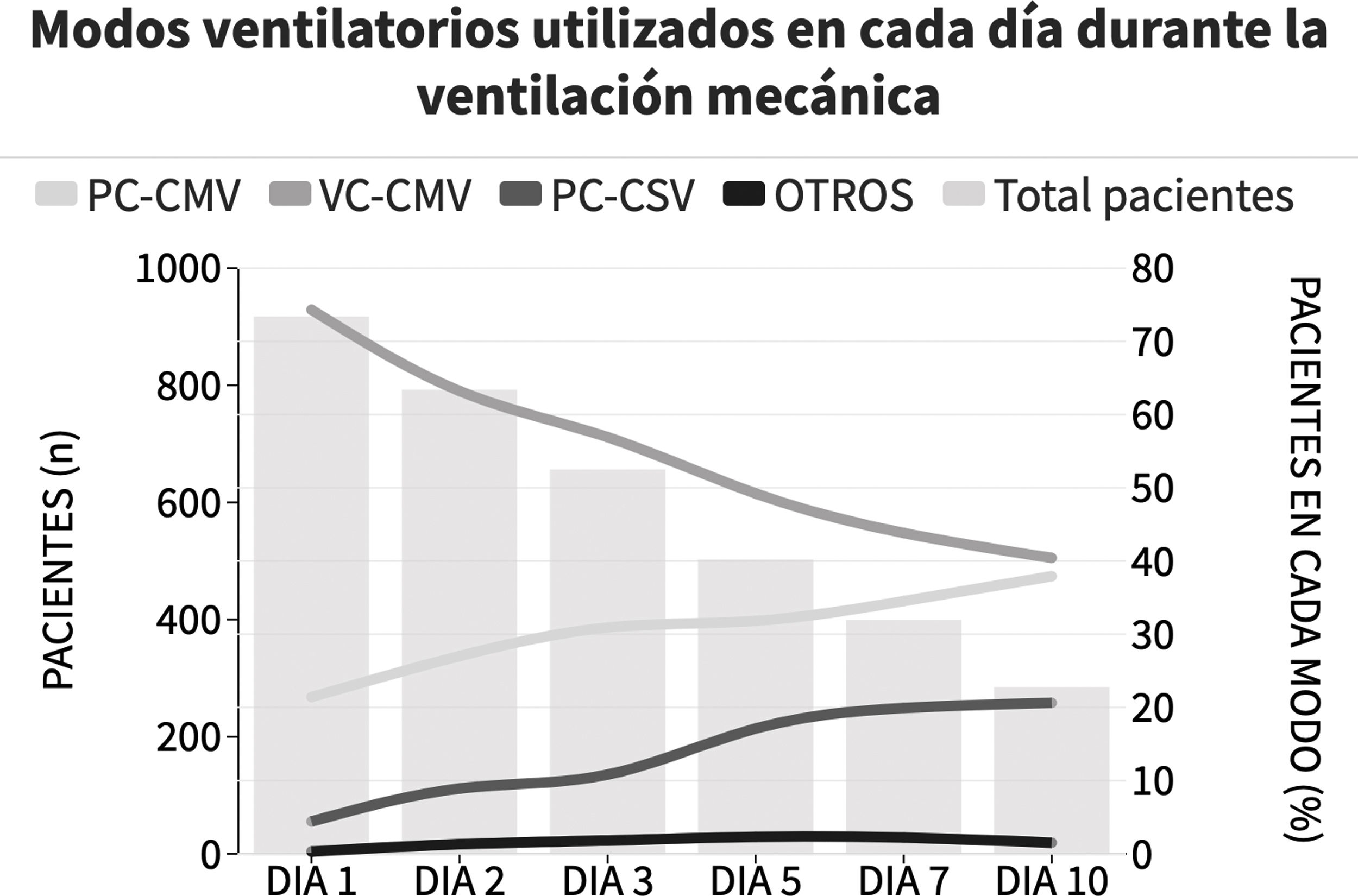
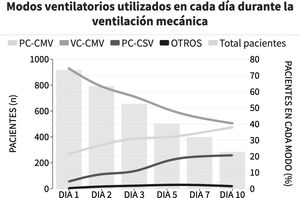
El modo de ventilación inicial fue ventilación mandatoria continua con control de volumen (VC-CMV) en el 75% de los casos (n=677) (fig. 2). Independientemente del modo de ventilación utilizado, el volumen corriente espirado (Vt) fue inferior a 8ml/kg de peso corporal predicho en el 75,1% de los casos (n=663), con una presión positiva al final de la espiración (PEEP) inferior a 8 cmH2O en el 64,8% (n=585). La presión meseta se midió en más del 80% de los casos (n=781). La presión meseta media (DE) y la driving pressure fueron 18 (4,6) y 11,2 (3,9) cmH2O, respectivamente. En el primer día de ventilación mecánica, la presión pico, la presión meseta y la driving pressure fueron significativamente más bajas en el grupo de sobrevivientes (p<0,001) (fig. 3 y material complementario electrónico A).
Proporción de pacientes en ventilación mecánica según modo seleccionado durante la estadía en UCI.
Cada línea representa la proporción de pacientes en cada modo de ventilación mecánica a lo largo del seguimiento. La altura de las barras representan el número de pacientes cada día en la UCI. PC-CMV: Presión Control-Ventilación Mandatoria Continua; VC-CMV: Volumen Control-Ventilación Mandatoria Continua; PC-CSV: Presión Control-Ventilación Espontánea Continua.
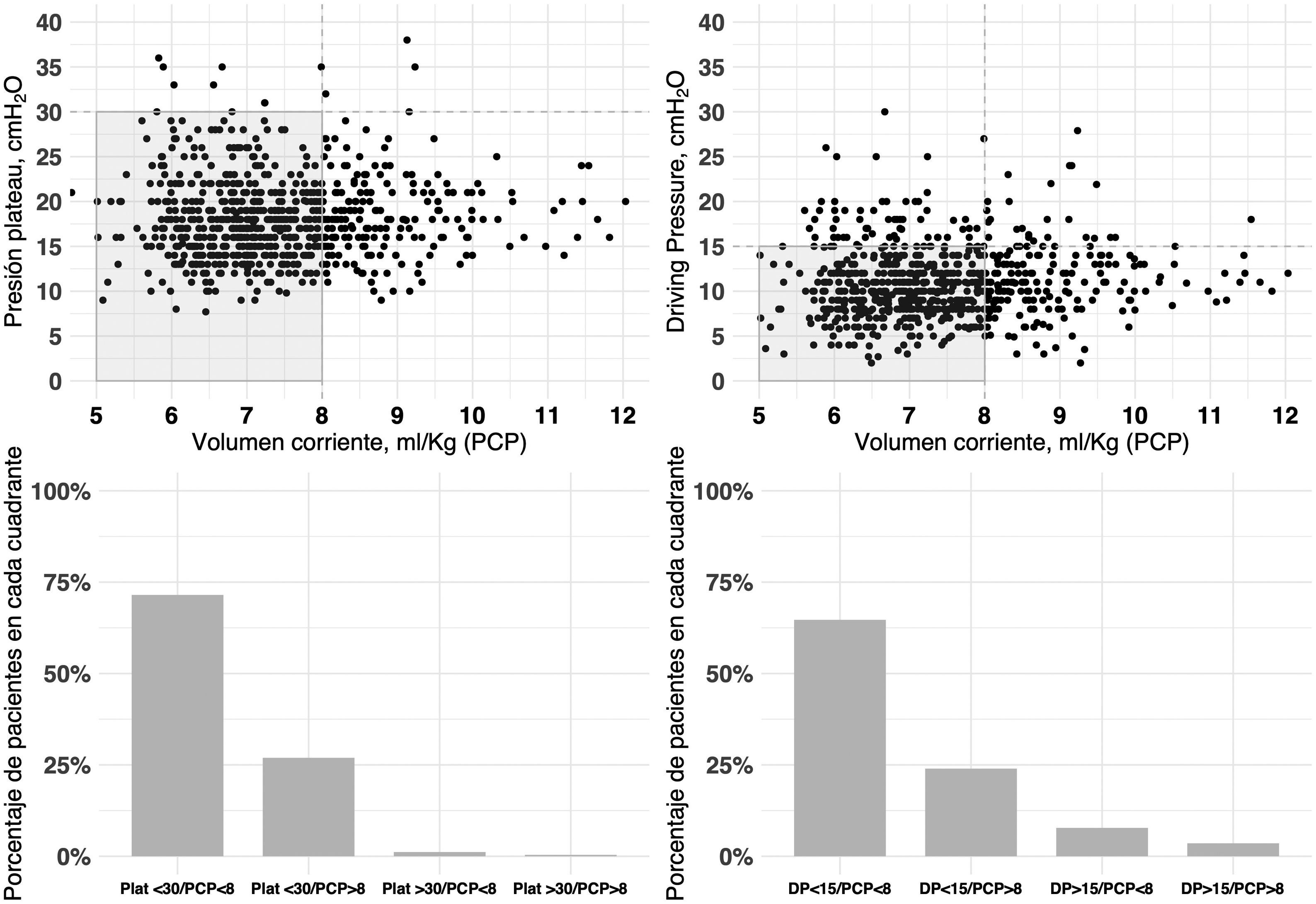
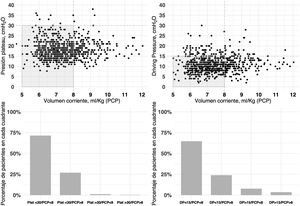
Relación entre la presión plateau, driving pressure y el volumen corriente (mL/kg) expresado en peso corporal predicho (PCP) durante el primer día de soporte ventilatorio.
La figura representa la distribución del volumen corriente del día 1 frente a la presión plateau (izquierda: figura superior e inferior) y del volumen corriente frente a la driving pressure (derecha: figura superior e inferior) para cada paciente. La mayoría de los pacientes se encontraban dentro de los límites de la ventilación protectora, definida como presión meseta inferior o igual a 30cmH2O, driving pressure inferior o igual a 15cmH2O y volumen corriente inferior o igual a 8mL/kg de peso corporal predicho. Los datos se refieren al primer día de ventilación mecánica.
Se registró sepsis en el 29,7% de los casos (n=281), neumonía asociada a la ventilación mecánica (NAVM) en el 17,6% (n=166) y síndrome de distrés respiratorio agudo (SDRA) en el 12,9% (n=122). La sedación se administró mediante infusión continua en el 86% de los sujetos incluidos (n=815) y el bloqueo neuromuscular (BNM) se utilizó en el 11,4% (n=108). El 57% de los pacientes (n=540) presentaba al menos un fallo orgánico, siendo el más frecuente el fallo cardiovascular (37,8%; n=359) (tabla 2).
Variables relacionadas con complicaciones durante la ventilación mecánica
| Variables | Total (n=950) | Vivos (n=526) | Muertos (n=424) | OR (CI 95%) | p-valor | Datos perdidosn (%) |
|---|---|---|---|---|---|---|
| NAVM, n (%) (n=945) | 166 (17,6) | 87 (16,6) | 79 (18,7) | 1,15 (0,82-1,61) | 0,402 | 5 (0,5) |
| Sepsis, n (%) (n=945) | 281 (29,7) | 108 (20,7) | 173 (41,0) | 2,67 (2,01-3,57) | <0,001 | 5 (0,5) |
| SDRA, n (%) (n=945) | 122 (12,9) | 39 (7,5) | 83 (19,7) | 3,04 (2,04-4,60) | <0,001 | 5 (0,5) |
| Prono, n (%) (n=945) | 41 (4,3) | 13 (2,5) | 28 (6,6) | 2,79 (1,45-5,63) | 0,003 | 5 (0,5) |
| Sedación en BIC, n (%) (n=945) | 815 (86,2) | 434 (83,0) | 381 (90,3) | 1,91 (1,29-2,85) | 0,001 | 5 (0,5) |
| Uso de BNM, n (%) | 108 (11,4) | 45 (8,6) | 63 (14,9) | 1,86 (1,25-2,81) | 0,003 | 0 (0) |
| DAUCI (n=946) | - | - | - | - | - | |
| Sí, n (%) | 142 (15,0) | 93 (17,8) | 49 (11,6) | 1 | N/A | 4 (0,4) |
| No, n (%) | 361 (38,2) | 276 (52,8) | 85 (20,1) | 0,58 (0,38-0,89) | 0,013 | |
| Delirium (n=945) | - | - | - | - | - | |
| Sí, n (%) | 168 (17,8) | 126 (24,1) | 42 (10,0) | 1 | N/A | |
| No, n (%) | 360 (38,1) | 266 (50,9) | 94 (22,3) | 1,06 (0,70-0,63) | 0,786 | 5 (0,5) |
| Sin falla de órganos, n (%) (n=950) | 410 (43,2) | 323 (61,4) | 87 (20,5) | 0,16 (0,12-0,22) | <0,001 | 10 (1) |
| Falla cardiovascular, n (%) (n=950) | 359 (37,8) | 124 (23,6) | 235 (55,4) | 4,03 (3,06-5,33) | <0,001 | 10 (1) |
| Falla hepática, n (%) (n=950) | 105 (11,1) | 33 (6,3) | 72 (17,0) | 3,06 (2,00-4,77) | 0,005 | 10 (1) |
| Falla renal, n (%) (n=950) | 302 (31,8) | 86 (16,3) | 216 (50,9) | 5,31 (3,95-7,20) | <0,001 | 10 (1) |
| Falla hematológica, n (%) (n=950) | 119 (12,5) | 31 (5,9) | 88 (20,8) | 4,18 (2,74-6.,) | 0,003 | 10 (1) |
| Falla neurológica, n (%) (n=950) | 139 (14,6) | 48 (9,1) | 91 (21,5) | 2,72 (1,88-3,99) | <0,001 | 10 (1) |
NAVM: neumonía asociada a la ventilación mecánica; SDRA: Síndrome de Distress Respiratorio Agudo; BIC: bomba de infusión continua; BNM: bloqueantes neuromusculares; DAUCI: debilidad adquirida en la unidad de cuidados intensivos (Ver suplemento electrónico C).
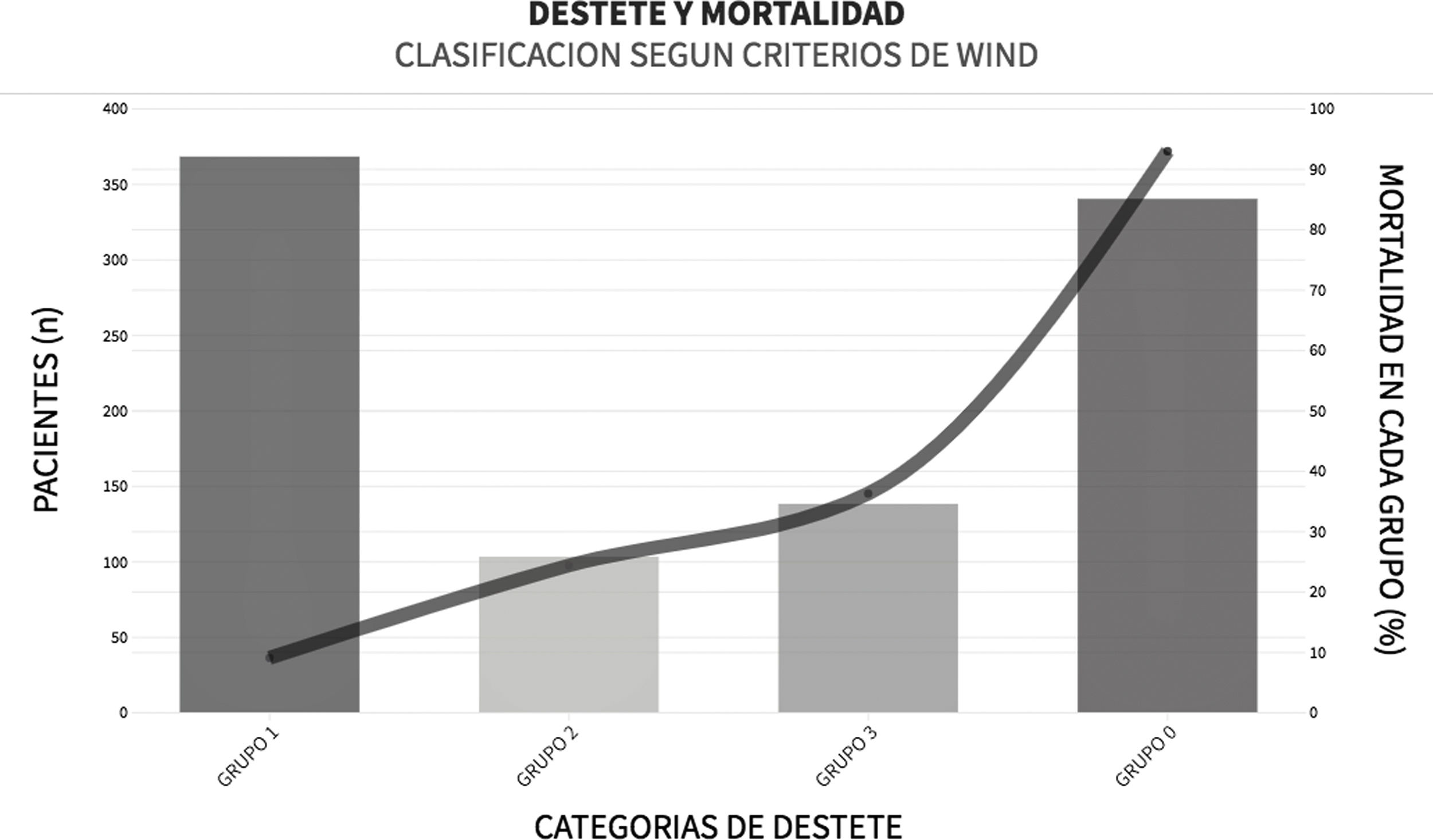
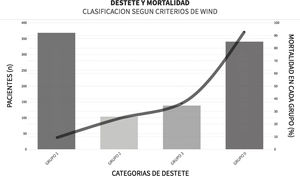
En cuanto al proceso de liberación de la VM, el 38,5% (n=365) de los pacientes fueron liberados dentro de las primeras 24 horas de su primera prueba de respiración espontánea (PRE) (fig. 4). La mediana [IQR] de días de VM fue de 6 [2-13]. La prueba de «tubo en T» se utilizó como método PRE en el 72,5% (n=419) de los casos. El 16% (n=75) de los pacientes fracasó a la extubación. Se utilizó ventilación no invasiva (VNI) para prevenir el fracaso de la extubación en el 6,8% de los casos (n=65). La proporción de pacientes traqueostomizados fue del 22,4% (n=213) (material complementario electrónico B).
Destete según la clasificación WIND14 y mortalidad dentro de cada grupo.
GRUPO 0: Nunca entró en el proceso de destete; GRUPO 1: Destete terminado dentro de las 24 horas siguientes a la primera prueba de respiración espontánea (PRE); GRUPO 2: Destete terminado entre el segundo día y la primera semana después de la primera PRE; GRUPO 3: No hubo destete exitoso siete días después de la primera PRE.
Esta figura muestra el número de pacientes (altura de las barras) para el grupo correspondiente de destete según WIND y la mortalidad (línea continua).
La mortalidad en UCI y hospitalaria fue del 44,6% (n=424) y del 47,9% (n=455), respectivamente, con una mediana (IQR) de 10 [5-20] y de 17 [9-30] días de estancia en cada caso (material complementario electrónico B). Entre los pacientes con IRA como principal causa de VM, las tasas de mortalidad más altas fueron en sepsis (62,6%, n=62), SDRA (60%, n=15) y neumonía (58%, n=52). De todas las variables consideradas en el modelo univariado e incluidas en el modelo multivariado, las identificadas como predictoras independientes de mortalidad en UCI fueron la edad (mayor de 70 años), la implementación de VNI antes de la VM, el diagnóstico de sepsis y el fracaso de extubación antes de las 72 horas (tabla 3).
Análisis de regresión logística múltiple para variables asociadas a mortalidad
| Mortalidad | |||
|---|---|---|---|
| Predictores | OR | IC (95%) | P-valor |
| Edad | |||
| Edad<40 años | Ref | Ref | Ref |
| Edad 40-70 años | 0,98 | 0,33-3,33 | 0,972 |
| Edad>70 años | 3,48 | 1,22-11,66 | 0,028 |
| Falla renal | 2,08 | 0,90-4,68 | 0,079 |
| Uso de VNI antes de VM | 2,76 | 1,02-7,10 | 0,038 |
| Sepsis | 2,46 | 1,09-5,47 | 0,027 |
| Falla hepática | 2,76 | 0,90-7,86 | 0,064 |
| Falla de extubación (72 h) | 4,50 | 2,05-9,90 | <0,001 |
VNI: ventilación no invasiva; VM: ventilación mecánica; IC: intervalo de confianza; OR: odds ratio; Área bajo la curva (ROC) para predecir mortalidad (95% IC): 0,79 (0,71-0,87).
Hosmer-Lemeshow X2: 8,654 (gl=8); P-valor=0,3804.
Este estudio multicéntrico aporta nuevos datos epidemiológicos sobre la ventilación mecánica en la Argentina. Nuestros hallazgos claves pueden resumirse de la siguiente manera: la mortalidad en UCI y hospitalaria de los pacientes sometidos a VM en la Argentina es superior a lo reportado internacionalmente6,8,10; tanto los días de VM como la necesidad de reintubación registrados fueron elevados; entre varios predictores potenciales la edad, el diagnóstico de sepsis, la utilización de VNI previo a la VM y la falla de extubación se relacionaron con mayor mortalidad.
Al igual que lo reportado en estudios internacionales, los motivos más frecuentes de inicio de la VM fueron la insuficiencia respiratoria aguda y coma.6,7,19.
En su estudio epidemiológico, Esteban et al.8 encontraron que el modo VC-CMV fue el más utilizado al inicio de la VM. Encontramos los mismos resultados en nuestro estudio; sin embargo, el porcentaje de utilización duplica al reportado anteriormente (EpVAr 2019: 74,9%; Esteban 2013: 38%).
Según datos derivados de nuestro estudio, la mortalidad en pacientes en VM durante más de 12 horas es alta en Argentina. Aunque la gravedad de los pacientes cuando ingresaron podría ser la razón de este alto porcentaje, otros estudios multicéntricos revelaron una mortalidad hasta un 15% menor en cohortes similares de pacientes en variables como la edad, SAPS II al ingreso y causas de VM6,8,10. En una población de similares características, Peñuelas y cols. atribuyen la mortalidad en UCI a cambios en la práctica clínica asociados a la implementación de una estrategia de ventilación protectora que permita mantener la presión de la vía aérea al final de la inspiración por debajo del nivel que se ha considerado perjudicial para el pulmón20. Sin embargo, el ajuste del ventilador durante el primer día no parece estar asociado con la mortalidad. Al igual que en otros informes internacionales, encontramos que variables como Vt y PEEP estaban dentro de rangos que podríamos considerar aceptables en términos de protección pulmonar6,7,10. También encontramos que los valores registrados en variables de monitorización como la driving pressure y la presión meseta fueron bajos21–23. Encontramos una alta tasa en el registro de la presión meseta (90%), un porcentaje muy superior al registrado en el estudio LUNG SAFE (42%), lo que podría mostrar interés en la protección pulmonar23. Esto podría explicarse por el aumento de la adherencia al uso de protocolos de ventilación mecánica protectora24.
Encontramos cuatro variables independientes que se asociaron con mayor mortalidad: edad (mayor de 70 años), diagnóstico de sepsis, uso de VNI antes de la VM y falla en la extubación. Al igual que Estenssoro y cols. describieron en 201825, el requerimiento de ventilación mecánica en pacientes diagnosticados de sepsis es un predictor independiente de mortalidad. Desafortunadamente, no podemos proporcionar información sobre la implementación de la VNI como primera estrategia de soporte ventilatorio, ya que no se registraron los pacientes que tuvieron éxito en la VNI de inicio. Además, en relación al fracaso de la extubación, los pacientes no parecen haber sido extubados prematuramente ya que nuestra mediana de días de VM es similar a la reportada por Esteban en 20138. Sin embargo, el porcentaje de pacientes que son extubados dentro de las primeras 24 horas de la primera PRE es menor que lo informado por el estudio WIND (38,5% vs. 57%) 14. La PRE con «tubo en T» se utilizó en una gran proporción de pacientes (72,5%) a pesar de las últimas publicaciones en relación al proceso de destete de la VM; esta estrategia ha demostrado ser más exigente que otras para pacientes en VM26–29. Se sabe que la sedación puede tener un impacto negativo en los días libres de VM y en los días de UCI30,31. Según las variables registradas por nuestros investigadores, una gran proporción de pacientes estuvieron bajo sedación profunda en algún momento de su estancia en VM a pesar de que casi la mitad de los pacientes no presentaban fallas orgánicas. Esto podría ser un indicador del uso excesivo de sedantes en nuestra población, lo que podría haber afectado los resultados. Además, un dato que podría llevarnos a pensar en el uso excesivo de sedación es que, en nuestro estudio, el modo VC-CMV es el modo que se usó con mayor frecuencia, incluso al décimo día de VM, mientras que otros estudios reportan el uso de modos espontáneos por encima de otros modos antes de la primera semana de VM7-9.
Si bien se debería evaluar en un estudio diseñado específicamente para ello, creemos que el alto porcentaje de mortalidad reportado en nuestro estudio podría reflejar los obstáculos presentes en toda Argentina para la implementación rutinaria de protocolos relacionados con la atención general del paciente, como los descriptos en las guías PADIS32. Sin embargo, estos resultados disímiles en cuanto a mortalidad podrían reflejar diferencias en los recursos humanos y tecnológicos que no fueron considerados en nuestro estudio, o podrían reflejar los hallazgos de los estudios LUNG SAFE e ICON, en los que los países de ingresos medios bajos mostraron una mayor mortalidad por sepsis y SDRA que los países de ingresos altos33,34. Factores económicos y organizativos complejos en los países de ingresos medios bajos explican los peores resultados para los pacientes de la UCI. Las inequidades profundas, definidas como diferencias sistemáticas, injustas y evitables en los determinantes de la salud, como el nivel socioeconómico, la demografía y la geografía, pueden generar diferencias en el acceso a los servicios de salud en diferentes subgrupos de población, lo que afecta los resultados relacionados con la salud35. Además, en los países de ingresos medios bajos, los sistemas de salud suelen estar fragmentados en los sectores público y privado, que mantienen las diferencias según el nivel socioeconómico y afectan la prestación de atención de la salud, particularmente los cuidados críticos36. Llamativamente, en nuestro estudio no encontramos diferencias en la mortalidad entre estos sectores de la salud. Quizás esto se pueda explicar por el hecho de que tampoco encontramos una diferencia estructural en los recursos humanos, con una distribución similar en las proporciones médico/paciente, enfermera/paciente y kinesiólogo respiratorio/paciente entre un sector y en el otro (datos no publicados).
Sin embargo, nuestro estudio tiene algunas limitaciones. Primero, este es un análisis de datos clínicos recolectados prospectivamente de una amplia gama de UCIs en todo el país, con diferentes condiciones entre los pacientes y diferentes prácticas clínicas, algunas de las cuales podrían estar relacionadas con los resultados. Sin embargo, hemos realizado un análisis teniendo esto en cuenta en el modelo para minimizar el posible sesgo relacionado con las variables y, aunque hemos utilizado modelos multivariados, la presencia de factores de confusión no medidos puede persistir. En segundo lugar, los datos faltantes constituyen un problema en este tipo de estudios ya que favorecen la mala interpretación de los resultados. Para reducir este impacto se eliminaron los registros con más del 10% de datos faltantes en las variables relevantes. Por último, los datos recopilados en Argentina podrían no ser representativos de otros países de ingresos medios bajos y de otras regiones.
ConclusionesEl presente estudio permitió describir las características y evolución clínica de los pacientes que recibieron ventilación mecánica en Argentina, encontrando como principal resultado que la mortalidad fue mayor a la reportada en estudios internacionales. La edad, el diagnóstico de sepsis, el uso de la ventilación mecánica no invasiva como soporte inicial y el fracaso de la extubación se identificaron como variables predictoras independientes que aumentan el riesgo de muerte, siendo algunas de ellas potencialmente modificables. La información obtenida en este estudio resulta fundamental para nuestra especialidad, y constituye la base para el desarrollo de protocolos de atención destinados a optimizar el manejo de los pacientes en VM con el fin de mejorar los resultados en nuestro país.
Conflicto de interesesGAP recibió financiación para programas de enseñanza por parte de Medtronic Argentina y para programas de enseñanza por parte de Vapotherm Inc, EE. UU.
EG actualmente es empleado de Medtronic Argentina.
Los patrocinadores arriba enumerados no tuvieron ningún papel en el diseño del estudio, la recolección y el análisis de los datos, ni en la preparación del manuscrito.
Contribuciones de los autoresGAP concibió y diseñó el estudio, recogió, interpretó y analizó los datos, buscó en la literatura y redactó el manuscrito. EG, MA y JHD diseñaron el estudio, recogieron los datos y revisaron críticamente el manuscrito. EN diseñó el estudio, recogió los datos y revisó críticamente el manuscrito y analizó los datos.
Todos los autores aprobaron la versión final del manuscrito y aceptaron ser responsables de todos los aspectos del trabajo para garantizar que las cuestiones relacionadas con la exactitud e integridad de cualquier parte del trabajo se revisaran y resolvieran adecuadamente.
Judith Sagardía (Hospital Nacional Dr. Alejandro Posadas, Buenos Aires), Gretel R. Baez (Hospital de Trauma y Emergencia Dr. Federico Abete, Buenos Aires), Silvia Zidarich (Hospital Italiano de Córdoba, Córdoba), José Robles (Sanatorio Parque, Santa Fe), María del Carmen Gorostegui (Hospital Dr. Oscar Alende, Buenos Aires), Raul A. Gomez (Sanatorio de los Arcos, CABA), Marcela Ducrey (Hospital Italiano de Buenos Aires, CABA), Norberto Tiribelli (Complejo Médico PFA Churruca Visca, CABA), Lorena Krzisnik (Hospital el Cruce Dr. Nestor Kirchner, Buenos Aires), Evangelina Pereira Zamora (Hospital E. Vera Barros, La Rioja), Belen Spath (Clínica la Sagrada Familia, CABA), Marcela Gil (Hospital San Bernardo, Salta), Lorena Impagliazzo (Hospital del Carmen, Mendoza), Federico Iglesias (Hospital Italiano de La Plata, Buenos Aires), Ignacio Castro (Hospital Central, Mendoza), Sofia Iriarte (Sanatorio Nuestra Señora del Rosario, Jujuy), Carlos G. Sosa (Hospital de Clínicas José de San Martín, CABA), Santiago Izza (Hospital Cullen, Santa Fe), Maria R. Marteau Gonzalez (Hospital Español de Rosario, Santa Fe), Antonella Teves (Hospital Escuela Gral. José de San Martín, Corrientes), Damian Zarza Benitez (Sanatorio Trinidad Quilmes, Buenos Aires), Valeria Rienzi (Hospital General de Agudos Dr. Cosme Argerich, CABA), Leonardo Montelar (Hospital Provincial del Centenario, Santa Fe), Estela C. Cañete (Hospital Central de Formosa, Formosa), Alejandra Barrientos (Hospital Naval Pedro Mallo, CABA), Gaston Schmidt (Instituto Médico de Alta Complejidad, CABA), Alfredo Kamegawa (Clínica y Maternidad Suizo Argentina, CABA), Santiago Saavedra (Hospital Alemán, CABA), María L. Feijoo (Hospital Regional Dr. Ramon Carrillo, Sgo. del Estero), Daniel Varela (Hospital Universitario Fundación Favaloro -UTI 2, CABA), Manuel Ferreyra (Hospital Córdoba, Córdoba), Guillermo Chiappero (Hospital Fernandez, CABA), Silvia Bagnolo (Clínica Modelo de Lanus, Buenos Aires), Federico Puzzo (Clínica Monte Grande, Buenos Aires), Pablo Saul (Hospital Francisco Javier Muñiz, CABA), Hernán Nunia (Sanatorio Allende Nueva Córdoba, Córdoba), Mariana Piatti (Hospital Público Provincial de la Ciudad de Córdoba San Roque - UTI 1, Córdoba), Georgina Leites (Sanatorio San José, CABA), Daniela I Gilgado (Sanatorio Anchorena de San Martín, Buenos Aires), Gustavo Bongiorni (Sanatorio Allende Cerro, Córdoba), Romina Pratto (Sanatorio Anchorena Recoleta, CABA), Guillermina Garcia (Sanatorio Colegiales, CABA), Janet Vallejos (Hospital Eva Perón, Buenos Aires), Vanina E. Perri (HIGA Luisa Cravenna de Gandulfo, Buenos Aires), Sabrina Cagide (Hospital Houssay, Buenos Aires), Verónica Galende (Hospital Público Provincial de la Ciudad de Córdoba San Roque - UTI 2, Córdoba), Laura Bergallo (Sanatorio Mapaci, Santa Fe), Ariel A. Zacco (Hospital Nodal Dr. Alejandro Gutierrez, Santa Fé), Betsabe Calvet (Clínica Santa María, Mendoza), Mariana Aguirre (Hospital Santojanni-SR, CABA), Federico Camelli (Sanatorio Finochietto, CABA), Ricardo Gonzalez (Hospital Fiorito, Buenos Aires), Gustavo Chaparro (Instituto Médico Platense, Buenos Aires), Jose Gelmetti (HIGA San Martín de La Plata, Buenos Aires y Hospital Español, Buenos Aires), Cinthia Ferreyra (Hospital Escuela de Agudos Dr. Ramon Madariaga, Misiones), Claudia Aramayo (Hospital del Señor del Milagro, Salta), Alejandro Risso (Sanatorio Otamendi, CABA), Marcelo G Alonso (Clínica Pasteur, Neuquén), Mariela Mogadouro (Sanatorio Trinidad de Palermo, CABA), Lucas Semorile (Clínica de los Virreyes, CABA), Ayelen Baqueiro (Hospital Artemides Zatti, Río Negro), Florencia Di Vruno (Hospital Area Programa Bariloche Ramón Carrillo, Neuquén), Mariano L. Braccini (Instituto de Cardiología Juana Francisca Cabral, Corrientes), Eliana Roggero (Hospital Eva Perón, Santa Fé), Guillermo Pardal (HIGA San Roque, Buenos Aires), Roberto Teira (Instituto Argentino de Diagnóstico y Tratamiento, CABA), Ariel Chena (Hospital Luis C. Lagomaggiore, Mendoza), Sebastian Fredes (Sanatorio Mitre, CABA), María J. Sakugawa (HZGA Mariano y Luciano de la Vega, Buenos Aires), Adrian Gallardo (Sanatorio Clínica Modelo de Moron, Buenos Aires), Mariana Greca (Policlínico PAMI 1, Santa Fe), Anabella Reboredo (Clínica la Pequeña Familia, Buenos Aires), Mercedes N. Ruffo (Hospital Dr. Guillermo Rawson, San Juan), Mauricio Petre (Hospital de Alta Complejidad Cuenca Alta SAMIC, Buenos Aires), Marta Di Maria (HIGA Petrona V. de Cordero de San Fernando, Buenos Aires), Marcelino Díaz (Sanatorio Santa Fe, Santa Fe), Marco Bezzi (Hospital Santojanni UCI, CABA), Cecilia Ruffo (Clínica Sociedad Española de Socorros Mutuos, Mendoza), Pablo Lovazzano (CEMIC H.U. Saavedra, CABA), Mariano Setten (CEMIC H.U. POMBO, CABA), Maria C Villafañe (Hospital Carrillo de Ciudadela, Buenos Aires), Silvina Picon Fuster (Hospital Italiano de San Justo, Buenos Aires), Patricia Cordeiro (Sanatorio Juncal, Buenos Aires), María A Garcia (Hospital Misericordia Nuevo Siglo, Córdoba), Marina Busico (Clínica Olivos, Buenos Aires), Luciana Ayala Nogueira (Hospital Militar Regional de Paraná, Entre Ríos), Daniela V. Morales (Clínica Universitaria Reina Fabiola, Córdoba), Luis D. Fedes (Clínica San Agustín, Neuquén), Roberto Stratta (Sanatorio Santa Fe, Santa Fe), Iona García (Sanatorio de la Ciudad S.R.L, Chubut), Mónica Stefe (Trinidad Ramos Mejía, Buenos Aires), Monica Conde (Hospital Universitario UAI, CABA), Antonio Abdala (Hospial Alvarez, CABA), Tatiana Ruiz Jalil (Clínica Bazterrica, CABA), Alberto Quereda (Hospital Municipal del Carmen de Chacabuco, Buenos Aires), Dario S. Villalba (Hospital de Chivilcoy, Buenos Aires), Lucrecia Garcia Iriarte (Policlínico Modelo Cipolletti, Río Negro), María L. Quiles (Clínica del Valle, Chubut), Martin C. Lugaro (Hospital Profesor Dr. Luis Guemes, Buenos Aires), Marcelo Camargo (Hospital San Luis, San Luis), Pablo Staffolani (Hospital Santa Isabel de Hungría, Mendoza), Veronica N. Kosaka (Hospital de Autogestión SAMIC Iguazú, Misiones), Ana Mazzola (Hospital San Felipe, Buenos Aires), María V. Vilaseca (Trinidad San Isidro, Buenos Aires), Facundo Puchulu (Hospital Justo José de Urquiza, Entre Rios), Marianela B. Canil (Clínica Zabala, CABA), Josefina Argañaraz (Hospital Centro de Salud Zenón Santillán, Tucumán), Deborah Gelabert (Clínica 25 de Mayo, Buenos Aires), Jorge Gonzalez Nizzo (Sanatorio Adventista del Plata, CABA), Jose A. Grucci (Hospital Madre Catalina, San Luis), Veronica Lozano (Hospital Público Autogestión SAMIC el Dorado, Misiones), Ivonne Kunzi (Hospital de Rehabilitación Respiratoria María Ferrer, CABA), Matias Brizuela (Sanatorio Privado del Intenterio SRL, Tucumán), Gustavo Werber (Instituto de Transplante y Alta Complejidad – ITAC, CABA), Patricia A. Domenichini (Hospital Italiano Regional del Sur, Buenos Aires), Fernando Rios (Sanatorio Las Lomas, Buenos Aires), Melina Esteves (Hospital Privado Dr. Raul Matera, Buenos Aires), Damian Fernandez (Clínica Pasteleros, CABA), Ignacio Ledesma (Hospital Privado de Cordoba, Córdoba), Janina Lebus (Hospital Central Reconquista, Santa Fe y Sanatorio Norte SRL, Santa Fe), Nahuel Dargains (HIEA y C San Juan de Dios, Buenos Aires), Ayelen Garcia (Hospital Regional V. Sanguinetti, Chubut), Florencia Pugliese (Hospital Dr. D. Velez Sarsfield, CABA), María V. Migueles (Centro Integral de Salud Banda, Sgo. del Estero), Federico J. Gimenez (Centro de Cuidados Intensivos, San Juan), Daniela Inchaurrondo (Clínica Argentina, La Pampa), Sabrina E. Díaz (Sanatorio Español, Santa Fe), Daniela Coria (Hospital Público Descentralizado Dr. Marcial V. Quiroga, San Juan), Luis Corsiglia (IPENSA, Buenos Aires), Carlos A. Morales (Sanatorio Lavalle, Jujuy), Agustina Quijano (Hospital Público de Autogestión Dr. Arturo Oñativia, Salta), Fernanda Ignisci (Hospital Municipal de Agudos Dr. Pedro Ecay, Buenos Aires), Natalio O Grazziani (Clínica Santa Clara de la Provincia de San Juan, San Juan), María S. Fernandez Altamirano (Clínica Santa Maria, Córdoba), Agustina Jarque (Hospital Ramón Santamarina, Buenos Aires), Santiago Burgos (Hospital Regional de Ushuaia, Tierra del Fuego), Luis Sepúlveda (Clínica Adventista Belgrano, CABA), Nicolas Iezzi (Instituto de Investigaciones Médicas Alfredo Lanari, CABA), Marta Verduguez (Hospital Simplemente Evita, Buenos Aires), Melisa Diiorio (Hospital Sirio Libanes, CABA).
Este estudio fue presentado por G.A. Plotnikow en el 30° Congreso Argentino e Internacional de Terapia Intensiva, 4 de noviembre de 2020, Argentina (2.° Premio al mejor estudio del Congreso).