Este estudio analiza comparativamente las características clínicas, funcionales y oncológicas de los pacientes con cáncer, valorados para ingreso en la UCI, con el objetivo de identificar factores asociados a la admisión y desarrollar modelos predictivos específicos.
DiseñoSe realizó un estudio prospectivo, observacional y multicéntrico.
ÁmbitoTreinta y tres servicios de medicina intensiva de España.
Pacientes o participantesSe incluyeron pacientes con edad ≥18 años con tumores sólidos o neoplasias hematológicas valorados para ingreso en la UCI entre enero y junio de 2024.
IntervencionesNo hay intervención.
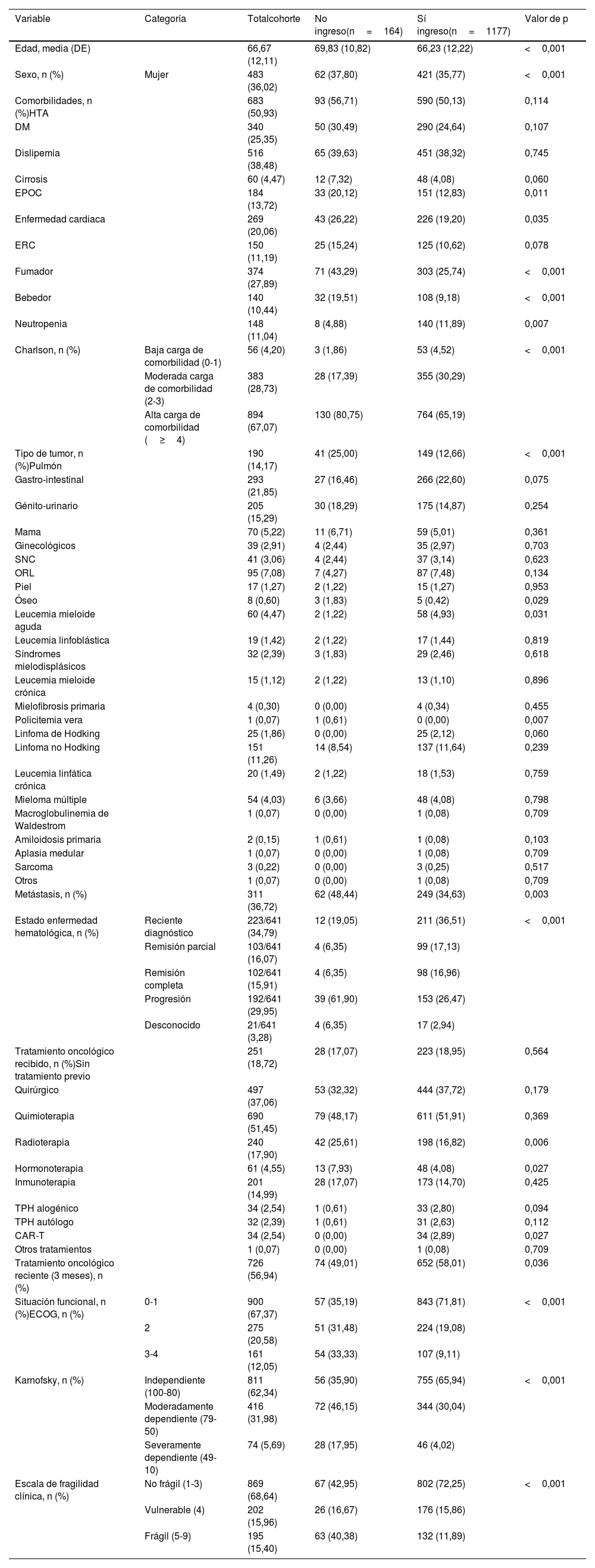
Variables de interés principalesSe recogieron variables demográficas, clínicas, funcionales, oncológicas y de gravedad, analizando diferencias entre los pacientes ingresados y no ingresados mediante regresión logística multivariante y modelos predictivos tipo LASSO.
ResultadosSe incluyeron 1.341 pacientes, ingresando en la UCI 1.177 (87,8%). La neutropenia, una edad menor o haber recibido un tratamiento oncológico reciente, entre otras, se asociaron a una mayor probabilidad de ingreso en la UCI. Los pacientes con metástasis o progresión de enfermedad hematológica presentaron menor probabilidad de ingreso. Los modelos predictivos mostraron una alta capacidad discriminativa tanto para tumores sólidos (con un área bajo la curva [AUC]: 0,79) como hematológicos (AUC: 0,82).
ConclusionesSe han desarrollado modelos predictivos de ingreso en la UCI seleccionando las variables no de forma aislada, sino en función de su contribución conjunta al poder predictivo global. El modelo denominado completo (Modelo 1) mostró la mejor capacidad predictiva, con un AUC: 0,79 (IC 95%: 0,75-0,84) para tumores sólidos y de 0,82 (IC 95%: 0,76-0,88) para tumores hematológicos.
This study compares the clinical, functional, and oncological characteristics of patients with cancer assessed for ICU admission, with the aim of identifying factors associated with admission and of developing specific predictive models.
DesignA prospective, observational, multicentre study.
SettingThirty-three Intensive Care Units (ICUs) across Spain.
Patients or participantsPatients aged 18 years or older with solid tumors or haematological malignancies assessed for ICU admission between January and June 2024 were included.
InterventionsNone.
Main variables of interestDemographic, clinical, functional, oncological, and severity variables were collected. Differences between admitted and non-admitted patients were analyzed using multivariate logistic regression and LASSO-type predictive models.
ResultsOne thousand three hundred forty-one patients were included, with 1,177 (87.8%) admitted to ICU. Neutropenia, younger age, and recent oncologic treatment, among other factors, were associated with a higher likelihood of ICU admission. Patients with metastasis or progression of the haematological disease had a lower probability of admission. The predictive models demonstrated high discriminative ability for both solid tumors (AUC 0.79) and haematological malignancies (AUC 0.82).
ConclusionsWe developed prognostic models for ICU admission by applying a multivariable approach, whereby variables were selected based on their joint contribution to the overall predictive accuracy rather than in isolation. The full model (Model 1) showed the best predictive capacity, with an area under the curve (AUC) of 0.79 (95% CI: 0.75-0.84) for solid and 0.82 (95% CI: 0.76-0.88) for haematological tumors.
Artículo
Diríjase al área de socios de la web de la SEMICYUC (www.semicyuc.org ) y pulse el enlace a la revista.