Los pacientes quemados pueden necesitar ingresos prolongados en el Servicio de Medicina Intensiva, tanto para la atención inicial como para el tratamiento pre y postoperatorio de las múltiples cirugías que precisan. La reanimación inicial del paciente quemado crítico requiere una adecuada monitorización para calcular la fluidoterapia necesaria para reponer las pérdidas y asegurar la perfusión tisular, pero sin excesos que aumenten el edema intersticial. Además, la monitorización puede evaluar la respuesta inflamatoria sistémica, que puede llevar a shock y a disfunciones orgánicas. Tras esta fase inicial nos encontraremos con un paciente crítico que requiere múltiples reintervenciones en situaciones no óptimas, por lo que necesitará cuidados especiales durante un largo periodo. Además, el Servicio de Medicina Intensiva ofrece la atención postoperatoria específica para la cirugía reconstructiva y el trasplante de tejidos compuestos (miembro superior y cara), en los que el éxito depende de un riguroso control mediante la monitorización y el tratamiento adecuados.
Burned patients may need prolonged admissions in the Intensive Care Service, both for initial care and for the pre and postoperative treatment of the multiple surgeries they require. The initial resuscitation of critically burned patients requires adequate monitoring to calculate the fluid therapy necessary to replenish the losses and ensure tissue perfusion, but without excesses that increase interstitial edema. In addition, monitoring can evaluate the systemic inflammatory response that can lead to shock and organic dysfunctions. After this initial phase we will find a critical patient who requires multiple reinterventions in non-optimal situations, so he will need special care over a long period of time. In addition, the Intensive Care Service offers specific postoperative care for reconstructive surgery and the transplantation of composite tissues (upper limb and face) in which its success depends on a rigorous control through adequate monitoring and treatment.
Las quemaduras constituyen un problema de salud pública a nivel mundial, y según la OMS provocan casi 200.000 muertes al año, de las cuales la mayoría se producen en los países más pobres. No existen datos exactos sobre la incidencia de lesiones por quemadura, pero en nuestro entorno se estiman en alrededor de 300 pacientes quemados por 100.000 habitantes y año, de los cuales unos 15 requieren ingreso hospitalario y solo una pequeña parte son ingresados en unidades de cuidados intensivos. El tratamiento de las quemaduras ha evolucionado a lo largo de los últimos años, reduciendo su mortalidad pero aumentando el impacto en las secuelas funcionales, estéticas y de calidad de vida. Todo esto conlleva un elevadísimo costo directo e indirecto por la pérdida de salarios, la atención prolongada de deformidades y los traumas emocionales. Las secuelas funcionales continúan siendo de gran relevancia en este grupo de pacientes, encontrando restricción de movimiento en el 20% de los mismos, incluso 5años después de la lesión. Los cambios estéticos afectan al 43% de los pacientes, incluso con quemaduras menores. El impacto en el ámbito laboral es muy importante, llegando a afectar al 50% de los pacientes adultos, y con una incapacidad laboral de hasta el 5%1.
Los pacientes con quemaduras extensas son pacientes críticos que requieren múltiples intervenciones quirúrgicas durante sus prolongadas estancias. Su pronóstico depende de una adecuada reanimación inicial, de un buen plan quirúrgico y de una adecuada continuidad asistencial entre cirugías. La escisión y la cobertura precoces han mejorado su pronóstico, pero el momento de la intervención y la cantidad de superficie a tratar en cada intervención debe ajustarse a la situación clínica del paciente. De igual forma, en las cirugías y en las curas posteriores debe tenerse en cuenta el estado del paciente para que estos procedimientos se realicen en las mejores condiciones y así puedan obtener los mejores resultados. Esto es extensible a patologías como la necrólisis epidérmica tóxica, que requieren un tratamiento semejante2.
Otras cirugías, como la reconstrucción de pérdidas de sustancia con colgajos o injertos, el reimplante y el trasplante de tejidos compuestos, exigen un adecuado tratamiento y una apropiada monitorización para asegurar el éxito.
Paciente quemado críticoLas quemaduras extensas no solo destruyen el tejido, sino que también activan la respuesta inflamatoria mediada por citoquinas. Sus primeras consecuencias son las pérdidas de fluidos, que ocasionan hipovolemia e incluso shock. Pero además se puede asociar un componente cardiogénico por bajo gasto cardiaco y después un componente distributivo por respuesta inflamatoria3. También pueden asociar alteraciones pulmonares y de la vía aérea superior. Por todo ello, los pacientes con quemaduras graves requerirán ingreso en una unidad de quemados críticos, ya que necesitan una fluidoterapia estrechamente monitorizada y en muchas ocasiones fármacos vasoactivos, ventilación mecánica, analgosedación, técnicas de reemplazo renal, etc.4.
Atención inicialPara la reposición de fluidos se han propuesto varias fórmulas, y la más usada es la del Hospital de Parckland5. Esta fórmula estima las necesidades en 4ml de cristaloides ×kg×% de superficie corporal quemada en 24h, de las cuales la mitad se infunden en las primeras 8h y el resto en las 16 siguientes. Clásicamente se ha utilizado Ringer lactato para evitar la acidosis hiperclorémica que produce el suero salino cuando se utiliza en cantidades abundantes; sin embargo, últimamente se están introduciendo otros cristaloides balanceados6. Mayor discusión existe en el uso de coloides, aunque lo más aceptado es utilizar albúmina a partir de las primeras 8-12h en los pacientes con quemaduras mayores del 30%7. Pero las fórmulas solamente sirven como orientación inicial, ya que no tienen en cuenta la profundidad, las comorbilidades, la presencia o no de síndrome de inhalación, etc.8.
Si no hay grandes alteraciones en la presión arterial y en la frecuencia cardiaca y la diuresis horaria se mantiene en 0,5-1ml/kg podemos asumir que no hay gran déficit de volemia9. Sin embargo, en casos graves necesitamos una monitorización más compleja, ya que estos parámetros pueden estar influidos por muchos otros factores y su correlación con el gasto cardiaco y la precarga no es suficientemente buena.
Hace unos años se vio que en muchas ocasiones se aportaba mucho más volumen del calculado por las fórmulas, lo que provocaba un aumento de salida de líquidos al espacio intersticial. A este fenómeno se le denominó fluid creep, y se debe sobre todo al mayor uso de opiáceos, y también al mayor uso de la ventilación mecánica o a la búsqueda de objetivos de reanimación inadecuados10.
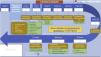
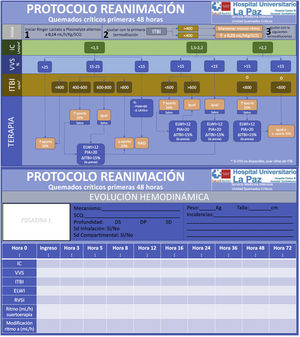
Actualmente la monitorización más utilizada es la termodilución transpulmonar, que calcula gasto cardiaco, volúmenes de precarga y agua extravascular pulmonar (EVLW), y que además puede ofrecer cálculos continuos de gasto cardiaco y de la variación del volumen sistólico. La reanimación puede ser guiada por estos dos últimos. La variación del volumen sistólico es un buen predictor de respuesta a fluidos, pero en los pacientes en ventilación espontánea o con arritmias no es tan útil y debemos usar los parámetros estáticos de precarga (volumen sanguíneo intratorácico o volumen global telediastólico). Sin embargo, no en todo paciente respondedor a fluidos está indicado aportar fluidos hasta normalizar los parámetros, ya que la alteración de la permeabilidad puede hacer que no se retengan en el espacio intravascular y el objetivo de normalizar únicamente provoque un aumento del edema. Por eso, otros parámetros, como el EVLW o la presión intraabdominal y la tendencia de parámetros de precarga pueden alertar contra el exceso de aporte. Con estos datos y otros, como presión arterial media y niveles de lactato, realizamos un árbol de actuación buscando corregir las alteraciones hemodinámicas y asegurar la perfusión tisular11,12 (fig. 1).
Protocolo de fluidoterapia en el paciente con quemaduras superiores al 20% de superficie corporal quemada.
Dp: quemadura dérmica profunda; Ds: quemadura dérmica superficial; ELWI: Extravascular Lung Water Index; IC: índice cardiaco; ITBI: Intratoracic Blood Index; PAM: presión arterial media; PIA: presión intraabdominal; RVSI: resistencias vasculares sistémicas indexadas; SCQ: superficie corporal quemada; SD: quemadura subdérmica; VVS: variación de volumen sistólico.
Otro aspecto es la repercusión respiratoria debida a la alteración de la permeabilidad vascular pulmonar, que, asociada a hipoproteinemia y disminución de la presión oncótica, puede aumentar el EVLW. Por ello, en un alto porcentaje de pacientes es necesaria la ventilación mecánica, y aunque no existen suficientes evidencias se recomiendan las mismas medidas de ventilación protectora que en otras patologías13. Además, la disminución de la compliance torácica en quemaduras torácicas y la hipertensión intraabdominal alteran aún más la función respiratoria.
En caso de coexistir inhalación de humos puede haber alteraciones de las vías respiratorias y del parénquima pulmonar ya desde el inicio. El síndrome de inhalación de humos puede sospecharse cuando el accidente ha tenido lugar en un ambiente cerrado, hay quemaduras faciales, vibrisas quemadas, esputo carbonáceo, estridor y carboxihemoglobina elevada. Se ha recomendado la intubación precoz por la posibilidad de obstrucción de la vía aérea por edema, pero la ventilación con presión positiva puede incrementar las necesidades de fluidos y empeorar el pronóstico. Por ello, solo debería realizarse si es necesario; en el resto de los casos es mejor vigilar y, en caso de haber sido intubado, valorar la posibilidad de extubación precoz14,15. No se recomienda el uso de corticoides ni de antibióticos profilácticos de forma rutinaria, y los anticoagulantes nebulizados no han demostrado suficiente efectividad16,17. Además, debe utilizarse cianocobalamina a dosis elevadas ante la sospecha de intoxicación por cianuros, y oxígeno al 100% ante la sospecha de monóxido de carbono.
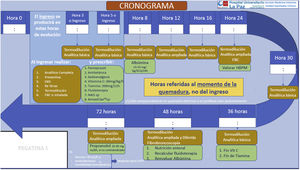
Otras actuaciones necesarias son el tratamiento del dolor y prevenir y corregir la hipotermia. También se ha propuesto la administración de dosis elevadas de vitaminaC para disminuir la respuesta inflamatoria18 (fig. 2).
Las quemaduras eléctricas son un caso especial, ya que pueden acompañarse de arritmias y rabdomiólisis. En estos pacientes deben aportarse más fluidos para conseguir una diuresis mayor y también pueden añadirse bicarbonato sódico, manitol o furosemida19.
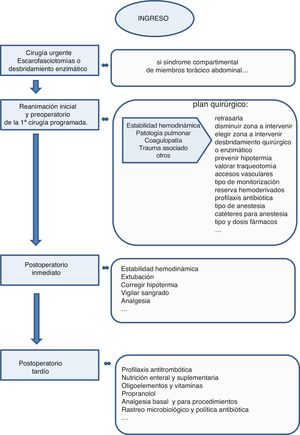
Ya desde el primer momento la coordinación con cirugía plástica se hace necesaria para evitar la aparición de síndromes compartimentales mediante un tratamiento conservador como medidas posturales, vigilar y limitar el aporte de fluidos. En el caso de que se instaure el síndrome es necesario proceder al tratamiento quirúrgico urgente de escaro-fasciotomías o desbridamiento enzimático en la localización afectada (fig. 3).
Periodo preoperatorio y cirugíaTras las alteraciones iniciales, la principal causa de morbimortalidad en estos pacientes es la sepsis, por lo que la escisión y la cobertura precoz de la quemadura disminuyen las posibilidades de colonización y sepsis y, por tanto, mejoran el pronóstico20. Pero esta cirugía debe hacerse en condiciones clínicas adecuadas, lo que no ocurre en muchas ocasiones, ya que el paciente puede no haber recuperado la estabilidad hemodinámica y tener alteraciones respiratorias21. En estos casos es necesaria una estrecha comunicación entre el equipo quirúrgico y los intensivistas para adecuar el momento, el tipo y la magnitud de la cirugía a la situación del paciente.
En los últimos años, además de las técnicas quirúrgicas habituales se ha introducido el uso de desbridamiento enzimático con una crema de bromelaína, que es capaz eliminar la escara de forma más selectiva y que puede aplicarse en la unidad de cuidados intensivos sin necesidad de trasladar al paciente a quirófano. Esta técnica parece tener ventajas, pero puede desencadenar una respuesta inflamatoria sobreañadida22,23.
En el plan quirúrgico se estimarán las pérdidas sanguíneas para adecuar la reserva de hemoderivados. Las necesidades de transfusión han disminuido con la utilización de trombina tópica, el uso de torniquetes y los vasoconstrictores tópicos24,25, y también con la reducción del objetivo mínimo de hemoglobina hasta los 7g/dl26. La utilización del desbridamiento enzimático en vez de la escisión quirúrgica clásica parece haber disminuido las necesidades de transfusión27. En determinados pacientes se ha utilizado la transfusión sanguínea autóloga hemodilucional28.
También deben programarse los accesos vasculares, la monitorización necesaria y las medidas para evitar la hipotermia, y se valorará la necesidad o no de traqueotomía (por las lesiones cervicofaciales, o porque se prevea intubación prolongada).
La analgosedación es fundamental desde el principio29. Debemos tener en cuenta que la pérdida intravascular de proteínas da lugar a hipoalbuminemia, lo que modifica el volumen de distribución de muchos medicamentos. Por otro lado, la disminución del gasto cardiaco, del flujo renal y del hepático puede disminuir la eliminación de determinados fármacos. Así, por ejemplo, pueden requerirse mayores dosis de opiáceos y de propofol. En las cirugías posteriores, o si la primera cirugía se demora más de 48h, debe evitarse la succinilcolina, ya que existe un aumento de receptores de acetilcolina que liberan potasio al despolarizarse y pueden provocar una hiperpotasemia rápida30. La anestesia regional puede facilitar el procedimiento quirúrgico, disminuir el dolor postoperatorio y facilitar la rehabilitación, aunque no puede utilizarse de forma única cuando las quemaduras o las zonas dadoras para los injertos están en zonas diferentes. La anestesia epidural o espinal no debe ser usada en desbridamientos extensos por el riesgo de sangrado e hipovolemia.
En el paciente quemado no debe utilizarse la antibioterapia de forma sistemática, aunque sí debe utilizarse en el perioperatorio. En estos pacientes debemos ajustar las dosis por las alteraciones en el volumen de distribución31,32.
Postoperatorio inmediatoEn este periodo las complicaciones más frecuentes son el sangrado, la hipotermia y las alteraciones hemodinámicas derivadas de la nueva agresión. Estas últimas son especialmente importantes, ya que de la adecuada perfusión periférica depende el éxito de la cobertura con injertos autólogos y que aumente o no la profundidad de la quemadura y de las zonas dadoras de los injertos. Otra decisión importante es el momento para la retirada de la ventilación mecánica4.
También debemos ajustar la analgesia teniendo en cuenta las necesidades basales y las necesidades extra ante cambios posturales, curas u otros procedimientos. Para esto son necesarios protocolos que añadan a los opiáceos otros fármacos como ketamina, dexmedetomidina o clonidina, así como el uso de catéteres para analgesia locorregional3.
Postoperatorio tardío o entre cirugíasEn este periodo nos encontramos ante un paciente crítico en el que es muy importante la continuidad asistencial para facilitar la recuperación, evitar complicaciones y preparar al paciente para la siguiente cirugía. En este sentido, deben reiniciarse la profilaxis antitrombótica y la nutrición lo más precozmente posible. La nutrición enteral debe suplementarse con vitaminas y oligoelementos y en ocasiones con nutrición parenteral por los frecuentes ayunos periquirúgicos o peri-procedimientos con sedación. Además de intentar reducir lo más posible los periodos de ayuno peri-procedimientos, también se debe intentar controlar la respuesta hipercatabólica con propranolol33.
En este periodo se va desarrollando una gran tolerancia a los opiáceos y además puede aparecer dolor neuropático, prurito e incluso hiperalgesia. El acetaminofeno, los antiinflamatorios no esteroideos, la clonidina, la gabapentina y los antidepresivos tricíclicos pueden disminuir el dolor nociceptivo y neuropático34,35.
Las curas y los baños terapéuticos ocasionan dolor y producen hipotermia, además de ser una nueva agresión y provocar la liberación de citoquinas. Por ello, estos procedimientos requieren analgosedación, en la que la ketamina tiene una especial importancia ya que a su excelente efecto analgésico se añade que preserva la estabilidad hemodinámica y que no deprime la función respiratoria espontánea, por lo que puede evitar la intubación orotraqueal, aunque necesita premedicación con benzodiacepinas o propofol a dosis bajas para evitar la disforia que puede asociar. Otras alternativas son la dexmedetomidina, que también proporciona sedación y analgesia con poca depresión respiratoria y la anestesia inhalatoria. Finalmente existen tratamientos coadyuvantes no farmacológicos que disminuyen la ansiedad y el dolor, entre los que destaca la musicoterapia36.
No se recomienda la antibioterapia profiláctica, pero los pacientes quemados están más predispuestos a la infección por la ausencia de barrera cutánea, por los accesos vasculares, por la mayor probabilidad de translocación bacteriana y por la inmunodepresión que asocian. Por ello se debe realizar un frecuente rastreo microbiológico para conocer la flora colonizadora y, en caso de infección, poder ajustar la antibioterapia37.
Es muy frecuente que los pacientes necesiten múltiples reintervenciones, bien porque la gran extensión no recomiende la realización de toda la escisión y cobertura en un solo momento, bien porque el porcentaje de zona injertada con éxito sea insuficiente.
Perioperatorio en cirugía reconstructivaLos colgajos libres son una de las técnicas de reconstrucción de las pérdidas de sustancia frecuentemente utilizadas en cirugía plástica. Los colgajos se diferencian de los injertos en que son porciones de tejido vascularizado por un eje. Presentan una gran complejidad, lo que en ocasiones obliga a monitorización postoperatoria y a un manejo clínico cuidadoso, especialmente en las intervenciones de más de 6h. Los pacientes con complicaciones quirúrgicas o con determinados factores de riesgo deben ser monitorizados y tratados en unidades de cuidados intensivos, y el resto requerirán al menos áreas de cuidados intermedios con personal de enfermería especializado38. Los factores de riesgo a considerar son edad avanzada39, cardiopatía isquémica, dependencia alcohólica, diabetes mellitus40, tabaco41 y obesidad42.
Intraoperatorio y postoperatorioEl factor más importante es el mantenimiento de un flujo sanguíneo adecuado a través del pedículo vascular. La hipovolemia, la hipotermia y el dolor son las principales complicaciones a evitar43. Por tanto, hay que realizar un aporte de volumen adecuado: ni escaso, que comprometa el flujo, ni excesivo, ya que puede producir edema y trombosis del colgajo. Para asegurar la presión de perfusión en muchas ocasiones se necesitan fármacos vasoactivos44. También deben evitarse hematocritos por encima del 40%, por la elevada viscosidad, y solamente se recomienda la transfusión con hematocritos por debajo del 25%45.
Un caso especial es el de la microcirugía sobre cabeza y cuello, ya que en estos pacientes puede ser necesario prolongar la ventilación mecánica para asegurar que no existe obstrucción de la vía aérea superior, y también puede ser necesario prolongar el tiempo de sedación para evitar complicaciones debidas a malposiciones u otros motivos46.
La monitorización del colgajo requiere personal entrenado que de forma frecuente y durante unos 3días vigilen el relleno capilar, el color, el edema, la temperatura y el sangrado. El doppler, la saturación de oxígeno, la flujometría láser doppler y la angiografía de fluorescencia permiten una monitorización más objetiva, y en los colgajos enterrados son especialmente útiles el doppler implantable y la microdiálisis47.
Actualmente se recomienda utilizar los protocolos de profilaxis antibiótica en cirugía limpia-contaminada durante 7días, poniendo especial atención a pacientes con factores de riesgo, tiempo quirúrgico prolongado, uso de colgajo óseo y malnutrición48.
El tratamiento antitrombótico postoperatorio es muy controvertido, pero un metaanálisis reciente concluye que los antitrombóticos no reducen el riesgo de trombosis ni de pérdida de colgajo, pero sí aumentan el riesgo de hematoma49.
Las medidas posturales pueden evitar la sobrecarga venosa y el edema, especialmente en los miembros inferiores, por lo que se eleva el miembro en el que se realiza la microcirugía50.
Finalmente, las causas más frecuentes de pérdida del colgajo son la trombosis (venosa: arterial=2:1) y la obstrucción del pedículo51 (por causas locales o por infección).
Reimplantes y trasplanteEl reimplante de miembro superior ha tenido un gran desarrollo en las últimas dos décadas, sobre todo por la mejor selección del paciente, por la mejora de la técnica microquirúrgica, por la mejora del equipamiento y por la extensión de la indicación de los injertos venosos, alcanzando tasas de éxito entre el 80 y el 90%. Sin embargo, el objetivo de la cirugía no debe quedarse en la supervivencia del injerto, sino que debe ampliarse al resultado funcional del reimplante en cuanto a sensibilidad, rango articular, fuerza, intolerancia al frío y vuelta al ambiente laboral de los pacientes52.
En estos pacientes las cirugías son largas y pueden tener complicaciones semejantes a las ya mencionadas en los colgajos, por lo que necesitan una monitorización y un manejo postoperatorio superponible al de los colgajos libres53. La monitorización con pulsioximetria en esa extremidad es sencilla y aporta datos continuos, por lo que puede servir de aviso precoz ante diversos problemas que dificulten la perfusión de la extremidad. El doppler es una forma sencilla de monitorización que puede utilizarse de forma periódica y en situaciones en que la pulsioximetria muestre alteraciones. Además, son necesarias las monitorizaciones habituales para pacientes críticos con el objetivo de asegurar una adecuada situación hemodinámica. A pesar de todos los avances en monitorización, el factor más importante para el éxito o el fallo del reimplante sigue siendo la técnica microquirúrgica. Sin embargo, será la calidad de la piel, la reconstrucción tendinosa y ósea, así como la recuperación sensitiva, las que marcarán el resultado funcional y, por tanto, el éxito final o no del reimplante.
Los estudios de coste-beneficio que comparan el reimplante contra el cierre directo del muñón muestran que los centros con mayor número de pacientes, y con reimplantes de forma regular, consiguen mayores tasas de éxito, con mejor satisfacción del paciente y menor tasa de complicaciones54. Diversos estudios muestran que el reimplante es superior en términos funcionales al cierre del muñón y a la protetización del mismo cuando la lesión es en el antebrazo55,56.
En cuanto al tratamiento, consistirá en la profilaxis antibiótica y en el resto de las medidas habituales. A pesar de las mejoras en la técnica quirúrgica, continúa habiendo una gran controversia acerca del riesgo-beneficio de la antiagregación o anticoagulación. Actualmente no existe un criterio uniforme para el uso de antiagregación o anticoagulación52, aunque se recomienda evitar el uso de anticoagulantes para reimplantes por encima del codo por riesgo de sangrado57,58.
Además del reimplante de un miembro propio, existe la posibilidad de realizar trasplante de miembro superior de donante. Estos trasplantes deben realizarse en pacientes muy seleccionados y su cirugía suele requerir tiempos de quirófano muy prolongados, por lo que en el postoperatorio inmediato podemos encontrarnos con las complicaciones habituales de los reimplantes. La hipotermia y la respuesta inflamatoria sistémica son frecuentes y en ocasiones pueden incluso llegar ocasionar fracaso multiorgánico. De hecho, se han intentado cuádruples trasplantes de miembros que han fracasado por este motivo59. Dados los riesgos, en estos momentos el trasplante de miembros inferiores no está recomendado de forma general. La monitorización necesaria será la misma que en el caso de los reimplantes. Además, en el postoperatorio tardío y posteriormente debemos monitorizar los niveles de los inmunosupresores para evitar rechazos y efectos secundarios de estos fármacos. También debemos estar vigilantes por las posibles complicaciones infecciosas de los pacientes inmunosuprimidos.
ConclusionesEl paciente quemado es un paciente crítico que requiere múltiples cirugías y procedimientos, lo que hace imprescindible un manejo integral coordinado y dinámico, ajustado a la situación clínica en cada momento. Además, necesita una monitorización más o menos compleja pero constante. Del mismo modo, el perioperatorio de la cirugía reconstructiva requiere un manejo integral para evitar complicaciones sistémicas y asegurar el éxito del colgajo, del reimplante o del trasplante.
FinanciaciónNinguna.
Conflicto de interesesLos autores declaran que no existe conflicto de intereses.
A Eva Herrero de Lucas, Eva Flores Cabeza, Lucia Cachafeiro Fuciños y a todo el personal médico y de enfermería que trabaja en la Unidad de Quemados Críticos del Hospital Universitario La Paz.