INTRODUCCIÓN
La enfermedad pulmonar obstructiva crónica (EPOC) es la quinta causa de muerte en EE.UU.1. Aunque no disponemos de una información similar en otros países, es muy probable que estos hallazgos sean extrapolables a otras áreas, y que en cualquier caso estemos ante una patología responsable de un elevado número de fallecimientos. Dentro de este grupo, la bronquitis crónica representa, aproximadamente, el 85% del total y el enfisema el 15%.
La exacerbación de la patología de base es el motivo fundamental del ingreso en el hospital. Las causas de esta exacerbación son, principalmente, la infección respiratoria en un 48% de los casos y la insuficiencia cardíaca congestiva en el 26%2,3. Entre un 2-10% de los ingresos de las Unidades de Cuidados Intensivos (UCI) son enfermos con reagudización de la EPOC4,5. Varios estudios han descrito el pronóstico de los enfermos con EPOC que precisan ingreso en la UCI o que requieren ventilación mecánica5-19. Estos estudios presentan como limitación el que se realizaran en una única unidad con un tamaño muestral pequeño.
El objetivo de este estudio es analizar las variables que se asocian a la mortalidad de los enfermos que requieren ventilación mecánica debido a una reagudización de la EPOC ingresados en 361 UCI de 20 países.
PACIENTES Y MÉTODOS
Pacientes
Análisis retrospectivo de 522 pacientes con reagudización de una EPOC, que precisaron ventilación mecánica durante más de 12 horas. Esta cohorte de enfermos supone un 10% de los 5.183 enfermos incluidos en el estudio internacional de ventilación mecánica realizado entre el 1 y el 31 de marzo de 1998 en 361 UCI de 20 países20.
Protocolo
Para cada enfermo incluido en el estudio se registraron las siguientes variables:
1. Al ingreso en la UCI. Datos demográficos: género, edad, peso, situación funcional previa al ingreso en la UCI (normal, disnea de esfuerzo, disnea de reposo, oxigenoterapia domiciliaria, ventilación mecánica [invasiva o no invasiva] domiciliaria), fecha de ingreso en la UCI, nivel de gravedad en el momento de ingreso en la UCI estimado por el Simplified Acute Physiologic Score (SAPS II), fecha de inicio de la ventilación mecánica, gases arteriales previos a la intubación, utilización de ventilación no invasiva.
2. Complicaciones desarrolladas durante el tiempo de ventilación mecánica hasta un máximo de 28 días: barotrauma, síndrome de distrés respiratorio agudo (SDRA), neumonía asociada a ventilación mecánica, sepsis, fracaso cardiovascular, fracaso renal agudo, insuficiencia hepática y coagulopatía. La sepsis, la neumonía y el SDRA fueron considerados como complicación tan sólo si aparecían después de las 48 horas de haberse iniciado la ventilación mecánica. El diagnóstico de cada complicación se realizó de acuerdo a definiciones previamente publicadas21 y si los criterios diagnósticos se cumplían, al menos, en dos días consecutivos.
3. Al alta de la UCI: fecha de extubación, necesidad de reintubación y fecha de reintubación, fecha y situación al alta de la UCI y fecha y situación al alta del hospital.
Análisis estadístico
Los resultados se expresan en forma de media (desviación estándar [DE]), mediana con percentil 25 (P25) y 75 (P75) o de porcentaje. Las variables cuantitativas fueron comparadas con la prueba de la «t» de Student o con el test de la U de Mann-Whitney y las cualitativas con la prueba de la χ2 o el test de Fisher. Se consideró significativa una diferencia cuando el valor de p fue menor de 0,05.
Para estimar las variables relacionadas con la mortalidad se utilizó un análisis de particiones recursivas tipo C&RT (Classification and Regression Trees) con el programa estadístico Answer Tree 3.1. Este método identifica, mediante un análisis de regresión, el punto de corte o valor umbral para cada variable, que proporciona la mejor separación entre los enfermos que sobreviven y los que fallecen. Para las variables continuas, el valor umbral es cualquiera de los valores representados en los datos, mientras que en las variables dicotómicas, el punto de corte se establece entre la ausencia o la presencia de una categoría. Las particiones empiezan tras evaluar la capacidad de cada variable para separar a los fallecidos de los supervivientes; así, la variable que da lugar a la mejor división se convierte en la primera rama del árbol. Este procedimiento se repite para cada uno de los dos subgrupos que han resultado de la primera división, hasta que no sea posible obtener más particiones por no haber diferencias significativas entre fallecimientos y supervivientes o haya menos de 25 enfermos en uno de los grupos resultantes. Este método, además de dibujar un árbol de clasificación, nos permite obtener subgrupos de enfermos con diferentes combinaciones de variables asociadas que conllevan distinto riesgo de mortalidad. Una vez identificados los subgrupos de riesgo, se realiza un modelo de regresión logística para estimar la odds ratio para mortalidad de cada subgrupo. Los subgrupos obtenidos se introducen en el modelo como una variable dummy, que compara cada subgrupo con el que tiene una menor mortalidad.
Las variables introducidas en el análisis fueron: edad, SAPS II, género, situación funcional basal, oxígeno domiciliario, ventilación domiciliaria, presión parcial de oxígeno en sangre arterial (PaCO2) previa a la intubación, PaO2/fracción inspiratoria de oxígeno (FiO2) previa a la intubación, acidosis respiratoria previa a la intubación, ventilación no invasiva con éxito, barotrauma, SDRA, sepsis, neumonía asociada a la ventilación mecánica, fracaso cardiovascular, fracaso renal agudo, fracaso hepático, coagulopatía e hipoxemia definida como una peor relación PaO2/FiO2, durante la ventilación mecánica menor de 200 y duración del soporte ventilatorio. Los criterios para la introducción de las variables en el análisis fueron la significación estadística en el análisis univariante y la relevancia clínica, aunque en el análisis univariante no fuese significativa la diferencia.
RESULTADOS
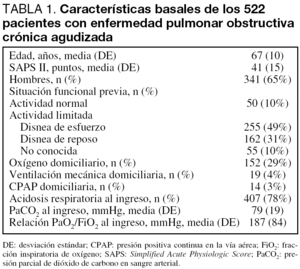
En la tabla 1 se muestran las características basales de los enfermos incluidos en el estudio.
En 85 enfermos (16%) se utilizó ventilación mecánica no invasiva al ingreso en la UCI. De ellos, 22 enfermos (26%) precisaron intubación. La mortalidad de este grupo fue de un 27% frente a un 9% de los enfermos que no precisaron intubación y a un 24% de los enfermos que fueron intubados al ingreso en la UCI (p = 0,03).
Trescientos veintiocho pacientes (63%) fueron extubados. La tasa de reintubación fue de un 22%. En 51 pacientes (10%) se realizó traqueostomía. La mediana hasta que se realizó la traqueostomía fue de 10 días (P25: 7, P75: 18). En la tabla 2 se muestran los días de ventilación mecánica, días de desconexión, días de estancia en la UCI y en el hospital en el total de la población y en los enfermos que fallecieron y sobrevivieron.
La mortalidad global en la UCI fue de un 22% y la mortalidad en el hospital de un 30%. Las variables asociadas a la mortalidad en la UCI en el análisis univariante fueron: el nivel de gravedad al ingreso en la UCI (SAPS II medio en los enfermos que fallecieron: 45 ± 16 frente a 39 ± 14 en el grupo superviviente, p < 0,001), la actividad limitada (riesgo relativo 1,9; intervalo de confianza para el 95%: 1,1 a 3,5), el desarrollo de complicaciones durante la ventilación mecánica (barotrauma [riesgo relativo 7,6; intervalo de confianza para el 95%: 2,5 a 22,6], SDRA [riesgo relativo 12,9; intervalo de confianza para el 95%: 2,7 a 63,4], neumonía asociada a ventilación mecánica [riesgo relativo 2,7; intervalo de confianza para el 95%: 1,6 a 4,4] y sepsis [riesgo relativo 6,8; intervalo de confianza para el 95%: 3,4 a 13,5]), la disfunción de órganos (fracaso cardiovascular [riesgo relativo 7,5; intervalo de confianza para el 95%: 4,2 a 13,3], fracaso renal agudo [riesgo relativo 8,7; intervalo de confianza para el 95%: 4,8 a 15,8], fracaso hepático [riesgo relativo 12,9; intervalo de confianza para el 95%: 2,7 a 63,4] y coagulopatía [riesgo relativo 10,5; intervalo de confianza para el 95%: 3,3 a 33,7]) y la duración del soporte ventilatorio: mediana en el grupo fallecido 7 días (P25: 4, P75: 12) frente a 5 días (P25: 3, P75: 8) en el grupo superviviente; p < 0,001. El éxito de la ventilación no invasiva se asoció con una reducción de la mortalidad (riesgo relativo 0,3; intervalo de confianza para el 95%: 0,1 a 0,8).
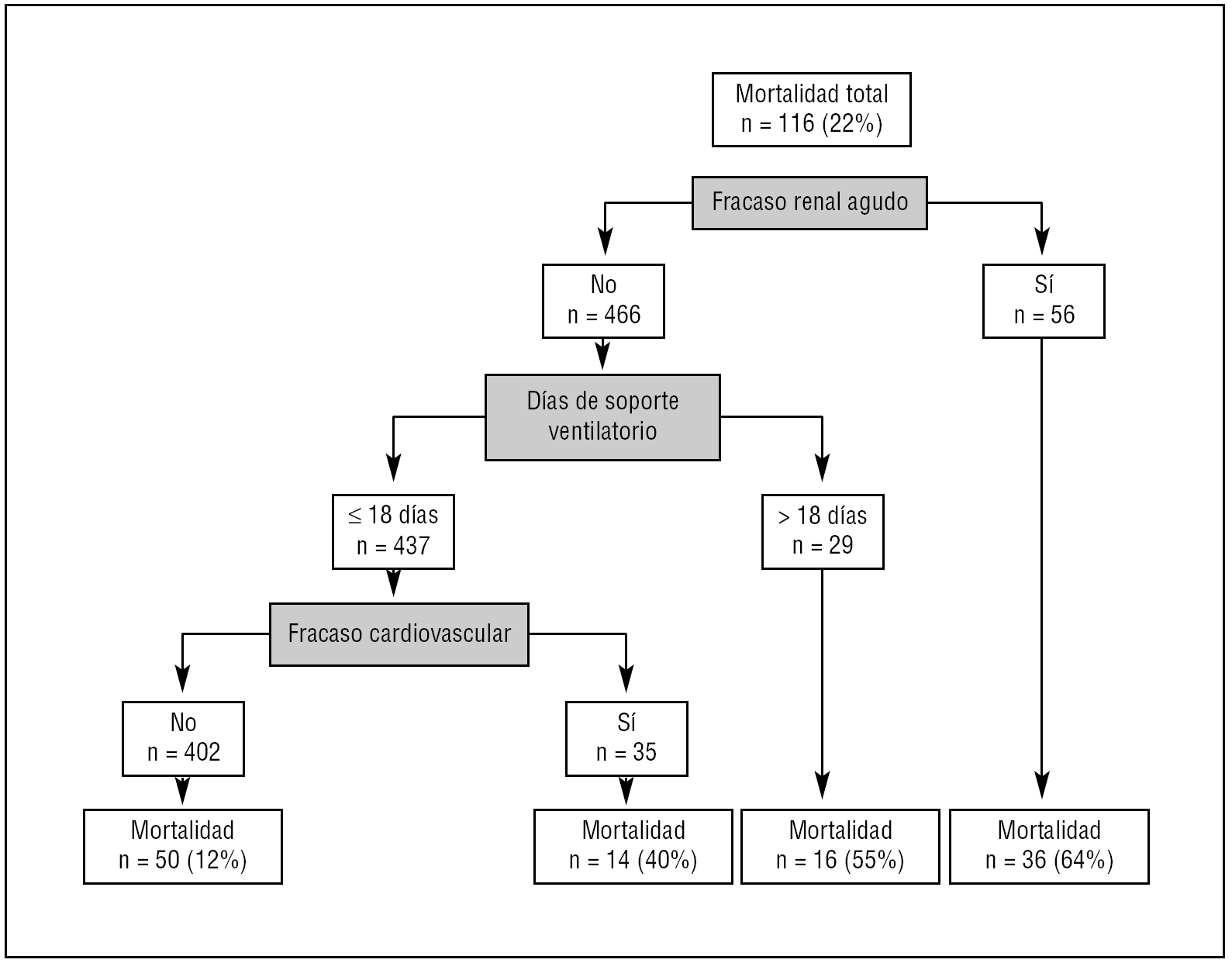
En la figura 1 se muestra el árbol de decisión resultante del análisis de particiones recursivas. El riesgo de mortalidad, estimada por el análisis de regresión logística, en cada subgrupo derivado del análisis de particiones recursivas se muestra en la tabla 3.
Figura 1. Árbol resultante del análisis de particiones recursivas.
DISCUSIÓN
En nuestro estudio la mortalidad en la UCI de los enfermos con una reagudización de la EPOC fue del 22% y la mortalidad hospitalaria del 30%. Las variables que se asociaron con la mortalidad en la UCI fueron: desarrollo de disfunción renal y cardiovascular y la duración del soporte ventilatorio.
La mortalidad de los enfermos con EPOC que requieren ventilación mecánica ha sido descrita en diferentes estudios y se estima entre un 6 y un 51%5-19. Estas diferencias son, probablemente, debidas a diferencias en la situación basal previa a la inclusión en los estudios, así como a diferencias en el tamaño de la muestra analizada. En nuestro estudio, que es el de mayor tamaño muestral, la mortalidad en la UCI está en un nivel intermedio respecto de lo previamente publicado.
Un aspecto que merece atención especial en el tratamiento de los enfermos con EPOC es la utilidad de la ventilación mecánica no invasiva. Los resultados obtenidos en ensayos clínicos muestran un beneficio de la aplicación precoz, antes de que el enfermo desarrolle una acidosis respiratoria grave, de la ventilación no invasiva en enfermos con EPOC22. La tasa de utilización de ventilación no invasiva en nuestro estudio fue inferior a la publicada en otros estudios23 debido a que en nuestro estudio sólo se incluyeron pacientes con una duración de la ventilación mecánica superior a 12 horas, lo cual podría haber contribuido a excluir enfermos a los que se les aplicó ventilación no invasiva durante un tiempo más corto. Un hallazgo de nuestro estudio fue que los enfermos que, inicialmente, fueron tratados con ventilación no invasiva y precisaron intubación tuvieron una mayor mortalidad que los enfermos que fueron intubados desde su ingreso en la UCI. Esta observación coincide con la publicada en un ensayo clínico que compara la ventilación no invasiva con la ventilación invasiva en enfermos con EPOC reagudizada24. Pero, a pesar de que el retraso en la intubación podría ser un factor asociado a la mortalidad, el hecho de que los enfermos que son tratados con ventilación no invasiva con éxito tengan una mortalidad muy inferior a los enfermos con ventilación invasiva hace recomendable esta técnica en enfermos con EPOC.
Diferentes estudios han evaluado las variables que se relacionan con la mortalidad de los enfermos con EPOC que requieren ventilación mecánica5-19. Los factores relacionados con el pronóstico descritos en estos estudios van desde factores relacionados con la situación basal del enfermo, como el grado de disnea6 o el volumen espiratorio máximo en un segundo (VEMS)7,13, hasta el desarrollo de disfunción de órganos durante la estancia en la UCI10,12,17,18. En nuestro estudio, aplicando una metodología que permite definir grupos de pacientes con diferentes probabilidades de muerte, hemos encontrado como factores independientemente relacionados con la mortalidad la disfunción renal y cardiovascular acorde a lo descrito en otros estudios y un soporte ventilatorio prolongado que sería uno de los hallazgos principales de nuestro estudio.
Previamente a nuestro estudio, varios autores9-11,15,17 habían analizado el valor pronóstico de la duración de la ventilación mecánica en enfermos con EPOC. Excepto Nevins y Epstein15, ningún otro autor había encontrado relación entre tiempo de ventilación mecánica y mortalidad. Pero a diferencia del estudio de Nevins y Epstein, donde un tiempo de ventilación mecánica superior a las 72 horas se asociaba a peor pronóstico, en nuestro estudio el punto de corte que mejor discriminaba fue de 18 días, lo que supone un tiempo de soporte ventilatorio muy prolongado (la mediana del tiempo total de soporte ventilatorio en nuestra cohorte fue de 5 días [rango intercuartil 3 a 9]). La interpretación de esta observación podría ser que en un porcentaje de enfermos con EPOC que no desarrollan fracaso de órganos y que, por diferentes razones, no pueden ser desconectados de la ventilación mecánica, este último factor es el que determina su mal pronóstico. La actuación sobre la disminución de los días de soporte ventilatorio, bien acortando el tiempo de ventilación mecánica con el tratamiento antibiótico y/o con esteroides sistémicos25,26, o el tiempo de weaning, con la implementación de protocolos de weaning21 podría mejorar el pronóstico de este subgrupo de enfermos.
Varias son las posibles limitaciones del estudio. La primera es que, exceptuando la disnea, no se registró la situación funcional basal del enfermo estimada por las pruebas de función respiratoria, algunas de las cuales, como el VEMS o la hiperinflación pulmonar estática medida por la relación entre la capacidad inspiratoria y la capacidad pulmonar total (IC/TLC) tienen una relación significativa con la mortalidad13,27. Lo mismo ocurre con otras variables relacionadas con el pronóstico de los enfermos con EPOC, como las alteraciones en los parámetros nutricionales3,5,11,13, la presencia o ausencia de cor pulmonale3,5,11,18 o índice de masa corporal3. Por último, el hecho de que se trate de un estudio observacional no intervencionista, donde sólo se incluyeron los enfermos ingresados en las UCI participantes que requieren ventilación mecánica durante más de 12 horas, podría producir un sesgo de selección de los enfermos, y aquellos que tienen una peor situación basal no se consideraron candidatos a ingresar en la UCI.
En conclusión, en nuestra cohorte de enfermos con EPOC reagudizada observamos una mortalidad en la UCI de un 22% y en el hospital de un 30%, tasas inferiores a las descritas en enfermos ventilados por otras causas. Las variables asociadas a la mortalidad fueron el desarrollo de disfunción renal y disfunción cardiovascular durante el tiempo de ventilación mecánica y la duración del soporte ventilatorio.
Declaración de conflicto de intereses
Los autores han declarado no tener ningún conflicto de intereses
*Financiado por la beca 98/0233, la Red GIRA (G03/063) y la Red RESPIRA (C03/11) del Fondo de Investigaciones Sanitarias.
APÉNDICE
Los investigadores del Internacional Study of Mechanical Ventilation fueron:
ARGENTINA: Coordinadores:C. Apezteguia, F. Palizas. R. Alasino (Hospital Municipal de Urgencias, Córdoba); R. Bastianelli (Hospital Militar, Villa Revol); J. Berón (Hospital Pablo Soria, San Salvador); C. Bevilacqua (Clínica Modelo de Morón, Morón); M. Cafaro (Hospital Regional Río Gallegos, Río Gallegos); E. Capparelli (Hospital Eva Perón, San Martín); G. Cardonatti (Hospital San Isidro, San Isidro); R. Correa (Hospital Central, Mendoza); A. Díez (Hospital Provincial del Centenario, Rosario); E. Estensoro (Hospital Escuela José de San Martín, La Plata); J. Fara (Policlínico Ferroviario, Rosario); R. Fernández (Hospital Italiano, Guaymallén); G. Fernández Cid (Hospital E. Tomú, Buenos Aires); H. Ferraro (Corporación Médica de San Martín, San Martín); A. Galaverna (Hospital Zonal Bariloche, Bariloche); C. Galleti (Sanatorio Allende, Córdoba); G. García (Hospital Clemente Álvarez, Rosario); G. Gelardi (Hospital Pri- vado del Sur, Bahía Blanca); S. Giannasi (Hospital Italiano, Buenos Aires); R. Guidi (Hospital Italiano Garibaldi, Rosario); L. Huespe Gardel (Hospital Escuela José F. de San Martín, Corrientes); C. Irrazábal (Hospital de Clínicas José de San Martín, Buenos Aires); O. López (Sanatorio Santa Isabel, Buenos Aires); G. Menga (Hospital María Ferrer, Buenos Aires); O. Otero (Centro Oncológico de Excelencia, Gonnet); F. Pálizas (Clínica Bazterrica, Buenos Aires); P. Pardo (Sanatorio de la Trinidad, Buenos Aires); C. Plaza (Sanatorio Julio Méndez, Buenos Aires); G. Raimondi (FLENI, Buenos Aires); A. Raimondi (Sanatorio Mater Dei, Buenos Aires); E. Romero (Hospital Privado Centro Médico, Córdoba); L. de Rosa (Sanatorio Quintar, San Salvador); C. Sáez (Sanatorio Británico, Rosario); A. Sarsino (Hospital Juan A. Fernández, Buenos Aires); P. Schoon (Hospital Profesor Luis Güemes, Haedo); C. Sola (Hospital José Penna, Bahía Blanca); C. Stöltzing (Hospital Guillermo Rawson, San Juan); J. Taccone (Instituto Alfredo Lanari, Buenos Aires); C. Tolosa (Hospital Córdoba, Córdoba); M. Torreno (Sanatorio Modelo Quilmes, Quilmes); E. Turchetto (Hospital Privado de la Comunidad, Mar de Plata); R. Valenti (CEMIC, Buenos Aires); R. Vargas (Policlínico Neuquen, Neuquen); L. Vasta (Sanatorio San Patricio, Buenos Aires); L. Vázquez (Hospital Español, Godoy Cruz); Vetere (Hospital Israelita Ezrah, Buenos Aires); F. Villarejo (Hospital Profesor Alejandro Posadas, Haedo); N. Wainsztein (Hospital Privado Fundación Favaloro, Buenos Aires); O. Yunk (Hospital Español, Buenos Aires); G. Zabert (Clínica Pasteur, Neuquen).
BOLIVIA: Coordinador:F. Sandi Lora. L. Moya (Hospital Juan XXIII, La Paz); E. Salazar (Hospital Japonés, Santa Cruz); J.C. Zapata (Hospital Obrero, La Paz).
BRASIL: Coordinador:C.M. David. S.M. Ajeje Lobo (Hospital de Base de São José do Rio Preto, São José do Rio Preto); A.B. de Almeida (Hospital das Clínicas da Univers. Federal, Uberlândia); M.A. Braga (Hospital Biocor, Belo Horizonte); I. Buselato Chen (Hospital Nossa Senhora das Graças, Curitiba); M. Chaves Craveiro de Melo (Hospital São Lucas, Belo Horizonte); R.N. Darwich (Hospital Prontocor, Belo Horizonte); C.M. David (Hospital Clementino Fraga Filho, Rio de Janeiro); R. Goldstein Alheira Rocha. (Hospital Samaritano, São Paulo); R. de Macedo Bosco (Hospital Madre Teresa, Belo Horizonte); J.M. Nogueira (Hospital Universitario São José. Belo Horizonte); E. Oliveira (Hospital Vera Cruz, Belo Horizonte); S.F. Pinto (Casa de Saúde São José, Campo Grande); S.F. Pinto (Santa Casa de Campo Grande, Campo Grande); S.F. Pinto (Univ. Fed. Mato Grosso do Sul, Campo Grande); J.L. da Rocha Paranhos (Santa Casa de Misericordia, São João del Rei); L.R. de Siqueira Musolino (Irmandade da Santa Casa de Misericordia, São Paulo).
CANADÁ: Coordinador:T.E. Stewart. R. Fowler (Wellesley-Central Hospital, Toronto). J. Granton (Toronto Hospital General Division, Toronto); J. Granton (Toronto Hospital Western Division, Toronto); R. Hodder (Ottawa Civic Hospital, Ottawa); B. Kashin (Peel Memorial Hospital, Brampton-Ontario); S. Lapinsky (Mount Sinai Hospital, Toronto); D. Mazer (St Michael's Hospital, Toronto); R. McLean (Sunnybrook Health Sciences Centre, Toronto); T. Rogovein (St Joeseph's Health Centre, Toronto).
CHILE: Coordinador:L. Soto. G. Bugedo (Hospital Pontificia Universidad Católica, Santiago); P. Hernández (Instituto Nacional del Tórax, Santiago); C. Ortega (Hospital Regional Concepción, Concepción); L. Soto (Hospital de Coquimbo, Coquimbo); L. Schölz (Hospital de Osorno, Osorno).
COLOMBIA: Coordinador:M. González. H. Atehortua (Clínica Sta. María. Centro Cardiovascular, Medellín); C. Cadavid (Hospital Pablo Tobón Uribe, Medellín); D. Camargo (Hospital Universitario, Barranquilla); C. Dueñas (Hospital Universitario, Cartagena); A. Guerra (Hospital General, Medellín); M. Granados (Fundación Valle de Lilly, Cali); R. Panesso (Clínica Las Américas, Medellín); M.A. Perafán (Clínica Shaio, Bogotá).
ECUADOR: Coordinador:J. Raad. B. Guevara (Hospital Carlos Andrade, Quito); J. Molina (Hospital Militar, Quito); J. Raad (Hospital Militar, Quito).
ESPAÑA: Coordinadores:A. Esteban, F. Frutos-Vivar. J.M. Allegre (Hospital Nuestra Señora del Rosell, Cartagena), S. Alonso (Hospital Joan XXIII, Tarragona), A. Álvarez Ruiz (Hospital General Río Carrión, Palencia), B. Álvarez Sánchez (Hospital General, Alicante), M.T. Antuna (Hospital de Cabueñes, Gijón), J.M. Añón (Hospital Virgen de la Luz, Cuenca), P. Arribas (Hospital 12 de Octubre, Madrid), A. Ayensa (Hospital Virgen de la Salud, Toledo), A. Azcárate (Hospital Nuestra Señora de Aranzazu, Donostia), J. Blanco (Hospital del Río Hortega, Valladolid), G.M. Besso (Hospital Carlos Haya, Málaga), L. Cabré (Hospital de Barcelona, Barcelona), F. Carrizosa (Hospital General, Jérez de la Frontera), J. Castañeda (Hospital Clínico, Valladolid), R. de Celis (Hospital de Galdakao, Galdakao), J.A. Conesa (Hospital Clínico Universitario San Carlos, Madrid), J. Diarte (Complejo Hospitalario, Ciudad Real), A. Díaz Lamas (Complejo Hospitalario Cristal Piñor, Orense), R. Fernández (Consorci Hospitalari del Parc Taulí, Sabadell), M. Ferrer (Hospital Clinic i Provincial, Barcelona), D. Fontaneda (Hospital Virgen Blanca, León), P. Galdós (Hospital General, Móstoles), A. García Jiménez (Hospital Arquitecto Marcide, El Ferrol), J. García Pardo (Hospital Juan Canalejo, La Coruña), J. Gener (Hospital Germans Trias i Pujol, Badalona), J.A. Gómez Rubí (Hospital Virgen de la Arrixaca, Murcia), G. González Díaz (Hospital Morales Meseguer, Murcia), S. González Prado (Hospital Josep Trueta, Girona), C. Homs (Hospital General San Jorge, Huesca), J. Ibañez (Hospital Son Dureta, Palma de Mallorca), F. Jara (Hospital Mutua, Terrassa), M. León (Hospital Arnau de Vilanova, Lleida), A. Lloria (Complejo Hospitalario Rebullón, Pontevedra), J. López Díaz (Hospital La Paz, Madrid), M.R. Lorenzo (Complejo Hospitalario Materno-Infantil, Las Palmas de Gran Canaria), S. Macías (Hospital General, Segovia), J.A. Maldonado (Hospital de la Serranía, Ronda), J. Maynar (Hospital Santiago Apostol, Vitoria), A. Moreno (Complejo Hospitalario de San Millán-San Pedro, Logroño), A. Mota (Hospital General Universitario, Elche), T. Mut (Hospital General, Castellón), M. Nolla (Hospital General de Cataluña, Sant Cugat del Vallés), F. Ortega (Hospital Universitario de Valme, Sevilla), R. de Pablo (Hospital Príncipe de Asturias, Alcalá de Henares), E. Palazón (Hospital General Universitario, Murcia), V. Parra (Hospital de Sagunto, Sagunto), A. Peral (Hospital Gregorio Marañón, Madrid), J.C. Portela (Complejo Hospitalario Xeral-Calde, Lugo), A. Ramírez (Hospital Nuestra Señora de Sonsoles, Ávila), J.A. Ramos (Hospital de Poniente, El Ejido), P. Revuelta (Hospital Universitario de Canarias, La Laguna), M. Rey (Complejo Hospitalario, Santiago de Compostela), J.J. Rodrigo (Hospital Nuestra Señora del Pino, Las Palmas de Gran Canaria), J.C. Rodríguez Borregan (Hospital Marqués de Valdecilla, Santander), J.A. Rodríguez Sarria (Hospital General, Elda), A. Rubio (Hospital Ramón y Cajal, Madrid), S. Ruiz Navarro (Hospital General Ciudad de Jaén, Jaén), V. Sagredo (Hospital Vir-gen de la Vega, Salamanca), P. Saura (Centre Hospitalari, Manresa), M.J. Serralta (Hospital Universitario de San Juan, Alicante), J.F. Solsona (Hospital del Mar, Barcelona), F. Suárez Sipmann (Fundación Jiménez Díaz, Madrid), F. Taboada (Hospital General de Asturias, Oviedo), S. Temprano (Hospital Severo Ochoa, Leganés), J.P. Tirapu (Hospital de Navarra, Pamplona), M.V. de la Torre (Hospital Universitario Virgen de la Victoria, Málaga), P. Ugarte (Hospital Marqués de Valdecilla, Santander), M. Valledor (Hospital de San Agustín, Avilés), I. Vallverdú (Hospital de la Santa Creu i Sant Pau, Barcelona), C. Vaquerizo (Hospital 12 de Octubre, Madrid), A. Viñuales (Hospital Lluis Alcanyis, Xátiva).
ESTADOS UNIDOS: Coordinador:A. Anzueto. S.M. Aguayo (Atlanta VA Medical Center, Decatur); R. Alagar (Allegheny General Hospital, Pittsburgh); R.K. Albert (Denver Health Medical Center, Denver); T.K. Aldrich (Montefiore Hospital & Medical Center, Bronx); K. Amoosa (Medical College of Wisconsin, Milwaukee); N. Anandarao (New York Methodist Hospital, Brooklyn); D.C. Angus (University of Pittsburg, Pittsburgh); A.C. Arroliga (Cleveland Clinic Foundation, Cleveland); M.F. Azrieli (Jacobu Medical Center, Bronx); R.A. Balk (Medical Center - 203 Jelke, Chicago); P.W. Bates (Maine Medical Center, Porthland); J.F. Beamis, Jr. (Lahey Hitchcock Medical Center, Burlington); P.E. Bellamis (Chs Dept of Medicine, Los Angeles); D.J. Bower (Atlanta VA Medical Center, Decatur); J.P. Bradley (William Beaumont Medical Center, El Paso); R.P. Byrd, Jr. (University of East Tennese, Jonesboro); V.J. Cardenas, Jr. (University of Texas Medical Branch, Galveston); L.J. Caruso (University of Florida, Gainesville); B.R. Celli (St. Elizabeths Medical Center, Boston); G. Clermon (University of Pittsburg, Pittsburgh); S.J. Coole (Carl T. Hayden VA Medical Center, Phoenix); T.A. Dillard (Commander MCHJ-MPU, Tacoma); L.E. Efferen (SUNY Health Science Center, Brooklyn); E.W. Ely, Jr. (Vanderbilt Lung Transplant Program Newline, Nashville); P. Factor (Michael Reese Hospital & Medical Center, Chicago); T.M. Fitzpatrick (Walter Reed Army Medical Ctr, Washington); R. Fowler (Wellesley-Central, Toronto); G.N. Giacooppe, Jr. (MCHJ-MPU, Tacoma); K.K. Guntupalli (Texas Med Ctr - Ben Taub Gen Hospital, Houston); J.B. Hall (University of Chicago, Chicago); M.E. Hanley (Denver Medical Center, Denver); M.T. Haupt (Oregon Health Science University, Portland); G.B. Hayes (St. Elizabeths Medical Center, Boston); D.E. Heiselman (Akron General Medical Center, Akron); F.C. Hiller (University of Arkansas Med Science, Little Rock); J.D. Hinze (The Univesity of Texas Health Science Center at San Antonio, San Antonio); R.D. Hite (Bowman Gray School of Medicine, Winston-Salem); R.C. Hyzy (Henry Ford Hospital, Detroit); A. Jubran (Edward Hines VA Hospital, Hines); C.A. Kaplan (University of Missouri Columbia, Columbia); M.S. Karetzky (Newark Beth Israel Med Ctr, Newark); S.A. Kurenhy (Truman Medical Center, Kansas); K.V. Leeper, Jr. (Emory University School of Medicine, Atlanta); H. Levy (University of New Mexico, Alburquerque); T. Lo (Loma Linda University, Loma Linda); M.J. Mador (Buffalo VA Medical Center, Búfalo); G.P. Marelich (University of California Davis Med Ctr, Sacramento); M.A. Matthay (University of California, San Francisco); N.R. McIntyre (Duke University Medical Center, Durham); S.A. Metter (Maine Medical Center, Port- land); M.S. Niederman (Winthrop Univesity Hospital, Mineola); J.R. Norman (Univesity of Mississippi Medical Center, Jackson); D.R. Oullette (Brooke Army Medical Center, Fort Sam Houston); P. Parsons (Denver Medical Center, Denver); R.G. Patel (VA Medical Center, Jackson); R.C. Perkins,II (University of Texas Health Center at Tyler, Tyler); M.E. Petrini (University of Miississippi Medical Center, Jackson); M.R. Pinsky (University of Pittsburg, Pittsburgh); A. Pohlman (Edward Hines VA Hospital, Hines); K.W. Presberg (Medical College of Wisconsin, Milwaukee); M.P. Rocha (Carl T. Hayden VA Medical Center, Phoenix); W. Rodríguez Cintron (San Juan VA Medical Center, San Juan); M.J. Rosen (Beth Israel Medical Center, New York); T.M. Roy (James Quillen College of Medicine, Mountain Home); G. Rudelfeld (Harborview Medical Center, Seattle); M.J. Rumbak (University Florida, Tampa); S.J. Ruoss (Stanford University Medical Center, Stanford); G.A. Schmidt (University of Chicago, Chicago); R.F. Schneider (Beth Israel Medical Center, New York); C.N. Sessler (Medical College of Virginia, Richmond); C.S. Shim (Jacobi Medical Center, Bronx); L. Smith (Rush-Presbyterian-St Lukes Medical Center, Chicago); C. Strange (MUSC 96 Jonathan Lucas St, Char-leston); J.I. Sznajder (Michel Reese Hospital & Medical Center, Chicago); S. Tessler (Maimonides Me- dical Center, Brooklyn); V. Whyte (Loma Linda University, Loma Linda); L. Wilkelmeyer (Loma Linda University Medical Center MC 1521, Loma Lin- da); R.G. Wundering (501 Crews Wing, Memphis); M.H. Zaman (The Brookdale Hosp Med Ctr, Brooklyn); L.H. Zimmerman (San Francisco VA Medical Center, San Francisco).
FRANCIA: Coordinador:L. Brochard. P. Andrivet (Centre Médico-Chirurgical de Bligny, Bris-sous-Forges); D. Annane (Hôpital Raymond Poincaré, Garches); C. Arich (CHU de Nimes, Nimes); F. Baud (Hôpital Lariboisière, Paris); F. Bellenfant (Hôpital Cochin, Paris); R. Boiteau (Hôpital Louise Michel, Evry); F. Brivet (Hôpital A. Béclère, Clamart); M. Canonne (C.H.G. Les Feugrais, Elbeuf); J.P. Cardinaud (Hôpital Pellegrin-Tripode, Bourdeaux); E. Clémenti (Centre Hosp. Dept, La Roche/Yon); P. Charbonneau (C.H.U. Côte de Nacre, Caen); J. Chastre (Hôpital Bichat, Paris); R. Chauveau (C.H. André Grégoire, Montreuil-Ss-Bois); C. Chopin (CHRU - Hôpital B, Lille); J.M. Descamps (Centre Hospitalier de Niort, Niort); D. Dreyfuss (Hôpital Louis Mourier, Colombes); J.P. Faller (C. Hosp. de Belfort, Belfort); F. Fraisse (Hôpital Delafontaine, Saint-Denis); C. Girault (Hôpital Charles Nicolle, Rouen); C. Guérin (Hôpital Croix Rousse, Lyon); E. Guerot (Hôpital Boucicaut, Paris); F. Hilpert (Hôpital Ballanger, Aulnay-sous-Bois); L. Holzapfel (Centre Hospitalier, Bourg-en-Bresse); F. Jardin (Hôpital Ambroise Paré, Boulogne Vignancourt); O. Jonquet (Hôpital Gui de Chauliac, Montpellier); E. L'Her (CHU de la Cavale Blanche, Brest); Y. Lefort (Hôpital Henri Mondor, Creteil); O. Leroy (Centre Hospitalier, Tourcoing); Y. Le Tulzo (CHU Pontchaillon, Rennes); Ch. Mayaud (Hôpital Tenon, Paris); H. Mentec (Hôpital Victor Dupouy, Argenteuil); A. Mercat Hôpital Bi-cétre, Kremlin-Bicetre); B. Misset (Hôpital Saint-Joseph, Paris); P. Moine (Hôpital Bicêtre, Bicetre); G. Nitemberg (IGR, Villejuif); L. Papazian (Hôpital Sainte Marguerite, Marseille); A. Rabbat (Hôpital Hô-tel-Dieu, Paris); T. Similowski (Hôpital Pitié Salpétrière, Paris); L. Soufir (Hôpital Saint-Louis, Paris); D. Tardy (Hôpital Saint-Camille, Bry-sur-Marne); F. Thaler (CM Chirurgical Foch, Suresnes); B. Vallet (Centre Hospitalier Univ., Lille); D. Villers (C.H.U. Nantes, Nantes); M. Wysocki (Institut Mutualiste Montsouris, Paris); J.F. Zazzo (Hôpital A. Béclère, Clamart).
GRECIA: Coordinador:D. Matamis. D. Georgopoulus (Heraklion University Hospital, Heraklion); M. Gianakou (Ahepa University Hospital, Thessaloniki); D. Lagonidis (Papanikolaou Hospital, The-ssaloniki); G. Nakos (Ioanina University Hospital, Ioanina); K. Stavrakaki (Evangelismos Hospital, Athens); G. Thomopoulus (Laikon Hospital, Athens).
IRLANDA: Coordinador:G. Fitzpatrick. M. Donnelly (Adelaide and Meath Hospital, Dublin); J. Moriarty (St. James Hospital, Dublin); B. O'Sullivan (Waterford Regional Hospital, Waterford); G. Shorten (Cork University Hospital, Cork).
ITALIA: Coordinador:P. Pelosi. Cositi (Pol. Umberto I, Roma); G. Iapichino (Hospital S. Paolo, Milano); P. Pelosi (Policlínico, Milano); A. Pesenti (Dsp. S. Gerardo, Monza).
MÉXICO: Coordinador:J. Elizalde. F. Aguilera Almazán (Hospital General Regional N.º 1, Chihuahua); M. Benítez Cortazar (Hospital Universitario de Puebla, Puebla); R. Carrillo Speare (Hospital PEMEX Sur, México DF); R. Castaño (Hospital de Cardiología del CMN, México DF); R. Corral (Hospital Excel. Tijuana, Baja California); D.M. D'Ector Lira (Hospital Metropolitano, México DF); G. Díaz Polanco (Hospital de Traumatología Magdalena de las Salinas, México DF); J.J. Elizalde (Hospital ABC, México DF); R. Envila Fisher (Hospital Morelos, Chihuahua); R. Envila Fisher (Hospital Clínica del Parque, Chihuahua); G. Franco G. (Hospital General de México, México DF); P. García Balbuena (Hospital General «Fernando Quiroz», México DF); O. Gayoso Cruz (Hospital Regional «Adolfo López Mateos», México DF); L. Green (Instituto Nacional de Cancerología, México DF); J.O. Herrera Hoyos (Centro Médico Las Américas, Mérida); J. Hinojosa (Hospital Angel Leaño, Guadalajara); J. Huerta (Clínica Londres, México DF); V.A. Juárez (Hospital Santelena, México DF); M. Loera (Hospital General Durango, Durango); C. López Alzate (Clínica del Mar, Mazatlán); E. López Mora (Instituto Nacional de Cardiología, México DF); S. Martínez Cano (Hospital Hidalgo Aguascalientes, Aguascalientes); R. Mendez Reyes (Hospital Regional 1º de Octubre, México DF); M. Mendoza (Hospital General de la Villa, México DF); O. Narváez Porras (Instituto Nacional de Enfermedades Respiratorias, México DF); E. Ortiz (Hospital General Irapuata, Guanajuato); A. Padua (Hospital General Torreón, Coahuila); M. Poblano (Hospital Juárez, México DF); V. Pureco Reyes (Hospital Regional «20 de Noviembre», México DF); W. Querevalum (Hospital Central Cruz Mexicana, México DF); A. Quesada (Hospital Ntra. Sra. de la Salud, San Luis Potosí); A. Ramírez Rivera (Hospital de Enfermedades Cardiovasculares y del Tórax. IMSS, Monterrey); A. Tamariz (Hospital Clínica del Centro, Chihuahua); A. Tamariz (Hospital Central Universitario, Chihuahua); A. Vargas (Hospital General de Pachuca, Pachuca); C. Vázquez (Hospital General Celaya, Guanajuato).
PERÚ: Coordinador:A.M. Montañez. M. Contardo (Edgardo Rebagliati Martins - UCI 7.º B, Lima); E. Durand (Guillermo Almenara Irigoyen-IPPS, Lima); M. Manrique (Hospital «José Casimiro Ulloa», Lima); J.C. Meza (Centro Médico Naval, Lima); J. Muñoz (Edgardo Rebagliati Martins - UCI 2.º C, Lima); J. Pacheco (Hospital del Apoyo «María Auxiliadora», Lima); C. Salcedo (Hosp. Nacional «Daniel Alcides Carrión», Lima); J. Silva (Hospital Central FAP, Lima); C. Torres (Hospital Nacional «Arzobispo Loayza», Lima).
PORTUGAL: Coordinador:J. Pimentel. P. Amaro (Centro Hospitalario de Gaia, Gaia); F. Faria (Instituto Portugués de Oncología, Porto); P. Freitas (Hospital Fernando da Fonseca, Amadora-Sintra); P. Martins (Hospital Universidade, Coimbra); E. Sabino (Hospital García de Orta, Almada); J. Salcher (Hospital de San José. UUM, Lisboa); E. Silva (Hos-pital Senhora do Desterro, Lisboa).
REINO UNIDO: Coordinador:P. Nightingale. O. Akinpelu (Chorley & District Hospital, Chorley); D. Bardgett (Macclesfield District General Hospital, Macclesfield); A. Batchelor (Royal Victoria Informary, Newcastle upon Tyne); R. Beale (Guy's Hospital, London); K. Burchett (Queen Elizabeth Hospital, King's Lynn); N. Coleman (North Staffordshire Royal Infirmary, Stoke on Trent); A. Conn (Wansbeck General Hospital, Ashington); D. Edbrooke (Royal Hallamshire Hospital, Sheffield); N. Fergusson (Countess of Chester Hospital, Chester); I. Grant (Rotherham District Hospital, Rotherham); K. Gunning (Addenbrooke's Hospital, Cambridge); J. Harper (Royal Liverpool University Hospital, Liverpool); D. Higgins (Southend Hospital, Westcliffe-on-Sea); D. Jayson (Southport & Formby General Hospital, Southport); R. Loveland (Wexham Park Hospital, Slough); L. Lynch (Birmingham Heartlands Hospital, Birmingham); I. Macartney (North Manchester General Hospital, Manchester); E. Major (Morriston Hospital, Swansea); S. Mousdale (Blackbum Royal Infimary, Blackburn); N. Soni (Chelsea and Westminster Hospital, London); D. Watson (Walsgrave Hospital, Walsgrave).
TÚNEZ: Coordinador:F. Abroug. A. Bchiz (Hospital F. Bached, Sousse); J. Ben Khelil (Hospital A. Mami, Ariana); S. Bern Lakhal (Hospital Rabta, Tunis); B. Bouhaja (Hospital Mongi Slim, La Marsa); H. Chelly (Hospital Fattouma Bourguiba, Sfax); S. El Atrous (Hospital Fattouma Bourguiba, Monastir); S. Ghedira (Hospital Charles Nicolle, Tunis); H. Thabet (CAMUR. Tunis).
URUGUAY: Coordinador:C. Rodrigo. H. Bagnulo (Maciel, Montevideo); C. Rodrigo (Asociación Española Primera, Montevideo); M. Rodríguez (Hospital de Paysandú, Montevideo).
VENEZUELA: Coordinador: G.D´Empaire. J. España (Hospital Universitario, Caracas); F. Pérez (Hospital de Clínicas, Caracas); R. Zerpa (Hospital Militar, Caracas).
Correspondencia: Dr. F. Frutos Vivar.
Unidad de Cuidados Intensivos.
Hospital Universitario de Getafe.
Ctra. de Toledo, km 12,500.
28905 Madrid. España.
Correo electrónico: ffrutos@ucigetafe.com
Manuscrito aceptado el 15-VII-2005.