INTRODUCCION
En el momento de ingreso hospitalario, métodos sencillos y accesibles, como la anamnesis, la exploración física o el análisis detallado del electrocardiograma (ECG) de 12 derivaciones se han relacionado con las complicaciones y pueden ser útiles para elegir la estrategia terapéutica más adecuada y para obtener de manera temprana una aproximación pronóstica del paciente1.
Se han publicado varios estudios en los que se intenta determinar el valor predictivo del ECG de ingreso en el infarto agudo de miocardio (IAM). La mayoría de ellos han cuantificado el tamaño del IAM mediante la magnitud de la elevación del segmento ST2-4, el número de derivaciones afectadas enfrentando la zona de lesión5-7, o en función de alteraciones presentes en el complejo QRS y segmento ST8,9. Cohen et al7 encontraron que el número de derivaciones con elevación del segmento ST durante la realización de una angioplastia a la arteria descendente anterior se correlacionaba con el tamaño angiográfico del IAM. Aldrich et al5 describieron una fórmula que correlacionaba el número de derivaciones con ascenso del punto J con el tamaño del IAM. Mauri et al10, en un subestudio del GISSI, encontraron una relación entre el número de derivaciones afectadas durante un IAM anterior y la mortalidad. Sin embargo, Murray et al11 sólo describieron una débil correlación entre el número de derivaciones con ascenso del segmento ST y el tamaño del IAM determinado por la técnica del tecnecio 99 pirofosfato. Yusuf et al12 y Nielsen2 no encontraron ninguna correlación entre el número de derivaciones con ascenso del segmento ST y el pico de la isoenzima MB de la creatincinasa (CK-MB) o la mortalidad. Otros autores han descrito una mayor mortalidad en aquellos pacientes que en el momento de ingreso tienen el segmento ST más elevado13.
Estos estudios previos referentes a la capacidad pronóstica del ECG en el IAM se han centrado fundamentalmente en mediciones absolutas de la elevación del segmento ST y, aunque con datos contradictorios, en general se acepta que una mayor elevación del segmento ST y un número más elevado de derivaciones afectadas en la cara enfrentada a la zona de lesión se relacionan con un mayor tamaño del IAM y un peor pronóstico. Birnbaum et al14 han identificado un grupo de alto riesgo a través del análisis de la distorsión terminal del complejo QRS que cursa con un mayor tamaño de infarto y un menor grado de reperfusión. Los mecanismos de esta asociación son desconocidos. Se ha sugerido la importancia de la circulación colateral15,16. En definitiva, la distorsión terminal del complejo QRS parece relacionarse con el grado de daño miocárdico y podría tener cierto significado para predecir el grado de reperfusión postrombólisis.
El objetivo de este estudio es intentar hallar algún grado de asociación entre el patrón electrocardiográfico de ingreso del IAM y aquellos pacientes con mayor probabilidad de trombólisis ineficaz.
PACIENTES Y MÉTODOS
Pacientes
Se analizaron retrospectivamente 254 pacientes ingresados de manera consecutiva en la unidad coronaria (UC) durante el período 1992-1996. Se incluyeron en el estudio todos aquellos pacientes con un IAM de menos de 6 h de evolución y que presentaban en el ingreso una imagen electrocardiográfica con onda T positiva sin desarrollo de onda Q.
Los criterios diagnósticos de IAM fueron: dolor torácico de características isquémicas de más de 30 min de duración, aumento de la creatinincinasa (CK) y de su isoenzima CK-MB por encima del doble del valor de referencia de nuestro laboratorio, y cambios electrocardiográficos evolutivos característicos de IAM.
Todos los pacientes finalmente estudiados recibieron tratamiento trombolítico antes de la sexta hora desde el inicio de los síntomas.
Criterios electrocardiográficos
Los pacientes se agruparon según el patrón ECG de ingreso, definido por la presencia o ausencia de distorsión de la porción final del complejo QRS8.
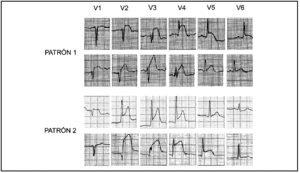
La distorsión final del QRS (patrón 2) se definió como la presencia de una elevación del punto J mayor o igual al 50% de la onda R en derivaciones frontales, y/o la desaparición de la onda S en derivaciones precordiales. Dichas alteraciones debían apreciarse por lo menos en 2 derivaciones adyacentes enfrentadas a la zona de lesión (fig. 1).
Figura 1. Ejemplos de los diferentes patrones en un IAM de localización anterior. Se define como patrón 2 en las derivaciones precordiales la desaparición de la onda S. En el primer ejemplo de patrón 2 se aprecia una ausencia de la onda S, y en el ejemplo inferior de dicho patrón existe una elevación del punto J superior al 50% de la onda R.
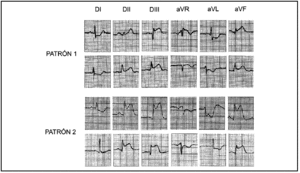
Los pacientes sin distorsión de la parte final del complejo QRS (patrón 1) eran aquellos en los que, a pesar de diferentes grados de elevación del segmento ST en el ECG, en todos los complejos el punto J estaba por debajo del 50% de la onda R en las derivaciones frontales, y/o preservaban la onda S en las derivaciones precordiales (fig. 2).
Figura 2. Ejemplos de los diferentes patrones en un IAM de localización inferior. Se define el patrón 2 en esta localización si existe una elevación del punto J mayor o igual al 50% de la onda R. En ambos ejemplos de la figura 2 se aprecia un diferente grado de elevación del segmento ST, pero el punto J es superior al 50% de la altura de la onda R.
La elevación del segmento se midió manualmente hacia el 0,05 mV más cercano en cada derivación, a 0,08 ms desde el punto J.
Criterios indirectos de reperfusión
Se consideraron criterios indirectos de reperfusión: el pico temprano de CK y CK-MB antes de las 14 h del inicio de los síntomas17,18, y/o un descenso del segmento ST superior al 50%19 y/o la negativización de la onda T a las 2 horas postrombólisis20-23.
Variables estudiadas
Se recogieron variables individuales como la edad, el sexo, el tipo de fibrinolítico utilizado y el tiempo transcurrido desde el inicio de los síntomas hasta la realización de la trombólisis.
Se realizó un seguimiento hospitalario tras el tratamiento valorando el peor grado de Killip alcanzado durante la estancia de los pacientes en la UC y la presencia de disfunción ventricular izquierda, a través de la fracción de eyección (FE) medida mediante ecocardiografía. También se recogió información referente a la estratificación de riesgo post-IAM, valorando la presencia de arritmias malignas (taquicardia ventricular y fibrilación ventricular), aparición de angina post-IAM y evolución fatal. También se ha intentado asociar el patrón electrocardiográfico con la evolución clínica y los resultados de la ergometría y coronariografía.
Análisis estadístico
Se analizaron los datos mediante el paquete estadístico SPSS, expresándose las variables en medias y desviación estándar (DE). Se utilizó el test de la t de Student para analizar diferencias en variables continuas y el de la χ2 para variables categóricas. Se realizó un análisis de regresión logística multivariante y se calcularon la odds ratio (OR) y el intervalo de confianza (IC) del 95%. Un valor de p inferior a 0,05 fue considerado como estadísticamente significativo.
RESULTADOS
De los 254 pacientes analizados, 30 fueron excluidos por bloqueo de rama derecha o izquierda, 39 por IAM previo y 35 casos más por retraso superior de 6 h desde el tiempo de inicio de los síntomas hasta la realización de la fibrinólisis.
Se estudiaron 150 pacientes: 131 eran varones y 19 mujeres, con una media de edad de 60 (10) años (rango, 32-82 años).
La localización del IAM fue la siguiente: 80 pacientes presentaban IAM inferior, 59 IAM anterior, ocho IAM lateral y tres IAM sin onda Q.
En 100 pacientes no se observó distorsión de la porción final del complejo QRS y en 50 casos sí se apreció dicha distorsión (33 pacientes con IAM inferior, 14 con IAM anterior y tres con IAM lateral).
No hubo diferencias entre los dos grupos en cuanto a la edad o el sexo de los pacientes (tabla 1), ni respecto al tiempo transcurrido desde el comienzo de los síntomas al inicio de la trombólisis (221 [82] min en el patrón 1 y 224 [76] min en el patrón 2; p = 0,82). Tampoco se encontraron diferencias respecto al fibrinolítico empleado, utilizándose en 78 casos (78%) rtPA en el patrón 1 y en 39 ocasiones (78%) en pacientes con patrón 2. La estreptocinasa se empleó en 22 casos (22%) con patrón 1 y en 11 (22%) con patrón 2 (p = 1).
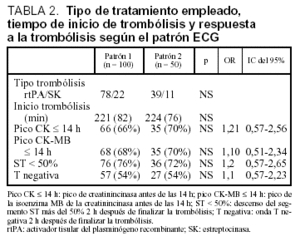
El tamaño del IAM valorado mediante el pico máximo de CK y CK-MB (tabla 2) fue mayor en los pacientes con distorsión final del complejo QRS, independientemente de la localización del infarto. El pico de CK en los pacientes con patrón 1 fue de 2.251 (1.564) U y 281 (186) U de CK-MB, mientras que los pacientes con patrón 2 presentaron un pico de CK de 3.207 (1.663) U y 403 (226) U de CK-MB (p < 0,01).
La evolución clínica de los pacientes durante su estancia en la UC fue peor en el grupo de los que presentaban distorsión final del complejo QRS respecto a los que no la presentaban: mayor incidencia de clase Killip III/IV (OR = 5,4; IC del 95%, 1,01-29,1; p < 0,01) y mayor disfunción ventricular izquierda grave medida mediante ecocardiografía (FE < 35%) (OR = 3,2; IC del 95%, 1,06-9,66; p < 0,01). Los pacientes con IAM anterior y patrón de distorsión final del complejo QRS fueron los que presentaron con más frecuencia una evolución a clase Killip III-IV (OR = 12,8; IC del 95%, 1,3-128; p < 0,05) y FE más bajas, siendo en todos los casos menor del 50% (OR = 16,9; IC del 95% 2,8-102,4; p = 0,01).
Al analizar de manera global la presencia de criterios indirectos de reperfusión no se encontraron diferencias estadísticamente significativas entre los dos grupos de pacientes, según el patrón ECG (ta-bla 3). Los enfermos tratados con rtPA presentaban una mejor reperfusión respecto a los tratados con estreptocinasa en cuanto a tiempo (pico CK < 14 h en 85 frente a 16 pacientes; p < 0,05) y evolución ECG (ST < 50% en 94 frente a 18 pacientes; p < 0,05), independientemente del patrón ECG de ingreso.
Si relacionamos los criterios de reperfusión con la localización del IAM, los enfermos con IAM de localización anterior, sin presentar diferencias en cuanto a la precocidad de los picos de CK y CK-MB respecto a los que tenían IAM inferior, sí tenían mayor persistencia del segmento ST elevado (p < 0,05) y de la onda T positiva (p < 0,05) en los ECG posfibrinólisis. Estas diferencias, sin embargo, no se mantenían al introducir el patrón ECG en el análisis.
En la estratificación de riesgo posterior realizada a estos enfermos no se encontraron diferencias significativas entre ambos grupos.
En aquellos pacientes a los que se les realizó cateterismo cardíaco (n = 33) no se apreciaron variaciones en cuanto al número de vasos afectados (p = NS).
Posteriormente, con las variables significativas del análisis univariado se realizó una regresión logística, en la que sólo la FE < 35% reveló una asociación con la distorsión final del complejo QRS (OR = 3,2; IC del 95%, 1,06-9,66; p < 0,05)
DISCUSION
El patrón ECG de ingreso como factor pronóstico. Estudios previos
Diversos autores han estudiado las alteraciones del complejo QRS en relación con el pronóstico de los pacientes, apreciando una correlación de la distorsión del complejo QRS (patrón 2) en el ECG de ingreso con un mayor pico de CPK, más disfunción ventricular y mayor mortalidad9,14,24-26.
Aunque, a diferencia de algunos autores, no encontramos una mayor prevalencia de la distorsión del complejo QRS en los IAM anteriores, nuestro estudio corrobora que los pacientes con patrón 2 en el ECG de ingreso tienen infartos de mayor tamaño, medidos por elevación enzimática, con peor clase Killip durante su estancia en la UC y con una FE inferior, alcanzando todas estas variables significación estadística. De esta manera se establece un grado de asociación evidente entre el patrón ECG de ingreso y las variables previamente descritas.
Explicación electrofisiológica del patrón inicial
Se desconoce, por el momento, el origen de la distorsión de la porción final del complejo QRS. Para Birnbaum et al14,27, esta distorsión podría deberse a una alteración de la velocidad de conducción en las fibras de Purkinje. Este retraso en la conducción provoca un aumento de la onda R y una desaparición de la onda S.
Como el sistema de Purkinje es menos sensible a la isquemia que las células miocárdicas, el grado de isquemia debe ser mayor, debido a que la oclusión coronaria es completa, a la falta de circulación colateral o a la inexistencia de un precondicionamiento miocárdico previo gracias a la presencia de episodios de angina antes del IAM. A pesar de que Birnbaum et al, en un subanálisis retrospectivo, no encontraron diferencias en el grado de circulación colateral, estos datos no coinciden con nuestras observaciones16. Lee et al26 también han observado recientemente que la ausencia de circulación colateral se asocia al patrón de distorsión terminal del complejo QRS.
Limitaciones del estudio. Determinación del grado de asociación entre la respuesta al tratamiento trombolítico y el patrón ECG de ingreso
La principal limitación del estudio es la de no disponer de coronariografía en todos los pacientes ya que, en líneas generales, los datos clínicos indirectos no son buenos marcadores de reperfusión, y no hay ningún dato ni conjunto de datos clínicos que sean predictivos de repermeabilidad coronaria. Los criterios indirectos de reperfusión utilizados en este trabajo están ampliamente descritos en la bibliografía y son aplicados de manera rutinaria en todas las unidades coronarias17-23. Así, por ejemplo, el pico temprano de CK y CK-MB presenta una sensibilidad del 84%, una especificidad del 85%, un valor predictivo positivo del 98% y un valor predictivo negativo del 64%17. Otro de los datos clínicos indirectos de reperfusión, el análisis del segmento ST, es quizás el parámetro más estudiado en la bibliografía. Califf et al19 encontraron que, en el 96% de los casos con normalización del segmento ST después de la infusión de rtPA, la arteria coronaria responsable del IAM estaba permeable.
Se han llevado a cabo estudios que han correlacionado la imagen ECG de ingreso con el resultado del tratamiento trombolítico, según la elevación del segmento ST o la puntuación del complejo QRS28, sugiriéndose que la fibrinolisis reduciría más el tamaño del IAM en pacientes sin distorsión final del complejo QRS27. Nosotros no hemos encontrado diferencias entre los patrones ECG respecto a la presencia de criterios indirectos de reperfusión (pico temprano de CK y CK-MB, descenso del segmento ST mayor del 50% y negativización de la onda T) tras tratamiento trombolítico.
Por otra parte, en la posterior estratificación de riesgo realizada a estos enfermos no hubo diferencias en cuanto a la presencia de angina post-IAM o el resultado de la ergometría. Con la limitación de no disponer de coronariografía en todos los pacientes, en aquellos casos en los cuales se llevó a cabo no encontramos diferencias en cuanto al número de vasos afectados, al igual que se ha descrito previamente14.
En este estudio, por tanto, el patrón ECG de ingreso no se asocia con la respuesta al tratamiento trombolítico, ni con la aparición de complicaciones isquémicas post-IAM.
CONCLUSION
En nuestro grupo de pacientes, el patrón electrocardiográfico de ingreso en el IAM, clasificado según la distorsión de la porción final del complejo QRS, no se asocia con la respuesta al tratamiento trombolítico, aunque sí existe un grado de asociación entre dicha alteración electrocardiográfica y la aparición de disfunción ventricular izquierda y mayor tamaño del IAM.
AGRADECIMIENTO
Agradecemos a Ll. Llompart su colaboración en la realización de las figuras.