INTRODUCCIÓN
El síndrome de respuesta inflamatoria sistémica (SRIS) es consecuencia de la activación del sistema inmunitario y la reacción inflamatoria masiva provocada por una liberación sistémica de citocinas, en respuesta a diversos procesos patológicos de etiología tanto infecciosa como no infecciosa. El infarto agudo de miocardio (IAM) y la lesión por isquemia-reperfusión se incluyen dentro de las causas no infecciosas que pueden desencadenar el desarrollo de este síndrome1. Además, se ha demostrado que en los pacientes con síndrome coronario agudo e IAM, la presencia de marcadores inflamatorios sistémicos es un predictor adecuado de pronóstico adverso y un método útil para la estratificación del riesgo en los mismos2,3.
Este estudio fue diseñado con el propósito de evaluar la incidencia, el perfil clínico y el pronóstico intrahospitalario de los pacientes con IAM revascularizados con angioplastia primaria (AP) que presentaban el diagnóstico de SRIS.
PACIENTES Y MÉTODOS
Se estudió de forma prospectiva durante el año 2004 a 110 pacientes ingresados de forma consecutiva en la Unidad de Coronarias del Hospital Universitario de Canarias con el diagnóstico de IAM y que fueron tratados con AP. El estudio se llevó a cabo de acuerdo a los principios de la Declaración de Helsinki y de la Asamblea Médica Mundial, el protocolo de estudio fue aprobado por el Comité de Ética local y se obtuvo el consentimiento informado de los pacientes participantes en el estudio. El procedimiento revascularizador fue realizado con éxito en la totalidad de los pacientes con el reestablecimiento del flujo coronario grado TIMI 3 en la arteria responsable del infarto. La AP con implantación del stent fue realizada por un operador experto, de acuerdo a la técnica habitual, a través del abordaje por vía femoral. Todos los pacientes recibieron 300 mg de ácido acetilsalicílico y nitroglicerina a razón de 10 µg/min antes del procedimiento, 5.000 unidades de heparina intravenosa al comienzo del mismo, seguido de tantos bolos como fueron necesarios para mantener un tiempo activado de coagulación de al menos 300 segundos, abciximab durante el procedimiento con bolo e infusión intravenosa ajustados según el peso corporal y durante 12 horas después del mismo. Posteriormente recibieron 300 mg de ácido acetilsalicílico y 75 mg de clopidogrel diariamente. La administración de bloqueadores beta e inhibidores de la enzima convertidora de angiotensina (IECA) después de la AP se dejó a criterio del facultativo responsable del paciente en cada caso.
Fue criterio de exclusión de los pacientes en el estudio la presencia de signos clínicos de infección en algún órgano o tejido, o de sepsis. Se obtuvieron muestras y cultivo de sangre, esputo, orina, catéter intravenoso, exudados y heces en todos los casos de sospecha.
Se definió como diagnóstico de SRIS4 la presencia concomitante de al menos dos de los siguientes criterios: temperatura corporal > 38 ºC o < 36 ºC, frecuencia cardíaca > 90 lpm, hiperventilación con frecuencia respiratoria > 20 rpm o PaCO2 < 32 mmHg y leucocitos ≥ 12.000 cel/µl o < 4.000 cel/µl. La presencia de estos criterios se valoró y por tanto el diagnóstico de SRIS se estableció en las primeras 48 horas después de la realización de la AP. Durante este período, el personal médico de la plantilla de la Unidad Coronaria realizó en todos los pacientes un estudio ecocardiográfico bidimensional y se determinó la fracción de eyección del ventrículo izquierdo (FEVI) según el método biplano de Simpson5.
Para el análisis estadístico de los datos se utilizó el paquete estadístico SPSS 11.0 (SPSS Inc., Chicago, Illinois). Las variables cualitativas se expresan como porcentajes y las variables continuas se expresan como media ± desviación estándar (DE). Se comprobó la proximidad a la normalidad de las distribuciones de las variables mediante la prueba de Kolmogorov-Smirnov. Para comparar dos variables cualitativas se utilizó la prueba de la Chi-cuadrado. Las diferencias de las medias entre dos variables cuantitativas con distribución normal se analizaron con la prueba de la «t» de Student. Se efectuó un análisis de regresión logística binaria para determinar qué variables eran predictoras independientes de la presencia de SRIS. Se incluyeron en el modelo variables como factores de riesgo cardiovascular convencionales, la edad, el sexo varón, la localización anterior del infarto, la FEVI y los niveles de troponina Ic. Con la finalidad de determinar qué factores eran predictores independientes de mortalidad intrahospitalaria en los pacientes de nuestro estudio, se realizó un análisis multivariado siguiendo el método por pasos hacia atrás, tomando la mortalidad como variable dependiente e incluyendo en el modelo todas las variables potencialmente confundentes y de importancia clínica tales como edad, sexo, factores de riesgo coronario, localización del infarto, concentración máxima de troponina I, presencia de SRIS y FEVI. A tal efecto, se categorizó como baja la FEVI < 40% por ser éste el valor a partir del cual este parámetro constituye un factor asociado a la mortalidad en el IAM6. Se consideró estadísticamente significativo un valor de p < 0,05.
RESULTADOS
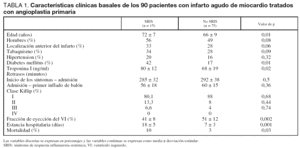
El estudio incluyó, finalmente, a 90 pacientes con IAM tratados con AP, los cuales constituyeron nuestra población de estudio. En la tabla 1 se recogen, de forma resumida, los datos clínicos de los pacientes. Tal como se muestra en la misma, se diagnosticó SRIS en 15 de los 90 pacientes (16,6%). Los pacientes con diagnóstico de SRIS presentaron, de forma significativa, mayor edad, mayor frecuencia de diabetes mellitus, niveles más elevados de troponina I y una FEVI más baja respecto de los pacientes sin diagnóstico de SRIS. Hubo una mayor prevalencia de SRIS en los pacientes con localización anterior del infarto, pero sin alcanzar diferencias significativas. No hubo diferencias significativas en el tratamiento recibido por los pacientes.
En los pacientes con diagnóstico de SRIS fueron significativamente mayores la estancia hospitalaria y la mortalidad intrahospitalaria que en aquellos sin dicho diagnóstico.
En el análisis de regresión logística binaria para determinar qué variables se asociaban a la presencia de SRIS, sólo la presencia de diabetes mellitus (OR: 1,7; IC 95%: 1,2-1,9; p = 0,02) y una menor fracción de eyección (OR: 2,3; IC 95%: 1,5-3,1; p = 0,01) se asociaron con un riesgo incrementado de desarrollo de SRIS.
En el análisis multivariable resultó que la presencia de SRIS se mostró, de manera independiente, como variable predictora de mortalidad (OR: 3,3; IC 95%: 1,3-6; p = 0,001) (tabla 2).
DISCUSIÓN
El principal hallazgo de nuestro estudio ha sido que el SRIS puede presentarse en pacientes con IAM revascularizados con AP y que los pacientes que lo presentan tienen una mayor estancia hospitalaria y un peor pronóstico.
El SRIS representa la respuesta inflamatoria que se desencadena ante una amplia variedad de procesos que se acompañan de una lesión tisular más o menos extensa y que, en cierta manera, forma parte de los propios mecanismos defensivos fisiológicos. Sus manifestaciones clínicas son expresión de la reacción inflamatoria masiva provocada por la liberación sistémica de mediadores endógenos de la inflamación, y la activación de diversos tipos celulares relacionados con ella1. Aunque las mismas son consideradas inespecíficas, numerosas evidencias científicas han puesto en relación la presencia de dichas manifestaciones con la existencia de unos niveles circulantes elevados de una amplia serie de mediadores de la inflamación y la activación de células relacionadas con la misma4,7.
La isquemia prolongada puede provocar una lesión tisular y orgánica severa, pero la reperfusión puede inducir un daño que puede ser incluso peor8. El IAM revascularizado mediante AP proporciona un excelente modelo clínico para el estudio del daño provocado por isquemia-reperfusión. En un estudio previo, nuestro grupo ha demostrado un incremento del estrés oxidativo como mecanismo mayor de daño tisular, así como de activación inflamatoria en pacientes con IAM revascularizados mediante AP9. Se ha demostrado que la misma angioplastia puede inducir, en los pacientes coronarios, una respuesta inflamatoria que es debida, fundamentalmente, a daño en la pared arterial y a la activación de células y la liberación de diversos mediadores de la inflamación10,11. Además, los inflados repetidos del balón durante la angioplastia provocan fenómenos de isquemia-reperfusión que pueden contribuir aún más a ello.
Se dispone de poca información sobre la relación que puede existir entre la presencia de SRIS, las características clínicas de los pacientes que lo presentan y sus consecuencias pronósticas en pacientes con IAM tratados con AP. En un artículo recientemente publicado, Kohsaka S et al12 informan sobre la presencia de SRIS tras IAM complicado con shock cardiogénico en una serie de 302 pacientes pertenecientes al ensayo SHOCK. Estos autores encontraron que un 18% de los pacientes desarrollaron SRIS. Nosotros hemos encontrado una incidencia similar, aunque los pacientes del ensayo SHOCK no son comparables con los de nuestro estudio. Coincidimos, sin embargo, con el hallazgo encontrado en esta serie de pacientes del ensayo SHOCK, en que la presencia de SRIS es un predictor significativo de incremento del riesgo de muerte en pacientes con IAM.
Los pacientes con SRIS de nuestro estudio fueron de mayor edad que la de los pacientes con SRIS descritos en otras series por otros autores, pero de acuerdo con ellos, la edad no fue un predictor independiente del desarrollo de SRIS12,13.
Se ha demostrado en un estudio previo que el desarrollo de SRIS parece estar asociado al tamaño del infarto. Valencia et al14 encontraron, en una serie de 1.903 pacientes pertenecientes al ensayo CARDINAL, que cuanto mayor resultó el tamaño del infarto, menor fue la fracción de eyección, y mayores fueron la respuesta inflamatoria, el desarrollo de insuficiencia cardíaca, de shock cardiogénico y peor fue el pronóstico. En nuestro estudio, el tamaño del infarto no fue una variable específicamente recogida, sin embargo, hemos encontrado un nivel significativamente mayor de la troponina Ic y una fracción de eyección significativamente menor en los pacientes que presentaban SRIS en comparación con los pacientes que no lo presentaban. En nuestro estudio, no obstante, la FEVI fue predictor independiente asociado al desarrollo de SRIS. Varias razones podrían explicar, al menos en parte, estos hallazgos:
1. Una menor fracción de eyección podría reflejar un mayor tamaño del infarto, como previamente se ha sugerido14.
2. La liberación de mediadores de la inflamación durante el IAM también puede producir la expresión de altos niveles de óxido nítrico sintasa inducible y, consiguientemente, altos niveles de óxido nítrico y peroxinitritos que provocarían, como es sabido, una mayor depresión de la contractilidad miocárdica15.
La asociación que hemos encontrado entre la existencia de diabetes mellitus y la presencia de SRIS representa otro interesante hallazgo que aporta el presente estudio: la diabetes mellitus fue una variable predictiva independiente de otras variables de confusión potenciales tales como la edad, el sexo, la presencia de hipertensión arterial, el hábito tabáquico y el tratamiento con bloqueadores beta e IECA sobre la presencia de SRIS. Coincidimos, en este hallazgo, con Patel et al13, quienes han demostrado en un estudio reciente la existencia de una relación significativa entre la diabetes mellitus y la presencia de una intensa respuesta inflamatoria sistémica. La presencia de inflamación sistémica se asocia con la existencia de resistencia insulínica y de diabetes mellitus. Además, evidencias científicas han demostrado que la inflamación ejerce un importante papel en los pacientes diabéticos, dada la fuerte asociación que existe entre inflamación sistémica, la diabetes mellitus, la presencia y la progresión de enfermedad coronaria16.
En nuestro estudio los pacientes con SRIS presentaron mayor mortalidad. Dada la asociación encontrada entre la presencia de SRIS, la existencia de diabetes mellitus y de una menor fracción de eyección, el hecho de que la mortalidad de los pacientes con SRIS sea mayor que la de los pacientes sin él podría explicarse en función de que los mismos constituirían un grupo de enfermos más graves y con mayor mortalidad per se (diabéticos, menor FEVI). Sin embargo, el análisis multivariante demuestra que, tras ajustar para éstas y otras variables también relacionadas con la mortalidad, la presencia de SRIS se mostró como un factor independiente predictor de mortalidad en los pacientes con IAM revascularizados con AP (tabla 2).
Nuestro estudio tiene, no obstante, algunas limitaciones. En primer lugar, el relativo pequeño número de pacientes incluidos en el mismo, en comparación con el de otras series mayores de pacientes. En segundo lugar, el hecho de que no fueron determinados de forma sistemática marcadores bioquímicos de respuesta inflamatoria sistémica, y esta limitación nos priva de un interesante análisis acerca de la relación que pudiera existir entre el SRIS y el IAM tratado con AP. La asociación entre inflamación, inestabilidad de la placa ateromatosa coronaria y manifestaciones clínicas es, de manera indudable, extremadamente compleja.
En conclusión, en este estudio demostramos que el SRIS puede presentarse en pacientes con IAM revascularizados con AP, y que su presencia está asociada con un peor pronóstico y una mayor estancia hospitalaria en este tipo de pacientes. El SRIS es clínicamente fácil, simple y barato de identificar y su diagnóstico aporta una información pronóstica útil en los pacientes con IAM revascularizados con AP.
Declaración de conflicto de intereses
Los autores han declarado no tener ningún conflicto de intereses.
Correspondencia: Dr. M. J. García González.
Unidad de Coronarias. Servicio de Cardiología. Hospital Universitario de Canarias.
Ctra. La Cuesta Taco. Ofra, s/n.
San Cristóbal de La Laguna.
38320 Santa Cruz de Tenerife. España.
Correo electrónico: mjgg181262@hotmail.com
Manuscrito aceptado el 21-II-2007.