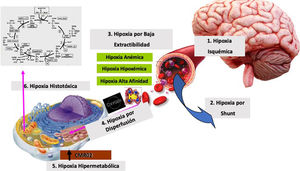
Habitualmente, en el manejo del paciente con traumatismo cráneo-encefálico grave (TCEG), las recomendaciones suelen ir dirigidas al control de la presión intracraneal, siendo llamativa la ausencia de indicaciones específicas sobre el manejo de la anemia1. Fisiopatológicamente, si no tenemos en cuenta los niveles de hemoglobina (Hb), probablemente pudiéramos alcanzar un nivel adecuado de presión de perfusión cerebral, pero con una calidad deficiente en la oxigenación tisular (fig. 1). Es incuestionable que nuestras prácticas en este contexto deben perseguir las recomendaciones europeas «Patient Blood Management», para intentar minimizar las pérdidas sanguíneas, optimizar la hemostasia y, por tanto, evitar de forma multidisciplinar la anemización del paciente, evitando transfusiones innecesarias2.
No obstante, el principal problema al evaluar la literatura relacionada con el TCEG es la heterogeneidad de los estudios, dado que habitualmente se entremezclan con pacientes con TCE moderado, así como los autores usan umbrales transfusionales diferentes, basados en el hematocrito o en las cifras de Hb. A su vez, debemos destacar que la mayoría de los trabajos observacionales presentan vertientes dirigidas a evaluar bien el impacto de la anemia, bien los efectos de la transfusión de hematíes en el pronóstico tras la lesión cerebral traumática3–7.
Concretamente, determinados grupos indican de manera fehaciente que la anemia en el TCE asocia a una mayor probabilidad de complicaciones, así como incrementa la mortalidad3,4. Otros estudios, donde la hipótesis de trabajo fue inversa a la descrita, mostraron que mantener la Hb por encima de 9g/dl, se asocia a un mejor pronóstico funcional5.
A pesar de lo anteriormente descrito, debemos subrayar que la solución no puede pasar por transfundir sistemáticamente a esta subpoblación de pacientes neurocríticos. De hecho, hay autores que identifican que la transfusión de concentrados de hematíes asocia un mal pronóstico a largo plazo6–8. En este sentido, el grupo de Desjardins et al. realizó una revisión sistemática sobre este tema, destacando la imposibilidad de extraer conclusiones definitivas por falta de poder estadístico debido a la falta de homogeneidad de los protocolos evaluados9. No obstante, señalan que la transfusión sanguínea se asoció a un peor pronóstico funcional, tanto en el TCE moderado como en el grave. En contraposición a estos trabajos, un reciente estudio retrospectivo identificó que una actitud transfusional restrictiva podría ser una práctica segura y coste efectiva10.
A pesar del interés que puede suscitar la importancia de las estrategias transfusionales en el TCEG, el número de ensayos clínicos disponibles hasta la fecha es escaso. Podemos destacar el clásico análisis post-hoc de McIntyre et al. de 2006. En este trabajo los autores no evidencian diferencias en la morbimortalidad ante una estrategia restrictiva transfusional (7-9g/dl) frente a una liberal (Hb: 10-12g/dl)11. No obstante, a pesar de los limitantes inherentes al diseño, es llamativo que la inclusión de pacientes no comprendiera un nivel de conciencia concreto, evaluado mediante la Glasgow Coma Scale, así como al analizar las características de la población apenas existían antecedentes personales de consideración entre ambos brazos. Posteriormente, se publicó el ensayo clínico de Robertson et al. con un planteamiento dual, tanto en el umbral transfusional, como en la posible utilidad de la eritropoyetina12. A pesar de la expectación inicial del ensayo, podemos identificar varios limitantes. En primer lugar, tuvieron que someterse a un cambio de protocolo secundario a la administración de eritropoyetina, hecho que prolongó el ensayo durante seis años. Segundo, los pacientes en cada grupo presentaron niveles de Hb por encima del valor objetivo. Tercero, el tamaño muestral por grupo fue relativamente bajo. En sus resultados, los autores no objetivaron diferencias en la supervivencia ni en el pronóstico. Resaltar, que el grupo de transfusión liberal desarrolló un mayor número de infecciones, de eventos tromboembólicos y de síndrome de distrés respiratorio. Recientemente se ha publicado el pilotaje del estudio TRAHT, donde se muestra que es factible el diseño del ensayo clínico, así como adelanta que los pacientes incluidos en el grupo de transfusión liberal presentaban una tendencia a una mejor recuperación y menor mortalidad. Los autores postulan, que optimizar la oxigenación cerebral, puede ser un factor clave en sus resultados13. En resumen, tendremos que esperar el resultado definitivo no solo de este ensayo clínico, sino también de los trials TRAIN y HEMOTION, para poder disponer de una mayor evidencia al respecto. Sin embargo, no podemos olvidar que los ensayos clínicos parten de situaciones idealizadas, dado que pacientes complejos con comorbilidades y tratamientos previos, no suelen formar parte de estos trabajos.
A su vez, es evidente que no podemos subrogar nuestras actuaciones transfusionales en el paciente con TCEG a un simple número de una analítica, máxime cuando en unidades especializadas se dispone de sistemas de neuromonitorización multimodal que pueden dar información fidedigna por diferentes ángulos fisiopatológicos, de la verdadera situación cerebral. En este sentido, encontramos varios trabajos que han analizado la capacidad de la PtiO2 para reconocer situaciones de anemia e hipoxia cerebral, así como han constatado los efectos de la transfusión sobre la oxigenación del cerebro14,15. Derivado del trabajo descrito de Robertson et al. encontramos un subanálisis orientado a la información obtenida de la neuromonitorización del paciente con TCEG12,16. Los autores identifican que el grupo con una estrategia restrictiva desarrollaban más episodios de hipoxia cerebral cuando el sensor se ubicaba en áreas sanas del cerebro. No obstante, no identificaron diferencias en la mortalidad entre la estrategia restrictiva frente la liberal. Posteriormente, el grupo de Leal-Noval et al. desarrolló un interesante ensayo clínico, donde el umbral transfusional era guiado por la Hb y por los datos de la rSO2. Los autores pudieron constatar una menor necesidad transfusional, cuando se usaban ambos triggers, sin identificar diferencias entre ambos grupos17.
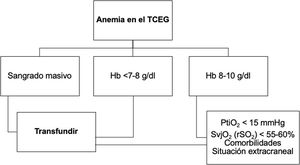
Llegados a este punto, podemos afirmar que no existe una evidencia clara y suficiente que nos revele cuando deberíamos transfundir al paciente con TCEG con unos niveles de Hb comprendidos entre 8-10g/dl. La toma de decisiones en ese dintel continúa siendo hoy en día una zona gris, abierta al debate, donde sin duda precisamos más información a la hora de establecer la indicación transfusional. En estos casos, y a tenor de lo previamente descrito, consideramos que la figura 2, puede ser una buena guía de actuación. De esta forma aprovecharíamos toda la información posible obtenida mediante la neuromonitorización avanzada, cuando nos encontremos en esa franja de incertidumbre transfusional, una vez descartadas otras causas de hipoxia tisular (fig. 1). Si bien, debemos reconocer que no en todos los centros se realiza de manera sistemática la monitorización de la PIC, junto con la PtiO2 y la rSO216,18. Por último, debemos sopesar los antecedentes previos del paciente, así como la presencia de otras lesiones traumáticas sangrantes asociadas al TCEG.
En definitiva, es importante destacar la necesidad de ampliar el conocimiento en esta área de actuación del paciente que sufre un TCEG para establecer las indicaciones transfusionales mediante criterios objetivos, seguros y eficientes.
Conflicto de interesesNo existe conflicto de intereses relacionado con este trabajo.