INTRODUCCIÓN
El tubo endotraqueal representa una carga respiratoria añadida a los pacientes que precisan ventilación mecánica. Las cargas resistivas aumentan el trabajo respiratorio de los pacientes, siendo la mayoría de estas cargas debidas al diámetro del tubo endotraqueal, es decir, cuanto más estrecho el tubo traqueal, mayor es la resistencia inducida. Para intentar obviar este trabajo adicional, los médicos frecuentemente aumentan el soporte ventilatorio a sus pacientes. Los métodos generalmente disponibles para ello son la presión de soporte (PSV) y, en menor medida, la presión continua positiva en la vía aérea (CPAP). Ambos sistemas reducen el trabajo respiratorio de los pacientes, siendo la PSV el más ampliamente utilizado. Se han publicado algunas recomendaciones para el uso de PSV en situaciones específicas. Fiastro et al1 encontraron que el nivel de PSV necesario para compensar la carga del tubo traqueal era proporcional al flujo inspiratorio e inversamente proporcional al diámetro del propio tubo traqueal. Por otra parte, Brochard et al2 encontraron que la PSV podía compensar el trabajo respiratorio adicional creado por el tubo traqueal, pero que el rango de PSV necesario era muy amplio. Además, observaron que los pacientes con bronconeumopatía crónica precisaban mayor nivel de PSV para conseguir la compensación total del tubo traqueal.
La ventilación asistida proporcional (PAV) es un modo ventilatorio que recientemente se ha incorporado en los ventiladores convencionales. Se caracteriza por ayudar el esfuerzo respiratorio de los pacientes por medio de la aplicación de presión positiva a las vías aéreas. Lo original es que la presión ejercida es directamente proporcional al flujo aéreo y al volumen de aire generados por el paciente. Con esta técnica, el médico decide cuánto soporte va a recibir el paciente en base a modular los multiplicadores de presión respecto al flujo y respecto al volumen, también llamados compensadores de resistencia y de elastancia, respectivamente.
Desde un punto de vista teórico, tanto PSV como PAV podrían tener una eficacia similar para compensar la resistencia del tubo traqueal. Para una resistencia dada, básicamente definida por el diámetro del tubo traqueal y el flujo inspiratorio, la PSV aplicaría la cantidad de presión necesaria para compensar esta resistencia, mientras que la PAV aplicaría la presión resultante del multiplicador de flujo. No obstante, el efecto tanto de la PSV como de la PAV variarán ante cambios en las características mecánicas pulmonares del paciente.
La hipótesis del presente estudio es que, debido a las diferencias en el diseño, la compensación producida por la PAV podría verse menos influida ante cambios en el flujo aéreo, patrón respiratorio y mecánica pulmonar, que la compensación producida por la PSV.
MATERIAL Y MÉTODOS
Modelo mecánico de pulmón
Empleamos un modelo de pulmón consistente en dos pulmones comerciales (Medishield, England) que permite modificaciones en la resistencia y compliancia. Los pulmones se conectan a una pieza en Y con resistores variables y están confinados en una caja de plexiglás. En esta caja podíamos simular la presión muscular al generar una presión negativa controlada con un espirómetro rodante Ohio 822 (Ohio Instruments, Madison, WI, USA). El espirómetro estaba específicamente adaptado por medio de un circuito eléctrico integrado que controlaba un motor lineal conectado al pistón para variar la presión en la caja según la orden de comando seleccionada. Puede encontrarse una descripción completa del sistema en Younes et al3. Para este estudio, adaptamos un circuito separado con el que controlar la frecuencia respiratoria, la partición entre tiempo inspiratorio y espiratorio (Ti/Ttot) y la rampa de aceleración de la presión negativa generada. Combinando estos parámetros podíamos generar diferentes flujos y tiempos inspiratorios. Estos efectos se conseguían independientemente del tubo traqueal empleado y de las características mecánicas del pulmón seleccionadas. En nuestro laboratorio habíamos medido que el retraso en la señal desde el inicio de la generación de presión negativa y el inicio de flujo inspiratorio era de 20 milisegundos. La limitación de este modelo es que la máxima presión negativa generada es de 17 cm H2O.
Medimos el flujo aéreo con un pneumotacógrafo (Hans Rudolph Inc 3700, Kansas City) y el volumen se obtuvo por integración electrónica de la señal de flujo. La presión de vías aéreas se midió con un transductor de presión diferencial (MicroSwitch 140PC) conectado al extremo proximal del tubo traqueal. Las señales se transformaron con un convertidor analógico-digital y se almacenaron en un ordenador personal para posterior análisis con el programa Windaq (DataQ Instruments Inc, Ohio) a una frecuencia de 50 Hz.
Protocolo
En este estudio usamos un prototipo de ventilador (Winnipeg Ventilator, Manitoba, Canada) que actúa como generador de flujo. Cada fase del estudio constaba de tres pasos. Primero, generábamos un patrón respiratorio dado con los pulmones conectados sin tubo traqueal al ventilador en modo CPAP con presión de cero. Segundo, añadíamos el tubo traqueal y aumentábamos la PSV hasta el punto que se consiguiera el mismo volumen corriente que en la fase previa sin tubo traqueal. En el tercer paso, cambiábamos a PAV aumentando el multiplicador de flujo hasta conseguir el mismo volumen que en el primer paso. Dado que en los tres pasos la presión negativa creada por el "esfuerzo muscular" se mantenía constante, alcanzar el mismo volumen corriente indicaba una compensación completa del trabajo inducido por el tubo traqueal. Así analizamos el efecto de tubos traqueales de 6, 7, 8 y 9 mm de diámetro interior.
Para cada uno de los tubos traqueales analizamos la capacidad de PSV y PAV para compensar la carga impuesta por el tubo a diferentes flujos inspiratorios (0,4, 0,6, 0,8 y 1 l/s) y con diferentes tiempos inspiratorios (0,5, 1 y 1,5 s).
Posteriormente evaluamos el efecto que inducía en la eficacia de PSV y PAV el cambio en la mecánica pulmonar, variando la compliancia del modelo desde el original de 100 ml/cm H2O, hasta 40 y 20 ml/cm H2O, y cambiando la resistencia desde el original de 3 cm H2O/l/s hasta 10 y 20 cm H2O/l/s.
Finalmente analizamos la eficacia de la PSV según fuera la aceleración en llegar a la máxima PSV, pasando del original de 0,05 segundos hasta 0,1, 0,2 y 0,4 segundos.
Análisis estadístico
Para cada grupo de medidas realizadas en diferentes condiciones de flujo, tiempo, etc., se aplicaron análisis de regresión lineal y ajuste de mínimos cuadrados. No se emplearon análisis de significación estadística dado que en un sistema mecánico como éste, la variabilidad es ínfima y no hay limitación en el número de muestreo.
RESULTADOS
Efectos del flujo y del diámetro del tubo traqueal
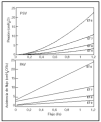
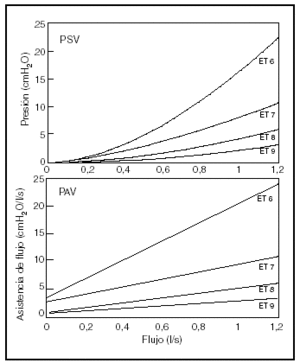
El nivel de PSV necesario para compensar la carga impuesta por el tubo traqueal se correlacionó con el flujo aéreo (fig. 1). Esta correlación para cada tubo traqueal mostró el mejor ajuste con una función exponencial del tipo PSV = a*Flujob4,5. Por el contrario, la asistencia de flujo con PAV mostró una correlación lineal con el flujo aéreo (fig. 1). Este diferente comportamiento representa que la varianza de la PSV fue el doble que la varianza con PAV en el rango de flujos estudiados.
Figura 1. Efecto de diferentes flujos inspiratorios sobre el nivel de presión requerido en PSV (arriba) y sobre la asistencia de flujo en PAV (abajo).
Efecto del tiempo inspiratorio
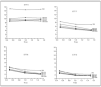
El aumento del tiempo inspiratorio de 1 a 1,5 segundos indujo un descenso del 5% en el nivel de soporte para cada tubo traqueal tanto con PSV como con PAV. Llamativamente, el acortamiento del tiempo inspiratorio hasta 0,5 segundos requirió un aumento del 10% del soporte necesario en PSV y PAV para conseguir el mismo volumen corriente (fig. 2).
Figura 2. Efecto de diferentes tiempos inspiratorios en el nivel de asistencia con PAV y con PSV con diferentes rampas de aceleración, para un flujo inspiratorio fijo de 0,6 l/s.
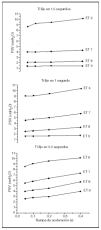
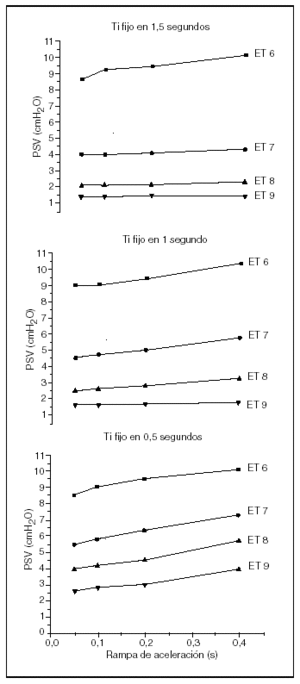
Para cualquier tiempo inspiratorio, una aceleración menor en la PSV (es decir, tiempos de ascenso más largos) precisaron mayores niveles de PSV para alcanzar la compensación completa del tubo traqueal, como se muestra en la figura 3. Este efecto además se veía magnificado en caso de seleccionar tiempos inspiratorios más cortos.
Figura 3. Efecto de las diferentes rampas de aceleración en PSV para diferentes tiempos inspiratorios (arriba = 1,5 s, centro = 1 s y abajo = 0,5 s).
Efecto de la mecánica pulmonar
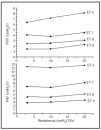
En la última parte del estudio, observamos que a mayor resistencia se precisaba mayor PSV (fig. 4), mientras que con mayor compliancia se necesitaba mayor PAV (fig. 5), aunque la magnitud del efecto era mucho menos importante que los efectos del flujo y del tiempo inspiratorio.
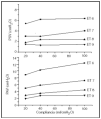
Figura 4. Efecto de los cambios en la resistencia sobre el nivel de PSV (arriba) y PAV (abajo) manteniendo fijos el flujo inspiratorio (0,45 l/s), el tiempo inspiratorio (0,85 s), la compliancia (100 ml/cm H2O) y la rampa de aceleración (0,05 s).
Figura 5. Efecto de los cambios en la compliancia sobre el nivel de PSV (arriba) y PAV (abajo) manteniendo fijos el flujo inspiratorio (0,45 l/s), el tiempo inspiratorio (0,85 s), la resistencia de vías aéreas (3 cm H2O/l/s) y la rampa de aceleración (0,05 s).
DISCUSIÓN
En este estudio hemos demostrado que tanto PSV como PAV son útiles para compensar el exceso de trabajo respiratorio inducido por el tubo traqueal. No obstante, la PAV se ve menos influida que la PSV por cambios en el patrón respiratorio, principalmente del flujo inspiratorio y del tiempo inspiratorio.
El papel del tubo traqueal como una carga durante la ventilación es bien conocido1,2,4. El aumento del trabajo respiratorio es atribuible mayoritariamente al trabajo resistivo necesario para contrarrestar las propiedades resistivas del tubo traqueal. Esta resistencia no es lineal debido a las características de flujo no laminar que ocurren con el paso del aire a través de tubos largos y estrechos.
En la práctica clínica, la PSV es el método más ampliamente utilizado para intentar contrarrestar la carga inspiratoria impuesta por el tubo endotraqueal. En 1988, Fiastro et al1 mostraron en sujetos sanos la capacidad de la PSV para compensar la resistencia causada por el tubo traqueal y confirmaron el impacto del diámetro del tubo y del flujo inspiratorio como los mayores determinantes del nivel de PSV requerido. No obstante, debido al diseño del estudio, no apareció información sobre la influencia de la mecánica pulmonar en la compensación del tubo traqueal. Posteriormente Brochard et al2 probaron el efecto beneficioso de la PSV para reducir el trabajo respiratorio causado por el tubo traqueal, esta vez en pacientes críticos. Encontraron además que el nivel de presión variaba sustancialmente entre pacientes dependiendo de si existía o no enfermedad pulmonar crónica. Una vez más, por su diseño, no disponemos de información sobre el efecto de diferentes flujos, tiempos inspiratorios o rampas de aceleración.
Para intentar responder a estas cuestiones diseñamos este estudio para definir el papel del tiempo inspiratorio, la mecánica pulmonar y el flujo inspiratorio sobre la compensación del tubo traqueal tanto en PSV como con PAV. Así, nuestros resultados concuerdan con los previamente publicados en algunos aspectos, al tiempo que complementan otros no descritos. Así mismo, este estudio refuerza la idea defendida por Brochard6 de que la PSV no es modo ventilatorio tan simple como parece inicialmente. Bonmarchand et al7 probaron que aumentando el flujo aéreo inicial durante PSV se reducía el trabajo respiratorio en pacientes con enfermedad pulmonar obstructiva crónica (EPOC). Encontraron que rampas de aceleración lentas se asociaban a aumentos del trabajo respiratorio, de la magnitud de la presión esofágica generada y del electromiograma del diafragma. Las relaciones entre la rampa de aceleración y el trabajo respiratorio vinieron moduladas por la actividad del centro respiratorio estimada a través de la presión de oclusión o P0,1. En nuestro modelo, con una "activación muscular respiratoria" controlada, las rampas de aceleración lentas en PSV causaron un menor volumen corriente, lo que obligó a tener que aumentar el nivel de presión para conseguir mantenerlo. De la misma manera, el impacto de estas aceleraciones lentas se magnificó con tiempos inspiratorios muy cortos, por un mayor desacoplamiento ventilatorio8,9.
En nuestro conocimiento, no existen datos comparando la eficacia de PAV para compensar el tubo traqueal. Nuestros datos se ajustan firmemente al modelo físico de un componente resistivo no lineal. Por ello, para un diámetro de tubo dado, el nivel de asistencia de flujo no es constante sino proporcional al flujo. Por este mismo componente resistivo, la presión cae siguiendo una ecuación exponencial, mientras que la resistencia sigue una relación lineal y, por ello, el impacto ante cambios en el flujo inspiratorio fue mayor con PSV que con PAV.
Concluimos que tanto la PSV como la PAV pueden compensar el trabajo inducido por el tubo traqueal y que la PAV parece menos influenciable por el patrón respiratorio.
AGRADECIMIENTOS
Al equipo del Dr. Magdy Younes del Health Sciences Center de Winnipeg (Manitoba) por el tiempo que me dedicaron durante la realización del presente trabajo.
Financiación: Beca BAE (ref 95/5660) del Fondo de Investigación Sanitaria del Ministerio de Sanidad y Consumo.