INTRODUCCIÓN
El trasplante de órganos sólidos se ha consolidado como una terapéutica efectiva en múltiples patologías, para las que ofrece una mayor expectativa vital, con una buena calidad de vida.
En la última década estamos asistiendo a un aumento de las listas de espera de receptores potenciales de órganos, y a pesar de que el número de donantes de órganos se ha incrementado en los últimos años y con ello el número de órganos susceptibles de ser trasplantados, existe un disbalance entre la oferta real de órganos y la demanda de los mismos.
La donación de órganos es un hecho altruista y solidario y puede ser materializado de varios modos. En nuestro país la mayoría de las donaciones proceden de donantes a corazón latiente, y sólo un muy escaso porcentaje de donantes a corazón parado. En el momento actual y con objeto de aumentar la oferta de órganos se están utilizando estrategias como la utilización de un órgano para dos receptores, la utilización de órganos procedentes de pacientes de mayor edad o la realización de trasplantes dominó. Con el mismo fin se contempla la opción de la donación de órganos procedentes de donantes vivos, que requiere requisitos específicos, y se plantea la posibilidad en un futuro de los xenotrasplantes1,2.
En España teníamos una tasa de 33 donantes por millón de población (pmp) en el año 2001, muy superior a la de los países de nuestro entorno3, que se mantiene en 2003, a pesar de lo cual las listas de espera siguen aumentando.
Nuestro objetivo prioritario como especialistas implicados en el proceso de donación es conseguir el mayor número de órganos viables, para lo que es necesario mejorar en todas las fases del proceso, fundamentalmente en la detección del donante potencial, y posteriormente en el mantenimiento del paciente en situación de muerte encefálica potencial donante de órganos.
La mayoría de los trasplantes efectuados en nuestro país se llevan a cabo con órganos procedentes de donantes a corazón latiente en situación de muerte cerebral certificada según la legislación vigente4. La cantidad y calidad de estos órganos va a depender de muchos y variados factores, desde la rápida detección de los donantes potenciales de órganos, pasando por el exquisito mantenimiento de los mismos y la correcta coordinación entre la extracción y la asignación de los órganos extraídos, y la gran mayoría de este complejo proceso transcurre en nuestras Unidades.
En este estudio nos planteamos conocer cómo manejamos en las Unidades de Intensivos a nuestros donantes reales de órganos y qué recursos invertimos en sus cuidados.
MATERIAL Y MÉTODOS
Estudio de cohortes retrospectivo de todos los donantes reales generados en la Unidad de Cuidados Intensivos (UCI) de adultos del Hospital Regional Carlos Haya de enero de 1997 a diciembre de 2001.
Hemos analizado un total de 114 protocolos de donación, correspondientes a los donantes reales, registrando en todos ellos el nivel de gravedad al ingreso junto a datos demográficos, de diagnóstico y manejo así como órganos extraídos (tipo y número).
Los datos se encuentran incluidos en la historia clínica informatizada existente en nuestra Unidad que no ha sufrido alteraciones durante el período de estudio, tanto en su forma como en la codificación usada.
Para la recogida de datos hemos usado una hoja específica diseñada para tal fin, con definiciones consensuadas por los investigadores y ha sido completada tan sólo por los mismos.
Todas las complicaciones recogidas se refieren a la fase de enclavamiento o son posteriores a la misma.
Se consideró hipotensión una presión arterial (PA) sistólica menor de 100 mmHg de más de una hora de duración, diabetes insípida una diuresis horaria mayor de 300 ml/h durante más de dos horas seguidas con sodio sérico mayor de 145 mEq/l aun en la ausencia de determinación de osmolaridad sanguínea y urinaria, ya que esta determinación no la poseían todos los pacientes, hipotermia como una temperatura tomada por vía axilar menor de 36°C, hipertensión arterial una PA sistólica mayor de 180 mmHg durante el período de enclavamiento, y taquicardia una frecuencia cardíaca mayor de 120 latidos por minuto también durante el período de enclavamiento.
El tratamiento aplicado se refiere asimismo al período circunscrito a la fase de enclavamiento y con posterioridad a la misma.
Se analizaron los datos disponibles en la Coordinación de Trasplantes de nuestro Hospital referentes a los indicadores de calidad en el proceso de donación, que se consideraron de interés para el estudio.
En el análisis estadístico los datos se muestran como media y desviación estándar (DE) para las variables continuas excepto para las medidas de tiempo, que se muestran como mediana (rango intercuartil). Las variables categóricas se expresan como frecuencia (%). Se ha realizado una prueba de la "t" de Student (U de Mann-Whitney para variables con número insuficiente de casos) y el análisis de la varianza para comparar variables continuas y la prueba del Chi2 para el análisis de variables categóricas. Los cálculos se realizaron con el paquete estadístico SPSS para Windows®.
RESULTADOS
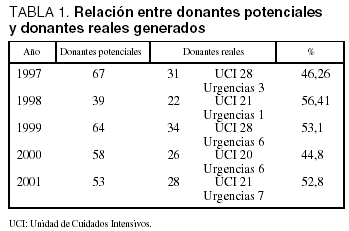
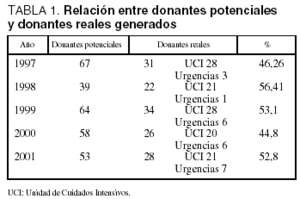
La evolución en el período de estudio entre donantes potenciales y donantes reales generados en la UCI se muestra en la tabla 1.
La relación entre fallecimientos en el Hospital y en la UCI frente a donantes reales en el período de estudio se muestra en la tabla 2.
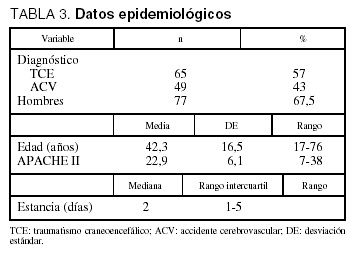
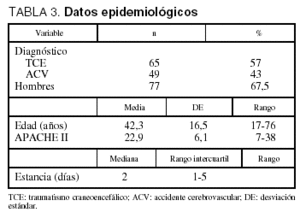
Se incluyeron un total de 114 pacientes donantes reales, de los cuales 77 (67,5%) eran hombres, con una edad media de 42,3 (16,5) años, cuyo diagnóstico de ingreso en la Unidad fue mayoritariamente traumatismo craneoencefálico (TCE) (65 pacientes, 57%). Los datos epidemiológicos se muestran en la tabla 3.
La evolución durante el período de estudio de los motivos de ingreso y edad de los donantes se muestra en la tabla 4.
El 28,1% de los pacientes presentaba un Glasgow Coma Scale (GCS) de 3 al ingreso, el 56,1% entre 4 y 8, y el 15,9% mayor de 9.
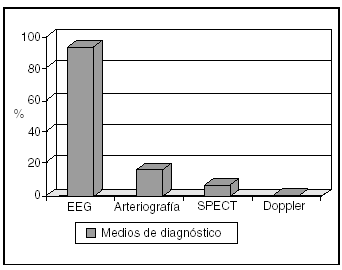
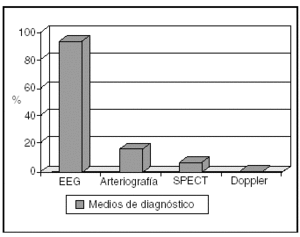
El diagnóstico de muerte cerebral fue efectuado por electroencefalograma (EEG) en 107 (93,9%) pacientes, mientras que la totalidad de métodos empleados para su diagnóstico se muestra en la figura 1.
Figura 1. Métodos diagnósticos de muerte cerebral. EEG: electroencefalograma; SPECT: tomografía computarizada por emisión de fotón único.
Se procedió a monitorización arterial invasiva en 73 (64%) pacientes y a inserción de vía venosa central en 105 (92,1%), obteniéndose medición de presión venosa central (PVC) en 89 (78,1%).
En el grupo de pacientes con GCS 3 al ingreso, se monitorizó invasivamente la PA en el 54,9%, y la PVC en el 90,6%.
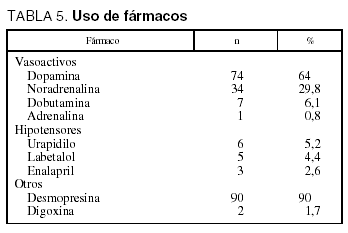
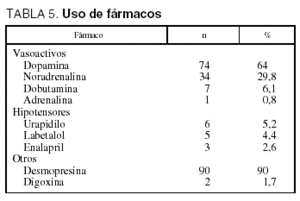
Se utilizaron fármacos inotrópicos y vasoactivos en 98 (86%) pacientes y 14 (12,3%) precisaron del uso de fármacos hipotensores.
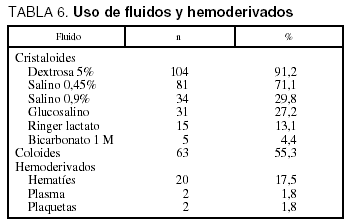
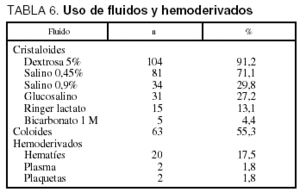
El uso de estos y otros fármacos se muestra en la tabla 5 y el de fluidos y hemoderivados en la tabla 6.
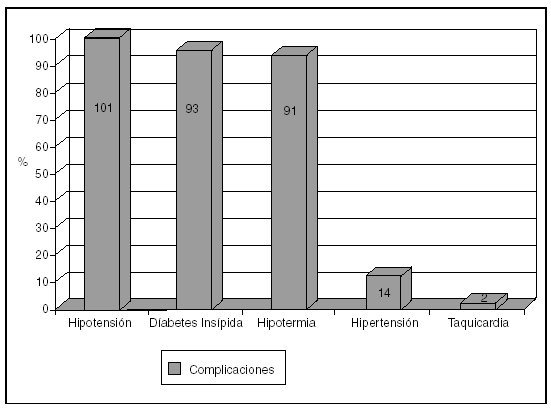
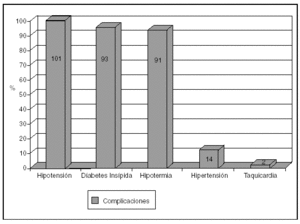
Las complicaciones más frecuentes fueron la hipotensión arterial, que desarrollaron 101 (88,6%) pacientes, la diabetes insípida en 93 (81,6%) y la hipotermia en 91 (79,8%), seguido de una miscelánea, que se muestra en la figura 2.
Figura 2. Frecuencia de aparición de complicaciones.
Un solo paciente no desarrolló ningún tipo de complicación, 24 (21,1%) 1 complicación, 68 (59,6%) 2 complicaciones, 20 (17,5%) 3 complicaciones y 1 (0,9%) 4 complicaciones.
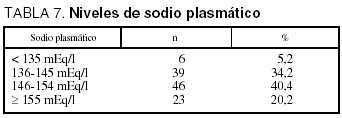
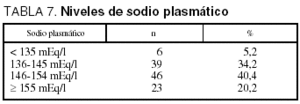
Sesenta y nueve pacientes (60,6%) presentaron hipernatremia, detallándose los niveles de sodio de la totalidad en la tabla 7.
No se produjo ninguna pérdida de donantes en el mantenimiento, una vez diagnosticada la muerte encefálica, durante el período de estudio.
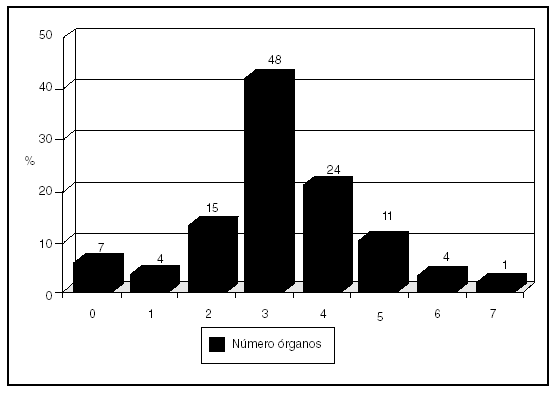
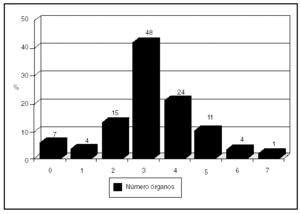
Se obtuvieron 3,2 (1,4) órganos/paciente, oscilando entre ninguno en 7 pacientes (3 de ellos por problemas técnicos y 4 por inviabilidad de los órganos) hasta 7 órganos en un paciente, siendo el órgano más extraido el riñón seguido del hígado, datos que se muestran en la figura 3 y tabla 8.
Figura 3. Número de órganos extraídos por paciente.
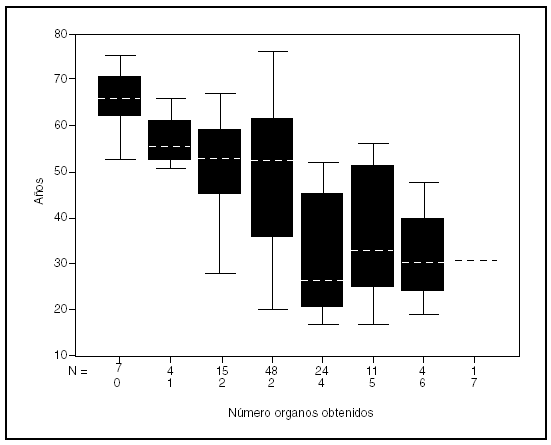
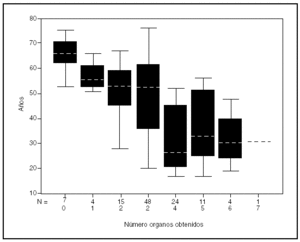
Existió una estrecha correlación entre el número de órganos extraidos por donante con la edad de los mismos, ya que las donaciones de hígado, riñón, corazón y páncreas fueron más frecuentes en donantes más jóvenes (p < 0,05) y el número de órganos disminuyó (p< 0,01) con la edad del donante, 32 (11) años de los donantes de 7 órganos frente a 65,9 (7,4) en los que no se extrajo ningún órgano, como se muestra en la figura 4.
Figura 4. Número de órganos extraídos según edad del donante. Número de órganos = 260, número de pacientes = 114.
No existió ninguna relación entre el número de órganos extraídos con el resto de las variables estudiadas: sexo, número total de complicaciones ni complicaciones individuales (hipertensión, hipotensión, taquicardia, hipotermia, diabetes insípida y alteraciones del sodio).
El 25% de los pacientes permanecieron más de un día en la Unidad y el 50% más de dos días.
DISCUSIÓN
La necesidad de obtención de órganos y tejidos con fines de trasplante es un hecho indiscutible, soportado por el incremento de las listas de espera en los últimos años, las cuales muestran una tendencia creciente3.
A pesar que el "modelo español" se ha erigido en referente en cuanto a los buenos resultados obtenidos en número de donantes/pmp, con una estructura específica y centralizada que coordina de manera eficaz el proceso en su conjunto5,6 hasta el punto de que ha sido imitado en otros países7, la escasez de órganos sigue siendo un problema sanitario de primer orden. En este sentido, entre los objetivos a cumplir en los Centros Hospitalarios dependientes del Servicio Sanitario Público Andaluz, el correcto proceso de donación y trasplante es uno de los objetivos asignados a este ejercicio.
Dado que la mayoría de los donantes potenciales de órganos se encuentran ingresados en nuestras Unidades, nuestra labor no se limita sólo al manejo correcto del donante, sino a la detección precoz de todos aquellos donantes potenciales, ya que es un hecho sabido que un porcentaje no despreciable de donantes se pierden por no haber sido identificados como tales, tanto en Europa como en Estados Unidos8,9.
En este sentido, la relación entre fallecimientos en nuestro Hospital y en la UCI frente a donantes reales (4,01% de media para este período) se ajusta a lo considerado como aceptable por la Organización Nacional de Trasplantes (ONT).
En cuanto a la efectividad global en nuestra Unidad (medida como porcentaje de donantes reales/muerte encefálica) se sitúa en el 50,6% de media, similar a lo reportado por la ONT según el Programa de Garantía de Calidad en el Proceso de Donación para el período 1998-2001 en los Hospitales con Servicio de Neurocirugía, como es el nuestro.
Una vez identificado el donante potencial y con el fin de poner en marcha el complejo engranaje que culmina en la donación, es fundamental una estrecha relación con la Coordinación de Trasplantes Hospitalaria, puesto que la figura del Coordinador de Trasplantes aglutina los conocimientos técnicos y tiene la formación específica y la capacidad logística necesaria para asegurar la viabilidad del proceso en su conjunto10.
Diagnosticada la muerte cerebral y aceptado el paciente como donante potencial, e incluso antes de la entrevista familiar para obtener el consentimiento a la donación, punto clave en este proceso y en el que los intensivistas tenemos también un papel preponderante11.12, nuestro planteamiento del paciente debe cambiar. A partir de ese momento el tratamiento debe ser nuevamente revisado y adaptado a otras necesidades específicas que incluyen la corrección de las alteraciones hemodinámicas y metabólicas propias de la muerte encefálica con el fin de preservar la viabilidad de los órganos.
Nuestro perfil de donante real, objeto de esta revisión, es un hombre joven que ha sufrido un traumatismo craneoencefálico, al igual que lo reportado en otras series13. Según los datos de la ONT, desde el año 1996 se viene reflejando un aumento de los accidentes cerebrovasculares (ACV) hemorrágicos como causa de ingreso fundamental de estos pacientes, hecho que no coincide con nuestros datos durante el período de estudio ni con posterioridad al mismo, dado que en el año 2003 objetivamos un porcentaje del 47% para ambas patologías. La explicación a esto la podríamos encontrar en que algunos enfermos con ACV hemorrágico y GCS menor de 5, considerados como no susceptibles de tratamiento quirúrgico por el neurocirujano tras su valoración en el área de Urgencias, se derivan a su Hospital de procedencia.
El GCS que presentan nuestros pacientes se sitúa mayoritariamente por debajo de 8 cuando llegan a la Unidad, concretamente más del 80% de los donantes reales ingresan con un GCS < 8, y un 28% del total llegan ya en GCS de 3. La explicación a esto la encontramos en que nuestro Hospital es centro de referencia y no sólo atendemos a los TCE de nuestra área sino de toda la provincia, y además se trasladan desde otros centros, públicos o privados, cuando la exploración clínica es compatible con muerte cerebral, para completar el protocolo. Está demostrado que los hospitales con mayor número de camas tienen un mayor porcentaje de donantes potenciales, como parece lógico, así como de donantes reales14.
El EEG ha sido la prueba instrumental confirmatoria más utilizada, apoyándose en arteriografía o tomografía computarizada por emisión de fotón único (SPECT) en aquellos casos en que los pacientes se encontraban sometidos a coma barbitúrico. A pesar de que con la nueva legislación es suficiente con la realización de dos exploraciones clínicas compatibles, el protocolo de nuestro Hospital mantiene el EEG como prueba instrumental, realizando tan sólo una exploración clínica, motivo por el que a partir del año 2000 no ha disminuido el número de EEG efectuados.
En cuanto al doppler transcraneal, que no ha sido utilizado como prueba confirmatoria en este estudio, sí ha sido realizado en los dos últimos años en un elevado porcentaje de nuestros pacientes en muerte cerebral. Se trata de una técnica sencilla y fácilmente reproducible a la cabecera del paciente15, obviando por tanto el riesgo de traslado a la sala de radiología vascular en estos enfermos tan inestables.
El uso de otras técnicas diagnósticas ha sido despreciable, y sólo se utilizó SPECT, a pesar de considerarse una técnica diagnóstica válida aplicada a pacientes sometidos a tratamiento con fármacos depresores del sistema nervioso central, al igual que otras técnicas isotoporadiológicas16,17, en aquellos casos de coma barbitúrico en que la realización de la arteriografía no era posible por problemas técnicos, ya que el riesgo de traslado de los enfermos y el tiempo necesario para su realización en nuestro medio es muy similar al de la arteriografía.
En cuanto a la monitorización a la que se somete a estos pacientes, llama la atención la escasa proporción de monitorización arterial en los pacientes cuyo GCS de ingreso es de 3, que apenas supera el 50%, dato sorprendente habida cuenta de que la práctica totalidad de ellos presentan hipotensión. La mayoría de estos pacientes permanecen ingresados más de 12 horas antes de su traslado a quirófano, por lo que este punto está siendo objeto de revisión.
Entre la sueroterapia administrada observamos que destaca la dextrosa al 5%, lo que se explica por el frecuente uso de fármacos inotrópicos y vasoactivos, no habiendo sido prescrita en ningún caso como sueroterapia de mantenimiento.
Las complicaciones más frecuentemente desarrolladas fueron la hipotensión, la diabetes insípida y la hipotermia.
La muerte encefálica provoca una disfunción de los centros hipotalámicos y bulbares que regulan tanto el tono vasomotor como neuroendocrino y la temperatura. Cualquier alteración debida a la disfunción de estos centros puede conducir a la parada cardíaca si no se corrige de forma adecuada. Por esto el correcto mantenimiento del donante de órganos supone un conocimiento de la fisiopatología propia de la muerte cerebral y del tratamiento adecuado de cada una de las múltiples alteraciones posibles que se presentan en esta situación, lo que ha sido objeto de amplias revisiones en la literatura18,19.
La hipotermia severa y mantenida puede causar inestabilidad hemodinámica, depresión miocárdica y arritmias que pueden conducir a la asistolia con pérdida del donante20, por lo que entre las medidas básicas en el período de mantenimiento se encuentra la administración de calor, que nosotros efectuamos con manta térmica como primera opción y, en casos refractarios, mediante la administración de sueroterapia caliente, a pesar de lo cual nuestros resultados nos muestran que estas medidas no son totalmente efectivas.
La destrucción del centro vasomotor provoca una disminución de las resistencias periféricas y vasodilatación. En general inicialmente responde al aporte enérgico de volumen, que precisa ser complementado en ocasiones con soporte vasoactivo, que en nuestra serie necesitaron más de dos tercios de los pacientes, hecho habitual en el mantenimiento del donante21.
En cuanto a la diabetes insípida, la desarrollaron más del 80% de nuestros pacientes. Su mecanismo fisiopatológico es la destrucción del tracto hipotálamo-hipofisiario, lo que disminuye la producción y liberación de hormona antidiurética. Su frecuencia es muy elevada, y algunos autores muestran la existencia de factores de riesgo de presentación de esta complicación, como ciertos hallazgos en la tomografía axial computarizada como es el caso de la desviación de la línea media o la existencia de hipodensidades hipotalámicas22. Su corrección implica, además del uso de la desmopresina deficitaria, el enérgico aporte de volumen a base de fluidoterapia hiposódica, a la par que el aporte necesario del potasio perdido por las abundantes diuresis. El control del medio interno en estos casos debe ser muy estrecho y las cifras de sodio mantenidas en rango normal para evitar el daño de los órganos a trasplantar, que pueden verse muy alterados por la hipernatremia, estando demostrado en algunos injertos la disfunción primaria de los mismos por este motivo, como ocurre en el trasplante hepático23.
En nuestros pacientes, sólo un 34% mantenían el sodio en rango normal, mientras que más del 60% estaban hipernatrémicos cuando se trasladaron a quirófano, y un 20% del total de pacientes tenían un sodio que excedía de 155 mEq/l, hechos que requieren una atenta reflexión en cuanto al manejo de la fluidoterapia que empleamos, si bien otras series reportan datos similares, con un 31% de hipernatremia mayor de 15024.
Posiblemente otras alteraciones neuroendocrinas distintas a la diabetes insípida, como el déficit de glucocorticoides o de hormonas tiroideas, deban ser corregidas en vistas a mejorar la viabilidad de los órganos, estando descrito un aumento del número de órganos extraídos por paciente cuando se les somete a un tratamiento hormonal enérgico25.
El número de órganos extraídos por paciente en nuestra serie fue proporcional a la edad del donante, extrayéndose más órganos en los pacientes más jóvenes, al igual que lo referido en otras series26, lo cual es lo habitual debido a las alteraciones patológicas propias del envejecimiento tisular, fundamentalmente la arterioesclerosis.
Por otra parte la extracción de órganos como el pulmón o el corazón requieren unos requisitos particulares que impiden su uso en determinadas circunstancias, por lo que su mantenimiento es objeto de revisiones y protocolos específicos27,28.
La donación multiorgánica fue la regla y la media de órganos extraídos por paciente se situó en tres, siendo los órganos más frecuentemente extraídos los riñones y el hígado.
El mantenimiento del donante de órganos debe ser efectuado de acuerdo a protocolos de actuación escritos y uniformes que aseguren la adecuada monitorización y el correcto tratamiento según las demandas específicas e individualizadas de cada paciente, para lo que se requiere un adiestramiento profesional acorde al perfil del médico intensivista, que precisa ser apoyado por un personal de enfermería asimismo adiestrado y motivado para esta función.
A pesar de cumplir con los requisitos previamente mencionados, los objetivos de mejora siempre deben estar presentes para asegurar una asistencia de calidad.