Las guías de práctica clínica recomiendan la estrategia invasiva precoz ajustada al riesgo (EIPAR) en pacientes con síndrome coronario agudo sin elevación del segmento ST (SCASEST). El objetivo fue analizar la aplicación de la EIPAR, sus condicionantes e impacto sobre el pronóstico en pacientes con SCASEST ingresados en Unidades de Cuidados Intensivos Cardiológicos (UCIC).
DiseñoEstudio de cohortes prospectivo.
ÁmbitoUCIC de 8 hospitales en Cataluña.
PacientesPacientes consecutivos con SCASEST entre octubre del 2017 y marzo del 2018. El perfil de riesgo se definió mediante los criterios de la Sociedad Europea de Cardiología.
IntervencionesSe definió como EIPAR la realización de coronariografía en las primeras 6 h en pacientes de muy alto riesgo o en 24 h en pacientes de alto riesgo.
Variables de interésMortalidad/reingreso a los 6 meses.
ResultadosSe incluyó a 629 pacientes (edad media 66,6 años), 225 (35,9%) de muy alto riesgo y 392 (62,6%) de alto riesgo. La estrategia invasiva fue mayoritaria (96,2%). La EIPAR se aplicó en 284 pacientes (45,6%), especialmente pacientes más jóvenes, con menos comorbilidades. Estos pacientes presentaron menor estancia en UCIC y hospitalaria, así como menor incidencia de SCA, revascularizaciones y menor incidencia de muerte/reingreso a 6 meses. Tras ajustar por factores de confusión, la asociación entre adherencia y muerte/reingreso a 6 meses persistió de manera significativa (razón de riesgos: 0,66 [0,45-0,97] p = 0,035).
ConclusionesLa EIPAR se aplica en una minoría de SCASEST ingresados en UCIC, asociándose con una menor incidencia de eventos.
Current guidelines recommend a risk-adjusted early invasive strategy (EIS) in patients with non-ST-segment elevation acute coronary syndrome (NSTEACS). The present study assesses the application if this strategy, the conditioning factors and prognostic impact upon patients with NSTEACS admitted to Intensive Cardiac Care Units (ICCU).
DesignA prospective cohort study was carried out.
SettingThe ICCUs of 8 hospitals in Catalonia (Spain).
PatientsConsecutive patients with NSTEACS between October 2017 and March 2018. The risk profile was defined by the European Society of Cardiology criteria.
InterventionsEIS was defined as the performance of coronary angiography within the first 6hours in patients at very high-risk or within 24hours in high-risk patients.
Outcome variablesMortality or readmission at 6 months.
ResultsA total of 629 patients were included (mean age 66.6 years), of whom 225 (35.9%) were at very high risk, and 392 (62.6%) at high risk. Most patients (96.2%) underwent an invasive strategy. EIS was performed in 284 patients (45.6%), especially younger patients with fewer comorbidities. These patients had a shorter ICCU and hospital stay, as well as a lesser incidence of ACS, revascularization and death or readmission at 6 months. After adjusting for confounders, the association between EIS and death or readmission at 6 months remained significant (hazard ratio: .66, 95% confidence interval .45-.97; P=.035).
ConclusionsThe EIS was performed in a minority of NSTEACS admitted to ICCU, being associated with better outcomes.
La generalización del intervencionismo coronario percutáneo ha provocado una progresiva reducción en la mortalidad del síndrome coronario agudo (SCA) en los últimos años, especialmente en el infarto agudo de miocardio con elevación del segmento ST (IAMCEST)1. Las guías de práctica clínica (GPC) recomiendan la estrategia invasiva (EI) precoz en las primeras 24 h en pacientes con SCA sin elevación del segmento ST (SCASEST) de alto riesgo, así como su realización en las primeras horas en casos de muy alto riesgo2,3. La organización de la asistencia coordinada supone un reto organizativo y un consumo de recursos sanitarios no despreciable4. Aunque en los últimos años la adherencia a las recomendaciones en el SCA ha aumentado5,6, existe escasa información sobre la aplicación de la EI precoz ajustada al riesgo (EIPAR) en los pacientes con SCASEST en nuestro medio.
Los objetivos de este estudio fueron: a) analizar la aplicación de la EIPAR; b) describir los factores asociados a dicha estrategia, y c) analizar su impacto pronóstico en una serie de pacientes no seleccionados con SCASEST ingresados en Unidades de Cuidados Intensivos Cardiológicos (UCIC).
Pacientes y métodosÁmbito y población de estudioSe trata de un registro prospectivo multicéntrico llevado a cabo en 8 UCIC de Cataluña durante un período de 6 meses (entre el 1 de octubre del 2017 y el 31 de marzo del 2018). Dicho estudio fue avalado y coordinado por el Grup de Treball de Cures Agudes Cardiològiques de la Societat Catalana de Cardiologia, al que están adscritas todas las UCIC participantes. Todos los centros participantes cuentan con UCI general y UCIC, y plena disponibilidad (24h/7 días) de laboratorio de hemodinámica. Además, en 6 de los centros existe un programa de cirugía cardíaca y en 3 de ellos programa de trasplante cardíaco y soporte ventricular de corta duración. Este registro fue diseñado para analizar el impacto de la EIPAR en el pronóstico a 6 meses en estos pacientes.
Criterios de inclusión: se incluyó de forma prospectiva y consecutiva a pacientes ingresados en las UCIC de los centros participantes con diagnóstico de SCASEST, definido como la presencia de dolor torácico compatible con SCA con al menos uno de los siguientes: 1) alteraciones electrocardiográficas sugestivas de isquemia miocárdica, y 2) elevación de marcadores de daño miocárdico.
Como único criterio de exclusión se consideró la imposibilidad de obtener el consentimiento informado para la participación en el registro.
Recolección de variablesLos datos se recogieron de forma prospectiva durante el ingreso por parte de los investigadores locales, utilizando formularios estandarizados específicos. Se registraron datos demográficos, características clínicas basales, datos analíticos, electrocardiográficos, ecocardiográficos, así como la realización y el tiempo desde el ingreso hasta la realización de coronariografía.
Se recogió asimismo la evolución clínica intrahospitalaria (tratamientos administrados, requerimiento de procedimientos invasivos, complicaciones y mortalidad hospitalaria). Se calcularon las escalas de riesgo CRUSADE7 y GRACE8 para cada paciente. Los parámetros hemodinámicos (frecuencia cardíaca, la presión arterial sistólica) y el grado Killip se registraron al ingreso en la UCIC. El aclaramiento de creatinina al ingreso se calculó mediante la fórmula de Cockcroft-Gault9. El área de superficie corporal se calculó utilizando la fórmula de Mosteller10. Para la positividad de la troponina no se consideraron aquellos casos en los que dicha anormalidad ocurrió como consecuencia de la revascularización.
Para la definición de perfil de riesgo de los pacientes se utilizaron los criterios de riesgo de la Sociedad Europea de Cardiología2. Se consideraron pacientes de muy alto riesgo aquellos que presentaran al menos una de las siguientes condiciones: angina refractaria, inestabilidad hemodinámica, shock cardiogénico, insuficiencia cardíaca aguda, arritmias ventriculares o paro cardiorrespiratorio. Del mismo modo, se consideraron pacientes de alto riesgo aquellos que presentaran elevación de troponina sérica, diabetes mellitus o valores de escala GRACE > 140, sin presentar criterios de muy alto riesgo.
Al tratarse de un estudio observacional, el manejo de los pacientes siguió la práctica clínica habitual, de acuerdo con las recomendaciones vigentes. El tratamiento antitrombótico y la realización de coronariografía se dejaron a criterio del equipo médico responsable, de acuerdo con la estrategia de actuación de cada centro. En caso de realizarse coronariografía, la elección del acceso vascular, los fármacos antitrombóticos y stents u otros dispositivos quedaron a decisión del operador.
Se definió como EIPAR: a) la realización de coronariografía en las primeras 6 h del ingreso en la UCIC en los pacientes de muy alto riesgo, o b) coronariografía en las primeras 24 h en pacientes con criterios de alto riesgo.
Se realizó un seguimiento clínico a los 6 meses mediante visita presencial, revisión de historias clínicas o contacto telefónico con el paciente, familiares o médico de referencia. La variable de resultado principal del estudio fue el combinado de mortalidad global y reingreso a los 6 meses de seguimiento. Se recogieron asimismo la incidencia de reinfarto y las nuevas revascularizaciones coronarias. La asignación de la causa de la muerte se basó en el juicio clínico del médico que atendió al paciente en el momento de la muerte. Se consideraron muertes de origen cardíaco las causadas por infarto de miocardio, muerte súbita o insuficiencia cardíaca.
Análisis estadísticoLas variables cualitativas se expresan como frecuencias y porcentajes. Las variables cuantitativas se expresan como media y desviación estándar (DE) o como mediana y rango intercuartil si no se cumplían la distribución normal, que se comprobó con la prueba de Shapiro-Wilk. Se analizaron las características basales, el manejo clínico y la evolución clínica en función de la aplicación de la EIPAR. La asociación entre las variables categóricas se analizó mediante el test de la chi al cuadrado, con la corrección de continuidad cuando era necesario. El análisis de las variables cuantitativas en función de la adherencia a recomendaciones se realizó mediante el test de t de Student.
El impacto de la EIPAR en el combinado de muerte o reingreso a los 6 meses se analizó mediante regresión de Cox, tomando como variable independiente la aplicación de la EIPAR y como variable dependiente el combinado de muerte o reingreso a los 6 meses, respectivamente. Los potenciales confusores incluidos en el análisis debían de cumplir los siguientes requisitos11: a) asociación estadísticamente significativa (p ≤ 0,05), tanto con la exposición (aplicación de la EIPAR) como con el efecto (mortalidad o reingreso a los 6 meses); b) ser clínicamente razonable su potencial efecto confusor entre exposición y efecto, y c) no ser una variable intermedia en la relación entre ambos. Adicionalmente, se incluyeron en el análisis variables con una asociación previa con peor pronóstico en este escenario que no cumplieron el primero de los criterios mencionados (sexo, positividad de troponina, fracción de eyección del ventrículo izquierdo y presencia de enfermedad coronaria multivaso).
Se realizó asimismo un análisis accesorio sobre los factores asociados a la aplicación de la EIPAR, generándose un propensity score y realizándose posteriormente un análisis por parejas balanceadas por el valor de dicho propensity score. Se seleccionó a 348 pacientes (174 tratados mediante EIPAR y 174 no tratados mediante EIPAR). El análisis exploratorio de las características de los grupos no mostró diferencias significativas en las principales características clínicas entre ambas cohortes. Se analizó posteriormente el impacto de la EIPAR en la incidencia de muerte o reingreso mediante regresión de Cox con esta selección de pacientes.
Se realizaron curvas de supervivencia mediante Kaplan Meier y se evaluó la significación estadística de las diferencias mediante la prueba de log rank. Los análisis se realizaron mediante PASW Statistics18 (Chicago, IL, EE. UU.).
Aspectos éticosLa inclusión en el estudio no implicó ningún cambio en el manejo clínico de los pacientes. Todos los pacientes dieron por escrito el consentimiento informado antes de su inclusión en el estudio. Los datos de los pacientes fueron debidamente anonimizados y tratados de acuerdo con la legislación vigente. El protocolo de estudio ha sido revisado y aprobado por el Comité de Ética del centro coordinador del estudio (IRB00005523).
ResultadosDurante el período de estudio ingresaron un total de 629 pacientes con SCASEST, de edad media 66,6 años, siendo el 76,8% (483) varones. Globalmente, la serie presentaba un perfil de alto riesgo, con un porcentaje considerable de condiciones como diabetes (37,8%, 238), ictus previo (8,9%, 56) o vasculopatía periférica (16,9%, 106). Un 18,9% de los casos (119 pacientes) presentaba signos de insuficiencia cardíaca al ingreso y un 91,3% (574) presentaba elevación de troponina sérica. El valor medio de la escala GRACE en la serie fue de 141 (DE 36). Alrededor de un tercio de los pacientes (35,9%, 225) presentaba criterios de muy alto riesgo al ingreso, mientras que el 62,6% de los pacientes (392) presentaban criterios de alto riesgo.
La EI durante el ingreso fue mayoritaria (96,2%, 605 pacientes). La información sobre el intervalo hasta la coronariografía estaba disponible en 603/605 pacientes (99,7%). La mediana de horas entre el ingreso en la UCIC y la realización de coronariografía fue de 20 h (rango intercuartil 3-46 h). Globalmente, la EIPAR se aplicó en un 45,6% de los casos (284). Esta proporción fue de 54,6% en los pacientes de alto riesgo, siendo inferior en los pacientes con criterios de muy alto riesgo (31,3%).
Características clínicas en función de la adherencia a recomendacionesLos pacientes en los cuales se aplicó la EIPAR eran más jóvenes, con una menor prevalencia de comorbilidades como diabetes mellitus, hipertensión arterial, vasculopatía periférica, ictus o infarto de miocardio previo (tabla 1). Presentaban asimismo una menor prevalencia de fibrilación auricular, insuficiencia cardíaca previa y antecedentes de neoplasia, así como una menor carga de comorbilidad global y un menor número de fármacos de prescripción habitual. Respecto a la situación clínica al ingreso, los pacientes en los que se aplicó la EIPAR presentaban una menor proporción de signos de insuficiencia cardíaca al ingreso, una tendencia a mayor frecuencia cardíaca y valores significativamente más bajos de las escalas de riesgo GRACE y CRUSADE en comparación con el resto de los pacientes. Presentaban también valores superiores de hemoglobina y filtrado glomerular al ingreso, sin apreciarse diferencias significativas entre ambos grupos en el porcentaje de troponina positiva ni en la fracción de eyección de ventrículo izquierdo.
Características clínicas en función de la adherencia a guías en el momento de la estrategia invasiva
| EIPAR (n = 284) | No EIPAR (n = 341) | Valor de p | |
|---|---|---|---|
| Edad (años), media (DE) | 64,9 (12) | 67,9 (13) | 0,002 |
| Sexo masculino, n (%) | 219 (77,1) | 261 (76,5) | 0,866 |
| Índice de masa corporal (kg/m2), media (DE) | 27,8 (7) | 27,7 (5) | 0,864 |
| Área de superficie corporal (m2), media (DE) | 1,91 (0,2) | 1,89 (0,2) | 0,323 |
| Hipertensión arterial, n (%) | 193 (68,2) | 265 (77,7) | 0,007 |
| Diabetes mellitus, n (%) | 97 (34,2) | 139 (40,8) | 0,090 |
| Dislipidemia, n (%) | 187 (66,3) | 244 (72) | 0,127 |
| Tabaquismo activo, n (%) | 96 (34,4) | 86 (25,2) | 0,003 |
| Ictus previo, n (%) | 18 (6,3) | 38 (11,2) | 0,090 |
| Arteriopatía periférica, n (%) | 37 (13) | 69 (20,2) | 0,017 |
| Infarto de miocardio previo, n (%) | 63 (22,2) | 99 (29,3) | 0,044 |
| ICP previo, n (%) | 57 (20,1) | 64 (24,7) | 0,175 |
| Insuficiencia cardíaca previa, n (%) | 15 (5,3) | 40 (11,8) | 0,005 |
| Fibrilación auricular previa, n (%) | 20 (7) | 45 (13,2) | 0,012 |
| Hemorragia previa, n (%) | 14 (4,9) | 15 (4,4) | 0,760 |
| Neoplasia previa, n (%) | 27 (9,5) | 51 (15) | 0,039 |
| Índice de Charlson, media (DE) | 2,4 (1,6) | 2,7 (1,9) | 0,031 |
| Número de fármacos de prescripción habitual, media (DE) | 5,3 (4) | 6,6 (4) | 0,001 |
| Tensión arterial sistólica (mmHg), media (DE) | 137 (26) | 137 (25) | 0,804 |
| Frecuencia cardíaca (latidos/min), media (DE) | 79 (17) | 77 (19) | 0,098 |
| Clase Killip al ingreso ≥ ii, n (%) | 30 (10,6) | 89 (26,1) | 0,001 |
| Troponina positiva, n (%) | 261 (91,9) | 310 (90,9) | 0,660 |
| Hemoglobina al ingreso (g/dl), media (DE) | 13,7 (2) | 13,1 (2) | 0,001 |
| Aclaramiento de creatinina basal (ml/min), media (DE) | 92 (43) | 82 (44) | 0,002 |
| Glucemia al ingreso (mg/dl), media (DE) | 151 (86) | 152 (75) | 0,891 |
| FEVI (%), media (DE) | 54 (11) | 53 (12) | 0,185 |
| Escala GRACE, media (DE) | 136 (34) | 144 (36) | 0,005 |
| Escala CRUSADE, media (DE) | 25 (17) | 31 (19) | 0,001 |
| Escala PRECISE-DAPT, media (DE) | 20 (14) | 25 (16) | 0,001 |
DE: desviación estándar; EIPAR: estrategia invasiva precoz ajustada al riesgo; FEVI: fracción de eyección de ventrículo izquierdo; ICP: intervencionismo coronario percutáneo.
Los pacientes en los que se aplicó la EIPAR fueron tratados con menor frecuencia con clopidogrel, enoxaparina y diuréticos y con mayor frecuencia con ticagrelor, heparina no fraccionada y fondaparinux (tabla 2).
Manejo y evolución intrahospitalaria en función de la adherencia a recomendaciones sobre la estrategia invasiva
| EIPAR (n = 284) | No EIPAR (n = 341) | Valor de p | |
|---|---|---|---|
| Tratamiento farmacológico,media (DE) | |||
| Ácido acetilsalicílico | 282 (99,6) | 340 (99,7) | 0,895 |
| Clopidogrel | 169 (60,4) | 245 (72,1) | 0,002 |
| Ticagrelor | 121 (42,8) | 105 (30,8) | 0,002 |
| Prasugrel | 18 (6,4) | 12 (3,5) | 0,092 |
| Abciximab | 3 (1,1) | 1 (0,3) | 0,232 |
| Enoxaparina | 131 (47) | 213 (62,8) | 0,001 |
| Heparina no fraccionada | 98 (34,8) | 63 (18,6) | 0,001 |
| Fondaparinux | 89 (31,6) | 71 (21,1) | 0,003 |
| Diuréticos | 75 (26,7) | 140 (41,2) | 0,001 |
| Inotropos | 24 (8,5) | 23 (6,8) | 0,412 |
| Amiodarona | 18 (6,4) | 22 (6,5) | 0,974 |
| Digoxina | 5 (1,8) | 7 (2,1) | 0,519 |
| Betabloqueantes | 227 (81,1) | 267 (78,8) | 0,476 |
| IECA | 190 (67,9) | 223 (65,6) | 0,551 |
| Estatinas | 277 (97,9) | 332 (97,4) | 0,673 |
| Inhibidores de la bomba de protones | 275 (97,9) | 333 (97,9) | 0,947 |
| Datos angiográficos | |||
| Realización de coronariografía, n (%) | 284 (100) | 317 (93) | 0,001 |
| Horas hasta realización de coronariografía (mediana, p25-75) | 2,3 (0-14) | 45 (27-71) | 0,001 |
| Enfermedad multivaso, n (%) | 138 (48,6) | 159 (50,2) | 0,464 |
| Estenosis de tronco común, n (%) | 50 (17,6) | 45 (14,2) | 0,310 |
| Revascularización, n (%) | |||
| No | 71 (25) | 130 (38,1) | 0,028 |
| ICP | 175 (61,6) | 185 (54,3) | |
| Cirugía | 38 (13,4) | 26 (7,6) | |
| Revascularización completa, n (%) | 117 (41,2) | 105 (30,8) | 0,054 |
| Procedimientos | |||
| Marcapasos provisional | 6 (2,1) | 9 (2,6) | 0,664 |
| Contrapulsación intraaórtica | 7 (2,5) | 13 (3,8) | 0,341 |
| Ventilación mecánica invasiva | 34 (12) | 33 (9,7) | 0,369 |
| Ventilación no invasiva | 17 (6) | 29 (8,5) | 0,230 |
| Cánula nasal de alto flujo | 5 (1,8) | 16 (4,7) | 0,042 |
| Hipotermia terapéutica | 2 (0,7) | 2 (0,6) | 0,618 |
| Depuración extrarrenal | 2 (0,7) | 14 (4,1) | 0,006 |
| Evolución clínica intrahospitalaria | |||
| Hemorragias mayoresa, n (%) | 7 (2,5) | 18 (5,3) | 0,074 |
| Requerimiento de transfusión, n (%) | 7 (2,5) | 18 (5,3 | 0,074 |
| Angina recurrente | 11 (3,9) | 24 (7,1) | 0,085 |
| Reinfarto, n (%) | 2 (0,7) | 9 (2,6) | 0,059 |
| Bloqueo auriculoventricular, n (%) | 4 (1,4) | 9 (2,6) | 0,281 |
| Fibrilación ventricular, n (%) | 5 (1,8) | 4 (1,2) | 0,542 |
| Fibrilación auricular, n (%) | 25 (8,8) | 32 (9,4) | 0,784 |
| Ictus isquémico, n (%) | 2 (0,7) | 1 (0,3) | 0,434 |
| Empeoramiento de función renalb, n (%) | 63 (22,7) | 104 (31,2) | 0,019 |
| Mortalidad hospitalaria, n (%) | 4 (1,4) | 7 (2,1) | 0,385 |
| Días de estancia en UCI (mediana, p25-p75) | 1,4 (0,8-2,9) | 2,8 1,5-4,3) | |
| Días de estancia hospitalaria (mediana, p25-p75) | 5 (3-10) | 7 (5-12) | |
Las hemorragias mayores se definieron mediante la clasificación CRUSADE. Se definió empeoramiento de la función renal durante el ingreso como un aumento ≥ 25% de la creatinina sérica respecto a la basal en la analítica al ingreso.
EIPAR: estrategia invasiva precoz ajustada al riesgo; ICP: intervencionismo coronario percutáneo; IECA: inhibidores de la enzima conversora de angiotensina.
No se apreciaron diferencias significativas en el porcentaje de enfermedad coronaria multivaso ni en la proporción de afectación de tronco común izquierdo, aunque sí se apreció una mayor frecuencia de revascularización coronaria, fundamentalmente percutánea y con mayor frecuencia completa, en los pacientes en los cuales se aplicó la EIPAR. Tampoco se apreciaron diferencias significativas en la necesidad de procedimientos durante el ingreso, excepto una menor utilización de cánula nasal de alto flujo y depuración extrarrenal en los pacientes en los que se aplicó la EIPAR (tabla 2). Estos pacientes presentaron una incidencia ligeramente menor de complicaciones hemorrágicas, reinfarto y angina recurrente durante el ingreso, así como una menor frecuencia de empeoramiento de la función renal y una menor estancia en UCIC y hospitalaria, sin diferencias significativas en la mortalidad hospitalaria entre ambos grupos (tabla 2).
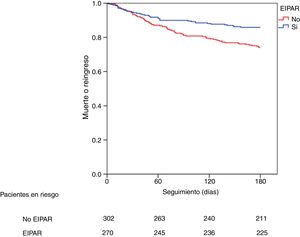
Impacto de la estrategia invasiva precoz ajustada al riesgo en el pronóstico a los 6 mesesLos pacientes en los cuales se aplicó la EIPAR presentaron una mejor evolución clínica tras el alta (tabla 3), con una menor incidencia de nuevo SCA, menor necesidad de nuevas revascularizaciones coronarias y una tendencia a menor mortalidad hospitalaria. Estos pacientes presentaron asimismo una incidencia claramente inferior del combinado de muerte o reingreso a los 6 meses (razón de riesgos [RR]: 0,53; intervalo de confianza [IC] del 95%, 0,38-0,76, p = 0,001) (tabla 4). Tras ajustar por potenciales confusores, la asociación entre aplicación de la EIPAR y la incidencia de muerte o reingreso continuó siendo significativa (RR: 0,66; IC del 95%, 0,45-0,97, p = 0,035) (tabla 4). La figura 1 muestra la incidencia acumulada de muerte o reingreso a los 6 meses en función de la aplicación de la EIPAR.
Manejo al alta y evolución posterior en función de la adherencia a recomendaciones sobre la estrategia invasiva
| EIPAR (n = 284) | No EIPAR (n = 341) | Valor de p | |
|---|---|---|---|
| Manejo farmacológico al alta hospitalaria | |||
| Ácido acetilsalicílico, n (%) | 260 (92,5) | 312 (93,1) | 0,771 |
| Clopidogrel, n (%) | 112 (39,9) | 150 (44,8) | 0,219 |
| Prasugrel, n (%) | 15 (5,3) | 12 (3,6) | 0,289 |
| Ticagrelor, n (%) | 93 (33,1) | 85 (25,4) | 0,035 |
| Rivaroxabán, n (%) | 0 | 3 (0,9) | 0,161 |
| Dabigatrán, n (%) | 5 (1,8) | 5 (1,5) | 0,512 |
| Apixaban, n (%) | 3 (1,1) | 5 (1,3) | 0,462 |
| Warfarina, n (%) | 7 (2,5) | 6 (1,8) | 0,547 |
| Acenocumarol, n (%) | 15 (5,4) | 39 (11,7) | 0,006 |
| Betabloqueantes, n (%) | 214 (76,2) | 246 (73,7) | 0,476 |
| Diuréticos, n (%) | 70 (24,9) | 122 (36,4) | 0,002 |
| IECA, n (%) | 158 (56,2) | 183 (54,6) | 0,691 |
| Estatinas, n (%) | 263 (93,6) | 311 (92,8) | 0,710 |
| Inhibidores de la bomba de protones, n (%) | 233 (82,9) | 283 (84,5) | 0,601 |
| Evolución clínica a los 6 meses | |||
| Reinfarto, n (%) | 8 (2,9) | 25 (7,9) | 0,009 |
| Nuevas revascularizaciones, n (%) | 13 (4,7) | 29 (9,1) | 0,038 |
| Mortalidad global (%) | 10 (3,7) | 23 (7,1) | 0,070 |
| Mortalidad o reingreso, n (%) | 47 (17,3) | 102 (31,2) | 0,001 |
EIPAR: estrategia invasiva precoz ajustada al riesgo; IECA: inhibidores de la enzima conversora de angiotensina.
Predictores de muerte o reingreso a los 6 meses
| Análisis univariado | Análisis multivariado | |||
|---|---|---|---|---|
| Variable | Hazard ratio(IC del 95%) | Valor de p | Hazard ratio(IC del 95%) | Valor de p |
| EIPAR | 0,53 (0,38-0,76) | 0,001 | 0,66 (0,45-0,97) | 0,035 |
| Edad (años) | 1,03 (1,02-1,05) | 0,001 | ||
| Sexo masculino | 0,67 (0,44-1,02) | 0,063 | ||
| Hipertensión arterial | 1,94 (1,26-2,98) | 0,002 | ||
| Diabetes mellitus | 1,91 (1,39-2,64) | 0,001 | ||
| Tabaquismo activo | 0,88 (0,72-1,08) | 0,229 | ||
| Ictus previo | 2,76 (1,89-4,02) | 0,001 | 1,84 (1,20-2,82) | 0,006 |
| Arteriopatía periférica | 2,36 (1,66-3,37) | 0,001 | 1,66 (1,12-2,47) | 0,012 |
| Infarto de miocardio previo | 2,08 (1,49-2,89) | 0,001 | 1,42 (0,96-2,09) | 0,080 |
| Insuficiencia cardíaca previa | 2,53 (1,64-3,89) | 0,001 | 1,93 (1,20-3,11) | 0,007 |
| Fibrilación auricular previa | 2,15 (1,43-3,25) | 0,001 | ||
| Neoplasia previa | 1,66 (1,10-2,51) | 0,016 | ||
| Índice de Charlson | 1,22 (1,12-1,32) | 0,001 | ||
| Número de fármacos de prescripción habitual | 1,12 (1,08-1,16) | 0,001 | ||
| Frecuencia cardíaca | 1,02 (1,01-1,02) | 0,001 | 1,01 (1,00-1,02) | 0,009 |
| Clase Killip al ingreso ≥ ii | 1,89 (1,55-2,29) | 0,001 | ||
| Troponina positiva | 1,83 (0,90-3,74) | 0,096 | ||
| FEVI | 0,97 (0,96-0,98) | 0,001 | ||
| Enfermedad multivaso | 1,39 (0,99-1,96) | 0,058 | ||
| Hemoglobina al ingreso | 0,81 (0,75-0,87) | 0,001 | ||
| Aclaramiento de creatinina basal | 0,99 (0,98-0,99) | 0,001 | 0,99(0,99-1,00) | 0,048 |
| Escala GRACE | 1,01 (1,00-1,01) | 0,001 | 1,00 (1,00-1,01) | 0,095 |
| Revascularización | 0,80 (0,57-1,13) | 0,212 | ||
EIPAR: estrategia invasiva precoz ajustada al riesgo; FEVI: fracción de eyección del ventrículo izquierdo; IC: intervalo de confianza.
Del mismo modo, el análisis realizado en la muestra de parejas balanceadas por el valor del propensity score obtenido mostró una asociación independiente entre la aplicación de la EIPAR y una menor incidencia de muerte o reingreso a los 6 meses (HR 0,57, IC del 95%, 0,36-0,89, p = 0,022).
DiscusiónLos principales hallazgos de este estudio son: a) la EIPAR se aplicó en una minoría (45,6%) de pacientes con SCASEST ingresados en UCIC; b) la aplicación fue mayor en pacientes jóvenes, con una menor carga de comorbilidades y un menor perfil de riesgo global, y c) la aplicación de la EIPAR se asoció con una menor incidencia de eventos durante el seguimiento.
El abordaje mediante EI en pacientes con SCASEST ha demostrado en varios estudios su beneficio pronóstico12,13. Por ello, las GPC recomiendan un abordaje invasivo en la gran mayoría de estos pacientes, sugiriéndose adaptar la precocidad de dicha EI al perfil de riesgo de los pacientes2. La información sobre la aplicación de la EIPAR en la práctica asistencial en nuestro medio es muy escasa.
Los datos de este estudio muestran que en menos de la mitad de los pacientes ingresados en UCIC por SCASEST se les realiza coronariografía invasiva en los tiempos recomendados. De forma interesante, los pacientes en los que se aplicó la EIPAR eran más jóvenes, con menor carga de comorbilidad y menores valores de escala GRACE. Esta aparente paradoja ha sido extensamente descrita con anterioridad, aunque fundamentalmente en pacientes ubicados en plantas de hospitalización convencional5,6. Los datos referentes a pacientes ingresados en Unidades de Críticos son mucho más escasos14-16. La ubicación del paciente con SCASEST en unidades asistenciales diferentes de UCIC está condicionado en muchas ocasiones por un determinado perfil de edad y comorbilidades. Además, es frecuente la coexistencia de un perfil de alto riesgo cardiológico (GRACE elevados, insuficiencia cardíaca aguda, troponina positiva), con un componente de riesgo «no tratable» (edad avanzada, comorbilidades, fragilidad)17,18. Cabe mencionar, en este sentido, la edad relativamente joven de los pacientes incluidos y el bajo porcentaje de mujeres en comparación con otras series19. En nuestra opinión, una de las principales fortalezas de este estudio es la de referirse exclusivamente a pacientes consecutivos ingresados en una UCIC, teóricamente plenamente candidatos a medidas invasivas de alta complejidad.
La EI fue muy mayoritaria en los pacientes de esta serie (96,2%), confirmando la tendencia al alza objetivada en diferentes registros en España en los últimos años5,6. Otros factores, como el grado de complejidad de los hospitales y su disponibilidad de recursos cardiológicos, pueden condicionar asimismo el porcentaje de pacientes tratados mediante EI20. Todos los centros participantes en este registro son centros terciarios con disponibilidad de laboratorio de hemodinámica, lo cual sin duda contribuyó a la alta tasa de EI observada en esta serie. Del mismo modo, el porcentaje de pacientes tratados mediante revascularización percutánea en este estudio fue significativamente superior respecto datos previos5,6.
Las mencionadas recomendaciones en el paciente con SCASEST se basan en algunos ensayos clínicos de pacientes con un alto grado de selección y un perfil de riesgo relativamente bajo21-23, lo que podría cuestionar su extrapolabilidad. En nuestra opinión, otro de los puntos fuertes de este estudio es haber incluido a pacientes consecutivos ingresados en este entorno clínico de toda Cataluña durante 6 meses, reflejando, a nuestro juicio, de forma fidedigna la práctica clínica cotidiana en nuestro medio.
La información sobre el momento idóneo de la EI en función de riesgo es más escasa. En concreto, la recomendación de realizar una estrategia precoz en pacientes de alto riesgo se basa en los resultados del estudio TIMACS24. En dicho ensayo se aleatorizó a 3.031 pacientes con SCASEST a EI precoz (< 12h) respecto a EI más tardía (> 36h), siendo el evento principal del estudio el combinado de muerte, infarto de miocardio o ictus a los 6 meses. La coronariografía se realizó con un tiempo medio de 14 h en el grupo de EI precoz. Aunque no se observó una reducción en la incidencia del evento primario entre ambos grupos, sí se describe una reducción de objetivo secundario compuesto por muerte, infarto o isquemia refractaria a los 6 meses. Del mismo modo, el análisis de subgrupos mostró una reducción de evento primario en aquellos pacientes de mayor riesgo (GRACE > 140).
Más recientemente, el estudio VERDICT25 aleatorizó a 2.147 pacientes con SCASEST a EI precoz (< 12h) vs. EI diferida (48-72h), siendo el objetivo principal del estudio el combinado de muerte, infarto de miocardio, hospitalización por isquemia recurrente u hospitalización por insuficiencia cardíaca. La coronariografía se realizó con un tiempo medio de 4,7 h en el grupo de EI precoz. Tampoco en este estudio se apreciaron diferencias significativas en la incidencia del evento primario entre ambos grupos, aunque en el subgrupo de pacientes de mayor riesgo (GRACE > 140) las diferencias fueron mayores (valor p para la interacción p = 0,023).
Finalmente, Jobs et al.26 realizaron un metaanálisis que incluyó a 5.324 pacientes con SCASEST procedentes de 8 ensayos clínicos. De forma similar, el beneficio en términos de mortalidad de la EI se apreció únicamente para la reducción de mortalidad solo en los pacientes con GRACE > 140, diabetes mellitus, edad > 75 años y con elevación de marcadores de daño miocárdico.
Los datos de nuestro estudio muestran también una mejor evolución clínica en los pacientes tratados mediante EIPAR. Además del hecho de tratarse de un registro observacional, la principal diferencia entre nuestro estudio respecto a los mencionados es que ya incluye la diferenciación por riesgo de forma similar a lo recomendado en las guías (es decir, EI más precoz en los pacientes de mayor riesgo) dentro del grupo en el que se aplicó la EIPAR. Cabe reseñar que los pacientes incluidos en nuestro registro presentaban un perfil de riesgo elevado, ya que un 35,9% cumplía criterios de muy alto riesgo y un 62,6%, de alto riesgo3.
El valor de escala GRACE se asocia a la probabilidad de presentar una enfermedad coronaria más severa y compleja (afectación de tronco común, descendente anterior proximal o enfermedad multivaso)27, lo que podría explicar que una actuación precoz mejorara el pronóstico. En el presente estudio, el valor medio de escala GRACE fue de 141, muy similar al de los pacientes incluidos en el VERDICT25. El hecho de que los pacientes tratados mediante EIPAR tuviesen una mayor tasa de revascularización a pesar de no existir diferencias en la proporción de enfermedad coronaria multivaso podría indicar una menor complejidad de la enfermedad coronaria en este subgrupo, lo que encajaría con el menor valor GRACE objetivado en estos pacientes. Además, en los pacientes en los que se aplicó la EIPAR se demostró una menor incidencia de nuevo SCA, nuevas revascularizaciones y una incidencia claramente menor de muerte o reingreso a los 6 meses. Ello podría estar en relación con el perfil de alto riesgo de los pacientes de este estudio. A pesar de que los grupos eran difícilmente comparables en su perfil de riesgo global, tras el exhaustivo análisis ajustado realizado se apreció una asociación entre la aplicación de la EIPAR y la incidencia de eventos a los 6 meses.
La EIPAR, en nuestro medio, presenta algunas dificultades, debido en parte a la marcada ocupación de los laboratorios de hemodinámica por factores como la diseminación del intervencionismo coronario percutáneo primario en España en el IMCEST28 o la creciente indicación de otro tipo de procedimientos (implante de prótesis aórticas percutáneas, revascularización de oclusiones coronarias crónicas)29. Por todo ello, la plena aplicación de la EIPAR en el SCASEST requiere un gran esfuerzo organizativo y logístico, con una notable inversión de recursos sanitarios (sistemas de traslado interhospitalario, dotación material y personal en los laboratorios de hemodinámica). En nuestra opinión, los datos de este estudio podrían reforzar la necesidad de avanzar en esta dirección para optimizar el manejo y el pronóstico de estos pacientes.
Este estudio presenta algunas limitaciones, como el tamaño de los subgrupos o el moderado número de eventos. Además, el hecho de tratarse de un estudio observacional no permite descartar la presencia de un cierto sesgo de selección, así como el potencial efecto de confusores no analizados (más aún teniendo en cuenta las considerables diferencias entre los pacientes sometidos o no a EIPAR). Por otro lado, en los pacientes de muy alto riesgo se consideró EIPAR un intervalo hasta la coronariografía menos estricto que las 2h estipuladas en las recomendaciones vigentes. Algunas variables potencialmente relevantes referidas al tratamiento médico (precocidad de tratamiento con inhibidores de la enzima conversora de angiotensina o betabloqueante, duración de la anticoagulación) no estaban plenamente disponibles. Finalmente, el tiempo de seguimiento de 6 meses podría ser insuficiente para detectar un mayor impacto de la EIPAR en el pronóstico.
A pesar de ello, en nuestra opinión este estudio aporta información relevante y novedosa sobre la aplicación de la EIPAR en pacientes con SCASEST ingresados en UCIC en nuestro medio, sus factores determinantes y su posible impacto en la evolución clínica. La optimización del manejo de este perfil de pacientes de alto riesgo podría conllevar notables consecuencias médicas, económicas y sociales.
En conclusión, la EIPAR se aplicó en una minoría de pacientes con SCASEST ingresados en UCIC. Los pacientes en los que se aplicó esta estrategia eran más jóvenes, con una menor carga de comorbilidades y un menor perfil de riesgo global. En los pacientes tratados mediante EIPAR se apreció una menor incidencia de eventos durante el seguimiento.
AutoríaMG, SM, CT, GB, DV, TO, JSR, JC, IH, MPR: recolección de los datos y revisión crítica del artículo.
IL, AA: recolección y análisis de los datos, elaboración de manuscrito.
JAGH, JA, AS, CG, JO, RA, AC: revisión crítica y contribución intelectual al artículo.
FinanciaciónNinguna.
Conflicto de InteresesNinguno.