La nefropatía asociada a contraste (NAC) ha sido considerada como una de las mayores causas de disfunción renal aguda (DRA) adquirida en el hospital, sin embargo, en los últimos años, diversos estudios sugieren que su riesgo está sobreestimado1,2. El grupo de trabajo de Cuidados Intensivos Nefrológicos de SEMICYUC realizó el estudio NEFROCON. Se trata de un estudio prospectivo, multicéntrico descriptivo, incluyendo a pacientes ingresados en UCI que fueron sometidos a una primera exploración radiológica con contraste durante tres meses, entre 2012 y 2013.
Definimos NAC como un ascenso de creatinina de 0,5 mg/dL o > 50% de la previa en las 72 horas tras la administración del contraste3.
El estudio fue aprobado por el Comité de Ética en Investigación Clínica (CEIC) del Hospital General Universitario de Castellón, y cada CEIC de los centros participantes determinó la necesidad, o no, de solicitar el consentimiento informado para la participación en el estudio.
Para el análisis univariante se emplearon test no paramétricos, analizando las variables categóricas mediante el test de Chi-cuadrado. Para el análisis de factores pronósticos se realizó un análisis multivariante mediante regresión logística múltiple por el método de paso atrás. Para evaluar el efecto de la profilaxis y de distintos tratamientos sobre el desarrollo de NAC, se construyó un modelo multivariante mediante regresión logística múltiple, calculando posteriormente un score de propensión.
Se analizaron 1.012 casos en 33 hospitales diferentes. Las características demográficas de la población de estudio, el tipo de contraste utilizado y la presencia de factores de riesgo para el desarrollo de DRA se muestran en la tabla 1 del material suplementario. En estos pacientes, se aplicaron medidas preventivas al 29,4% (18,6% de pacientes coronarios y 38,5% de pacientes no coronarios, p 0,001). Siguiendo las recomendaciones de las guías KDIGO4, se administró fluidoterapia (suero salino 0,9% o bicarbonato) a un 76,8% de los casos, siendo más frecuente la administración de salino intravenoso (72,1%). A un 23,2% de los pacientes se administró N-Acetil-Cisteína.
El análisis de las variables relacionadas con el desarrollo de NAC se muestra en la tabla 1. En nuestra población la desarrollaron el 12,1% de los pacientes, con claras diferencias entre pacientes coronarios (8,2%) y el resto de pacientes críticos (15,3%), p = 0,0001. Las características diferenciales entre ambos grupos se muestran en la tabla 2.
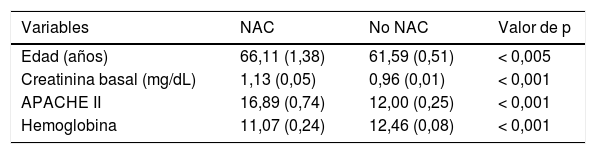
Desarrollo de NAC en relación con las variables analizadas. Análisis univariante
| Variables | NAC | No NAC | Valor de p |
|---|---|---|---|
| Edad (años) | 66,11 (1,38) | 61,59 (0,51) | < 0,005 |
| Creatinina basal (mg/dL) | 1,13 (0,05) | 0,96 (0,01) | < 0,001 |
| APACHE II | 16,89 (0,74) | 12,00 (0,25) | < 0,001 |
| Hemoglobina | 11,07 (0,24) | 12,46 (0,08) | < 0,001 |
| Factores de riesgo | Odds ratio | IC 95% |
|---|---|---|
| Cirrosis hepática | 3,29 | (IC 1,58 – 6,84) |
| Insuficiencia cardíaca | 2,65 | (IC 1,48 – 4,77) |
| Transplante | 7,45 | (IC 1,49 – 37,31) |
| ERC ≥ Grado II | 3,1 | (IC 1,76 – 5,46) |
| Diuréticos | 2,94 | (IC 1,97 – 4,39) |
| Fármacos vasoactivos | 3,12 | (IC 2,08 – 4,67) |
| Shock | 4,26 | (IC 2,86 – 6,33) |
| IAM | 0,55 | (IC 0,35 – 0,86) |
NAC: Nefropatía asociada a contraste. APACHE: Acute Physiology and Chronic Health Evaluation. IC 95%: Intervalo de confianza del 95%. ERC: Enfermedad renal crónica. IAM: Infarto agudo de miocardio.
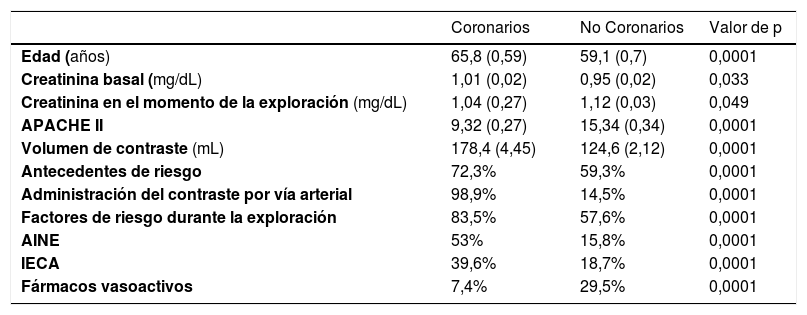
Características diferenciales de los pacientes coronarios y no coronarios
| Coronarios | No Coronarios | Valor de p | |
|---|---|---|---|
| Edad (años) | 65,8 (0,59) | 59,1 (0,7) | 0,0001 |
| Creatinina basal (mg/dL) | 1,01 (0,02) | 0,95 (0,02) | 0,033 |
| Creatinina en el momento de la exploración (mg/dL) | 1,04 (0,27) | 1,12 (0,03) | 0,049 |
| APACHE II | 9,32 (0,27) | 15,34 (0,34) | 0,0001 |
| Volumen de contraste (mL) | 178,4 (4,45) | 124,6 (2,12) | 0,0001 |
| Antecedentes de riesgo | 72,3% | 59,3% | 0,0001 |
| Administración del contraste por vía arterial | 98,9% | 14,5% | 0,0001 |
| Factores de riesgo durante la exploración | 83,5% | 57,6% | 0,0001 |
| AINE | 53% | 15,8% | 0,0001 |
| IECA | 39,6% | 18,7% | 0,0001 |
| Fármacos vasoactivos | 7,4% | 29,5% | 0,0001 |
APACHE: Acute Physiology and Chronic Health Evaluation. AINE: antiinflamatorios no esteroideos. IECA: fármacos inhibidores de la enzima convertidora de la angiotensina.
En el análisis multivariante, los factores de riesgo que se relacionaron de forma independiente con el desarrollo de NAC fueron la creatinina basal, la puntuación APACHE II, el nivel de hemoglobina, la administración de diuréticos y la presencia de shock. (tabla 2 del material suplementario). Sin embargo, cuando analizamos los datos por score de propensión, solo pudimos demostrar un aumento de la incidencia de NAC en aquellos pacientes que recibían diuréticos en el momento de la exploración (OR 1,89; IC 95% 1,17-3,04), relacionado también con un aumento significativo de la mortalidad (OR 1,85; IC 1,13-3,03).
En nuestra serie, obtuvimos una incidencia superior de NAC en pacientes con algún antecedente de riesgo para desarrollar DRA (OR 1,83; IC 95% 1,18-2,83). En general, estos factores de riesgo se caracterizan por ser procesos fisiopatológicos que limitan la capacidad de los riñones para compensar de forma adecuada el stress hemodinámico y microcirculatorio inducido por el contraste, destacando entre ellos la enfermedad renal crónica (ERC), considerada como el más potente predictor de NAC5. La incidencia es superior a medida que aumenta su estadío, fundamentalmente a partir de un estadío II. El efecto de los factores de riesgo es aditivo, y la probabilidad de desarrollo de NAC se incrementa a medida que aumentan el número de estos factores. En nuestra serie, obtenemos una incidencia del 13.7% en aquellos pacientes que presentan al menos un factor de riesgo, frente al 8.4% de pacientes que no presentaban ninguno, entre ellos, los diuréticos se constituyen como uno de los más importantes. La furosemida puede provocar cambios hemodinámicos sistémicos y a nivel renal, que exacerbarían los propios cambios producidos por el contraste. Una disminución en la resistencia vascular cortical podría desviar la sangre de la circulación medular6. Esto unido a la vasoconstricción provocada por el contraste, podría producir una disminución crítica en la tensión de oxígeno en las nefronas medulares, provocando un daño isquémico. Este empeoramiento de la función renal es lo que podría estar asociado al aumento de mortalidad, justificando la recomendación de no utilizar furosemida como profilaxis ni como tratamiento de la DRA7.
Al analizar a los pacientes coronarios (tabla 2), observamos que, de forma llamativa, a pesar de tener más factores de riesgo y la aplicación de menos medidas preventivas, la incidencia de NAC es inferior. Estos resultados se podrían justificar por la diferencia en el perfil de gravedad, con una puntuación de APACHE II inferior a la del grupo de pacientes no coronarios. Este score, además de haber sido utilizado ampliamente como predictor de mortalidad en pacientes críticos, podría ser útil como predictor del desarrollo de DRA en relación con la severidad de la patología del paciente.
En cuanto a las medidas preventivas, la expansión de volumen intravascular con cristaloides intravenosos podría contrarrestar el efecto de la vasoconstricción renal provocada por el contraste, disminuyendo su concentración y viscosidad en la luz tubular, sin embargo, existe un porcentaje de pacientes que siguen desarrollando disfunción renal. En esta línea, se han publicado recientemente diversos estudios que no demuestran un efecto beneficioso en la aplicación de suero salino, bicarbonato ni N-Acetil-Cisteína para la prevención de la NAC8,9.
Quizás una de las limitaciones más importantes del estudio fue la ausencia de grupo control y la falta de un mayor seguimiento clínico para determinar el curso evolutivo a largo plazo. A pesar del tiempo transcurrido hasta la publicación del estudio, los tipos de contraste utilizados fueron los recomendados por su menor nefrotoxicidad (contraste isoosmolar e hipoosmolar), solo en un 4,2% de los casos se utilizó contraste hiperosmolar. Otros sesgos que podríamos apuntar es que el análisis se realiza sobre una población muy heterogénea, y en centros diferentes, que aunque pudiera restar potencia al análisis estadístico, le da mayor validez externa, puesto que los resultados son más generalizables. Con respecto al efecto sobre los resultados, se realizó el análisis multinivel y no mostró efecto de los centros, habiendo analizado de forma separada a pacientes coronarios y no coronarios por regresión logística. Solo analizamos el primer episodio, y no podemos determinar si la repetición de exploraciones sucesivas en algunos pacientes podría influir sobre los resultados de la mortalidad. Por último, la aplicación de profilaxis fue muy heterogénea, y se realizó a criterio de los investigadores, al no ser un estudio controlado, aunque este sesgo se intentó controlar mediante el score de propensión.
Dada su compleja fisiopatología, el origen multifactorial de la DRA en Cuidados Intensivos10 y los múltiples factores que influyen en su patogénesis, en espera de resultados de nuevos estudios que determinen su toxicidad real, podríamos considerar la administración del contraste yodado como un factor de riesgo más, que puede contribuir al deterioro de la función renal en pacientes críticos. En este contexto, los diuréticos se constituyen como factor de riesgo importante, aumentando la incidencia de NAC y la mortalidad.
FinanciaciónEste estudio no ha recibido ningún tipo de financiación.
Conflictos de interesesLos autores declaran no tener conflictos de intereses.