INTRODUCCIÓN
El factor VIIa recombinante (rFVIIa) cataliza y amplifica la conversión de factor X a factor X activado en la superficie de las plaquetas en ausencia de factor tisular (FT). Se propone que la activación directa del factor X en factor Xa inicia la conversión de protrombina en trombina, produciendo el coágulo hemostático por la conversión de fibrinógeno en fibrina1-3. El riesgo de trombosis inducida por rFVIIa se describe como bajo2. Clínicamente ha sido utilizado desde hace años en pacientes hemofílicos4,5, y más recientemente su espectro de indicaciones ha ido aumentando a pacientes con hemorragias graves refractarias a tratamiento quirúrgico o manejo médico6-12. Se presenta una cohorte de enfermos críticos, que recibieron terapia con rFVIIa, describiendo datos clínico-epidemiológicos.
Los objetivos del presente estudio fueron evaluar aquellos marcadores asociados a mortalidad que permitiesen identificar de manera precoz a los enfermos con más posibilidades de supervivencia cuando se instaura terapia con rFVIIa.
PACIENTES Y MÉTODOS
El diseño del estudio fue observacional, descriptivo de una serie de casos clínicos, realizado de forma longitudinal y ambispectiva. La población de estudio fueron pacientes hospitalizados en el Servicio de Medicina Intensiva (UCI) del Hospital Marqués de Valdecilla, durante el período comprendido entre el 20 de julio del 2004 al 20 de julio del 2006, que recibieron tratamiento con rFVIIa. Los criterios de inclusión fueron: pacientes de cualquier sexo, internados en esta Unidad hospitalaria, de cualquier edad y con requerimiento de rFVIIa en algún momento de su estancia en UCI. Se recogieron mediante un formulario los datos de filiación, edad, sexo, patología causante de ingreso, escalas de gravedad (APACHE II, SOFA), así como parámetros analíticos y hemodinámicos antes y después de la administración de rFVIIa. Del mismo modo se clasificó a los enfermos en fallecidos o no durante el curso de su estancia en UCI, enumerando los días de estancia en UCI y hospitalaria.
Finalmente se recogieron las necesidades transfusionales de los enfermos antes y después del rFVIIa (concentrados de hematíes, concentrados de plaquetas, plasma fresco congelado y crioprecipitados).
Los criterios utilizados en la toma de decisión de transfundir fueron:
1. Transfusión de concentrados de hematíes en todos los casos con un valor de hemoglobina por debajo de 7 g/dl.
2. Transfusión de concentrados de hematíes a criterio médico en valores de hemoglobina entre 7-9 g/dl.
3. Transfusión de plasma fresco congelado a criterio médico en función del desarrollo de coagulación intravascular diseminada (CID), coagulopatía de consumo o hepatopatía.
4. Transfusión de plaquetas siempre que el recuento plaquetario fuese inferior a 20.000, con cifras superiores a criterio médico según el riesgo de sangrado y/o acto quirúrgico inminente.
Los criterios utilizados para la administración de rFVIIa fueron:
Pacientes con necesidad de transfusión masiva después de procedimiento quirúrgico sin coagulopatía previa.
Pacientes politraumatizados con hemorragia no controlable por otros medios que requieren transfusión masiva.
Hematomas cerebrales no traumáticos en evolución, con el fin de disminuir su volumen.
Pacientes con necesidad de transfusión masiva en hemorragia espontánea con riesgo vital.
En cuanto a los parámetros analíticos obtenidos previa infusión de rFVIIa, se registraron aquellos dentro de la primera hora preadministración. El valor de presión arterial sistólica (PAS), presión arterial diastólica (PAD) y diuresis horaria se obtuvo del valor medio de las tres horas previas, como máximo, antes de la infusión. Los parámetros postadministración se recogieron de la primera determinación analítica efectuada (menor a dos horas en todos los casos), y los valores de PAS, PAD y diuresis horaria de la media obtenida de las tres horas siguientes postadministración (no fue posible en dos casos por fallecimiento de los enfermos).
Se consideró controlada la hemorragia causante de la administración de rFVIIa en todos los casos en los que se consiguió normalización de los parámetros hemodinámicos, disminución significativa de las necesidades de transfusión de hemoderivados por corrección de valores analíticos y certificación, por visión directa o pruebas de imagen en aquellos casos en los que se pudiera, del cese de la hemorragia (en las tres horas siguientes a la última dosis de factor rFVIIa administrada).
La dosis administrada de rFVIIa fue de 100 mcg/ kg según protocolo institucional del Hospital Universitario Marqués de Valdecilla, consensuada la decisión de administración conjuntamente con el Servicio de Hematología de nuestro centro.
Los datos obtenidos se administraron en soporte informático en una base de datos en formato Microsoft Access, siendo utilizado como herramienta estadística el paquete de software GraphPad. El análisis estadístico se llevó a cabo de la siguiente manera: las medias se compararon mediante la «t» de Student o Anova y las proporciones con el test de Chi-cuadrado.
RESULTADOS
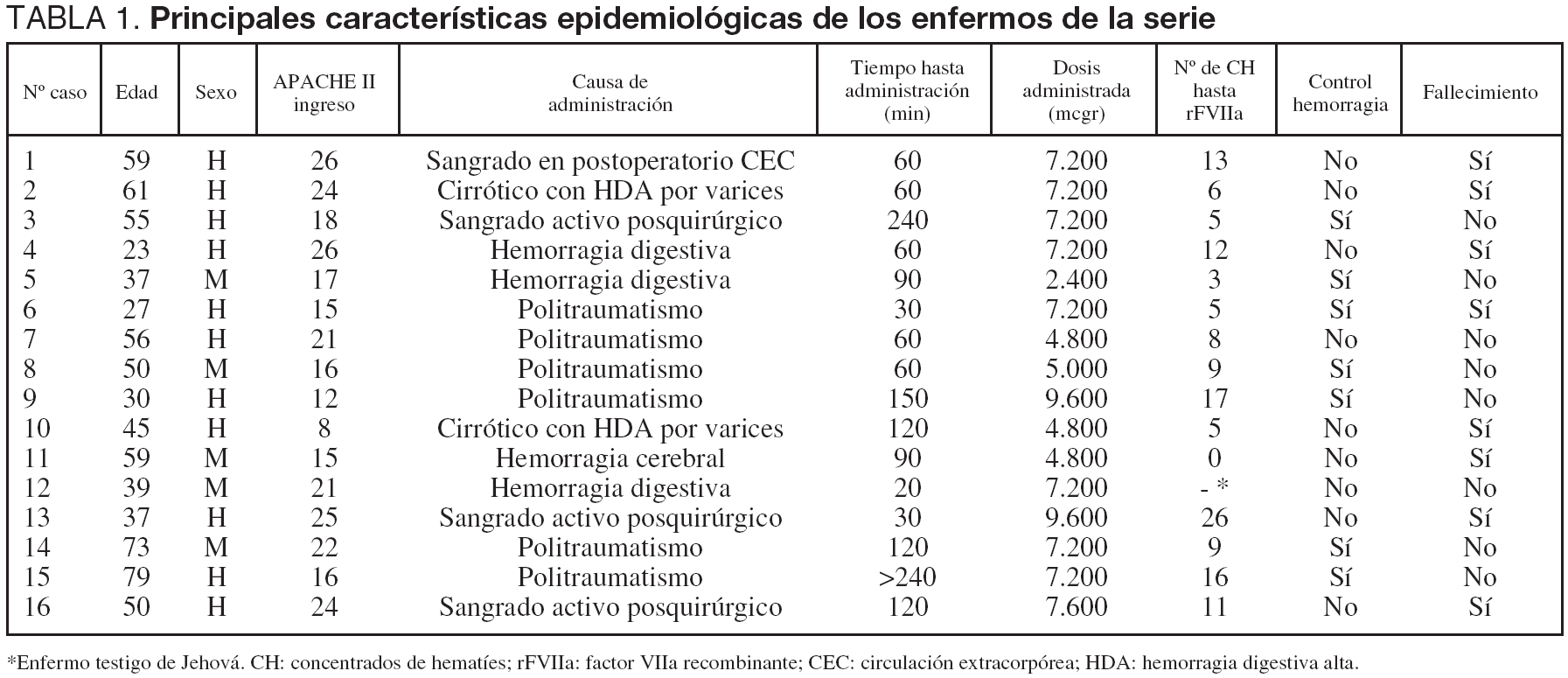
Se incluyeron un total de 16 enfermos, con una edad media de 48,75 años (DE ± 15,98). Las características clínico-epidemiológicas se describen en la tabla 1.
El número de hombres afectados fue el doble que el de mujeres, y la gravedad de los enfermos reflejada por las escalas utilizadas mostraron una mortalidad esperada por APACHE II aproximadamente del 32% para una puntuación media de 19 puntos.
La situación clínica de los enfermos antes y después de la administración del rFVIIa se resume en la tabla 2.
La situación clínica preadministración de rFVIIa se caracterizó por una situación de shock en prácticamente todos los casos, definido éste por un marco de hipotensión arterial moderada (PAS media menor de 90), apoyo inotrópico previo en el 62,5% de los casos y politransfusión. Los parámetros hemostáticos de nuestros pacientes definían una situación de trombopenia moderada, con razón normalizada internacional (INR) media de 1,61 y baja actividad de protrombina. Dentro de los requerimientos transfusionales destaca que en la mayoría de los enfermos se superaron los 10 concentrados de hematíes transfundidos.
Desde el momento de la indicación hasta la administración del fármaco transcurrieron 87,33 ± 56,87 minutos de media. La dosis administrada fue de 100 mcg/kg de peso.
En 4 (25%) enfermos fue necesaria la administración de una segunda dosis de rFVIIa. El tiempo de demora fue de 75 minutos de media.
Se controló la hemorragia en el 43,75% de nuestros casos. La mortalidad global de nuestra serie fue del 50%. La cohorte de enfermos presentó una estancia media en UCI de 12,18 días (DE ± 19,05) y 21,85 días de estancia media hospitalaria (DE ± 29,32).
Los datos demuestran que tras la administración de rFVIIa se produjo mejoría en los parámetros hemodinámicos medidos, así como una disminución de los requerimientos transfusionales. Por otro lado no fue posible la reducción de la necesidad de ventilación mecánica ni de fármacos inotrópicos en las primeras 24 horas postinfusión.
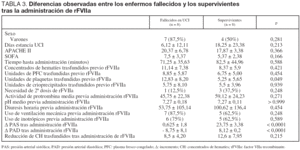
Finalmente se analizó la evolución clínico-analítica de los pacientes tras la administración de rFVIIa y su asociación a la mortalidad, como se muestra en la tabla 3.
Se encontró una mayor supervivencia en aquellos enfermos que presentaban scores de gravedad más bajos al ingreso. Del mismo modo se vio una tendencia a disminuir la mortalidad en aquellos enfermos en los que los requerimientos transfusionales preadministración de rFVIIa eran menores.
Esta tendencia llegó a la significación estadística al hablar de unidades de plaquetas transfundidas. No se observaron diferencias apreciables en la retirada de ventilación mecánica y/o inotrópicos en los dos grupos.
Finalmente, encontramos estadísticamente muy significativa la asociación entre el incremento de la PAS y PAD y la supervivencia de nuestros enfermos tras la administración de rFVIIa.
DISCUSIÓN
Presentamos una serie de enfermos críticos que necesitaron en algún momento de su ingreso en UCI rFVIIa para el control de una hemorragia grave.
En primer lugar se trata de una cohorte de enfermos heterogénea en cuanto a la causa responsable de la administración de rFVIIa. La mortalidad global de nuestra serie se sitúa en el 50%. Sin embargo, los enfermos traumáticos presentan una mortalidad del 16% (1 de 6), frente al 75% en los enfermos posquirúrgicos no traumáticos (3 de 4) o el 60% (3 de 5) en las hemorragias digestivas. Cuando comparamos nuestra mortalidad con la reportada en la literatura, observamos que en la serie de Martinowitz et al13 de 19 enfermos traumáticos se presentaba una mortalidad del 31%, frente al 40% en la serie de 5 pacientes de Dutton et al14. En cuanto a los enfermos posquirúrgicos no traumáticos la mayor serie de O´Connell et al15, de 40 enfermos, muestra una mortalidad del 57%, reducida al 23% en la serie de Eikelboom et al16, de 21 casos.
El porcentaje de enfermos en los cuales se consiguió la resolución de la hemorragia, se sitúa de manera global en el 43% en nuestra serie. Este dato se encuentra en inferioridad a las principales series descritas, donde la peor cifra se sitúa en el 45% de resoluciones completas en la serie de O´Connell et al15 (40 enfermos quirúrgicos no traumáticos), y llega hasta el 86% en el estudio de Eikelboom et al16 (21 enfermos quirúrgicos no traumáticos). Del mismo modo Martinowitz et al13 alcanzan el 79% de resoluciones en enfermos traumáticos. Estas diferencias observadas se podrían explicar por dos motivos principales: el primero es el hecho de que no se dispone de un criterio uniforme para considerar la resolución de la hemorragia; en segundo lugar la heterogeneidad de nuestra serie, con la presencia de enfermos cirróticos en ella, consideramos que no invalida, pero sí cuestiona la realidad de esta cifra.
El número de concentrados de hematíes transfundidos previa administración de rFVIIa tuvo un valor medio de 9,06 ± 6,76. Este valor es bastante inferior a los 55 ± 33 del estudio de Dutton et al14, o los 30 ± 18 de la serie de Martinowitz13. Sin embargo, en la mayor serie (40 enfermos) publicada hasta el año 2003 de O´Connell15 en enfermos quirúrgicos no traumáticos, la administración de rFVIIa se realizó cuando se habían transfundido 10 concentrados de hematíes de media. En estudios más recientes, como el de Kenet, randomizado, doble ciego, comparando placebo frente a rFVIIa en enfermos traumáticos, se consideraba la administración del fármaco en los enfermos que llegaban a requerir 8 concentrados de hematíes. Este estudio presentó una mortalidad a 30 días del 25% en los traumas directos tratados con rFVIIa, y del 24% en los traumatismos penetrantes6. Estos datos muestran la disparidad de criterios a la hora de elegir el momento óptimo para la administración de este fármaco. Apoyándose en la mayor eficacia del fármaco en el control de las hemorragias a lo largo de estos últimos años, se ha optado por una administración más precoz13-17.
La dosis de administración del rFVIIa ha sido otro de los grandes debates en el momento de usar este fármaco en enfermos «sin problemas hematológicos». La dosis administrada de 100 mcg/kg de peso en nuestra serie concuerda con la dosis media administrada en el estudio de Eikelboom et al16. Éste ha sido el estudio de más de 10 enfermos que mayor porcentaje de éxito obtuvo en la resolución de la hemorragia y menor mortalidad presentó, con un 86% y 23% respectivamente16. Por otro lado, más recientemente, la dosis propuesta de 200 mcg/kg de carga seguida de 100 mcg/kg a la hora y a las tres horas, en el estudio de Kenet6, redujo de manera significativa la necesidad de una transfusión masiva (más de 12 concentrados de hematíes después de la primera dosis de rFVIIa) en los enfermos con traumatismo directo que recibieron el factor frente al placebo, aunque no logró disminuir de manera significativa la mortalidad.
Finalmente, la dosis administrada en el caso de control volumétrico de las hemorragias cerebrales osciló entre 40 y 160 mcg/kg. La dosis de 160 mcg/kg obtuvo la mayor significación estadística cuando se valoró el control volumétrico de la hemorragia frente al placebo. Sin embargo, fue la dosis de 40 mcg/kg la que obtuvo mayor significación estadística cuando el parámetro valorado era la mortalidad18.
Por último, no encontramos diferencias significativas entre las variables asociadas a la administración del fármaco (tiempo desde la indicación hasta la administración y necesidad de segunda dosis de fármaco) entre los grupos de supervivientes y fallecidos. Tampoco se encontraron diferencias al comparar en estos dos grupos las variables relacionadas con la transfusión de hemoderivados previa a la administración del factor (concentrados de hematíes, plaquetas, plasma fresco congelado y crioprecipitados). El uso de ventilación mecánica o el de inotrópicos, como marcadores de morbilidad previo uso de rFVIIa, tampoco diferenciaron los grupos de vivos frente a los de exitus.
Por último, la mejora hemodinámica tras la administración del fármaco se constituyó en la más significativa diferencia entre los grupos de fallecidos y supervivientes.
La valoración de la reducción de las necesidades de concentrados de hematíes en los grupos de vivos y exitus no evidenció diferencias significativas. Creemos que el hecho de que la mayor parte de los enfermos fallecidos lo hicieran en las primeras horas tras la administración del fármaco pudo enmascarar este resultado, por disminuir obligatoriamente las necesidades de transfusión.
La eficacia del rFVIIa en el control de las hemorragias graves es un dato comprobado en distintos estudios, series de casos y casos clínicos aislados de la literatura médica19-22.
La presente serie de casos, con el inconveniente de su heterogeneidad y escaso número de enfermos, resalta el papel de la mejora hemodinámica como factor diferenciador entre aquellos enfermos que sobreviven y los que no lo hacen.
A pesar de las limitaciones, los resultados aquí presentados pensamos que sí pueden tomarse como punto de partida para estudios de mayor envergadura, a la hora de perseguir aquellos marcadores pronósticos a corto y largo plazo en estos enfermos.
Declaración de conflicto de intereses
Los autores han declarado no tener ningún conflicto de intereses.
Correspondencia: Dr. A. González Castro.
Servicio de Medicina Intensiva.
Hospital Universitario Marqués de Valdecilla.
Avda. Valdecilla, s/n.
39008 Santander.
Correo electrónico: jandro120475@hotmail.com
Manuscrito aceptado el 16-I-2007.