INTRODUCCIÓN
Tanto los antagonistas IIb/IIIa (AGIIb/IIIa), como las tienopiridinas, reducen el riesgo de eventos cardiovasculares adversos en pacientes con síndrome coronario agudo sin elevación de ST (SCASEST) sometidos a revascularización coronaria percutánea1-4. Sin embargo, los escasos estudios disponibles sobre la efectividad y seguridad de su uso combinado ofrecen resultados contradictorios, difíciles de interpretar debido a la heterogeneidad de los pacientes incluidos, la diversidad de fármacos y dosis utilizadas y las diferencias de diseño de los estudios. Por otro lado, la mayoría de los estudios carecen de suficiente poder estadístico para detectar un aumento del riesgo de fenómenos adversos infrecuentes, como las hemorragias mayores o la trombopenia.
Los objetivos de este estudio son:
1. Cuantificar la efectividad y seguridad de los antagonistas IIb/IIIa en pacientes sometidos a revascularización coronaria percutánea pretratados con tienopiridinas.
2. Explorar las posibles fuentes de heterogeneidad entre los estudios, en relación con el tipo de pacientes incluidos, tipo y dosis de AGIIb/IIIa utilizados y calidad metodológica de los mismos.
MÉTODOS
Fuentes de datos
Se hizo una búsqueda electrónica en Medline a través de PubMed (1990-2006), Embase (1988-2006), Pascal (2001-2006), Cochrane Library e ISI Proceedings (1990-2006). Dicha búsqueda se completó mediante la revisión manual de las referencias bibliográficas recuperadas en las fuentes anteriores. No se recurrió a consultar a los autores ni a la búsqueda específica de literatura gris.
Estrategia de búsqueda
La búsqueda electrónica incluyó una combinación de los descriptores de la población estudiada (angioplastia percutánea, isquemia miocárdica), de los fármacos utilizados (tienopiridinas: ticlopidina, clopidogrel, prasugrel; AGIIb/IIIa: tirofiban, epitifibátido, abciximab) y de los desenlaces clínicos evaluados (mortalidad, supervivencia, muerte, infarto, hemorragia, sangrado, trombocitopenia).
Criterios de inclusión/exclusión
Tras un cribado inicial por parte de uno de los investigadores (EMB) para descartar estudios irrelevantes, revisiones y publicaciones duplicadas, se identificaron los ensayos clínicos aleatorizados. Los estudios que pasaron el cribado inicial fueron examinados cuidadosamente por dos investigadores (AAL y FCO), que seleccionaron los que cumplían los siguientes criterios de inclusión:
1. Ensayos clínicos aleatorizados que evaluaban el efecto del tratamiento con AGIIb/IIIa en pacientes pretratados con tienopiridinas.
2. Datos suficientes para estimar el riesgo de muerte/infarto, y/o hemorragia/trombopenia a medio plazo.
3. Mínimo de 20 pacientes incluidos en el ensayo.
4. Idioma inglés, francés, español, portugués, italiano o alemán.
5. Publicaciones anteriores a febrero de 2006.
Extracción de los datos
De los estudios incluidos se extrajeron por duplicado datos de identificación, diseño y calidad del estudio y tablas de contingencia 2 x 2 para cada uno de los desenlaces analizables. En caso de discordancia entre los dos observadores, la codificación se realizó por consenso.
Análisis estadístico
Para cada estudio y desenlace clínico se estimó el riesgo relativo (RR) con su intervalo de confianza al 95%. La heterogeneidad entre los estudios se exploró mediante el análisis gráfico de los RR (diagrama de bosque, forest plot) y el estadístico Q. Dado el escaso número de estudios disponibles se calculó adicionalmente el I2, que valora la heterogeneidad independientemente del tamaño muestral5. El RR ponderado se estimó (cuando el grado de heterogeneidad lo permitía) mediante un modelo de efectos aleatorios6. La posibilidad de sesgo de publicación se evaluó gráficamente mediante la construcción del gráfico de embudo (funnel plot) y estadísticamente mediante el test de Egger7. Los análisis estadísticos se realizaron mediante el software StatsDirect® versión 2.5.5 y RefMan versión 4.2.
RESULTADOS
Estudios recuperados
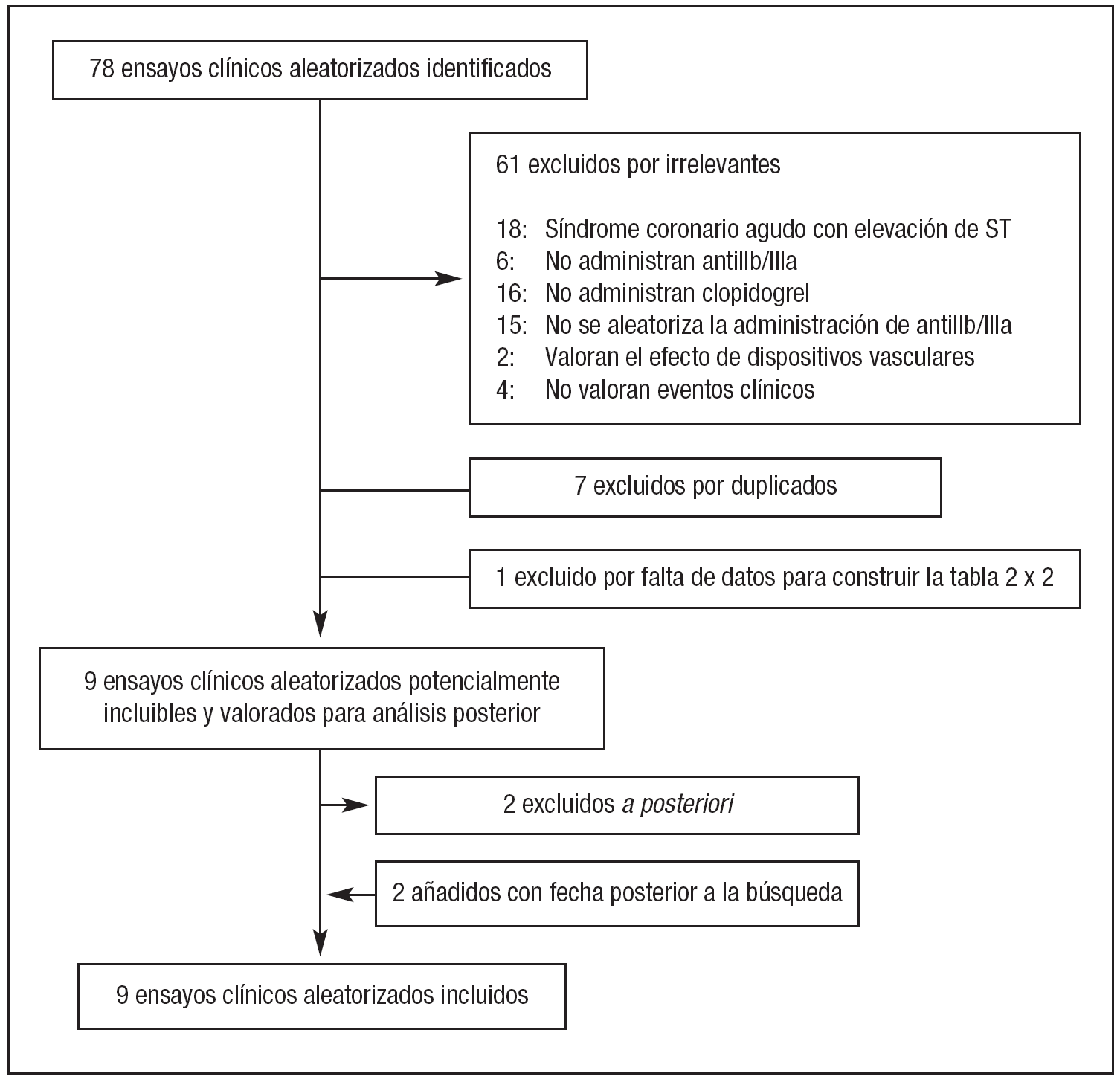
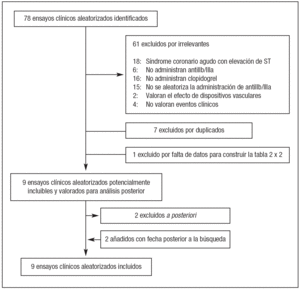
En una primera búsqueda se identificaron 837 documentos, de los cuales 78 eran ensayos aleatorizados. Tras la exclusión de los estudios irrelevantes y los duplicados se identificaron 9 ensayos potencialmente incluibles8-16. Dos de ellos se excluyeron posteriormente; en un caso14 porque no se observaron eventos cardíacos mayores durante el período de seguimiento, y en el segundo estudio (CLOTILDA)12 porque 31 de los 99 pacientes del grupo control habían recibido el tratamiento experimental. Con posterioridad a la fecha límite de la búsqueda se publicaron dos estudios relevantes17,18, detectados al margen de la estrategia anterior y que se decidió incluir en la revisión sistemática. Así pues, finalmente se incluyeron 9 ensayos aleatorizados8-11,13,15-18 que analizaban 8.604 pacientes. El diagrama de flujo de los artículos recuperados y excluidos y los motivos de esta decisión se presentan en la figura 1. La lista completa de artículos excluidos se puede solicitar a los autores.
Figura 1. Diagrama de flujo de artículos recuperados, incluidos y excluidos.
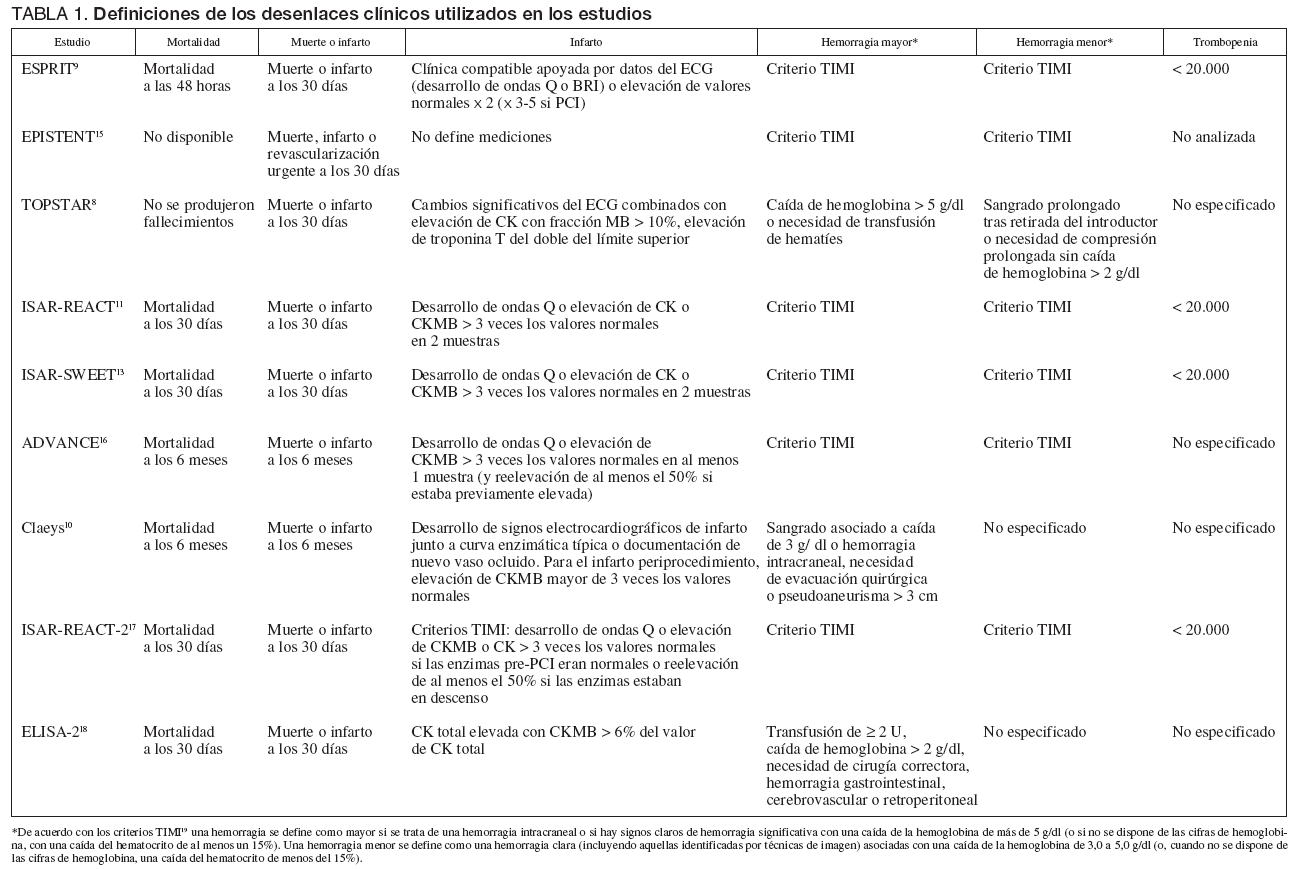
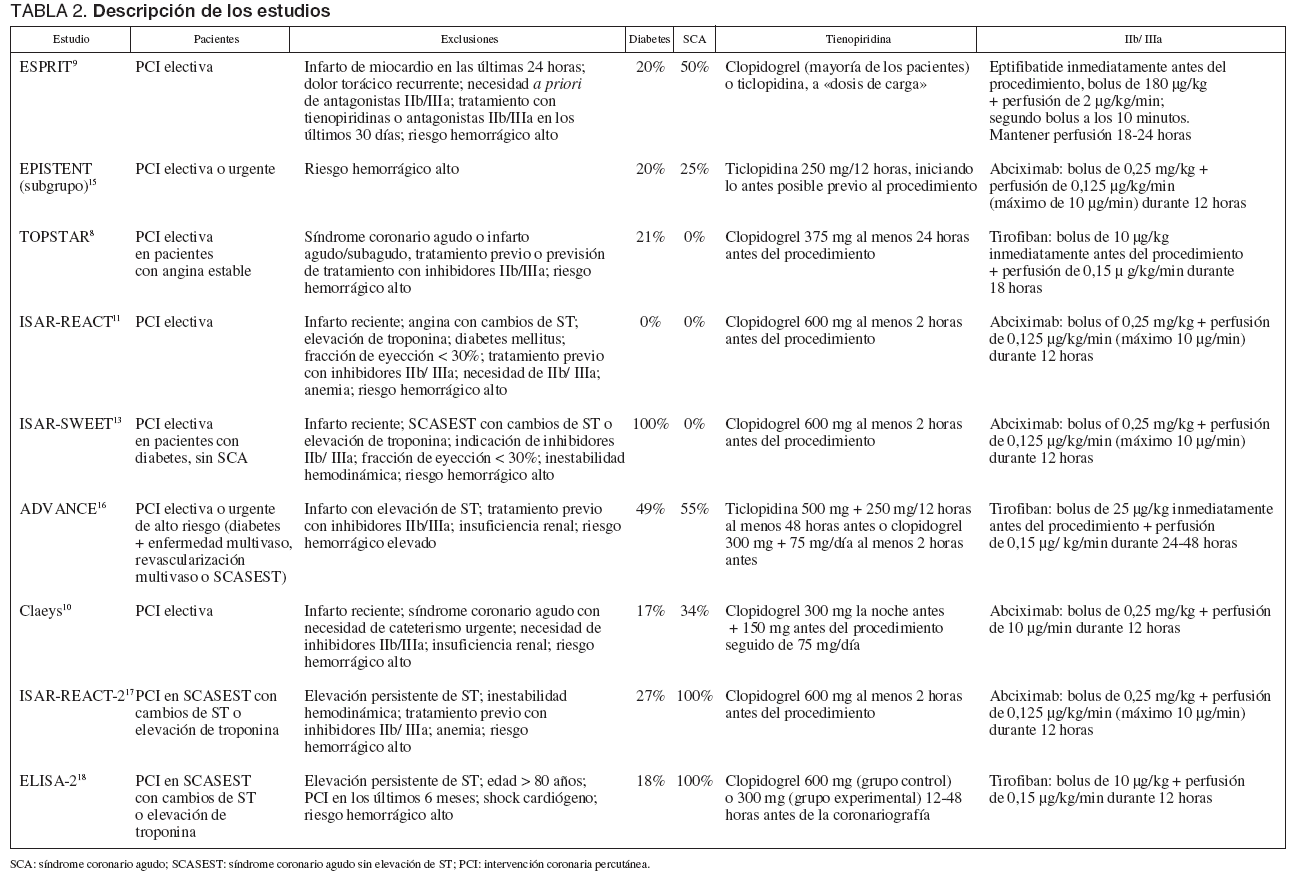
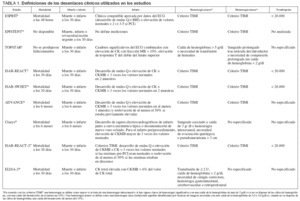
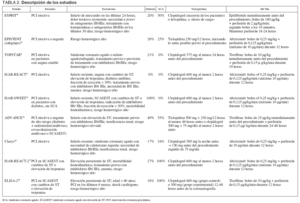
Las definiciones operativas de los desenlaces clínicos analizados difirieron ligeramente entre los estudios (tabla 1). Asimismo, éstos mostraron una gran heterogeneidad respecto al tipo de pacientes incluidos y los fármacos y dosis utilizados (tabla 2). Todos los estudios excluían pacientes con riesgo hemorrágico elevado. En conjunto, los ensayos disponibles tenían alta calidad metodológica (tabla 3). Cabe destacar que, excepto tres ensayos8,10,18, el resto cumplía tres o más de los 4 criterios de calidad examinados.
Riesgo de muerte o infarto a los 30 días
En tres estudios10,15,16 no pudo obtenerse directamente la incidencia de muerte o infarto a los 30 días, y se utilizó como proxy el riesgo de muerte o infarto a los 6 meses10,15 o el riesgo de muerte, infarto o revascularización a los 30 días16. Un cuarto estudio18 comunicó una incidencia de infarto de miocardio de alrededor del 50% debido a una definición permisiva de infarto, por lo que fue considerado como un outlier y se excluyó del análisis.
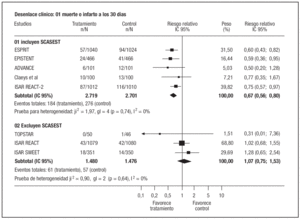
Con los datos analizados, la adición de un AGIIb/ IIIa conllevaba una reducción del riesgo de muerte o infarto a los 30 días de un 26% (RR: 0,74; IC 95%: 0,61-0,89; p = 0,0016). Este resultado fue consistente para la exclusión de los tres estudios sin datos sobre muerte o infarto10,15,16 o de los tres estudios de menor calidad metodológica8,10,18.
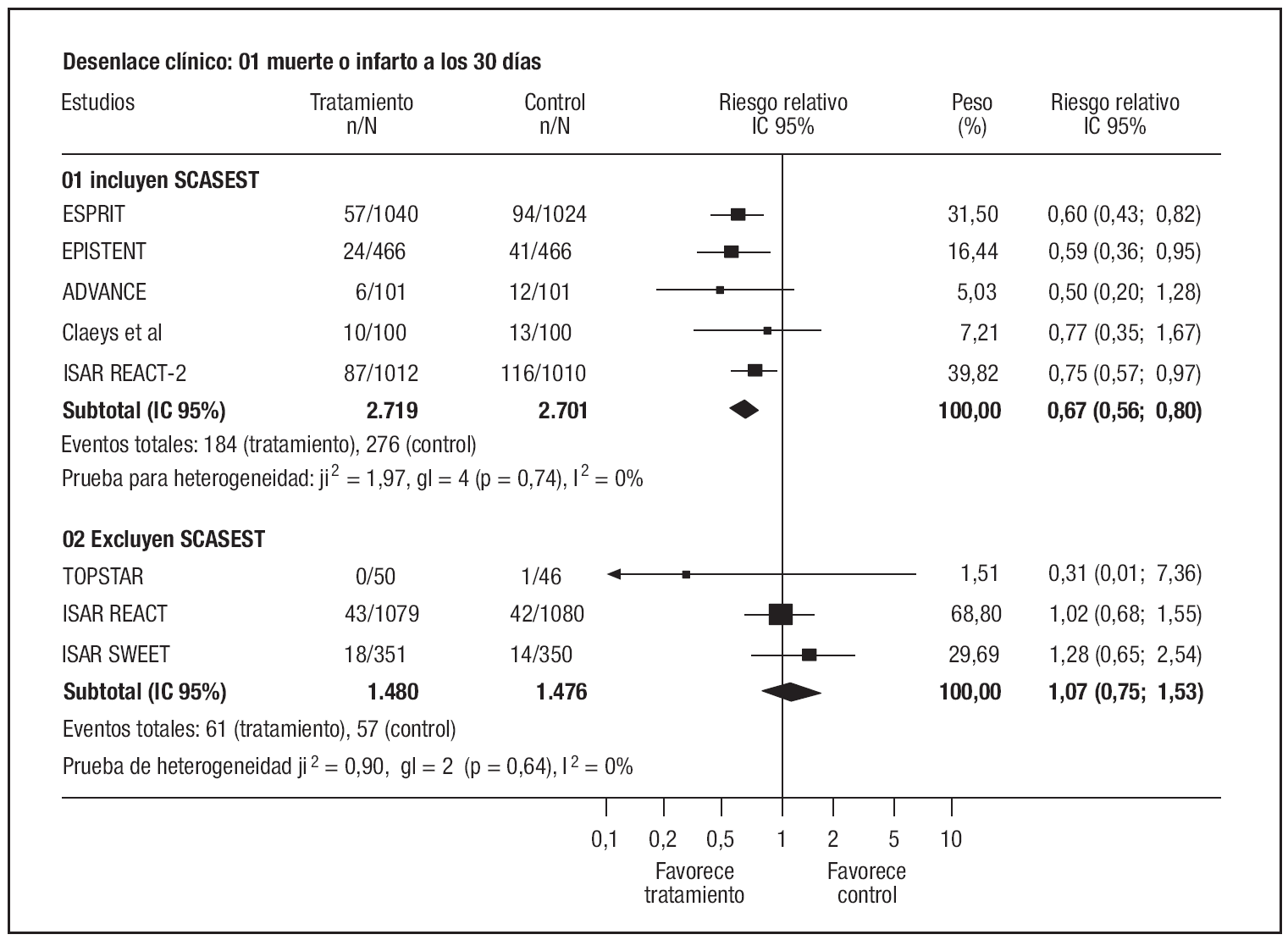
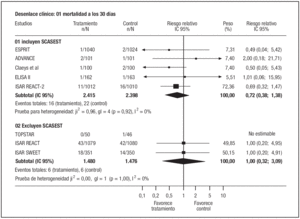
Al estratificar los estudios según el tipo de pacientes incluidos (fig. 2) se observó que los antagonistas IIb/IIIa eran efectivos en los ensayos que incluían pacientes con SCASEST (RR: 0,67; IC95%: 0,56-0,80), pero no en aquellos que excluían estos pacientes (RR: 1,07; IC95%: 0,75-1,53), con test de interacción significativo (p = 0,0175). A pesar de la heterogeneidad entre ambos estratos, los resultados en cada grupo fueron estadísticamente homogéneos (I2 del 0%). Dentro del estrato de estudios realizados en SCASEST, estos resultados fueron robustos para la exclusión del ensayo ISAR REACT 217 o la inclusión del estudio CLOTILDA12.
Figura 2. Riesgo de muerte o infarto a los 30 días.SCASEST: síndrome coronario agudo sin elevación de ST.
No se detectó interacción significativa respecto al tipo de AGIIb/IIIa empleado, ni indicios de sesgo de publicación (p test de Egger = 0,9771).
Mortalidad
No pudieron obtenerse datos de mortalidad en uno de los ensayos15. Otros tres adicionales no proporcionaban datos de mortalidad a los 30 días, pero sí de mortalidad a las 48 horas9 o a los 6 meses10,16, por lo que se utilizaron estos resultados como proxys.
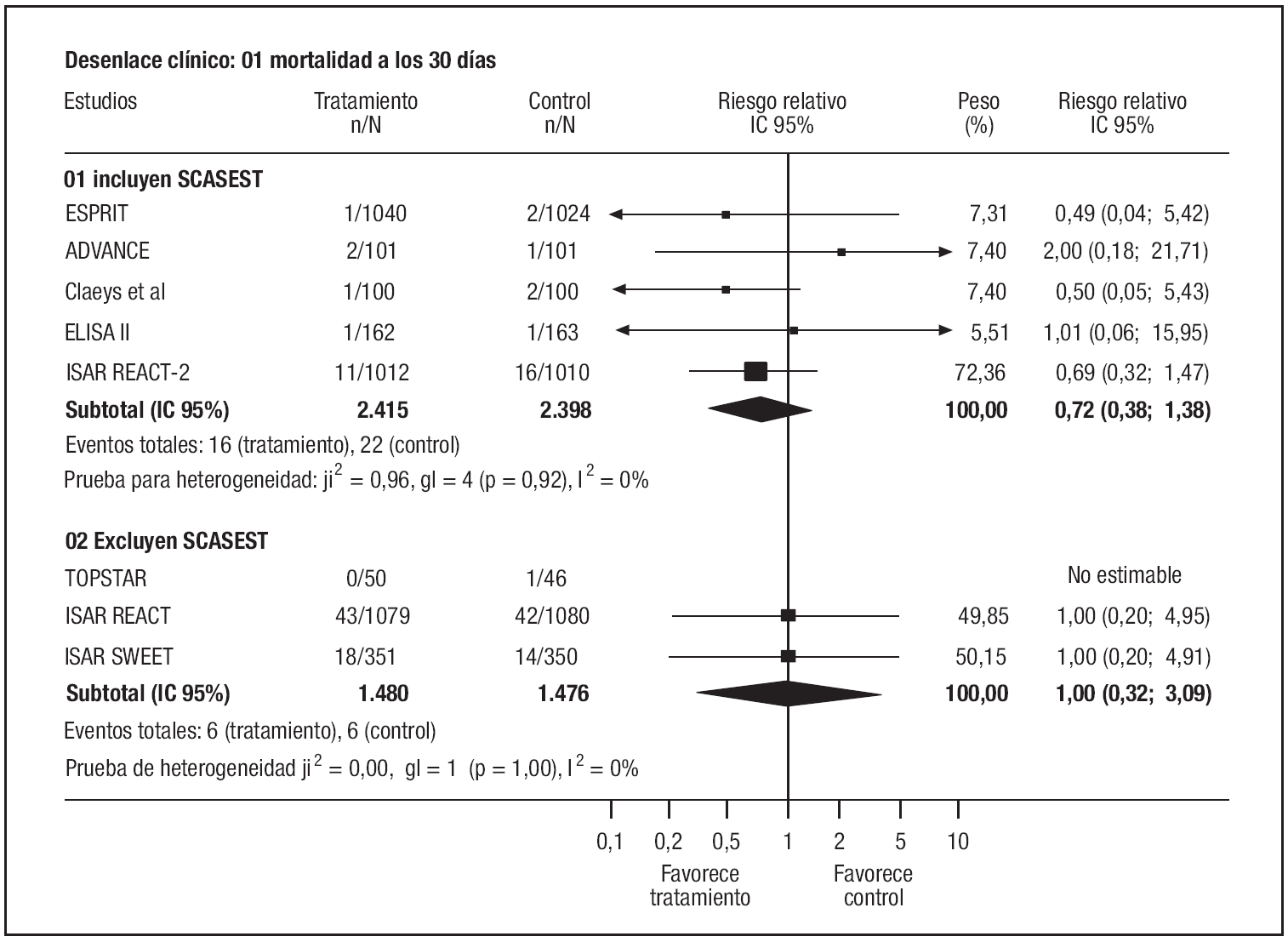
El metaanálisis realizado con los 8 ensayos restantes mostró una tendencia a la reducción de la mortalidad en el grupo experimental (RR: 0,78; IC 95%: 0,45-1,38) sin significación estadística. Esta tendencia favorable en el grupo experimental parecía circunscribirse a los ensayos que incluían pacientes con SCASEST (fig. 3), aunque la interacción no fue estadísticamente significativa. Tampoco hubo interacción estadística en relación con el tipo de AGIIb/IIIa utilizado. Estos resultados no cambiaron sensiblemente al excluir los ensayos con menos de tres criterios de calidad metodológica10,18. No hubo indicios de sesgo de publicación.
Figura 3. Mortalidad a los 30 días.SCASEST: síndrome coronario agudo sin elevación de ST.
Infarto de miocardio
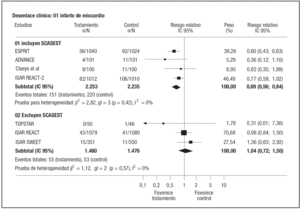
El metaanálisis realizado en los 7 estudios que disponían de la información adecuada demostró una reducción del 24% del riesgo de infarto a los 30 días en aquellos tratados con AGIIb/IIIa (RR: 0,76; IC 95%: 0,61-0,95; p = 0,0175). Los resultados fueron consistentes con la exclusión de los estudios de menor calidad metodológica. No hubo indicios de sesgo de publicación.
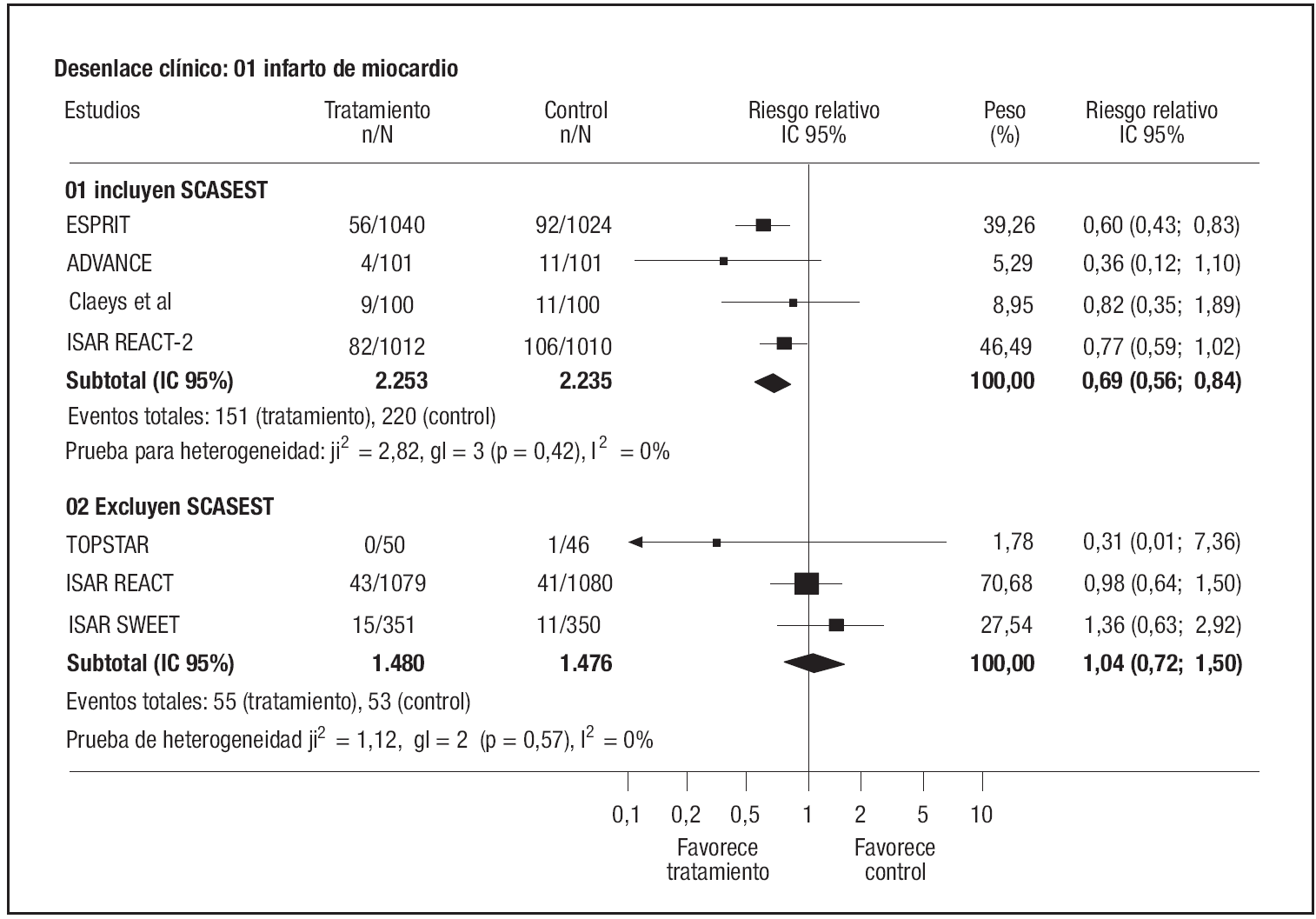
Los estudios que incluían pacientes con SCASEST mostraron una clara reducción del riesgo de infarto, que no se observó en los que los excluían (fig. 4), con una p limítrofe (p = 0,0551) en el test de interacción. Asimismo, el efecto se circunscribió a los ensayos que no utilizaban abciximab (p test de interacción: 0,0508).
Figura 4. Riesgo de infarto de miocardio.SCASEST: síndrome coronario agudo sin elevación de ST.
Hemorragias
Todos los estudios excepto tres8,10,18 utilizaron las definiciones de hemorragia mayor y menor del estudio TIMI19. En uno de los estudios incluidos16 no se produjeron hemorragias mayores.
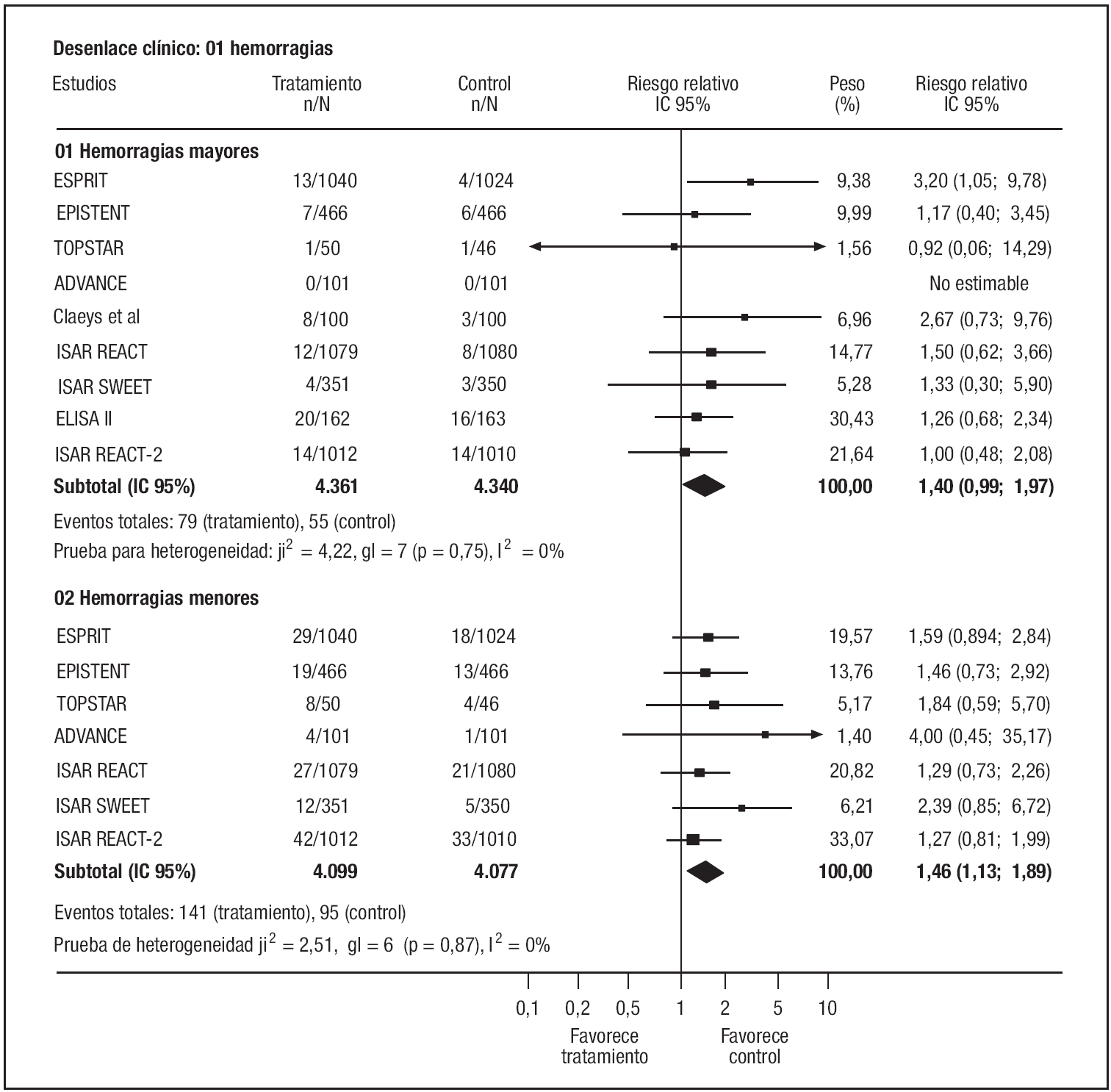
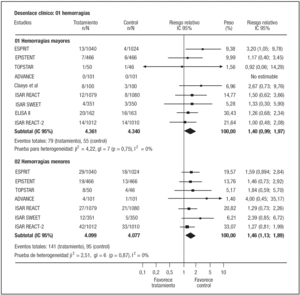
Los resultados respecto al riesgo de hemorragias mayores fueron altamente homogéneos (p test de heterogeneidad: 0,7536; I2 0%). Globalmente, la adición de AGIIb/IIIa se asoció con una fuerte tendencia (no significativa) al aumento del riesgo de hemorragias mayores (fig. 5). Este exceso de riesgo fue estadísticamente significativo cuando la ponderación se hizo con un modelo de efectos fijos (RR: 1,43; IC95%: 1,02-2,01).
Figura 5. Riesgo de hemorragias.
El riesgo de hemorragias menores asociado al uso adicional de antagonistas IIb/IIIa se pudo analizar en 7 estudios con resultados asimismo homogéneos y de magnitud similar a las hemorragias mayores, aunque aquí el exceso de riesgo sí alcanzó significación estadística (fig. 5).
Trombopenia
La asociación entre el uso de antagonistas IIb/ IIIa y la aparición de trombopenia grave pudo analizarse en 6 ensayos, aunque sólo 4 estudios9,11,13,17 la definían de forma operativa.
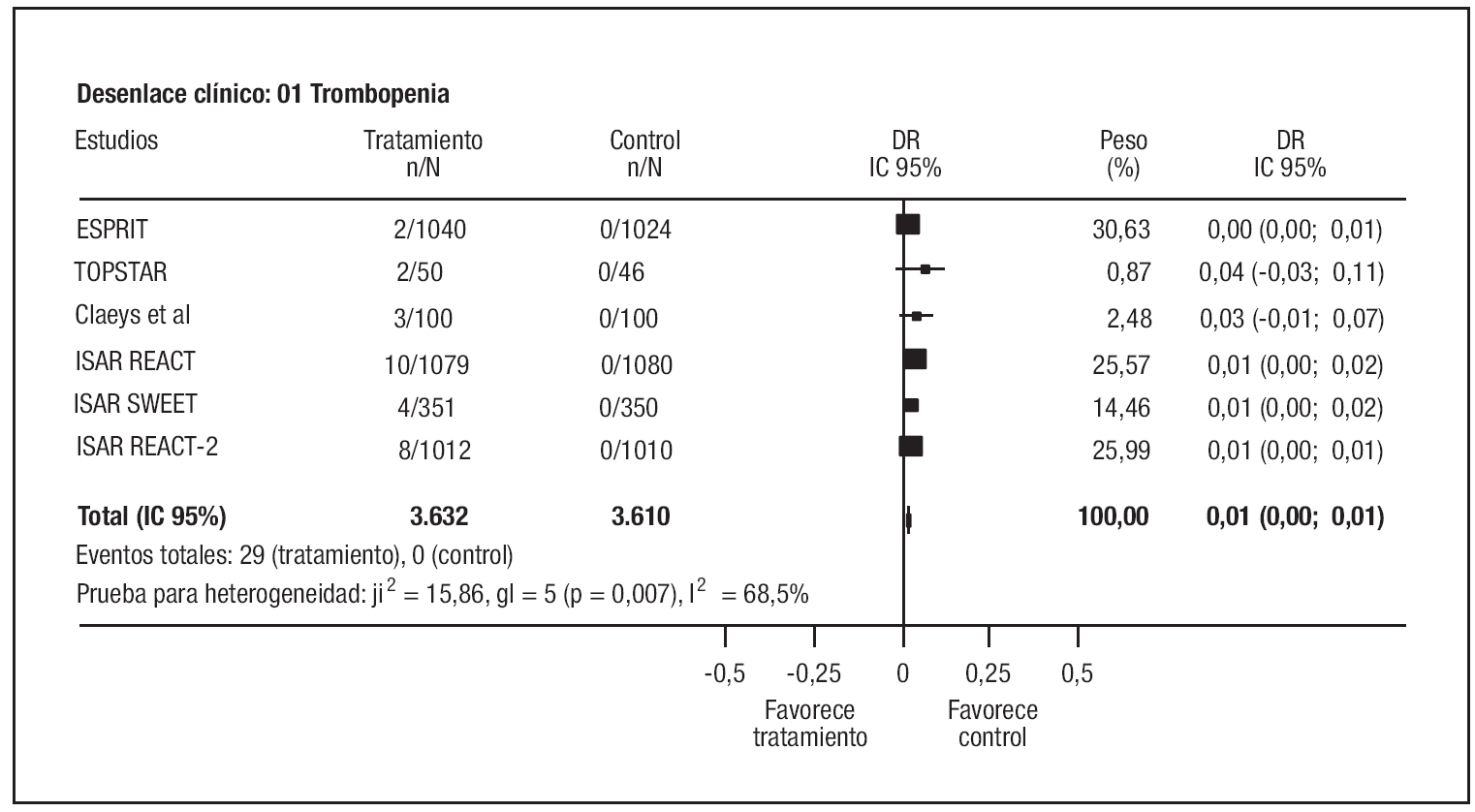
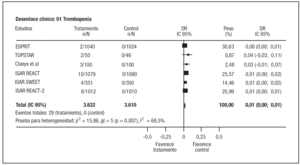
Se produjo trombopenia grave en 29 casos, todos ellos pertenecientes al grupo experimental (1% de los pacientes tratados con antagonistas IIb/IIIa). La magnitud del exceso de riesgo fue muy heterogénea, oscilando entre un 2 por 1.0009 y un 4%8 (p test de heterogeneidad: 0,0073; I2 68,5%) (fig. 6). Aunque el aumento del riesgo de trombopenia fue mayor en los ensayos con abciximab, no se pudo demostrar una interacción estadística entre el tipo de antagonista IIb/IIIa utilizado y el riesgo de plaquetopenia.
Figura 6. Riesgo de trombopenia grave.
DISCUSIÓN
Las guías clínicas para el manejo de pacientes con SCASEST más difundidas1,3,4,20 recomiendan la administración de un antagonista IIb/IIIa (aguas arriba o inmediatamente antes del procedimiento percutáneo) en pacientes ya tratados con heparina, aspirina y clopidogrel en los que se programa cateterismo e intervencionismo coronario.
Posteriormente se han publicado diversos ensayos aleatorizados en pacientes sometidos a intervencionismo coronario pretratados con clopidogrel con resultados contradictorios. En especial, los estudios ISAR REACT11 y el ISAR SWEET13 cuestionaron la utilidad del abciximab, al menos en pacientes que recibían altas dosis de carga (600 mg) de clopidogrel21. Sin embargo, estos dos estudios excluían pacientes con SCASEST. La controversia ha quedado en gran parte resuelta con la reciente publicación del ensayo ISAR REACT-217, cuyos resultados demuestran la efectividad de la triple terapia antiagregante en pacientes con SCASEST.
Los resultados de esta revisión sistemática y metaanálisis confirman que, en el conjunto de estudios analizados, la administración de AGIIb/IIIa a pacientes con SCASEST previamente tratados con tienopiridinas y sometidos a intervencionismo coronario reduce el riesgo de muerte o infarto a los 30 días. El beneficio de la triple antiagregación se produce proporcionalmente tanto en el riesgo de infarto de miocardio como en la letalidad, aunque sólo alcanzó significación estadística en el primero.
La revisión confirma la interacción entre el uso de AGIIb/IIIa y el tipo de pacientes incluido en el estudio. En efecto, el beneficio de la adición de un inhibidor IIb/IIIa se circunscribe a ensayos que incluyen pacientes con SCASEST, mientras que no se observa beneficio en aquellos que excluyen a estos pacientes.
Respecto a la efectividad comparada de los distintos AGIIb/IIIa utilizados, los resultados no son concluyentes. Aunque hubo una tendencia a una menor reducción de eventos cardiovasculares adversos en los estudios que utilizaban abciximab, la interacción no fue estadísticamente significativa. Por otro lado, los resultados podrían estar distorsionados por efecto confusión debido a la menor prevalencia de pacientes con SCASEST en los estudios que utilizaban abciximab (39% frente al 55%; p < 0,0001) y a las diferentes dosis de antiplaquetarios utilizadas.
Respecto a la seguridad de la triple terapia antiagregante, hasta ahora ningún ensayo individual había demostrado aumento del riesgo hemorrágico en el grupo experimental, probablemente debido a la baja potencia estadística de los ensayos individuales. Sin embargo, al ponderar los resultados de estos estudios mediante un metaanálisis se demuestra un aumento del riesgo de hemorragias menores en el grupo experimental de un 46% (IC95% 13-89%). El aumento del riesgo de hemorragias mayores es similar, si bien no alcanzó significación estadística debido probablemente a su menor incidencia. Por último, la adición de un AGIIb/IIIa se asoció a un aumento absoluto de trombopenias severas de un 1% (p < 0,0001).
La relación riesgo/beneficio de la triple antiagregación es claramente favorable. Así, para un paciente con SCASEST, programado para intervencionismo precoz, con un riesgo basal de muerte o infarto a los 30 días del 8% (similar al promedio de los pacientes del grupo control), la administración de un AGIIb/IIIa se asocia con una reducción absoluta del riesgo de aproximadamente un 2,7% (reducción relativa del riesgo del 33%), lo que supone que tratando a 37 pacientes se evita un caso de muerte o infarto. Asumiendo, en una estimación conservadora, que este paciente tiene un riesgo de hemorragia grave del 2% (el doble del promedio de pacientes del grupo control), el tratamiento con AGIIb/IIIa conlleva un aumento absoluto del riesgo del 0,8%, lo que supone que de cada 125 pacientes tratados con un antagonista IIb/IIIa se produce una hemorragia mayor adicional. Y respecto a las hemorragias menores, asumiendo un riesgo basal del 6% (el doble del promedio de pacientes del grupo control), el aumento absoluto del riesgo sería del 2,7%, lo que supone que de cada 37 pacientes tratados con inhibidores IIb/IIIa se produce una hemorragia menor adicional. En otras palabras, si tratamos a 1.000 pacientes con inhibidores IIb/IIIa (además de aspirina y clopidogrel) provocaremos 8 hemorragias mayores y 37 hemorragias menores adicionales, pero evitaremos 27 casos de muerte o infarto.
Esta revisión presenta algunas limitaciones. En primer lugar, la validez de la revisión está condicionada por la calidad de los estudios analizados (tabla 3). Sin embargo, la calidad global de los estudios fue aceptable, y el análisis de sensibilidad demostró que las conclusiones eran consistentes para la exclusión de estos estudios de menor calidad.
En segundo lugar, no se realizó una búsqueda específica de literatura gris; sin embargo, algunas de las bases de datos utilizadas (Pascal e ISI Proceedings) incluyen conferencias y comunicaciones a congresos que no se publican en las revistas científicas habituales y, por otra parte, el análisis de los datos no reveló asimetría en el gráfico de embudo que sugiriera la existencia de sesgo de publicación.
En tercer lugar, los estudios incluidos presentan una gran heterogeneidad clínica (tipo de pacientes incluidos, dosis y definición de desenlaces clínicos) que podrían comprometer la realización de un metaanálisis. En este punto hay que hacer algunas precisiones. Ante todo, el examen de la heterogeneidad era precisamente uno de los objetivos de la revisión, y ha permitido identificar subgrupos de pacientes que se benefician en distinto grado de la triple antiagregación. Por otro lado, aunque la heterogeneidad clínica era importante, dentro de cada subgrupo y desenlace analizado los resultados fueron llamativamente homogéneos, sin indicios de heterogeneidad estadística (I2 próximos a cero). Por último, los exhaustivos análisis de sensibilidad realizados descartan que los resultados del metaanálisis estén condicionados por la inclusión de outliers.
En resumen, a partir de esta revisión se obtienen las siguientes conclusiones:
1. La adición de antagonistas IIb/IIIa como tercer antiplaquetario en pacientes con SCASEST sometidos a intervencionismo coronario tratados con tienopiridinas y aspirina reduce el riesgo de eventos cardiovasculares adversos.
2. El uso de antagonistas IIb/IIIa no parece efectivo en pacientes con cardiopatía coronaria estable sometidos a angioplastia electiva.
3. Aunque aumenta el riesgo de trombopenia y complicaciones hemorrágicas, la relación riesgo/beneficio apoya el uso de la triple antiagregación en pacientes con SCASEST sometidos a intervencionismo coronario.
Declaración de conflicto de intereses
Los autores han declarado no tener ningún conflicto de intereses.
Correspondencia: Dr. J. Latour Pérez.
Servicio de Medicina Intensiva.
Hospital General Universitario de Elche.
C/ Camí Vell de l'Almàssera, 11.
03203 Elche. Alicante
Correo electrónico: jlatour@coma.es
Manuscrito aceptado el 4-XII-2006.