INTRODUCCION
Los problemastrombóticos son muy importantes en los pacientescríticamente enfermos, tanto por ser motivo de ingreso, comopor las complicaciones que se producen dentro del devenir de unproceso crítico.
Utilizamos eltérmino trombosis para designar tanto un proceso de lahemostasia desarrollado en un lugar del organismo en el que esinnecesario, como a la hemostasia inapropiada odescontrolada1. Mientras que en la trombosis arteriallas estructuras vasculares y las modificaciones de la hemostasiaplaquetaria desempeñan un papel importante, en la trombosisvenosa serían la estasis circulatoria y las alteraciones delmecanismo de coagulación las responsables de lahipercoagulabilidad. Hay que tener en cuenta también elpapel que tienen las alteraciones del mecanismofibrinolítico en la génesis de latrombosis.
El uso de losanticoagulantes en la práctica clínica ha variadoconsiderablemente en los últimos tiempos. En el presenteartículo analizamos la utilización de las heparinas,focalizando la atención en el enfermocrítico.
En los pacientescríticos el uso de heparinas está indicado en eltratamiento de enfermedades tales como: cardiopatíaisquémica (tanto la angina inestable como el infarto agudode miocardio), enfermedad cerebrovascular, enfermedadtromboembólica venosa (trombosis venosa profunda y embolismopulmonar), isquemia de miembros inferiores, y como profilaxis de laenfermedad tromboembólica y de la trombosis de los sistemasde depuración extrarrenal.
Aparte de lasafecciones mencionadas, debemos tener en cuenta el desarrollo deprocesos trombóticos diseminados que constituyen una causaimportante de fallo multiorgánico en los pacientessépticos. En estos enfermos se observa un aumento en eldímero D y del antígeno antiactivador tisular delplasminógeno, mientras que el factor XII y elplasminógeno están disminuidos, indicando unafibrinólisis activada. En una segunda fase evolutiva, lacapacidad del sistema fibrinolítico está muyinhibida. La actividad del activador tisular delplasminógeno puede ser indetectable por agotamiento delendotelio. La función del inhibidor del activador tisulardel plasminógeno está elevada al ser un reactante defase aguda, el tiempo de lisis del coágulo estáalargado y la *2 antiplasminaes normal. La coagulación se activa moderadamente, y lasplaquetas antitrombina III y proteína C estándisminuidas, el tiempo de protrombina alargado y elfibrinógeno normal. La gravedad de la enfermedad secorrelaciona con la extensión de lasalteraciones2.
Eltromboembolismo pulmonar es una de las principales causas de muerteen el medio hospitalario y una causa frecuente de muertedespués del alta. En muchas ocasiones el diagnósticoes difícil y se produce el fallecimiento en las primerashoras, por lo que se deberían adoptar todas las medidasdisponibles para prevenirlo. En la mayoría de los casos elembolismo pulmonar está precedido de una trombosis venosaprofunda y los principales factores de riesgo son la inmovilidad,la cirugía, especialmente si afecta a miembros inferiores,los antecedentes de enfermedad tromboembólica venosa, lastrombofilias y el cáncer. Al realizar profilaxis de latrombosis venosa profunda evitaremos el embolismo pulmonarasí como el síndrome posflebítico.
La heparina nofraccionada (HNF) y sus derivados, las heparinas de bajo pesomolecular (HBPM), son los anticoagulantes de elección cuandoes necesario un efecto anticoagulante rápido. Debido a suslimitaciones farmacocinéticas y a una dosis-respuestamás impredecible, el uso de la HNF se ha limitado alámbito hospitalario. Por el contrario, el uso de las HBPM esmás versátil, ya que se pueden utilizar tanto en elámbito intra como extrahospitalario, debido a suadministración subcutánea y a que no precisanmonitorización. Cuando se indica una anticoagulaciónprolongada el uso de HNF o HBPM se sigue del uso de anticoagulantesorales, aunque pueden establecerse tratamientos a largo plazo enrangos anticoagulantes con HBPM.
La HNFestá indicada en la prevención de la enfermedadtromboembólica venosa, en el tratamiento de la trombosisvenosa profunda y el tromboembolismo pulmonar, en el tratamientoprecoz de la angina inestable y del infarto agudo de miocardio, enla cirugía cardíaca con circulaciónextracorpórea, durante y después de la angioplastiacoronaria, en enfermos con stents coronarios y en pacientesselecionados con coagulación intravasculardiseminada.
Las HBPMestán indicadas en la profilaxis de la enfermedadtromboembólica venosa, en el tratamiento de la trombosisvenosa profunda y en el tromboembolismo pulmonar agudo.También están indicadas en el tratamiento precoz deenfermos con angina inestable3.
HEPARINAS NO FRACCIONADASFRENTE A HEPARINAS DE BAJO PESO MOLECULAR
La heparina esun glucosaminoglicano constituido por la unión de cadenasalternantes de D-glucosamina y ácido urónico,glucurónico o idurónico. La heparina no fraccionadaes una mezcla heterogénea de cadenas de sacáridos dediferente longitud, con un peso molecular que oscila entre 3.000 y30.000 D, que se obtiene a partir de la mucosa intestinal del cerdoo del pulmón de la vaca. El origen biológico tiene suimportancia pues la incidencia de trombocitopenia inducida porheparina, rara y compleja entidad inmunológica, es superiorcon las heparinas de origen bovino (2,9%) que con las de origenporcino (1,1%)4. En cuanto a sus característicasfarmacocinéticas, debemos destacar que no se absorbe porvía oral, se metaboliza en el hígado y sueliminación es renal.
El mecanismo deacción de la HNF consiste en la unión a laantitrombina III (AT-III), la cual presenta gran afinidad por latrombina (factor II) y el factor Xa4. La zona de laheparina con capacidad de unión a la AT-III es unpentasacárido ("pentasacárido crítico"), quese encuentra distribuido aleatoriamente a lo largo de todas lascadenas. Cualquier cadena que contenga este pentasacáridopuede unirse a la AT-III, causando un cambio conformacional en ellugar activo de fijación de la AT-III con el factor Xa, queacelera su interacción con este último produciendofinalmente su inactivación. En cuanto a la acción dela heparina sobre el factor II, es necesaria la formación deun complejo ternario heparina-AT-III-factor II para dar lugar a lainactivación de éste, y este complejo sólo sepuede formar con cadenas de al menos 18 sacáridos delongitud (peso molecular [PM] > 5.400 D)4. Aunque laHNF inhibe la acción de la trombina y del factor Xa, suefecto se produce fundamentalmente a expensas de lainhibición del factor Xa, debido a que la trombina unida ala fibrina requiere mayor dosis de heparina para conseguir suinhibición5. La importancia relativa de lainhibición del factor Xa y IIa no está del todoclara, pero clásicamente se ha relacionado la actividadantitrombótica con el factor Xa y la actividadanticoagulante (prohemorrágica) con el factor IIa.Además la heparina también puede inhibir a losfactores IXa, XIa y XIIa. Posee un efecto anticoagulante inmediatoy de desaparición rápida.
Cuando sometemosa la heparina a despolimerización química oenzimática obtenemos las HBPM, que son fragmentos de 2.000 a9.000 D. Las HBPM se unen a la antitrombina III, pero debido a queentre un 50-75% de las cadenas que forman estas moléculasposeen una "longitud crítica" menor de 18 sacáridos,son capaces de inhibir el factor Xa, pero no el IIa, lo quepodría implicar menores problemas hemorrágicosasociados4.
Las HBPM seadministran de forma subcutánea, siendo su biodisponibilidaddel 100%, con una vida media plasmática de dos a cuatroveces más prolongada que la HNF, produciéndose sueliminación también a través delriñón, por lo que está incrementada susemivida plasmática en enfermos con fallorenal4.
Aunque todas lasHBPM poseen unas características similares, existendiferencias entre ellas en cuanto a peso molecular, vida media yselectividad por el factor Xa3. En principio,después de todo lo expuesto, parece lógico pensar quela HBPM ideal sería aquella con un peso molecular másbajo y, por ello, con una mejor relación actividadanti-Xa/anti-IIa, de forma que se acentúe el efectoantitrombótico, minimizando el potencial hemorrágico.Otros factores importantes a tener en cuenta serían una vidamedía más prolongada y una menor capacidad deunión a plaquetas. En las tablas 1 y 2 se especifican lascaracterísticas de cada HBPM (actividad, ratioanti-Xa/anti-IIa, peso molecular y vida media).
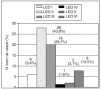
Como ya se hacomentado previamente, es muy importante la longitud de las cadenasde sacáridos en relación con la actividadfarmacológica. Cabe destacar que la bemiparina, consideradacomo una HBPM de segunda generación, se obtiene mediante unmétodo de fraccionamiento novedoso, que consiste en unabetaeliminación en medio no acuoso, consiguiéndoseuna óptima distribución de sus fragmentos, de talforma que el porcentaje de fragmentos de más de 6.000 D esmuy inferior al resto de las HBPM, con una proporciónelevada de cadenas por debajo de la longitud crítica (PM< 5.400 D), que presentan actividad antifactor Xa(antitrombótica) pero no actividad antifactor IIa(anticoagulante). En la figura 1 se ilustra la distribuciónde los fragmentos de diferente longitud de las HBPM.
Fig. 1.Distribución de los diferentes fragmentos de las heparinasde bajo peso molecular (HBPM).
La HNF tienelimitaciones de tipo farmacocinético debido a suunión no específica a proteínas ycélulas. Estas limitaciones se manifiestan como una pobrebiodisponibilidad a dosis bajas, variabilidad en su respuestaanticoagulante y una vida media corta. Algunas proteínas alas que se une la heparina forman los reactantes de fase agudapositivos, elevados en enfermos graves. La variabilidad en losvalores plasmáticos de las proteínas que ligan laheparina en pacientes con enfermedad tromboembólica y enpacientes graves es responsable de la respuesta anticoagulanteimpredecible de la heparina y de sus altos requerimientos enalgunos de estos enfermos (resistencia a la heparina)6.Aparte de las complicaciones hemorrágicas, comunes a todoslos anticoagulantes, la heparina puede producir trombocitopenia yosteoporosis. La eficacia limitada de la heparina en la anginainestable, angioplastia coronaria de alto riesgo ytrombólisis coronaria puede ser explicada por la incapacidadde inactivar la trombina ligada a la fibrina y el factor Xa unidoal complejo protrombinasa.
Comparadas conlas heparinas no fraccionadas, las HBPM poseen una menor capacidadde unión a proteínas no específicas con lacorrespondiente mejora en la predictibilidad dosis-respuesta.También es menor su unión a macrófagos, lo queexplicaría su vida media más prolongada, su menortasa de extracción hepática y su lentaeliminación renal. Además, tienen una capacidadreducida para unirse a células endoteliales, por lo que suabsorción es mayor, resultando en un óptimabiodisponibilidad. Por último, su baja unión aplaquetas se manifiesta como un menor riesgo de aparición defenómenos hemorrágicos y una incidencia baja detrombopenia inducida (TI). Sin embargo, en la actualidadestá contraindicado el uso de HBPM en la TI por HNF, ya queno se ha demostrado que sean eficaces en la sustitución porHNF en estos casos7.
La capacidad deunión a los osteoblastos también es menor que la dela HNF, lo que se puede asociar a una disminución depérdida ósea. Existe un ensayo clínico quesugiere que las HBPM se asocian con baja incidencia deosteoporosis, pero se deben realizar estudios másespecíficos, con un diseño apropiado, parademostrarlo8.
Aunque la HNFconstituye el anticoagulante de elección en pacientesembarazadas porque no atraviesa la barrera placentaria, existendatos que confirman que las HBPM tampoco atraviesan laplacenta9, así como estudios descriptivos quesugieren que éstas son seguras y eficaces en el tratamientode procesos tromboembólicos durante elembarazo10.
Las ventajasglobales de las HBPM respecto a la heparina no fraccionada son, portanto4,5: a) una vida media más larga, porlo que se pueden administrar en una o dos dosis al día;b) mejor biodisponibilidad, administrándose siemprepor vía subcutánea, permitiendo una mayor movilidaddel paciente y el tratamiento domiciliario, y c) menosvariabilidad individual y un efecto anticoagulante máspredecible, por lo que no es necesaria la monitorización deltiempo parcial de tromboplastina activado.
EFICACIA CLÍNICA DELAS HEPARINAS DE BAJO PESO MOLECULAR
Enfermedadtromboembólica
Profilaxis
Las HBPM soneficaces en la profilaxis de la enfermedad tromboembólicavenosa, tanto en pacientes quirúrgicos como médicos,de riesgo alto o moderado11.
En unmetaanálisis que incluía 36 ensayos clínicosdoble ciego y aleatorizados, con 16.583 pacientes de cirugíageneral (incluidas la cirugía ginecológica,urológica y oncológica) y cirugíaortopédica, se comparó la HNF con las HBPM. En lospacientes de cirugía general las dosis bajas de HNF y HBPMson igualmente eficaces en cuanto a la reducción detrombosis venosa profunda, aunque las dosis bajas de HBPM sonmás seguras (en relación con la importancia de lascomplicaciones hemorrágicas) que las HNF. Las dosis elevadasde HBPM en cirugía general no incrementaron la eficacia detratamiento, mientras que reducían su seguridad. En estemismo estudio, al realizar análisis adicionales (26 ensayosclínicos) se observaron diferencias significativas en cuantoal desarrollo de tromboembolismo pulmonar (TEP), siendo menor enlos grupos que recibieron HBPM. En cirugía ortopédicalas HBPM fueron más eficaces que la HNF, pero presentaron unperfil de seguridad similar12.
En algunosestudios recientes se ha observado que es más beneficiosocontinuar la profilaxis con HBPM en el domicilio hasta lamovilización completa del paciente (unos 30-35 díasdespués de la cirugía de cadera) que laadministración sólo en los primeros 10-14días10.
Recientemente sehan realizado dos estudios con bemiparina (no incluida en elanterior metaanálisis). En uno de ellos (se trataba de unestudio multicéntrico, aleatorizado y doble ciego) secomparaba frente a la HNF en la profilaxis de la trombosis venosaprofunda (TVP) y del tromboembolismo pulmonar (TEP) encirugía abdominal electiva. Se evaluó a un total de166 pacientes (84 en el grupo de la bemiparina y 82 en el de HNF)de ambos sexos, mayores de 40 años, candidatos acirugía abdominal electiva con un período deanestesia mayor de 30 min. No hubo ningún caso de TVP ni TEPen ninguno de los grupos. Tampoco hubo diferencias significativasen cuanto al período de inmovilización.Además, no hubo ningún caso de fallecimiento.Sólo hubo 3 casos de hemorragias mayores que precisarontransfusión y que ocurrieron en el grupo de la HNF(diferencia significativa). En cuanto a la aparición dehematomas en la herida quirúrgica y equimosis en el punto deinyección, también fueron significativamente de menorcuantía en el grupo de la bemiparina13. En elsegundo ensayo se comparaba la bemiparina con la HNF en laprofilaxis de la enfermedad tromboembólica venosa enpacientes sometidos a artroplastia total de cadera. En este ensayoclínico multicéntrico, aleatorizado y doble ciego, seincluyó a 300 pacientes y las principales variablesanalizadas fueron la incidencia de eventos tromboembólicos(TVP y TEP), así como las complicacioneshemorrágicas, incluyendo hematomas de la herida operatoria.Se evaluó a 149 pacientes por grupo, observándosemayor número de episodios tromboembólicos en el grupode la HNF, siendo las diferencias significativas. No hubodiferencias en cuanto a complicacioneshemorrágicas14.
Existen dosestudios que demuestran la eficacia de la HBPM en el pacienteneuroquirúgico. En ambos (que eran doble ciego yaleatorizados) se comparó la eficacia de medias decompresión decreciente frente a la combinación demedias y nadroparina15 o enoxaparina16. Enambos casos se identificó de forma significativa unareducción del riesgo de fenómenostromboembólicos posquirúrgicos y una reducciónneta de la incidencia postoperatoria de TVP y de TEP en los grupostratados con HBPM.
Enrelación con la profilaxis de la TVP en pacientes conenfermedad médica aguda, se ha publicado recientemente unensayo clínico multicéntrico y doble ciego, en el quese incluyeron pacientes con riesgo elevado de TVP (insuficienciacardíaca congestiva, insuficiencia respiratoria aguda que norequiriese ventilación mecánica, enfermedadreumática o enfermedad inflamatoria intestinal). Seincluyó a un total de 1.102 pacientes hospitalizados,mayores de 40 años, que recibieron de forma aleatoria 40 mgde enoxaparina, 20 mg de enoxaparina o placebo, por víasubcutánea una vez al día durante 6-14 días.La incidencia de TVP fue significativamente menor en el grupo querecibió enoxaparina 40 mg respecto del grupo placebo, y nose encontraron estas diferencias a la dosis de 20 mg. La incidenciade efectos adversos fue similar en los tres grupos de tratamiento.Los autores concluyen que la enoxaparina, administrada de formasubcutánea a dosis de 40 mg al día, es eficaz en laprofilaxis de TVP en pacientes con enfermedades médicasagudas17.
En el especialcaso del paciente politraumatizado se ha descrito una incidencia deTVP que oscila entre el 6 y el 90% dependiendo de la naturaleza delas lesiones y del método empleado para detectar el trombo.El TEP tiene una incidencia del 2 al 22% y se considera la terceracausa de muerte pasadas las 24 h del traumatismo18. Enun estudio de cohortes prospectivo realizado con pacientespolitraumatizados se ha encontrado una incidencia de trombosisvenosa profunda, documentada mediante flebografía, de un50%19. En un ensayo clínico reciente queincluía a 344 pacientes politraumatizados20, ysin evidencia de sangrado intracraneal, se comparó laadministración de dosis bajas de HNF con HBPM,iniciándose el tratamiento 36 h después del trauma.Comparada con la HNF, la HBPM redujo la tasa de trombosis venosa enun 44 frente a un 31% y la incidencia de trombosis proximal en un15 frente a un 6%. Sin embargo sólo hubo 6 episodios desangrado mayor y cinco de ellos ocurrieron en el grupo de laHBPM.
Tratamiento
En eltratamiento de la enfermedad tromboembólica hay variosmetaanálisis publicados. En el primero de ellos, realizadoen 1995, se incluyeron 13 estudios clínicos en los que seincluía a pacientes con TVP y se comparaba la eficacia delas HBPM respecto de la HNF. Los autores concluyeron que las HBPMeran al menos tan efectivas y seguras como las HNF, siendo menor lareducción de la mortalidad en el subgrupo de pacientes concáncer21. En otro metaanálisis realizadoposteriormente se comparaba de nuevo HBPM con HNF. Las variables deevaluación fueron las mismas que en el estudio anterior. Seincluyeron 20 estudios con un total de 3.333 pacientes. La HBPM seasociaron con reducción significativa en la mortalidad,menor número de episodios hemorrágicos mayores ymenor extensión del trombo. No se observaron diferenciassignificativas en cuanto a la recurrencia de fenómenostromboembólicos22. El más reciente,obtenido de la base de datos Cochrane, incluye 14 ensayosclínicos y a 4.754 pacientes, y se comparan las HBPM con laHNF. Con HBPM se reduce significativamente la mortalidad y elriesgo de hemorragias mayores, aunque la disminución deenfermedad tromboembólica recurrente no alcanza lasignificación estadística23.
Cardiopatíaisquémica
El tratamientode los enfermos con enfermedad coronaria inestable ha cambiadosustancialmente desde que se publicaron los primeros ensayosclínicos. Aparte del tratamiento con bloqueadores beta,nitritos, terapia trombolítica y ácidoacetilsalicílico más heparina, se han realizadoensayos clínicos usando HBPM en angina inestable e infartono Q.
En 1993, serealizó un estudio doble ciego, comparando dalteparina conplacebo en pacientes con enfermedad coronaria estable. Ladalteparina (10.000 U durante 2 semanas y 5.000 U durante otrasdos) se asoció con un aumento de la tolerancia al ejercicio.Además se observaron pequeños descensos en lafracción de eyección ventricular izquierda con elejercicio en el grupo de la dalteparina24.
En el estudioFRISC se demostró que el tratamiento con dalteparina (120U/kg) durante 6 días seguido de 7.500 U en dosisúnica durante otros 35-40 días, combinado con laaspirina, reducía la tasa de mortalidad y de infarto agudode miocardio (IAM) en pacientes que habían sufrido unepisodio de angina inestable. En total se incluyeron 1.506pacientes a los que se les administró dalteparina o placebo.A los 6 días se redujo el riesgo de IAM en un 63% en elgrupo de dalteparina. Más allá de los 6 días,cuando se administraban dosis más bajas, las diferenciasentre ambos grupos se redujeron. A los 40 días, elporcentaje de enfermos que precisaron revascularización oadministración de heparina intravenosa, sufrieron un IAM ofallecieron fue del 5,4% en el grupo de la dateparina y de un 10,3%en el grupo control25. En el estudio FRIC, queincluía a 1.482 pacientes, se observó que ladalteparina administrada a dosis de 7.500 U subcutánea unavez al día a partir del sexto día no era máseficaz que el placebo26. Sin embargo, en otro estudio laincidencia de muerte, infarto agudo de miocardio o anginarecurrente fue un 17% menor en el grupo que recibió HBPMrespecto del que recibió HNF, aunque la incidencia desangrado fue similar en ámbosgrupos27.
El estudio FRISCII se ha publicado en agosto de 1999. Es un estudio prospectivo,aleatorizado y multicéntrico, realizado en 2.457 pacientesen 58 centros. Se comparó la dalteparina con el placebo enpacientes con angina inestable. Se observó un descensosignificativo de muerte y de infarto agudo de miocardio durante 6meses en el grupo de la dalteparina respecto al grupo tratado conplacebo. De igual manera disminuyó la tasa de nuevosepisodios de angina hasta 6 meses después en el grupo de ladalteparina. Obtuvieron más ventajas del tratamiento condalteparina los enfermos ancianos, varones, con angina de largaduración, con dolor de reposo o descenso del segmento ST.Hubo descenso en la sintomatología y la necesidad denitratos y la tasa de reingresos se redujo en la mitad en el grupotratado con dalteparina. Aunque hubo más episodios desangrados mayores en el grupo de dalteparina, no existierondiferencias con placebo en cuanto a la presentación deaccidentes cerebrovasculares, sangrados intracraneales otrombocitopenia28.
En un estudiodoble ciego, prospectivo y aleatorizado, realizado en 1995, secomparó la eficacia del ácido acetilsalicílicosolo o en combinación con heparina convencional onadroparina en pacientes con angina inestable. Se incluyó enel estudio a 299 enfermos. El trabajo concluyó que el riesgototal de episodios adversos o de angina recurrente fuesignificativamente más bajo en los pacientes tratados conácido acetilsalicílico más nadroparina que enlos restantes grupos. Un número significativamentepequeño de pacientes que recibieron ácidoacetilsalicílico más nadroparina tuvieron isquemiasilente documentada por monitorización continua del segmentoST durante las primeras 48 h de estudio, comparados con aquellostratados con ácido acetilsalicílico másheparina convencional29.
El tratamientocon enoxaparina ha resultado más eficaz que la HNF en eltratamiento de la angina inestable y del infarto de miocadio no-Q.Esto se demostró en el estudio ESSENCE, en el que seincluyó a 3.571 pacientes a los que se administró deforma aleatoria enoxaparina, 1 mg/kg por víasubcutánea dos veces al día, o HNF en forma de bolo(5.000 U), seguido de una infusión continua según eltiempo parcial de tromboplastina. En ambos grupos se asocióácido acetilsalicílico. En este ensayoclínico, multicéntrico y doble ciego, seobservó que después de 14 días de seguimientoel riesgo de muerte, IAM o angina recurrente fue significativamentemenor en el grupo tratado con enoxaparina, respecto del grupo querecibió HNF (el 27 frente al 32,2%; p = 0,001).Además, el tratamiento con enoxaparina supuso menoresincrementos del factor de Von Willebrand (cuyo aumento en losprimeros 2 días se asoció con una mayor tasa de IAM ymortalidad). La incidencia de hemorragias mayores fue similar enambos grupos30.
En la actualidadno disponemos de evidencias acerca de la eficacia de las HBPM en eltratamiento del IAM. Se han realizado dos estudios con dalteparina.En el primero de ellos, un estudio abierto en el que seincluía sólo a 37 pacientes con IAM anterior, seobservó una disminución de la presencia de trombosventriculares izquierdos (8%) en los enfermos que recibierondalteparina, respecto a la incidencia publicada en labibliografía científica (25-45%). Debido aldiseño del estudio y al pequeño número depacientes incluidos en el mismo, no se puede concluir con certezaque la dalteparina sea eficaz en el tratamiento de estaentidad31. En otro ensayo clínico en el quetambién se incluyó a pocos pacientes (n = 101), peroaleatorizado y doble ciego, se observó una incidencia menorde episodios isquémicos durante las 6-24 h tras el iniciodel tratamiento del IAM, siendo del 16% en el grupo de ladalteparina respecto a un 38% en el grupo control (p =0,04)32.
Técnicas dedepuración extrarrenal
La dalteparina,al igual que la bemiparina, es un anticoagulante útildurante los procedimientos dialíticos. Se pauta una dosis de5.000 U en la línea arterial al inicio de la diálisis(de 3 a 4 h de duración). Los estudios realizados nodescriben complicaciones hemorrágicas nitrombóticas33. Existe otro método donde seinfunde una dosis de carga de 20 U/kg, seguido de unainfusión continua de 10 U/kg/h, realizado en un estudio de 2semanas con una media de 4,6 h de diálisis. La eficacia essimilar a la heparina estándar. El tiempo parcial detromboplastina activado y los tiempos de coagulación sealargaron en el grupo dalteparina, pero en menor cuantía quecon HNF34. La dalteparina estimula la actividadlipolítica del plasma en menor grado que la HNF en pacientesdializados, lo que puede minimizar el riesgo dehipertrigliceridemia35.
Se han descrito2 casos (2 enfermos politraumatizados) en los que se ha utilizadoenoxaparina satisfactoriamente en hemofiltración comoalternativa a la heparina. La enoxaparina se administró enla línea venosa con una dosis continua en un rango dedosificación recomendado por los autores entre 0,4 y 0,6mg/kg/día36.
En un estudiomulticéntrico y aleatorizado, publicado recientemente secomparaba la eficacia, seguridad y coste de dalteparina frente a laHNF como anticoagulantes durante la hemofiltración continua.Se incluyó a 57 pacientes que precisaronhemofiltración, bien por fallo renal o por síndromede respuesta inflamatoria sistémica. Se consideró eltiempo hasta el fallo de la hemofiltración como la variableprincipal de evaluación. Otras variables secundarias fueronel recuento plaquetario, el número de episodios de sangrado,la concentración de hemoglobina durante lahemofiltración y la necesidad de transfusión. No seencontraron diferencias en cuanto a la supervivencia del filtro conlas dos pautas de tratamiento, y la seguridad en ambos grupos fuesimilar. Sin embargo, el coste del tratamiento fue superior en elcaso de la dalteparina37. Por otra parte, los
autores indican en la discusión que se debe ser cuidadosoen la extrapolación de estos resultados a otras HBPM debidoa la heterogeneidad de la razón antifactor Xa:antifactorIIa.
Enfermedadcerebrovascular
Hasta la fechasólo disponemos de los resultados de un ensayoclínico controlado y aleatorizado (realizado en 312 enfermoscon accidente cerebrovascular agudo). Este estudio sugiere que lanadroparina puede mejorar el pronóstico de pacientes conictus isquémico durante la fase aguda. Los pacientesrecibieron dosis altas de HBPM (4.100 U por víasubcutánea dos veces al día), dosis bajas (4.100 Upor vía subcutánea una vez al día) o placebo,dentro de las 48 horas del inicio de los síntomas y,posteriormente, durante 10 días. En este período detiempo no hubo diferencias significativas entre los tres grupos detratamiento, pero a los 6 meses, teniendo en cuenta elparámetro "mal pronóstico" definido como muerte odependencia para actividades de la vida diaria, el 45% de lospacientes del grupo de altas dosis tuvo un pronóstico malo,comparado con el 52 y el 65% de los pacientes de los grupos debajas dosis y placebo, respectivamente, por lo que los autoresconcluyen que la nadroparina es efectiva en cuanto a unamejoría del pronóstico de la enfermedad a los 6meses38.
Trombosis inducida porcatéter
Existen muypocos datos acerca de la eficacia de las HBPM en estaindicación. Además de la publicación dealgunos casos aislados, disponemos de los resultados de unpequeño estudio en el que se incluyó a 5 enfermos contrombocitopenia y trombosis inducida por catéter de Hickman,a los que se administró enoxaparina, lo que dio lugar a larecanalización parcial o completa del mismo. En este trabajono se describen complicaciones secundarias al tratamiento, como eldesarrollo de hematomas o nuevas trombosis39.
Coagulaciónintravascular diseminada
En estudiosexperimentales se ha observado que la heparina puede inhibir deforma parcial la activación de la coagulaciónrelacionada con procesos sépticos y este efecto beneficiosose ha demostrado en algunos estudios en los que se incluyeronpacientes con coagulación intravascular diseminada(CID)40. Por otra parte, en ningún estudio lautilización de heparina en esta situación se haasociado con un incremento de fenómenos hemorrágicos.En la actualidad, con los datos de que disponemos se puede afirmarque la heparina probablemente es útil en pacientes con CID,particularmente en aquellos en los que se asocian fenómenostromboembólicos o depósitos extensos de fibrina(purpura fulminans o isquemia distal). Habitualmente a lospacientes que presentan un cuadro de CID, se les administraheparina a dosis bajas, 300-500 U/h en infusióncontinua.
Hay que destacarque también se han utilizado las HBPM como alternativa a laHNF en este tipo de pacientes. En un estudio multicéntrico,doble ciego, se incluyeron 125 pacientes, diagnosticados deCID41. Se asignó de forma aleatoria eltratamiento con la HNF o con una HBPM, observándose unamejoría en cuanto a los síntomas orgánicos del8,2 y del 20,5%, respectivamente. En cuanto a la eficacia global enlos casos que presentaban niveles de AT-III pretratamiento menoresde 21 mg/dl o menor del 70%, en el grupo que recibió HBPM sepuso de manifiesto una tasa de mejoría significativamentesuperior a la del grupo de HNF. Se produjo una mejoría delos síntomas de sangrado en un 33,3% de los pacientes conHBPM, siendo de un 18,5% en el grupo de la HNF, y la tasa deseguridad de la HBPM fue de un 93,4% respecto a un 79,7% con laHNF. Los autores de este estudio concluyen que las HBPM son agentesterapéuticos útiles en el tratamiento de pacientescon CID y que su eficacia y seguridad son significativamentesuperiores a las de la HNF.
En otro ensayoclínico, abierto, en el que se incluyó a 56 enfermos,se utilizó dalteparina en dosis de 75 U/kg/día eninfusión intravenosa continua durante 5 días. Lossíntomas de sangrado y las pruebas decoagulación/fibrinólisis mejoraron en el 46 y el 67%,respectivamente. En el 32% de los enfermos se observómejoría en cuanto al fracaso de órganos. En esteestudio la dalteparina a altas dosis no ofreció ventajaestadística sobre la administración de dosisbajas42. También se han descrito casosesporádicos de utilización de nadroparina en lacoagulación intravascular diseminada.
COSTE COMPARATIVO
En la profilaxisde la enfermedad tromboembólica venosa en pacientes deriesgo moderado el fármaco más barato es labemiparina, pero debemos tener en cuenta que con este compuestoexiste menos experiencia clínica. En pacientes de riesgoalto la más barata es nadroparina en los pacientes de menosde 70 kg de peso y bemiparina en los de más de 70 kg. En eltratamiento de la enfermedad tromboembólica la másbarata es nadroparina, pero como se tiene que administrar dos vecesal día, sería más adecuado elegir enoxaparinao dalteparina.
INDICACIONES DE HEPARINAS DEBAJO PESO MOLECULAR
Todas lasheparinas de bajo peso molecular comercializadas en España,excepto la tinzaparina, están autorizadas para la profilaxisde la enfermedad tromboembólica venosa y para laprevención de la coagulación de circuitoextracorpóreo en hemodiálisis. Para el tratamiento dela trombosis venosa profunda con o sin embolismo pulmonarestán autorizadas la enoxaparina, la dalteparina, lanadroparina y la tinzaparina. Para el tratamiento de la anginainestable y del infarto de miocardio sin onda Q se ha autorizado eluso de enoxaparina y dalteparina.
CONCLUSIONES
Las heparinasson los anticoagulantes de elección cuando se requiere unefecto anticoagulante rápido. Debido a la facilidad deadministración y de dosificación las HBPM hansustituido a la HNF, especialmente en el ámbitoextrahospitalario. En la anticoagulación a largo plazo eltratamiento con heparina se suele continuar con anticoagulantesorales, pero en algunas situaciones se puede administrar HBPM alargo plazo, por ejemplo durante el embarazo o en tromboembolismosrecurrentes durante el tratamiento con dosis adecuadas deanticoagulantes orales.
Las HBPM handemostrado ser más eficaces y seguras que la HNF en laprofilaxis y el tratamiento de la enfermedad tromboembólicavenosa, por lo que constituyen el tratamiento de primeraelección en estas indicaciones, a pesar de ser máscaras que la HNF. Existen datos suficientes que demuestran que lasHBPM son al menos igual de eficaces que la HNF en el tratamiento dela angina inestable, pero a diferencia de esta última no esnecesaria una monitorización.
Las HBPM poseennumerosas ventajas respecto a la heparina no fraccionada, tienenuna vida media más larga, por lo que se pueden administraren una o dos dosis al día, su biodisponibilidad es mejor, yse administran siempre por vía subcutánea,permitiendo así una mayor movilidad del paciente y eltratamiento domiciliario. La variabilidad individual tambiénes menor, y el efecto anticoagulante es más predecible,haciendo que no sea necesario monitorizar el tiempo parcial detromboplastina activado.
Aunque en muchasde las situaciones descritas a lo largo de esta revisión,las HBPM han resultado eficaces, todavía se deben realizarmás ensayos clínicos que incluyan un númeroelevado de pacientes para demostrarlo. De cualquier forma cabedestacar la excelente y reciente revisión sobre indicacionesde la profilaxis basada en la estratificación del riesgo(niveles de evidencia)43, que cuestiona, puntualiza yadapta a nuestro medio recomendaciones más clásicasestableciendo métodos de profilaxis eficaces en grupos deriesgo bien definidos.
En laactualidad, no disponemos de ensayos clínicos comparativosentre las distintas HBPM. Con la información disponiblehasta ahora parece que todas son igual de eficaces, aunque algunasde ellas no se han autorizado para ciertas indicaciones por lafalta de ensayos clínicos. Sin embargo, a pesar de que lasHBPM poseen unas características similares, existendiferencias entre ellas en cuanto a peso molecular, vida media yselectividad por el factor Xa y parece que la HBPM idealsería aquella con un peso molecular más bajo y, porello, con una mejor relación actividad anti-Xa/ anti-IIa, deforma que se acentúe el efecto antitrombótico,minimizando el potencial hemorrágico.