El shock cardiogénico (SC) es un cuadro clínico de alta complejidad que requiere un manejo centrado en resolver de forma precoz la causa condicionante y asegurar un soporte circulatorio. En caso de shock refractario, los sistemas de soporte circulatorio mecánico (SCM) permiten suplir al sistema cardiocirculatorio fracasado para evitar el desarrollo de fracaso multiorgánico. Existen diferentes tipos de SCM, y en los pacientes en SC se suelen contemplar dispositivos de corta (menos de 15 días) o intermedia duración (15-30 días). Para su elección se debe tener en cuenta la causa que ha condicionado el SC y aspectos como el ventrículo fracasado, la presencia/ausencia de insuficiencia respiratoria y el propósito del soporte. Los pacientes con SCM requieren un cuidado integral de enfermo crítico complejo con disfunción multiorgánica, haciendo hincapié en la monitorización y el control del dispositivo. Durante su manejo puede aparecer diferentes complicaciones y su retirada debe estar protocolizada.
Cardiogenic shock (CS) is a highly complex clinical condition that requires a management strategy focused on early resolution of the underlying cause and the provision of circulatory support. In cases of refractory CS, mechanical circulatory support (MCS) is employed to replace the failed cardiocirculatory system, thereby preventing the development of multiorgan failure. There are various types of MCS, and patients with CS typically require devices that are either short-term (< 15 days) or intermediate-term (15-30 days). When choosing the device the underlying cause of CS, as well as the presence or absence of concomitant conditions such as failed ventricle, respiratory failure, and the intended purpose of the support should be taken into consideration. Patients with MCS require the comprehensive care indicated in complex critically ill patients with multiorgan dysfunction, with an emphasis on device monitoring and control. Different complications may arise during support management, and its withdrawal must be protocolized.
El shock cardiogénico (SC) es un cuadro clínico de alta complejidad que requiere un manejo dinámico, escalonado, centrado en detectar y resolver de forma precoz las posibles causas subyacentes y asegurar un soporte circulatorio adecuado que evite el desarrollo de fracaso multiorgánico1. Para ello se requiere una monitorización hemodinámica completa y precoz2 que permita realizar una optimización inicial guiada por objetivos hemodinámicos3–6. Aquellos pacientes que persistan en situación de shock pese a las medidas iniciales7, requerirán una monitorización invasiva y ecocardiográfica avanzada para valorar y profundizar en la etiología, seleccionar la mejor estrategia terapéutica, monitorizar la respuesta a las medidas implementadas y plantear una estrategia de soporte circulatorio mecánico (SCM) adecuado8.
El objetivo fundamental de los SCM es suplir al sistema cardiocirculatorio fracasado para evitar el desarrollo de fracaso multiorgánico. De esta manera, los SCM deben conseguir un transporte de oxígeno (DO2) adecuado a los requerimientos de los órganos/tejidos (VO2), disminuir el consumo de oxígeno miocárdico para facilitar la recuperación de la función ventricular y proporcionar tiempo, bien para conseguir la mejoría de la función cardiaca, bien para realizar un trasplante cardiaco urgente, o para decidir si será trasplantable o subsidiario de una asistencia mecánica de más larga duración9.
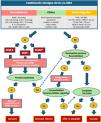
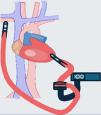
Clasificación y tipos de soporte circulatorio mecánicoLos avances tecnológicos han conducido a una importante diversificación de los SCM. Las clasificaciones se basan en aspectos como el nivel (parcial o global) y/o ventrículo (uni o biventricular) soportados, la vía de acceso al paciente (periférico o central), tipo de implante (percutáneo o quirúrgicos), los efectos hemodinámicos y/o cardiorrespiratorias que generan y, por supuesto, el tiempo objetivo de soporte, para lo que se plantea corta <15 días, intermedia 15-30 días y larga >30 días (fig. 1)10.
Clasificación de los soportes circulatorios mecánicos. AD-P: aurícula derecha-pulmonar; BCIAo: balón de contrapulsación intraaórtico; DL: Dual Lumen®; ECMO VA: oxigenación con membrana extracorpórea venoarterial; PD: ProtekDUO®; TH: TandemHeart®; VI: ventrículo izquierdo; VI-Ao: ventrículo izquierdo-aorta; VI-Ax: ventrículo izquierdo-axilar; VD: ventrículo derecho. * Percutáneo o quirúrgico según disponibilidad y urgencia.
En los pacientes en SC se contemplan dispositivos de corta o intermedia duración que suplan las características fisiopatológicas y anatómicas del paciente y la potencial recuperabilidad de la función órgano/específica cardiaca y/o pulmonar que haya fracasado. Asimismo, la experiencia y la evidencia científica disponible permite establecer un uso complementario de los mismos y planificar de forma adecuada una escalada o desescalada terapéutica11.
Soporte parcial izquierdoBalón de contrapulsación intraaórtico (BCIAo)El BCIAo continúa siendo un dispositivo de soporte mecánico circulatorio ampliamente utilizado dada su facilidad y rapidez de colocación12. Su mecanismo de soporte es bien conocido de manera que, durante el inflado, el incremento de la presión arterial diastólica mejora el flujo coronario, cerebral y renal, y en el desinflado, se reduce la poscarga, la presión telediastólica (PTDVI) y el trabajo miocárdico. Pese a ello, solo eleva discretamente el gasto cardiaco (0,5l/min) y en casos de SC refractario suele ser un soporte insuficiente.
El impacto del empleo del BCIAo sobre la mortalidad en el SC es controvertido dado que el ensayo clínico IABP SHOCK II no logró demostrar beneficios en la mortalidad a los 30 días13,14. Los metaanálisis posteriores tampoco evidenciaron una mejoría en la supervivencia a corto y medio plazo15. De hecho, las actuales guías clínicas no recomiendan su uso generalizado en el SC post-IAM16. Pese a ello, el BCIAo sigue siendo ampliamente utilizado, principalmente en centros que no disponen de otro tipo de SCM, como puente a trasladar el paciente a otro centro para un dispositivo de mayor soporte hemodinámico. Por otro lado, sigue siendo útil en algunos escenarios perioperatorios, como el shock poscardiotomía, las complicaciones mecánicas del IAM (insuficiencia mitral aguda y rotura del tabique interventricular) o la cirugía de revascularización de alto riesgo17. Además, ha despertado un creciente interés como estrategia de descarga de ventrículo izquierdo en los pacientes con oxigenación por membrana extracorpórea-venoarterial (ECMO VA) dado que parece reducir la mortalidad con menor número de complicaciones que otros dispositivos18.
Impella® (Abiomed, Danvers, MA)El SCM univentricular de flujo microaxial transvalvular, de implantación percutánea o quirúrgica, que se posiciona a través de la válvula aórtica en el VI, impulsando directamente la sangre desde la cavidad ventricular hacia la aorta mediante un flujo continuo. De esta forma, aumenta el gasto cardiaco, incrementa la presión arterial media y mejora la perfusión sistémica y coronaria. Además, el óptimo vaciado del VI, reduciendo la PTDVI, ayuda a la recuperabilidad cardiaca, ya que reduce la tensión parietal del VI, minimizando la demanda miocárdica de oxígeno19.
Dentro de los dispositivos de uso clínico actual destacan el Impella® CP y el Impella® 5/5.5. El primero se implanta de forma percutánea a través de un introductor de 14F a nivel de arteria femoral (AF) dejando su extremo a través de la válvula aórtica a unos 3,5-4cm de esta y puede alcanzar un flujo teórico de hasta 3,5-4l/min. El segundo es de mayor tamaño y se implanta quirúrgicamente, preferentemente a través de la arteria axilar, puede aportar un flujo teórico máximo de 5-5,5l/min y a diferencia del primero permite un tiempo de asistencia que puede llegar a los 30 días. A pesar de su facilidad de implante y buenos resultados, presentan como contraindicación la presencia de estenosis o insuficiencia aórtica grave, prótesis aórtica mecánica, enfermedad arterial periférica grave o la presencia de trombo en la válvula o en el VI20. Una contraindicación controvertida es la CIV postinfarto dado que se han reportado series con buenos resultados21.
Teniendo en cuenta los resultados de los últimos estudios, los SCM de flujo axial pueden constituir el primer dispositivo a usar en casos de SC por IAM o fallo univentricular izquierdo22, precisando la escalada a otros dispositivos si no hay mejoría, si progresa el deterioro clínico del enfermo o si se produce afectación concomitante de VD y/o pulmón. Revisiones sistemáticas recientes muestran resultados equiparables a la terapia ECMO23 y su uso combinado tras escalada a ECMO, proporciona mejores resultados que la ECMO aislada24,25.
TandemHeart® (Livanova)El SCM de VI que mediante una centrífuga de implantación percutánea extrae la sangre en la aurícula izquierda (AI) y la retorna en la AF. El implante se realiza a través de la vena femoral mediante una cánula de 21F que se posiciona en la AI de forma transeptal. A pesar de su excelente funcionamiento, las dificultades técnicas del implante y el fácil desplazamiento de la cánula de AI hacen que su utilización sea limitada en nuestro medio10.
CentriMag® (Abbott)El SCM de canulación quirúrgica que utiliza una bomba centrífuga de levitación magnética para extraer la sangre de una cámara cardiaca y llevarla al sistema circulatorio correspondiente. Es un sistema muy utilizado y tiene un flujo máximo teórico de hasta 10l/min. Puede utilizarse de forma univentricular izquierda, derecha o biventricular, permite intercalar un oxigenador para tener funciones de ECMO y tiene una aprobación para uso por encima de los 30 días26. En casos de soporte VI, aunque puede implantarse mediante esternotomía a nivel de la AI y la aorta, su implante se puede realizar mediante un abordaje miniinvasivo, drenando directamente el VI desde el ápex, a través de un minitoracotomía y estableciendo el retorno al paciente en la arteria axilar (material suplementario 1). En caso de ser utilizado como SCM de VD, la entrada de sangre al sistema se realiza a través de la vena femoral y el retorno al paciente a través de la arteria pulmonar mediante un tubo de dacrón (vía esternotomía).
Soporte parcial derechoLos SCM de VD suponen un porcentaje significativamente menor que los de VI, pero han ido emergiendo los últimos años y, salvo el CentriMag® que tendría una implantación quirúrgica, su implante es percutáneo27.
Impella RP®(Abiomed)Sistema de asistencia microaxial de implantación percutánea a nivel de AD por vía femoral que impulsa de sangre a nivel de la arteria pulmonar28.
ProtekDUO® (LivaNova)Cánula de doble luz (29F-31F) de implantación percutánea por vía transyugular a nivel de aurícula derecha (proximal) y arteria pulmonar (distal) que mediante una bomba centrífuga impulsa la sangre pudiendo aportar un flujo de hasta 5l/min. Además, puede intercalar un oxigenador y tener función de ECMO venopulmonar15,29.
Dual Lumen System® (Spectrum Medical)Cánula de doble luz de 24F, 27F o 31F que se implanta a través de la vena yugular interna y se conecta a una bomba centrífuga con o sin oxigenador. El circuito se establece entre el VD y la arteria pulmonar con un flujo máximo de 5l/min30.
Soporte globalOxigenación con membrana extracorpóreaLa ECMO, en su configuración venoarterial (VA) es un SCM global que genera un soporte cardiorrespiratorio y se puede indicar de forma inicial en cualquier contexto de disfunción ventricular uni/biventricular con o sin insuficiencia respiratoria31,32. Debido a la posibilidad de implante emergente, puede utilizarse en el contexto de parada cardio-respiratoria (PCR) como sistema de reanimación de rescate (ECMO RCP) habitualmente por vía periférica y de manera percutánea33.
El dispositivo consta de una bomba centrífuga que extrae la sangre del paciente desde el sistema venoso mediante una cánula, habitualmente por vía femoral de 19-27F de diámetro, y a través de un circuito lleva la sangre a través de un oxigenador que realiza el intercambio gaseoso y la retorna al paciente al sistema arterial mediante una cánula femoral o axilar de 15-21F. La canulación central, a través de esternotomía o toracotomía, también es posible pero debido a su mayor tasa de complicaciones es menos recomendada34,35. El tamaño de las cánulas, fundamentalmente la cánula venosa, es el factor mayor limitante al flujo con el que podemos asistir al paciente y se debe tener en cuenta a la hora de la planificación del soporte estimado y del acceso vascular por el que se va a implantar.
A pesar de reducir la demanda metabólica cardiaca y mejorar la hemodinámica del paciente, reduciendo la precarga del VD, debido a sus características, la ECMO puede condicionar un potencial problema de presurización del ventrículo izquierdo (VI). A medida que se precisa más flujo para asistir al paciente, la poscarga del VI aumenta, evitando su adecuado vaciamiento e incrementando las PTDVI. En los casos más graves, puede conllevar a un empeoramiento de la disfunción ventricular, cierre de la válvula aórtica, dilatación de la cavidad ventricular, edema pulmonar, aparición de eco-contraste espontáneo e incluso trombosis intracavitaria30. Esta situación puede minimizarse o evitarse mediante la utilización simultánea de un BCIAo o realizando un «venting» del VI a través de la AI, del VI o mediante un Impella®36. Este uso combinado, denominado ECMELLA o ECPELLA (material suplementario 2), a pesar de las potenciales complicaciones ha demostrado ventajas en estudios retrospectivos presentando menor mortalidad que con la ECMO VA aislada37,38.
En la tabla 1 se resumen los principales dispositivos, sus características y principales indicaciones.
Características de los principales dispositivos de soporte circulatorio mecánico
| BCIAo | Impella® CP/5.5® | Impella® RP | Centrimag® | ECMO VA | |
|---|---|---|---|---|---|
| Mecanismo | Inflado en diástole y desinflado en sístole. | Flujo axial continuo VI a aorta. | Flujo axial continuo VCI/AD a AP. | Flujo centrífugo continuo. | Fuljo centrífugo continuo con oxigenador. |
| Ventrículo asistido | VI | VI | VD | VD, VI y/o BiV | BiV |
| Flujo | 0,5-1l/min | 2,5-4l/min/5,5l/min | 2-4l/min | >5l/min | >5l/min |
| Mecanismo de soporte | Neumático | Flujo axial | Flujo axial | Flujo centrífugo | Flujo centrífugo |
| Efectos | ↑ Perfusión coronaria↓ PoscargaFacilita descarga VI | ↑ Perfusión sistémica↓ PTDVIDescarga directa VI | ↓ Presiones VD↓ Precarga VD | ↓ Llenado y distensión de cavidades drenadas | ↑ Poscarga y ↑ PTDVI↓ recarga VDSoporte respiratorio |
| Tamaño cánulaAcceso | 7-8FrAF | 13-21Fr /24FrAF/AAx | 22FrVF | 19-27Fr drenaje/15-21Fr retornoVD: AD-AP VI: VI-Ao/AAx | 19-27Fr drenaje/15-21Fr retornoVF-AF/VF-AAx /AD-Ao |
| Anticoagulación | − | + | + | ++ | +++ |
| Riesgo de sangrado | + | ++ | ++ | ++ | +++ |
| Riesgo de isquemia en MMII | + | ++ | ++ | ± (MMSS) | +++ |
| Notas: | Potencial uso con ECMO para descarga VI. | Potencial uso con ECMO para descarga activa VI (ECMELLA). | Mejora IC y disminuye PVC en fallo VD aislado. | Se puede asociar a (Protek-DUO®/Dual Lumen®±ECMO. | Permite asistencia cardiopulmonar global. No descarga VI. |
| Contraindicaciones | IAo severa, disección aórtica, enfermedad arterial periférica. | IAo severa, disección aórtica, enfermedad arterial periférica, trombo VI, prótesis aórtica mecánica. | Insuficiencia pulmonar severa, trombo VCI/AD/VD. | Propias de la cirugía torácica/cardiaca. | IAo severa, disección aórtica, enfermedad arterial periférica severa. |
AAx: arteria axilar; AD: aurícula derecha; AF: arteria femoral; Ao: aorta; AP: arteria pulmonar; BCIAo: balón de contrapulsación intraaórtico; BiV: biventricular; ECMO VA: membrana de oxigenación extracorpórea venoarterial; IAo: insuficiencia aórtica; IC: índice cardiaco; MMSS: miembros superiores; PTDVI: presión telediastólica de ventrículo izquierdo; PVC: presión venosa central; VCI: vena cava inferior; VD: ventrículo derecho; VF: vena femoral; VI; ventrículo izquierdo; VYI: vena yugular interna.
La indicación (tabla 2) y la estrategia de implante de los SCM varía en función de la causa que ha condicionado el SC y de las características de los pacientes que lo desarrolla. Antes del implante de un SCM hay que considerar una serie de aspectos que permitan tener una perspectiva completa del paciente, con especial atención a las expectativas en caso de ausencia de mejoría miocárdica tras varios días de soporte circulatorio (material suplementario 3)39. Además, hay que considerar algunas condiciones en las que el implante de estos dispositivos resultará fútil (tabla 3). Pueden plantearse 2 escenarios con manejo y pronóstico diferentes:
Causas de shock cardiogénico subsidiario de soporte circulatorio mecánico
| Causa |
|---|
| Síndrome coronario agudo |
| Complicaciones mecánicas de SCA (CIV, rotura cardiaca, rotura valvular) |
| Síndrome poscardiotomía (incluyendo incapacidad para el destete de la circulación extracorpórea) |
| Miocarditis |
| Disfunción primaria del injerto tras TxC |
| Arritmias ventriculares refractarias |
| Infección o intoxicación grave complicada con disfunción miocárdica |
| Hipotermia grave (<28°C) |
| TEP masivo |
| Vasoconstricción pulmonar hipóxica severa |
| Reagudización de insuficiencia cardiaca crónica |
| Miocardiopatías |
| Valvulopatía aguda |
| Procedimientos percutáneos de alto riesgo |
CIV: comunicación interventricular; SCA: síndrome coronario agudo; TEP: tromboembolismo pulmonar; TxC: trasplante cardiaco.
Contraindicaciones de implante de soporte circulatorio mecánico
| Absolutas |
|---|
| Cáncer metastásico |
| RCP prolongada sin perfusión tisular adecuada |
| Parada cardiaca no presenciada |
| Lesión cerebral grave irreversible |
| Fracaso multiorgánico grave e irreversible |
| Anomalías cromosómicas letales a corto plazo |
| Disección o insuficiencia aórticas no corregibles |
| Taponamiento cardiaco no corregible |
| Relativas |
|---|
| Edad avanzada |
| Trastornos hemorrágicos grave |
| Obesidad mórbida |
| Enfermedad arterial periférica grave (solamente para canulación periférica) |
| Enfermedades previas con mal pronóstico a largo plazo |
RCP: reanimación cardiopulmonar.
Son múltiples las enfermedades que pueden dar lugar a esta entidad de elevada morbimortalidad. El IAM constituye la primera causa, con una prevalencia variable (44-77%) y con notables diferencias temporales y geográficas. Por otro lado, el pronóstico difiere de la etiología del SC. Si bien diferentes artículos muestran una mayor supervivencia en pacientes con IAM, otros sugieren que el tromboembolismo pulmonar, la miocarditis aguda fulminante o la enfermedad valvular aguda tienen mejor pronóstico, siendo las arritmias ventriculares malignas las que muestran peores tasas de supervivencia. Estos trabajos son retrospectivos y la distribución de los diferentes dispositivos usados difiere de la actual, de modo que resulta difícil considerar la etiología como un factor pronóstico40–42.
En un intento de predecir la mortalidad para pacientes con SC a los que se implanta una ECMO, se han propuesto diferentes escalas de riesgo para apoyar la indicación. La más extendida es la escala SAVE Score que estratifica a los pacientes en 5 grupos de riesgo correlacionados con diferente supervivencia38. Menos conocidas en la práctica habitual son las escalas ENCOURAGE que fue diseñada sobre una población de pacientes con IAM o REMEMBER para pacientes con shock poscardiotomía tras cirugía coronaria43,44.
Insuficiencia cardiaca avanzada agudizadaEn pacientes con insuficiencia cardiaca avanzada (ICA) refractaria a terapias convencionales, los dispositivos de asistencia ventricular (DAV) se han erigido como una herramienta útil para mejorar su supervivencia y calidad de vida45. Para determinar el momento óptimo de implante de esta terapia es conveniente usar la escala INTERMACS que, si bien en los estudios iniciales mostraban mejores tasas de supervivencia, cuando el implante se llevaba a cabo sobre la población de pacientes más estables (INTERMACS 4-7), actualmente apenas el 15% se ubica en estas posiciones46. Este grupo de pacientes en ICA puede presentar una agudización con unas características y pronóstico distintas al SC de novo47. En caso de que esta agudización desemboque en una situación de SC, la terapia ECMO se ha relacionado con una supervivencia del 42% a un año, siendo los valores de lactato y una mayor puntuación en la escala SOFA preimplante los principales determinantes de la mortalidad48.
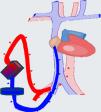
Estrategia inicialPara elegir el SCM adecuado hay que identificar el ventrículo disfuncionante y la existencia o no de afectación pulmonar. En caso de disfunción biventricular, con insuficiencia respiratoria y fallo circulatorio establecido, la ECMO suele ser la primera opción, buscando la mejor estrategia de canulación49 y considerando la frecuente necesidad de drenaje de las cavidades izquierdas28,29,50. En casos de disfunción univentricular, en ausencia de compromiso respiratorio, la elección del tipo de SCM dependerá del grado de soporte o flujo necesario, de la reversibilidad que condicionará el tiempo de soporte, las posibilidades de acceso e, incluso, de la disponibilidad en el centro (fig. 2)49,51.
Algoritmo de manejo inicial del shock cardiogénico con soporte circulatorio mecánico. BCIAo: balón de contrapulsación intraaórtico; BiV: biventricular; ECMO VA: oxigenación con membrana extracorpórea veno arterial; PTDVI: presiones telediastólicas de VI; SCM: soporte circulatorio mecánico; VD: ventricular derecho; VI: ventricular izquierdo; α: Según disponibilidad y objetivo de la terapia.
Fuente: modificado de Lorusso R, et al.
El manejo los pacientes con SCM incluye el cuidado integral de un enfermo crítico complejo con disfunción multiorgánica2, la monitorización y el control del dispositivo52,53. El uso de protocolos que homogeneicen los cuidados y aseguren una atención de calidad y segura es de gran utilidad54.
CardiovascularSe precisa de una monitorización continua electrocardiográfica, presión arterial invasiva (PA) y saturación de O2 (SatO2). La monitorización hemodinámica avanzada se realiza con el catéter de arteria pulmonar que proporciona información para el manejo de drogas vasoactivas, el flujo del SCM y para el destete. Los métodos de análisis de onda de pulso o termodilución habitualmente no son fiables por el flujo continuo que proporcionan los SCM. La presión venosa central es un parámetro útil, pero se debe valorar la tendencia más que el valor absoluto ya que puede estar interferido por la presión negativa de succión. El acceso ideal para la PA es la arteria radial derecha para monitorizar también el intercambio gaseoso nativo55.
La monitorización con el sistema Near-Infrared Spectroscopy (NIRS) permite observar cambios en la perfusión y oxigenación a nivel regional (cerebral, miembro canulado, etc.), detectar y controlar el desarrollo de síndrome del arlequín y optimizar la PA, la oxigenación y/o el flujo de la asistencia ante descensos del NIRS56,57.
En la evaluación diaria, se deben realizar ecocardiogramas frecuentes para objetivar la evolución cardiaca, la aparición de complicaciones (sobre todo la dilatación del VI en el ECMO VA) y evaluar la posibilidad de destete del dispositivo56,58.
El manejo hemodinámico se basa en ajustar el flujo del SCM, el aporte de fluidos y los fármacos vasoactivos a la situación hemodinámica, buscando una adecuada perfusión y transporte de oxígeno a los tejidos, una adecuada SatO2 venosa, IC propio, PAM y aclaramiento de lactato6.
El uso de inotropos es controvertido y se recomienda individualizar la dosis a cada situación. Son útiles para conseguir mejorar la eyección y evitar la dilatación ventricular y la estasis sanguínea, pero hay que administrar la mínima dosis y valorar su retirada lo antes posible59.
Con bajas resistencias vasculares sistémicas es necesario el uso de vasoconstrictores siendo la noradrenalina el fármaco de elección60. En pacientes con hipotensión refractaria, a pesar de dosis crecientes de NA, de debe plantear el uso de vasopresina, que ha demostrado utilidad y beneficio en diferentes contextos61,62. Otras opciones en casos refractarios, aunque con menor evidencia científica, podrían ser el azul de metileno intravenoso, la angiotensina II, los corticoides a dosis de estrés y los coadyuvantes metabólicos (hidroxocobalamina, tiamina y ácido ascórbico)63,64.
RespiratorioLas recomendaciones son las habituales en pacientes con shock utilizando estrategias de «protección pulmonar», con volúmenes tidal bajos (<6ml/kg), frecuencia respiratoria baja, PEEP óptima, evitar presión meseta elevada y la mínima concentración de oxígeno para evitar la hiperoxigenación. Es recomendable evitar en lo posible la ventilación mecánica invasiva65.
AnticoagulaciónLos SCM, excepto el BIAo, necesitan anticoagulación a dosis terapéuticas. La monitorización de la anticoagulación debe ser multimodal y se recomienda realizar protocolos en cada centro. El fármaco más utilizado es la heparina sódica en perfusión continua y su monitorización se realiza con varios métodos: Activated Clotting Time (ACT) entre 160-180s, tiempo de tromboplastina parcial activado (TTPa) ratio 1,5-2 y/o niveles del factor anti-Xa de 0,3-0,7UI/ml. Cada vez se utilizan más los inhibidores directos de la trombina (bivalirudina y argatrobán) por su seguridad, su acción más estable y no causar trombocitopenia inmune. A diferencia de la heparina, tienen el inconveniente de no disponer de antídoto66.
La dosis de anticoagulación debe ajustarse si aparecen hemorragias y puede suspenderse de forma transitoria manteniendo flujos de bomba altos para evitar trombosis. En pacientes posquirúrgicos, el inicio de la anticoagulación puede postponerse hasta controlar la hemorragia inmediata e incluso hasta la retirada de los drenajes. Puede empezarse con dosis bajas de heparina e ir aumentando cuando se comprueba la ausencia de hemorragias66. Los fenómenos trombóticos se monitorizan con ecografía tanto a nivel de cavidades cardiacas como en los vasos canulados o elementos del SCM58.
InfecciosoExiste una vulnerabilidad de estos pacientes a la infección por la canulación, la monitorización invasiva y la ventilación mecánica, entre otros La profilaxis antibiótica periprocedimiento no está recomendada de forma sistemática, solo en los casos de implante emergente donde se pierda la asepsia, si se utiliza un vaso con catéter previo, en procesos de canulación prologados por complicaciones, o si la canulación es central67. En los pacientes con SCM se deben realizar medidas para la prevención de infecciones (material suplementario 4). El diagnóstico de infección es complejo por la respuesta inflamatoria generada por la propia asistencia, la infravaloración de la fiebre por la hipotermia inducida por el SCM o por los intercambiadores de temperatura. Se debe sospechar ante cambios hemodinámicos no explicados, aparición de alteraciones metabólicas (acidosis, hiper/hipoglucemia, hipercapnia), o aumento de los reactantes de fase aguda.
RenalEl deterioro de la función renal es inherente al SC con SCM ya que el riñón es muy susceptible al flujo no pulsátil, aunque influyen otros aspectos como patologías previas, respuesta inflamatoria sistémica, disregulación del eje renina-angiotensina-aldosterona, aumento de la presión intratorácica /intraabdominal, fármacos nefrotóxicos, hipoxemia/hipercapnia grave, hemólisis, hipercoagulabilidad, etc.
Se requiere una estrecha vigilancia de la función renal, del balance hídrico y del control de los parámetros de hemólisis. Se recomienda la monitorización del grado de fracaso renal agudo (FRA) durante el SCM mediante escalas como la KDIGO68.
Neurológica y rehabilitaciónLa monitorización neurológica debe ser multimodal, encaminada al control de la sedoanalgesia y a la detección precoz de complicaciones. Es necesario realizar periódicamente ventanas de sedación y seleccionar la sedoanalgesia más adecuada. En los casos con ECMO, hay que evitar fármacos que se adhieran al circuito o a la membrana y administrar la dosis óptima69.
Se recomienda realizar exploración neurológica diaria (reactividad pupilar con luminiscencia y/o pupilómetro), monitorización con NIRS, monitorización con el índice biespectral (BIS) y medición de flujos cerebrales con doppler transcraneal. Se recomienda realizar un electroencefalograma basal en ciertas circunstancias (tras parada cardiaca, cirugías prolongadas o en casos de sangrados perimplantación) y posteriormente repetir ante aparición de signos de hipertensión intracraneal, mioclonías o convulsiones, dificultad en el despertar, shock refractario y disminuciones del BIS o NIRS. Se pueden plantear otras pruebas complementarias (potenciales evocados somatosensoriales, diámetro de la vaina del nervio óptico, TAC o angioTAC) en caso de sospecha de complicaciones70.
Debe prevenirse el delirio con medidas no farmacológicas o tratarlo de manera precoz para evitar complicaciones como reintubaciones, extubaciones o decanulaciones accidentales69.
La rehabilitación de los pacientes debe comenzar desde el inicio del implante del SCM, valorando si es posible la sedestación y/o la deambulación, así como la realización de ejercicio físico moderado. En los pacientes candidatos a trasplante cardiaco o a una intervención quirúrgica es fundamental, pues contribuye a mejorar el postoperatorio inmediato reduciendo el tiempo de ventilación mecánica, de estancia en la UCI y hospitalaria71.
Digestiva y nutricionalLa disfunción hepática aparece en un 15% de los pacientes, por lo que hay que vigilar la función hepatocelular, y ajustar la anticoagulación y los fármacos hepatotóxicos.
Se debe realizar un soporte nutricional precoz y completo, priorizar la nutrición enteral, y calcular las necesidades nutricionales de forma individual. Es importante realizar aportes vitamínicos, de minerales, hierro y otros micronutrientes según las necesidades individuales72.
ComplicacionesLas complicaciones en pacientes con SCM se deben a la combinación de factores relacionados con la patología subyacente y comorbilidades (etiología del shock, inmunosupresión, etc.), así como con la propia asistencia mecánica (invasividad, tiempo y tipo de soporte, uso de anticoagulación, etc.).
InfeccionesComo cualquier dispositivo intravascular, el uso de SCM supone un riesgo aumentado de infecciones (punto de inserción, bacteriemias e incluso endocarditis), que son potencialmente graves y suponen una disminución de la supervivencia73. La prevención es primordial, la técnica de implante debe ser estéril y son fundamentales los cuidados diarios de los puntos de inserción. Las infecciones requieren un tratamiento antibiótico óptimo (elección de fármaco, dosis, duración) e incluso la retirada del dispositivo en función de la causa y gravedad. Estos pacientes tienen un mayor riesgo de infecciones nosocomiales (neumonía asociada a ventilación mecánica, bacteriemias, etc.) con incidencias variables entre series y dispositivos73.
VascularesEl uso de SCM puede asociar la presencia de lesiones en el punto de inserción generando hematomas, sangrado y dolor localizado y trombosis secundarias a la alteración del flujo vascular por la canulación. Otras complicaciones menos frecuentes son la estenosis tras la retirada y la presencia de fístulas arteriovenosas.
EmbolígenasLa predisposición a la formación de trombos en los vasos sanguíneos canulados o pericánulas pueden provocar fenómenos tromboembólicos causando obstrucciones en vasos pequeños y en otros territorios durante la asistencia y tras su retirada. También hay una mayor tendencia a la formación de trombos en las cavidades cardiacas por la disminución del flujo sanguíneo propio o por la dilatación de las cavidades.
Se recomienda la monitorización ecocardiográfica y con ecografía vascular para la detección precoz de los fenómenos trombóticos, optimizar la anticoagulación y evitar la embolización. En caso de trombosis venosa profunda (TVP) tras la retirada de la ECMO para evitar la aparición de TEP, se debe mantener anticoagulación terapéutica con una duración controvertida58.
Hemorrágicas y hemólisisEl riesgo de sangrado tanto local (en el lugar de inserción) como sistémico está aumentado por el uso de los SCM y por los fármacos asociados (anticoagulación, antiagregación). Para el manejo del sangrado se debe cuantificar, valorar su repercusión, filiar la etiología con pruebas complementarias (endoscopia, angioTAC, fibrobroncoscopia), determinar las causas facilitadoras (trombocitopenia, déficit de factores, enfermedad de von Willebrand adquirida) y utilizar test (tromboelastograma o ROTEM) que guíen la terapia transfusional.
La hemólisis es frecuente con una incidencia variable entre dispositivos. La determinación de la hemoglobina libre es la prueba más específica para el diagnóstico. También se sospecha por el aumento de LDH, la disminución de haptoglobina, la anemización con ascenso de bilirrubina y los esquistocitos y hemoglobinuria. Se debe realizar un tratamiento etiológico (hipovolemia, malposición del dispositivo, existencia de trombos en el SCM) y prevenir las consecuencias de su aparición (hidratación y alcalinización urinaria con un pH urinario >6,5 a 7).
RenalesEl FRA se define como la elevación de creatinina tras el inicio de la ECMO o por la necesidad terapia de reemplazo renal (TRR), y su prevalencia oscila entre el 24-63%. Para su manejo, se recomienda el uso de diuréticos en casos de sobrecarga de volumen, la TRR y monitorizar los niveles plasmáticos de fármacos (antibióticos, etc.) con capacidad nefrotóxica74. En caso de aplicación de TRR, hasta un 50% de los pacientes, puede aplicarse a través de un catéter propio, o bien conectar, si lo permite, al circuito del SCM. En el caso de ECMO, hay múltiples opciones de conexión, se debe conocer sus ventajas e inconvenientes ajustándola a cada caso.
Distensión ventricular izquierdaEn los pacientes en SC, con una función del VI severamente deprimida, en ocasiones es insuficiente para eyectar la sangre de la circulación pulmonar. Este fenómeno se puede agudizar si existe un incremento de la poscarga secundaria a la presencia de un SCM paralelo (ECMO VA) o el uso de drogas vasoactivas. Éste produce una disminución del gasto del VI, un aumento de la PTDVI, un incremento de la presión capilar pulmonar con edema agudo de pulmón (EAP) y hemorragia pulmonar. A su vez, la imposibilidad de apertura de la válvula aórtica favorece la formación de trombos intracardiacos y en raíz aórtica. Por último, el deterioro de la oxigenación con aporte de sangre mal oxigenada a la circulación cerebral y coronaria puede producir deterioro neurológico y mayor disfunción miocárdica75.
La descarga óptima del VI es fundamental para la recuperación del miocardio en el paciente en SC y supone una de las ventajas de determinados dispositivos (Impella®, Centrimag®, etc.) frente a la ECMO VA. Para su detección se deben considerar parámetros ecográficos (ventricular izquierdo dilatado, insuficiencia mitral grave), clínicos (EAP, arritmias) y/o hemodinámicos (presión del pulso <10mmHg, PCP>18mmHg) y en caso de aparición se debe tratar precozmente76.
Su manejo debe ser escalonado, comenzando con medidas no invasivas (ajuste del flujo de la ECMO, uso de inotrópicos, reducción de vasoactivos e incluso uso de vasodilatadores), seguido de medidas invasivas no activas (BCIAo) y finalmente activas (Impella® CP, septostomía percutánea, drenaje apical de VI) si las medidas anteriores son insuficientes76. La identificación del umbral óptimo para realizar la descarga y el mejor método siguen siendo controvertidos y la elección se suele basar experiencia y capacitación de cada centro. Se debe tener en cuenta que no está indicada la descarga de forma profiláctica y sistemática77.
Fallo respiratorioLa etiología del fallo respiratorio en pacientes con SCM puede ser multifactorial (edema pulmonar cardiogénico, embolismo pulmonar, lesiones relacionadas con la ventilación mecánica, SDRA secundario a patologías concomitantes) y su manejo va dirigido a tratarlas. En caso de SCM tipo Centrimag® se puede intercalar una membrana en el circuito y en caso de Impella® CP sería necesario escalar a un ECMO VA o incluso a ECMO VV60.
Síndrome arlequín o norte/surPropio de los pacientes con ECMO VA fémoro-femoral, con recuperación miocárdica y daño pulmonar establecido. Consiste en la diferencia de oxigenación del hemicuerpo superior (hipoxémico) y el inferior (normoxigenado) y puede tener importantes consecuencias para la perfusión orgánica sobre todo cerebral. La prevalencia varía entre un 8,8 y un 13,3% según los estudios y su detección se puede realizar mediante el NIRS cerebral o la pulsioximetria diferencial. Para su manejo se puede puntualmente aumentar el flujo de la bomba hasta resolver la causa y/o optimizar la ventilación mecánica. En casos refractarios se puede añadir una cánula de retorno en conexión en «Y» a yugular (V-VA) o en la arteria axilar (V-AA), cambiar de tipo de configuración periférica (femoro-femoral a femoro-axilar) o pasar de periférica a central78.
Fallo ventrículo derechoEl fallo del VD en pacientes con DAV/SCM supone un desafío diagnóstico y terapéutico79. Si existe desde el inicio del SC (miocarditis, rechazo injerto, infarto del VD) de manera general estaría indicada una ECMO VA ya que proporciona un soporte biventricular. En casos de SC con SCM izquierdo, puede aparecer o agravarse tras su implante al aumentar la precarga del VD. Otra causa de aparición de disfunción derecha es la trombosis o el tromboembolismo pulmonar. El manejo implica una vigilancia hemodinámica y ecocardiográfica, se puede beneficiar de la administración de inotropos y/o vasodilatadores pulmonares (óxido nítrico inhalado) y, en casos refractarios a el implante de un SCM derecho (Impella® RP, etc.) o su paso a SCM global80.
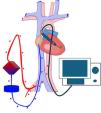
DesescaladaEl uso de SCM en situaciones en SC tiene como objetivo la estabilización del paciente hasta la resolución de la causa o la instauración un tratamiento definitivo. En este momento se debe plantear la retirada o desescalada del dispositivo60. Para la decisión de retirada, se deben evaluar diferentes parámetros que determinan una mayor probabilidad de destete y aunque cada centro suele tener su propio protocolo, todos incluyen una situación clínica mínima y una prueba de retirada previa 80. En caso de no darse la situación clínico/hemodinámica que permita la desconexión del SCM, se debe plantear la escalada a otro dispositivo de mayor duración o, incluso, en ausencia de contraindicaciones, el trasplante cardiaco. En caso de disfunción multiorgánica (>2 órganos) y/o nula probabilidad de recuperación clínica, se debería plantear la adecuación de medidas o la retirada del SCM previo al planteamiento de la posibilidad de donación de órganos y/o tejidos (fig. 3).
Algoritmo de retirada del soporte circulatorio mecánico en pacientes con shock cardiogénico. BCIAo: balón de contrapulsación intraaórtico; CW: potencia cardiaca; DMO: disfunción multiorgánica; ECMO VA: oxigenación con membrana extracorpórea; FAC: fracción de acortamiento; FEVI: fracción de eyección de ventrículo izquierdo; IC: índice cardiaco; IVT: integral velocidad tiempo; LTSV: limitación de terapia de soporte vital; LVAD: asistencia ventricular izquierda de larga duración; PAM: presión arterial media; PAPi: pulmonary artery pulsatility index; PAS: presión arterial sistólica; PCP: presión capilar pulmonar; PD: presión diferencial; PVC: presión venosa central; SC: shock cardiogénico; SCM: soporte circulatorio mecánico; SvO2: saturación venosa de oxígeno; TAPSE: desplazamiento sistólico del plano del anillo tricúspideo; TSVI: tracto de salida del ventrículo izquierdo; TxC: trasplante cardiaco; VD: ventrículo derecho; VI: ventrículo izquierdo.
*: Si ECMELLA, retirar primero ECMO y después Impella® CP.
Los SCM constituyen una herramienta terapéutica imprescindible y pese a su reducida evidencia, han supuesto un salto en el manejo del SC refractario. Su uso requiere una evaluación clínica y hemodinámica avanzada que permita establecer el momento y el tipo de soporte más adecuado. El curso clínico de estos pacientes es variable y no exento de complicaciones, requiere una evaluación multidisciplinar y una constante reevaluación de su uso e indicación. Son necesarios más estudios que aclaren múltiples aspectos del uso de los SCM en el paciente con SC, siendo los cuidados intensivos un pilar esencial a evaluar y desarrollar.
AutoríasLMV, AAG, JMGJ, JLPV y MPFG diseñaron el estudio, realizaron la revisión de la literatura y escribieron el manuscrito. LMV, JMGJ, AAG, JLPV y MPFG participaron en la diseño de tablas y en el diseño de figuras.
LMV, MPFG, JLPV, JMGJ y AAG revisaron la versión final del manuscrito.
Todos los autores leyeron y revisaron el manuscrito final.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.