La lesión medular traumática precisa una acción multidisciplinar, tanto para el tratamiento especializado de la fase aguda como para las complicaciones secundarias. La sospecha y/o el diagnóstico de una lesión medular es el primer paso para establecer un tratamiento correcto.
En esta revisión se aborda el manejo en la fase prehospitalaria y los aspectos característicos de la fase aguda. La monitorización respiratoria para una intubación selectiva precoz, la identificación y el tratamiento correcto del shock neurogénico son fundamentales para la prevención del daño medular secundario. En la actualidad el uso de esteroides no es un estándar en el tratamiento neuroprotector, siendo el control hemodinámico y la descompresión quirúrgica precoz pilares fundamentales.
La lesión medular traumática generalmente se presenta en el contexto de un politraumatismo que puede dificultar el diagnóstico. El examen neurológico y la selección adecuada de pruebas radiológicas evitan que pase desapercibida la lesión medular y otras lesiones asociadas, y ayudan a establecer el pronóstico.
Traumatic spinal cord injury requires a multidisciplinary approach both for specialized treatment of the acute phase and for dealing with the secondary complications. A suspicion or diagnosis of spinal cord injury is the first step for a correct management.
A review is made of the prehospital management and characteristics of the acute phase of spinal cord injury. Respiratory monitoring for early selective intubation, proper identification and treatment of neurogenic shock are essential for the prevention of secondary spinal cord injury. The use of corticosteroids is currently not a standard practice in neuroprotective treatment, and hemodynamic monitoring and early surgical decompression constitute the cornerstones of adequate management.
Traumatic spinal cord injury usually occurs as part of multiple trauma, and this can make diagnosis difficult. Neurological examination and correct selection of radiological exams prevent delayed diagnosis of spinal cord injuries, and help to establish the prognosis.
La lesión medular (LM) traumática es un problema neurológico devastador cuyo manejo requiere recursos sanitarios importantes, debido a que precisa una acción coordinada y multidisciplinar, no solo para el tratamiento altamente especializado de la fase aguda, sino también para las complicaciones secundarias asociadas que surgen a largo plazo1.
La incidencia mundial de la LM traumática es muy variable; aunque en 2007 se calculó una incidencia global de 2,3 casos/100.000 habitantes2, existe un amplio rango en la literatura publicada. En España, en concreto, los estudios epidemiológicos existentes son escasos, con cifras globales que oscilan entre 0,8 y 2,3 casos/100.000 habitantes3,4.
La LM traumática puede dar lugar a un espectro de problemas neurológicos, incluyendo la pérdida de la función motora y sensorial, intestino y disfunción de la vejiga, espasticidad, dolor neuropático y disreflexia autonómica.
La LM traumática aguda implica mecanismos primarios y secundarios de lesión. El mecanismo primario está relacionado con el daño mecánico inicial, debido a la deformación local y la transformación de energía que ocurre en la médula espinal en el momento de la lesión, y esta lesión es irreversible. Los mecanismos secundarios de lesión ocurren después del evento traumático inicial y conducen a la destrucción tisular durante las primeras horas tras la lesión. Estos mecanismos secundarios incluyen procesos tales como isquemia, degeneración axonal, disfunción vascular, estrés oxidativo, excitotoxicidad, desmielinización e inflamación que conducen a muerte celular, y son potencialmente prevenibles y/o reversibles. Este concepto es clave en el desarrollo de estrategias protectoras dirigidas a mejorar el pronóstico de los pacientes con LM traumática aguda.
Atención prehospitalaria y trasladoLas lesiones en la columna y en la médula generalmente se asocian con traumatismos de alta energía como accidentes de tráfico o caídas de altura, pero en personas mayores o con enfermedades previas en la columna se puede producir una LM con traumatismos poco importantes. La valoración inicial en la escena del accidente se realizará siguiendo la secuencia habitual de ABCDE. La protección de la columna es importante, pero no más que el manejo de la vía aérea, el control de la hemorragia y otros cuidados críticos.
Una exploración neurológica básica, observando la capacidad para movilizar las 4 extremidades (incluyendo las manos y los pies), ayuda al diagnóstico, sobre todo si el paciente precisa una intubación precoz. La presencia de algunos signos clínicos puede hacer sospechar LM aguda (tabla 1).
Signos de sospecha de lesión medular
| Debilidad o parálisis de extremidades |
| Alteraciones de la sensibilidad en tronco o en extremidades |
| Dificultad en la emisión del lenguaje (hipofonía) |
| Respiración abdominal |
| Hipotensión y bradicardia paradójica |
| Posición en flexión de codos |
| Dolor o deformidad en columna |
| Parestesias. Sensación de descarga eléctrica |
| Ausencia de dolor en presencia de lesiones previsiblemente dolorosas |
| Priapismo |
En la inmovilización de los pacientes traumáticos en la actualidad se aboga por una inmovilización selectiva, identificando quienes se beneficiarán de ella5-7. Los dispositivos utilizados se asocian con complicaciones como incremento de la presión intracraneal, dificultad para el abordaje de la vía aérea, restricción de la función pulmonar, dolor, agitación, úlceras por presión y prolongación del tiempo de traslado. La utilización de un collarín no limita completamente la movilidad en la columna cervical. Cuando se sospecha una lesión vertebral toda la columna debe ser inmovilizada, ya que la presencia de otra lesión vertebral no contigua se produce hasta en el 20% de los pacientes8. Aunque no está avalada por niveles altos de evidencia9,10 e incluso puede tener efectos negativos, la recomendación de inmovilización de pacientes con sospecha de lesión vertebro-medular se basa en consideraciones anatómicas, mecánicas y clínicas, en un intento de prevenir el desarrollo o el agravamiento de LM en presencia de una lesión vertebral inestable11.
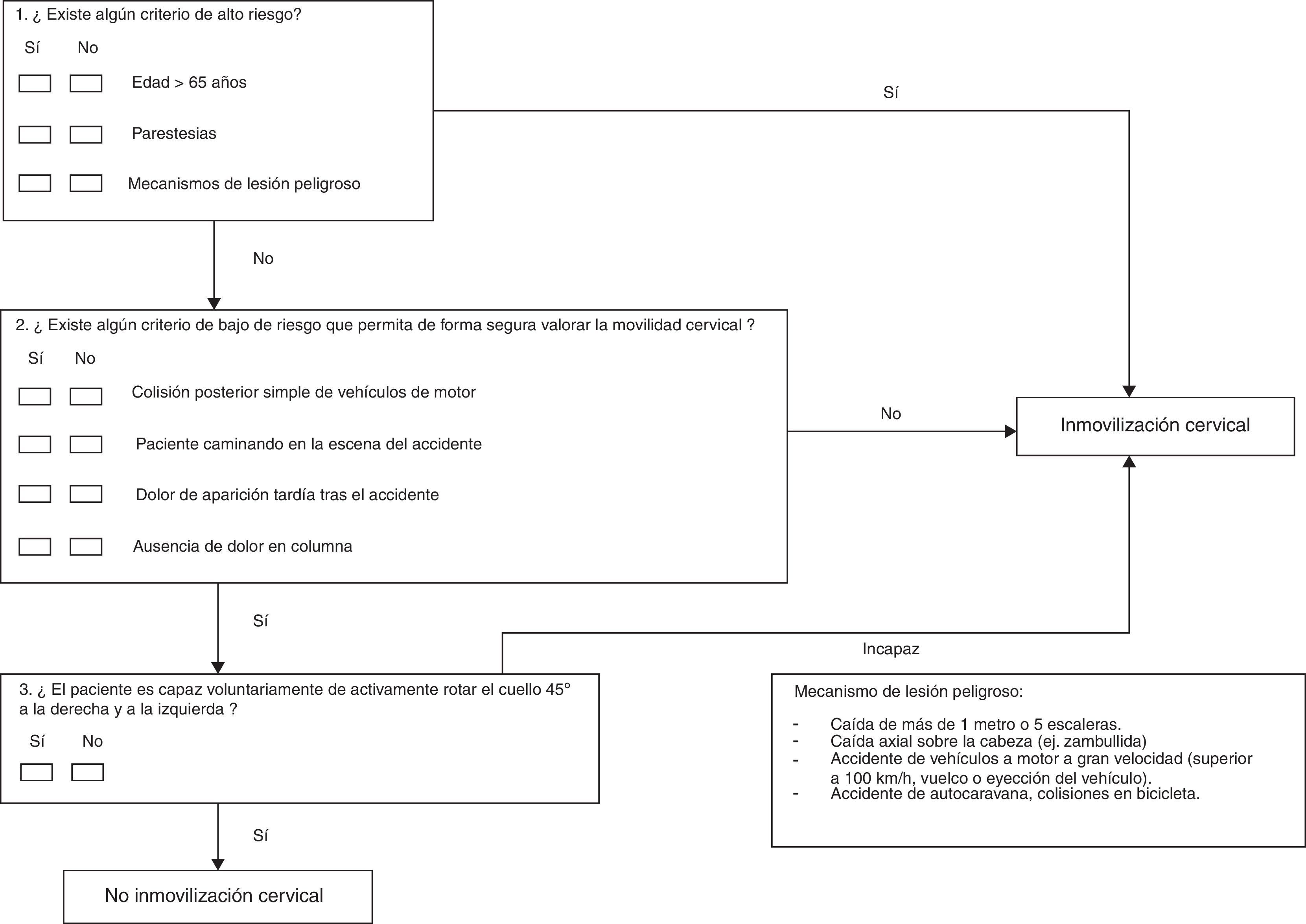
En los pacientes con trauma penetrante, sin síntomas neurológicos, la inmovilización no está indicada6,7,12. Para los pacientes con traumatismo cerrado se han desarrollado algoritmos con la intención de evitar la inmovilización indiscriminada13-16. Los criterios más utilizados en la emergencia extrahospitalaria son los propuestos por el National Emergency X-Radiography Utilization Study (NEXUS)14 y la Canadian C-Spine Rule (CCSR)15. El NEXUS establece 5 criterios de bajo riesgo que, si se cumplen, podrían excluir lesión cervical (tabla 2); el CCSR combina criterios de alto y bajo riesgo y la capacidad para rotar la cabeza 45°; el paciente está exento de riesgo y, por tanto, no requerirá inmovilización si presenta un criterio de bajo riesgo y además es capaz de voluntariamente rotar la cabeza 45°17 (tabla 3). Estos —o similares— algoritmos de inmovilización han sido incorporados a los protocolos de actuación de equipos de emergencia a nivel mundial5,17-21. La guía National Institute for Health and Care Excellence (NICE) de valoración y manejo de las lesiones en columna favorece los criterios CCSR en la valoración de la columna cervical, pero en sus indicaciones de inmovilización combina criterios NEXUS y CCSR. Aunque hay consenso en que debe aplicarse un algoritmo de inmovilización selectiva, no hay un acuerdo en cuál es el más apropiado. La Faculty of Pre-Hospital Care elaboró en el Reino Unido un documento de consenso, y sugiere que un algoritmo similar al propuesto por el NEXUS podría ser apropiado, pero este está todavía por determinar6. Aspectos discutidos en la literatura son la inclusión del mecanismo de lesión como criterio de riesgo, si deben aplicarse algoritmos diferentes en pacientes conscientes e inconscientes, y qué pacientes pueden autorrescatarse6,22,23.
El método habitual de inmovilización consiste en la utilización de una tabla espinal con correas y fijación de la cabeza junto con collarín cervical7,24. Sin embargo esta práctica, estándar para muchos equipos de emergencia, está cambiando. Los métodos de inmovilización pueden ser diferentes durante el rescate, la recogida y el transporte, y pueden ser modificados según la situación clínica del paciente, dando prioridad al ABC. En la atención al paciente traumático, maniobras de protección de la columna deben ser la norma hasta que pueda realizarse una evaluación clínica. Los dispositivos de inmovilización pueden ser difíciles de colocar en personas con determinadas características físicas (cuello corto o deformidad en la columna), que no colaboran o están agitadas, y además consumen tiempo en su aplicación. En estas circunstancias, y cuando es necesario un «rescate» rápido, se puede mantener una inmovilización manual en línea6,21 y posteriormente colocar un collarín cervical de talla adecuada si está indicado. Las movilizaciones se realizarán intentando mantener el eje vertebral, mediante tracción en línea de la columna cervical y evitando deformidades de la columna y el movimiento de cabeza y cuello. El método High Arm In Endangered Spine (HAINES), o el HAINES modificado, es más recomendado en la actualidad que el clásico «log-roll», ya que ocasiona menos movilidad en la columna25. La tabla espinal larga, el dispositivo de rescate de Kendricks y la camilla de tijera pueden también ser utilizados durante el rescate. La National Association of EMS Physicians y el American College of Surgeons Committee on Trauma limitan la utilización del tablero espinal a determinadas situaciones23, y es considerado como un dispositivo de «rescate», no de transporte6. Para el transporte, el colchón de vacío en combinación con collarín proporciona una inmovilización similar o superior a la tabla espinal y es más confortable21,26; el transporte también puede realizarse con seguridad en la camilla de la ambulancia, fijando correctamente al paciente con correas junto con collarín cervical23. En niños, debido a la desproporción de la cabeza con el cuerpo, y en personas con deformidad en cifosis de la columna, puede ser necesario añadir un almohadillado para respetar su postura y evitar deterioro neurológico. Las movilizaciones y transferencias se limitarán en la medida de lo posible, por lo que es importante disponer de material de inmovilización de intercambio entre el medio prehospitalario y el hospitalario.
La sospecha o el diagnóstico de una LM, junto con el traslado seguro a un centro hospitalario, es el primer paso para establecer un tratamiento correcto. Si existe compromiso vital, la derivación se realizará al hospital más cercano y en cuanto sea posible se derivará a un centro con atención especializada en LM (preferiblemente en las primeras 24h). La elección del medio de transporte dependerá de los medios de que se disponga, de la estabilidad del paciente y de la distancia al centro hospitalario27. No necesariamente hay que utilizar transporte aéreo, aunque puede recomendarse para distancias superiores a 80km28.
ABC y resucitaciónEn el entorno hospitalario deben continuarse las medidas de inmovilización y de apoyo vital y se realizarán los estudios radiológicos y los tratamientos específicos. El tratamiento de situaciones con riesgo vital es prioritario sobre cualquier estudio radiológico.
Como en todo paciente traumático, el manejo agudo de un paciente con LM requiere asegurar la vía aérea, la respiración y la circulación.
Vía aérea y respiraciónLa monitorización continua del fallo respiratorio es necesaria en todos los pacientes con LM cervical29. En las lesiones de C1-C2 no hay musculatura respiratoria eficaz. Las lesiones de C3-C4 producen parálisis frénica bilateral y la ventilación es dependiente de los músculos accesorios. Por tanto, los pacientes con lesión motora completa por encima de C5 casi invariablemente necesitarán soporte ventilatorio. Los pacientes tetrapléjicos con adecuada ventilación a costa de un importante trabajo respiratorio deben ser intubados y conectados a ventilación mecánica sin demora. Las lesiones por debajo de C5 producen parálisis de la musculatura intercostal y abdominal, y la mayoría necesitarán soporte respiratorio.
La pérdida de la capacidad respiratoria ocurre por agotamiento de la musculatura implicada en el proceso ventilatorio, hemorragia o edema medular ascendente, acúmulo de secreciones, atelectasias, otros traumas asociados u otras condiciones del paciente. Lesiones inferiores a T5 no suelen producir insuficiencia respiratoria de origen neuromuscular.
El edema pulmonar secundario a LM traumática puede ser cardiogénico (por altos niveles de catecolaminas y beta-endorfinas) y/o no cardiogénico (hiperpermeabilidad pulmonar). Estudios ecocardiográficos y los nuevos dispositivos de evaluación cardiopulmonar pueden ser de ayuda para conocer el mecanismo predominante. El tromboembolismo pulmonar y las neumonías pueden ser complicaciones que suelen presentarse después de las primeras 24h.
La intubación endotraqueal puede ser particularmente difícil en pacientes con LM cervical. El procedimiento a veces es necesario antes de confirmar la lesión y su localización, por lo que si un paciente requiere ser intubado tras un trauma, debe ser manejado como si tuviese una LM cervical, asegurando la vía aérea con el mínimo movimiento posible de la columna cervical. La técnica de intubación de urgencia ante una lesión sospechada o conocida de la columna cervical debe realizarse con una secuencia de inducción rápida (para reducir la tos y los movimientos espontáneos) con estabilización de la columna con tracción manual en línea24. La tracción debe ser cuidadosa para evitar distracción, sobre todo en lesiones de la unión occipitocervical. En pacientes con inmovilización cervical, la utilización del dispositivo Airtraq reduce el riesgo de fallo30. Hay una falta de evidencia de la utilidad de otros dispositivos de intubación.
Si no es preciso inicialmente asegurar la vía aérea ni el soporte ventilatorio, debe monitorizarse la necesidad de intubación a través de la PCO2 y la espirometría con medición de la capacidad vital (que tiene una excelente correlación con otras pruebas de función pulmonar) y la presión inspiratoria máxima (PImax)31,32. Esto supone una evaluación sencilla y global de la fuerza de la musculatura inspiratoria y son los mejores marcadores a pie de cama. En términos generales, la PImax estima la fuerza de los músculos inspiratorios (diafragma), se consigue a volumen residual y con el mayor esfuerzo inspiratorio. El fallo ventilatorio ocurre con más frecuencia tras el cuarto día de la lesión, y esto es relevante de cara a la monitorización y a la consideración de mantener la intubación postoperatoria en pacientes con intervención quirúrgica precoz, especialmente en aquellos en los que se realizan procedimientos quirúrgicos cervicales.
Circulación: prevención y tratamiento de la hipotensiónLa resucitación adecuada y precoz con fluidos es prioritaria en el tratamiento de la hipotensión, con el objetivo de mantener una perfusión adecuada y evitar el daño secundario del sistema nervioso central33. Se desconoce el objetivo de resucitación más apropiado y la presión arterial media (PAM) óptima para mantener la perfusión medular. Estudios no controlados que utilizaron fluidos y vasopresores para lograr una PAM de 85mmHg durante un mínimo de 7 días en pacientes con LM aguda han publicado resultados favorables34-36. Numerosos trabajos sostienen que debe identificarse la hipotensión, buscar la causa e iniciar resucitación con fluidos. Son necesarios más estudios para definir la PAM ideal y el papel de los fluidos y el soporte farmacológico en este objetivo.
El déficit de base inicial o el nivel de lactato pueden ser utilizados para evaluar el estado de shock y la necesidad de iniciar resucitación con fluidos37.
El shock neurogénico es frecuente en pacientes con LM aguda por encima de T638. Sin embargo, antes de asumir que la causa de la hipotensión es la LM, deben descartarse otras causas de inestabilidad hemodinámica en un paciente traumático, como son: hemorragia, neumotórax, daño miocárdico, taponamiento cardíaco, sepsis relacionada con lesión abdominal, insuficiencia suprarrenal, etc. El examen físico y los síntomas son poco sensibles en un paciente con LM, por lo que deben realizarse pruebas de imagen toraco-abdómino-pélvicas que permitan excluir otras posibles causas de hipotensión.
El shock neurogénico es secundario a la denervación simpática que conduce a la vasodilatación arterial y el secuestro de sangre en el compartimento venoso, y la interrupción de la inervación simpática cardíaca (T1-T4) con una actividad vagal sin oposición que promueve la bradicardia y reduce la contractilidad cardíaca. El shock neurogénico, por tanto, se caracteriza por una caída de la presión arterial y de las resistencias vasculares sistémicas con una respuesta de la frecuencia cardíaca variable. En todo politraumatizado con hipotensión y bradicardia se debe sospechar LM por encima de T6, especialmente si no hay signos de vasoconstricción periférica.
Estudios experimentales muestran que la hipotensión y la hipovolemia son perjudiciales para la médula espinal lesionada, contribuyendo a la hipoperfusión y perpetuando el daño secundario. Los niveles más altos de lesión se correlacionan con hipotensión más severa. Es esencial restaurar el volumen intravascular y, si es necesario, iniciar vasopresores36. Las bradi-disritmias pueden conducir a hipotensión y asistolia, y esto es más común en las primeras 2 semanas de la lesión. La hipoxia, las maniobras de manipulación laríngea o traqueal y la hipotermia exacerban la bradicardia. Se debe disponer de atropina siempre que se vaya a realizar una manipulación de la vía aérea en pacientes con LM cervical. La necesidad de agentes cronotrópicos (atropina, adrenalina, noradrenalina) o inhibidores de la fosfodiesterasa (aminofilina, teofilina) es más frecuente en pacientes con LM cervical. Los receptores β2 constituyen un objetivo atractivo para modular la actividad vagal y con ello aumentar la frecuencia cardiaca en ausencia de riesgos significativos39. El marcapasos cardíaco por bradicardia se reserva para los pacientes con bradicardia sintomática que no responden a tratamiento farmacológico.
TemperaturaEl sistema nervioso autónomo está interrumpido en lesiones por encima de T6, dando lugar a una alteración en la termorregulación debido a la incapacidad del hipotálamo para controlar la temperatura por pérdida del control vasomotor. Los pacientes pueden presentar hipotermia, así como incapacidad para disipar el calor corporal40. Monitorizar la temperatura es esencial durante el manejo de la fase aguda.
Diagnóstico de la lesión medular traumática agudaExploraciónLos efectos inmediatos de una LM completa incluyen pérdida de movimiento y sensibilidad por debajo del nivel de lesión. Además, se puede producir shock neurogénico, parálisis flácida de vejiga e intestino con retención urinaria e íleo paralítico, y afectación de todos los sistemas por debajo del nivel. También se produce, en su fase inicial, shock espinal, caracterizado por pérdida de la actividad refleja y flacidez infralesional; este periodo suele durar días o semanas; una vez superada esta fase, aparecerá la espasticidad.
El diagnóstico clínico comienza con el examen neurológico básico. Se debe evaluar, en la medida de lo posible, la pérdida de conciencia y el mecanismo de lesión. Si el paciente está consciente, es necesario realizar una valoración motora y sensitiva detallada. Sin embargo, tal valoración con frecuencia no es posible en un paciente politraumatizado, que además puede estar sedado o intubado. Por ello, es aconsejable ante estas circunstancias tratar al paciente como si tuviese una lesión vertebromedular; en la tabla 1 se detallan los signos de alarma que en el examen inicial pueden hacer sospechar su presencia.
El examen neurológico se realiza de acuerdo con los Estándares Internacionales para la Clasificación Neurológica de la Lesión Medular Espinal (http://asia-spinalinjury.org/wp-content/uploads/2016/02/International_Stds_Diagram_Worksheet.pdf) de la American Spinal Injury Association (ASIA) y de la International Spinal Cord Society41. Este sistema describe el nivel y la extensión de la lesión basándose en una exploración sistemática de las funciones sensitiva y motora. Además de tener valor pronóstico, esta exploración mediante la escala ASIA sirve para la monitorización de la evolución neurológica. Así, tenemos protocolizado realizar esta exploración al ingreso, a las 72h, al mes y al alta, y también ante determinadas situaciones ante las que se pueda sospechar un deterioro de la LM. La tabla 4 recoge definiciones básicas de términos usados en la valoración de la LM.
Definiciones de los términos básicos y clasificación ASIA
| Tetraplejia | Pérdida de función motora y/o sensitiva en los segmentos cervicales de la médula espinal por daño de los elementos neurales dentro del canal espinal. Origina trastorno de la función en brazos, tronco, piernas y órganos pélvicos |
| Paraplejia | Pérdida de función motora y/o sensitiva en los segmentos torácico, lumbar o sacro de la médula espinal por daño de los elementos neurales dentro del canal espinal. Origina trastorno de la función en tronco, piernas y órganos pélvicos |
| Dermatoma | Área de piel inervada por los axones sensitivos de cada nervio segmentario (raíz) |
| Miotoma | Músculo inervado por los axones motores de cada nervio segmentario (raíz) |
| Nivel motor | El grupo muscular llave más caudal cuyo balance muscular es 3/5 o más, siempre y cuando el balance muscular de los músculos llave por encima sea 5/5 |
| Nivel sensitivo | Dermatoma más caudal con sensibilidad algésica y táctil ligera normales en ambos lados del cuerpo |
| Nivel neurológico de lesión | Nivel más caudal en el que la función motora y sensitiva son normales |
| Nivel esquelético | Nivel en el que, por la radiología, se encuentra el mayor daño vertebral |
| Índice motor | Suma de las puntuaciones de la función motora (máximo 100) |
| Índice sensitivo | Suma de las puntuaciones de cada dermatoma; se valoran 28 dermatomas en cada hemicuerpo, con un total de 112 para el dolor y 112 para el tacto |
| Lesión completa | Ausencia de función motora y sensitiva en los segmentos sacros inferiores (S4-S5) |
| Lesión incompleta | Preservación de la función motora y/o sensitiva por debajo del nivel neurológico incluyendo los segmentos sacros S4-S5 |
| Zona de preservación parcial (ZPP) | Se refiere a dermatomas o miotomas por debajo del nivel neurológico que permanecen parcialmente inervados; el segmento más caudal con alguna función motora o sensitiva define la extensión de la zona de preservación parcial; solo en lesiones completas |
| Clasificación ASIA | |
| A: lesión completa | Ausencia de función motora y sensitiva que se extiende hasta los segmentos sacros S4-S5 |
| B: incompleta sensitiva | Preservación de la función sensitiva que se extiende hasta los segmentos sacros S4-S5 y con ausencia de función motora |
| C: incompleta motora | Preservación de la función motora por debajo del nivel neurológico y más de la mitad de los músculos por debajo del nivel neurológico tienen un balance muscular menor de 3 |
| D: incompleta motora | Preservación de la función motora por debajo del nivel neurológico y al menos la mitad de los músculos por debajo del nivel neurológico tienen un balance muscular mayor o igual a 3 |
| E: normal | Las funciones motora y sensitiva son normales en todos los segmentos |
Para el examen sensitivo se exploran 28 dermatomas en cada hemicuerpo (C2 a S4-S5, considerando este como un único dermatoma). En cada uno se valora la sensibilidad algésica (pinchazo de aguja) y táctil superficial (roce de algodón) según una escala de 3 puntos (0=ausente, 1=deterioro, 2=normal). Además se valora la sensación anal profunda mediante tacto rectal, registrándola como presente o ausente.
Se explora el balance muscular en 5 grupos musculares llave en el miembro superior y en 5 en el miembro inferior, en cada hemicuerpo. Se valora en una escala de 0 a 5, de acuerdo a la graduación del Medical Research Council. En el miembro superior se valora: flexión de codo (C5), extensión de carpo (C6), extensión de codo (C7), flexión de dedos (C8) y abductores del 5.° dedo (T1). En el miembro inferior se incluyen: flexión de cadera (L2), extensión de rodilla (L3), dorsiflexión de tobillo (L4), extensión de 1.er dedo (L5) y flexión plantar de tobillo (S1). Como parte del examen motor se valorará la contracción voluntaria del esfínter anal externo mediante tacto rectal, registrándola como ausente o presente.
El nivel sensitivo es el dermatoma intacto más caudal para ambas sensibilidades (tacto y dolor). El nivel motor se define por el músculo llave más caudal con un grado muscular de al menos 3, siempre y cuando los músculos llave por encima de ese nivel estén intactos (grado muscular 5); en las regiones donde no hay miotoma para valorar, el nivel motor se considera el mismo que el sensitivo.
El nivel neurológico de la lesión se refiere al segmento más caudal de la médula en el que las funciones sensitiva y motora son normales en ambos lados. Es el más cefálico de los niveles sensitivo y motor.
Escala de discapacidad ASIALas LM generalmente se clasifican como «completas» o «incompletas», basándose en la presencia de preservación sacra. Esta se refiere a la presencia de función sensitiva o motora en los segmentos sacros más caudales (preservación de tacto ligero o dolor en S4-S5, sensación anal profunda o contracción voluntaria del esfínter anal).
Una lesión completa se define como la ausencia de preservación sacra (función sensitiva o motora en los segmentos S4-S5), mientras que una lesión incompleta se define como la presencia de preservación sacra (alguna preservación sensitiva o motora en S4-S5).
La escala ASIA consta de 5 grados (tabla 4). El gradoA corresponde a una LM completa; los gradosB, C yD son lesiones incompletas de diferentes grados, y el gradoE indica una función sensitiva y motora normales (este grado se aplica siempre y cuando el paciente haya tenido algún grado de afectación medular que se ha recuperado).
Síndromes clínicos- •
Centromedular. Es el más frecuente de las lesiones incompletas. Caracterizado por mayor debilidad motora en miembros superiores que en inferiores, trastornos esfinterianos y grados variables de afectación sensitiva. Más frecuente en personas con cambios degenerativos vertebrales previos que sufren un mecanismo de hiperextensión42.
- •
Brown-Sèquard (hemisección medular). Cursa con parálisis y pérdida de sensibilidad profunda ipsilateral a la lesión y afectación contralateral de la sensibilidad termoalgésica. La hemisección pura es rara en LM traumática, combina síntomas de Brown-Sèquard y centromedular (síndrome de Brown-Sèquard plus).
- •
Medular anterior. Puede ocurrir por lesión directa de la parte anterior de la médula por retropulsión de un fragmento óseo o discal, o por lesiones de la arteria espinal anterior. Cursa con parálisis y afectación de la sensibilidad termoalgésica, con preservación de los cordones posteriores (tacto ligero y sensibilidad posicional).
- •
Cono medular. Lesión de médula sacra (cono) y de las raíces nerviosas lumbares dentro del canal neural. Produce parálisis de vejiga, intestino y miembros inferiores. Dependiendo del nivel, puede manifestarse como un cuadro mixto de motoneurona superior e inferior.
- •
Cola de caballo. Lesión de las raíces lumbosacras por debajo del cono medular dentro del canal neural. Su clínica es similar a la lesión de cono medular, del que puede ser difícil de distinguir.
La exploración radiológica en el diagnóstico de la LM traumática dependerá de las circunstancias del trauma, de la necesidad de realizar pruebas para el diagnóstico de lesiones asociadas y de las técnicas disponibles en cada centro.
Existen protocolos clínicos, recogidos en las guías de la Eastern Association of Trauma39, que permiten descartar lesiones de columna cervical en pacientes asintomáticos sin realizar estudios de imagen. Los criterios NEXUS14 y CCSR15 son muy sensibles para descartar lesiones cervicales significativas sin realizar estudios radiológicos. Los pacientes con dolor en columna, síntomas neurológicos y pacientes traumatizados inconscientes requieren evaluación radiológica. En los casos con lesiones asociadas encubridoras o alteración de consciencia de corta duración se puede optar por medidas de protección espinal hasta que se realice el tratamiento de estas lesiones o la recuperación del nivel de consciencia permita una valoración clínica adecuada, pero si la urgencia lo impone han de ser evaluados bajo los mismos criterios que el paciente politraumatizado inconsciente43.
En pacientes que precisan estudios radiológicos se recomienda estudio radiológico de toda la columna, ya que la incidencia de fracturas vertebrales múltiples se aproxima al 20%8. Tradicionalmente se realizaba radiología simple con proyecciones anteroposterior y lateral de toda la columna y, además, transoral en columna cervical. La tendencia actual es a realizar TAC con reconstrucción sagital y coronal44. La TAC helicoidal, aunque más cara, es más sensible y específica que la radiología convencional44,45: permite la identificación más fácil de fracturas que pueden pasar desapercibidas en la radiología simple, visualiza correctamente la uniones occipitocervical y cervicotorácica, proporciona una visualización completa de toda la columna con reconstrucciones que permiten caracterizar mejor la invasión de canal, y facilita información con vistas al tratamiento quirúrgico. Los estudios en flexión y extensión de radiografía simple son útiles para valorar inestabilidad secundaria a lesión ligamentosa, pero deben evitarse en la fase aguda de pacientes con déficit neurológico.
En el politraumatizado agudo habitualmente es difícil realizar una resonancia magnética (RM) de urgencia. La RM urgente está indicada en la LM traumática en la que los déficits neurológicos no se explican por los hallazgos radiológicos, o cuando se produce un deterioro neurológico para descartar la presencia de hematoma epidural u otra causa subsidiaria de tratamiento quirúrgico urgente. En el momento en que la situación clínica lo permita, se debe realizar una RM, porque es la prueba que puede detectar lesiones de tejidos blandos y ligamentos en el seno de la lesión neurológica, y además puede caracterizar adecuadamente el tipo de LM (contusión, edema, hemorragia, sección medular), complementando dicha información la evaluación clínica del ASIA para poder establecer el pronóstico de la LM. En pacientes con sección medular o hemorragia intramedular la recuperación neurológica generalmente será escasa o nula, y en aquellos con contusión o edema medular la recuperación puede ser mayor46,47. Además, la RM permite evaluar el compromiso del canal, el grado de compresión medular y la longitud de la lesión, siendo factores también importantes para predecir la severidad del daño y la recuperación48,49.
Valoración de lesiones asociadasEl mecanismo de LM puede ser el resultado de fuerzas de alta o baja intensidad. Son los traumatismos con alta energía los que se asocian con más frecuencia con lesiones a otro nivel, y en cerca del 37% de los casos los pacientes presentan fracturas múltiples50,51. El tipo de lesión asociada al traumatismo medular varía en función del nivel de la lesión, siendo más frecuente el traumatismo craneoencefálico en lesiones cervicales y el traumatismo toracoabdominal cuando la lesión es dorsal52.
En los pacientes con sospecha o confirmación de LM, al igual que en todo paciente traumatizado, debe realizarse una evaluación terciaria del traumatismo con el fin de disminuir la incidencia de lesiones no detectadas, ya que la exploración física puede estar interferida por el nivel de la lesión al existir alteraciones tanto de la sensibilidad como de la motilidad53,54. Es decir, tras la resucitación inicial es prioritario identificar y catalogar todas las lesiones. Para ello será necesario repetir la exploración física completa, evaluar el mecanismo de la lesión, las características basales (edad, comorbilidad y predisposición genética) y el nivel de LM55. Se completa con exámenes de laboratorio, la revisión de los estudios de imagen por expertos y la realización de estudios complementarios ante nuevos hallazgos clínicos. La valoración es tiempo-dependiente: se aconseja hacerla en las primeras 24h tras el traumatismo y repetirla cuando el paciente sea capaz de comunicarse53,54.
Las principales consideraciones en la valoración clínica de las lesiones asociadas son:
- a.
Documentar la presencia de traumatismo craneoencefálico, sobre todo en lesiones cervicales, para realizar una correcta evaluación neurológica y planificar la rehabilitación. Deberá realizarse precozmente mediante Escala de Coma de Glasgow (GCS)56.
- b.
Las lesiones toracoabdominales asociadas se buscarán en todos los pacientes con LM mediante imagen. La primera aproximación diagnóstica en el paciente inestable será realizando la ecografía Focused Abdominal Sonography for Trauma (FAST), aunque siempre que la situación clínica lo permita o si la ecografía es positiva es de elección la TAC57,58.
- c.
En las fracturas a nivel de extremidades-pelvis lo más importante es la estabilización precoz con el fin de mantener un buen rango de movilidad y facilitar la rehabilitación59.
- d.
En los impactos de muy alta energía tenemos que descartar lesiones aórticas, y si se añade la presencia de fractura/luxación a nivel cervical (fundamentalmente a nivel C1-3) debemos descartar lesiones vasculares cerebrales mediante angioTAC/RM60,61.
Junto con la evaluación terciaria del paciente con LM es necesario cuantificar la gravedad y estimar la probabilidad de supervivencia mediante escalas de gravedad del traumatismo, para facilitar la toma de decisiones y disminuir la morbimortalidad62,63. Las escalas traumatológicas deben valorar lesión anatómica, cambios fisiológicos que se producen y reserva funcional del paciente64,65.
Se han desarrollado múltiples escalas que se agrupan en función de diferentes aspectos (escalas anatómicas, fisiológicas y combinadas). En el paciente con LM se encuentran, dentro de las escalas más ampliamente citadas y utilizadas, el Injury Severety Score66, el Trauma Score Revised67 y el TRISS68, que junto con la inclusión de la GCS proporcionan una evaluación completa determinando qué pacientes podrían beneficiarse de la rehabilitación, y ayudan a optimizar los recursos. Además, en la valoración de los pacientes traumatizados con LM que ingresan en la UCI las escalas fisiológicas Acute Physiology and Chronic Health Evaluation (APACHE) y Secuential Organ Failure Assesment (SOFA) están validadas para predecir el pronóstico69,70.
En la valoración de lesiones asociadas del paciente medular es fundamental una adecuada valoración terciaria y establecer un pronóstico funcional mediante la combinación de diferentes escalas al no existir una escala universalmente aceptada.
NeuroprotecciónLos tratamientos actuales incluyen la descompresión quirúrgica, el control hemodinámico, y metilprednisolona en casos seleccionados. Sin embargo, estos tratamientos precoces se asocian a una modesta recuperación funcional.
La búsqueda de una estrategia neuroprotectora eficaz para prevenir la lesión secundaria en el ámbito de la LM traumática aguda sigue siendo una prioridad tanto en clínica como en investigación básica.
Los corticoides formaban parte del arsenal terapéutico inicial. La metilprednisolona se cree que actúa reduciendo la peroxidación de membranas y disminuyendo la inflamación. Tiene un efecto inmunomodulador inhibiendo la infiltración de neutrófilos y macrófagos en la médula espinal, lo que podría mejorar los resultados funcionales. Se han hecho 3 ensayos clínicos y otros estudios no aleatorizados, con importantes limitaciones, para estudiar el uso de metilprednisolona tras la LM traumática71-73. Teniendo en cuenta la evidencia actual, no se recomienda la administración de dosis altas de metilprednisolona en la LM traumática de forma generalizada74,75, de modo que su administración debe ser sopesada cuidadosamente en cada caso, según las características del paciente y la patología intercurrente, debido a sus posibles efectos secundarios en términos de infección, compromiso respiratorio, hemorragia gastrointestinal y muerte74,76. En concreto, no existe evidencia de que la administración de corticoesteroides tenga efecto beneficioso en caso de una LM traumática completa. Ante una LM aguda no estabilizada —o bien con deterioro neurológico— la administración de corticoesteroides podría iniciarse en las primeras horas, con pautas cortas y considerando los posibles efectos secundarios77.
Actualmente está en investigación el uso de algunos tratamientos en la LM traumática aguda, con un objetivo neuroprotector (riluzol, minociclina, G-CSF, FGF-2 y polietilenglicol) o estrategias neurorregeneradoras (condroitinasa ABC, péptidos autoensamblados y la inhibición Rho). Muchas terapias celulares (células madre embrionarias, células madre neurales, células madre pluripotentes inducidas, células estromales mesenquimales, células de Schwann, células envolventes olfatorias y macrófagos) también han demostrado ser prometedoras78-80.
Sin embargo, dados los múltiples factores que determinan la progresión de la lesión, la restauración de la médula espinal lesionada probablemente requiere diversas estrategias de reparación utilizadas de forma combinada79.
Algunos estudios experimentales han sugerido que el enfriamiento atenúa los mecanismos de lesión secundaria81. Estudios clínicos iniciales con enfriamiento directo de la médula durante la cirugía no mostraron beneficio. Sin embargo, un estudio reciente investigó el uso de hipotermia (33°C) con resultados favorables82. La evidencia es insuficiente para recomendar el uso de hipotermia sistémica83.
Conflicto de interesesNo hay conflicto de intereses por parte de ninguno de los autores.