INTRODUCCIÓN
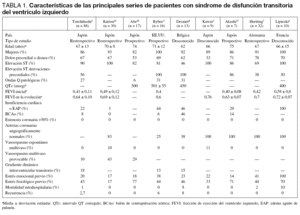
El síndrome de apical ballooning o abalonamiento, también conocido como síndrome de discinesia apical transitoria (SDAT) o cardiomiopatía de Takotsubo ha sido descrito recientemente. Los primeros casos aparecen en la población japonesa durante los años noventa1,2, aunque es en el año 2001 cuando se consolida como entidad independiente, describiéndose por Tsuchihashi et al de nuevo en Japón la primera serie de 88 pacientes3. Posteriormente, se han documentado más series de casos en EE.UU.4, Bélgica5 y en los últimos años también en otros lugares, de lo que se deduce que no existe asociación con determinadas áreas geográficas o grupos étnicos6-20. Del análisis de los casos descritos en las principales series publicadas (tabla 1) se infieren las principales características diferenciales del SDAT2-5,7,16-18: tiene lugar en mujeres de mediana edad (entre 50 y 70 años) y está precedido de un estrés físico o psíquico que actúa como desencadenante.
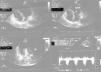
La disfunción apical transitoria se caracteriza por la morfología que adopta el ventrículo izquierdo, con el ápex redondeado y el cuello estrecho, originada por la hipocinesia, acinesia o discinesia de los segmentos apicales, e hipercontractilidad de los segmentos basales. Debe su nombre a un antiguo recipiente empleado para atrapar pulpos en los mares de Japón, que posee la misma forma que la que adopta el ventrículo izquierdo en la ventriculografía3,19,20.
Su aparición es aguda y transitoria, normalizándose la función ventricular de una a tres semanas, aunque se puede retrasar hasta dos meses. La ausencia de enfermedad aterotrombótica en las arterias coronarias de los pacientes que presentan este síndrome es condición indispensable para su diagnóstico2,4,18,19. Este criterio es importante, existiendo autores que consideran que no se puede realizar su diagnóstico si no se cuenta con una coronariografía precoz, en las primeras 24 horas de su aparición, aunque en la actualidad no existe un acuerdo sobre la obligatoriedad de la realización de exploraciones invasoras para llevar a cabo su diagnóstico. Unos autores admiten la realización tardía, otros preconizan la realización de ultrasonografía intravascular o ventriculografía con isótopos y finalmente se describen series que incluyen casos en los que no se realiza angiografía, al considerar que la realización de ecocardiograma o resonancia son también válidos para objetivar las alteraciones descritas21-23.
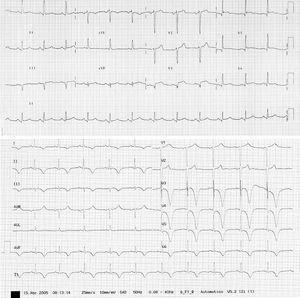
De etiología parcialmente conocida, se calcula que en nuestro medio aproximadamente el 1-2% de los pacientes con sospecha de infarto agudo de miocardio (IAM) padece en realidad este síndrome, pues la presentación clínica y electrocardiográfica del mismo es similar a la de los pacientes con síndrome coronario agudo, con la existencia de elevación del segmento ST más acusada en la cara anterior en el 90% de las ocasiones aunque con mayor elevación en V4-V6 que en V1-V3, a diferencia de los IAM anteriores-. En una cuarta parte de las ocasiones aparecen además ondas Q que desaparecen tras el período agudo, y prácticamente todos presentan a partir del segundo día ondas T negativas (fig. 1). El intervalo QT corregido (QTc) se encuentra más alargado que en el IAM. Todas estas alteraciones son transitorias, aunque la negatividad de la onda T puede prolongarse durante más tiempo24-32.
Figura 1. Electrocardiograma (ECG) de una paciente de 57 años durante el episodio agudo de disfunción del ventrículo izquierdo, donde se aprecia una elevación del segmento ST en la serie precordial e inferior (trazado ECG en la parte superior) y su evolución con el desarrollo de isquemia subepicárdica (trazado ECG en la parte inferior) y aparición de inversión de la onda T.
En el 50% de los pacientes existe también una ligera elevación de las enzimas cardíacas, con gran discrepancia entre su incremento y la extensión del área acinética a juzgar por las alteraciones en el electrocardiograma (ECG)3-5.
Aunque las alteraciones son por definición reversibles y el pronóstico habitualmente bueno, pueden existir en la evolución complicaciones como arritmias, insuficiencia cardíaca, estenosis subaórtica dinámica, shock cardiogénico, accidente cerebrovascular de origen embólico e incluso muerte (tabla 2)3,28-32.
En el presente trabajo se han revisado los artículos más relevantes acerca de la disfunción apical transitoria mediante la revisión de los mismos en las bases de datos Medline, EMBASE, BIOBASE y Web of Knowledge, deteniéndonos en las diversas hipótesis que intentan explicar su fisiopatología, (aún desconocida), y en los criterios clínicos para su diagnóstico, (no admitidos por todos los autores). Los términos empleados para la búsqueda han sido: Takotsubo cardiomyopathy, transient left ventricular apical syndrome, ballooning syndrome.
CRITERIOS QUE DEFINEN EL SÍNDROME
Se han empleado numerosos y diversos criterios en las diferentes series publicadas, sin embargo, y con las implicaciones terapéuticas que ello supone, aún no existe una definición de consenso del mismo. Conscientes de ello, y para facilitar su rápido reconocimiento, algunos autores como Abe18,33 y posteriormente Bybee de la Clínica Mayo19,34, proponen cuatro criterios basados fundamentalmente en su presentación clínica (tabla 3), para discriminar fácilmente este síndrome de otras patologías como el IAM:
1) La discinesia o acinesia transitoria de los segmentos apicales y medios del ventrículo izquierdo de distribución vascular correspondiente a más de una arteria epicárdica.
2) La ausencia de enfermedad coronaria obstructiva o evidencia de rotura aguda de placa en la angiografía.
3) La nueva aparición de anomalías en el trazado ECG, como elevación del segmento ST o inversión de la onda T.
4) Ausencia de traumatismo craneoencefálico reciente o hemorragia subaracnoidea, feocromocitoma, miocarditis, miocardiopatía hipertrófica o aturdimiento miocárdico de origen isquémico.
Dichos criterios pueden ser empleados cuando no existan otras causas evidentes que provoquen similares alteraciones en la función apical ventricular35, aunque para algunos autores la reversibilidad de la disfunción ventricular es un argumento suficiente para su diagnóstico36. Dentro de estos criterios, el grupo de Abe33 discrimina entre dos criterios mayores (entre los que se encuentran la reversibilidad de los trastornos de la contractilidad del ventrículo izquierdo y las alteraciones en el ECG) y dos menores (la existencia de un factor precipitante como el estrés físico o emocional y el ligero incremento de las enzimas cardíacas). Sin embargo, otros autores, como el grupo de Segovia et al37, proponen añadir otros criterios además de los mencionados, subrayando que la existencia de una coronariografía urgente normal es criterio diagnóstico per se, aunque la realización de la misma no es imprescindible, admitiendo la realización de exploraciones no invasoras como el ecocardiograma, la resonancia magnética cardíaca o la ventriculografía con isótopos asociadas a otras manifestaciones clínicas para lograr su diagnóstico15,21-23.
ETIOPATOGENIA
Éste es otro punto de controversia en el que no existe una única teoría propuesta. Debido a que la etiología de este síndrome permanece aún desconocida, especulativamente se han propuesto varios mecanismos implicados en su génesis, como el espasmo de las arterias epicárdicas, la alteración en la microvascularización coronaria o la disfunción miocárdica mediada por catecolaminas, entre otros.
Espasmo de las arterias coronarias
La hipótesis de un espasmo de las arterias coronarias epicárdicas como origen de esta entidad ha sido descrita desde las primeras descripciones, debido a la coincidencia del espasmo coronario y aturdimiento miocárdico en casos aislados. Sin embargo, el empleo de la coronariografía precoz en el SDAT muestra la presencia de espasmo espontáneo difuso en escasas ocasiones, y su reproducción mediante la prueba de provocación con ergonovina o acetilcolina únicamente resultó positiva en el 15-30% de los sujetos estudiados2-4,16,18. Abe et al buscaron la confirmación de este mecanismo realizando Doppler intracoronario de modo prospectivo en la fase aguda del SDAT sin encontrar tampoco lesiones significativas18.
Trastorno de la microvascularización
En ausencia de obstrucción coronaria se pensó en la existencia de un trastorno en la microvascularización coronaria que ocasionaría aturdimiento miocárdico y que podría ser el origen de la cardiomiopatía de Takotsubo. Así, la función de la microvascularización coronaria inmediatamente después de la presentación del SDAT se encuentra difusamente afectada, existiendo una disminución en la reserva del flujo coronario, tanto si es medida con técnicas invasoras (trombólisis en el infarto de miocardio [TIMI]) o no invasoras, mediante Doppler o tomografía por emisión de fotones (SPECT)5,16,19,38-42. Esta reducción transitoria de la reserva coronaria puede ser el mecanismo que produce la reversibilidad de este síndrome, aunque no queda claro si dicha disfunción en la microvascularización es el mecanismo primario en la patogénesis del síndrome, o bien si se trata de un fenómeno secundario43,44.
Disfunción miocárdica secundaria
a catecolaminas
Otra de las hipótesis considera a esta entidad como un síndrome metabólico determinado por una hiperactividad aguda del sistema simpático local secundaria a la descarga masiva de catecolaminas que provocaría un aturdimiento miocárdico4,45. La presencia frecuente de un estrés físico (traumatismo, intervención quirúrgica, etc.) o emocional que desencadena el síndrome en casi todas las series publicadas parece apoyar esta hipótesis3,7,9,10,17,20,45-58. La alteración transitoria en la actividad simpática cardíaca inducida por el estrés se ha puesto de manifiesto mediante pruebas de imagen como la gammagrafía cardíaca15,59,60. Se han observado, además, claras similitudes entre el SDAT y el aturdimiento miocárdico debido a la descarga de catecolaminas, que se encuentra presente en patologías como la hemorragia subaracnoidea o la crisis del feocromocitoma61. Otro argumento a favor es el descubrimiento de un modelo experimental de SDAT, en el que el estrés continuado provoca hipocinesia de la región anteroapical del ventrículo izquierdo, quedando atenuados los cambios en aquellos animales que recibían estrógenos suplementarios, o normalizándose tras realizar un bloqueo de los adrenorreceptores alfa o beta48.
Esta teoría, aunque prometedora, no aclara el origen del SDAT, pues no se ha podido comprobar la existencia de una elevada concentración de catecolaminas a nivel local (miocardio apical) durante la fase aguda del SDAT. Además, se desconoce por qué la disfunción afecta únicamente a los segmentos apicales, sobre todo si se tiene en cuenta que todo el miocardio recibe inervación simpática por igual. Autores como el grupo de Akashi encuentran una distribución de terminaciones nerviosas simpáticas y una mayor densidad de sus receptores, y un incremento en la respuesta al estímulo adrenérgico en el área apical, pero los resultados no han sido concluyentes17,62,63. El ligero aumento de las catecolaminas en sangre periférica durante la fase aguda tampoco explicaría este fenómeno, al tratarse de un hallazgo absolutamente inespecífico presente en la mayoría de enfermedades agudas.
Otras teorías
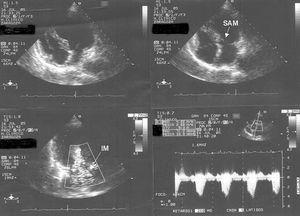
Otra de las hipótesis que explicarían esta patología es la existencia de anomalías en la arquitectura normal del miocardio. Así, Desmet4 y Kawai2 observan en algunos pacientes la presencia de un septo o «resalte» en la parte medial del tabique interventricular de morfología sigmoide (fig. 2), así como una orientación anormal en la inserción de la válvula mitral. Ambas variantes de la normalidad suceden con mayor frecuencia en mujeres y se cree que ante una intensa estimulación adrenérgica o una deshidratación condicionan un reducido volumen ventricular, predisponiendo a una obstrucción dinámica, grave y transitoria en el tracto de salida del ventrículo izquierdo (TSVI), al subdividir este ventrículo en 2 cámaras funcionalmente diferentes, con marcado aumento de la presión intraventricular en la pared ventricular distal de la cámara apical8,64-70. Dicha obstrucción provoca una isquemia subendocárdica secundaria a la reducción de la perfusión miocárdica, que no se corresponde a un territorio específico de una arteria coronaria, y que es el sustrato del aturdimiento miocárdico presente en este síndrome. Autores como Merli han podido demostrar estos hallazgos mediante el empleo de la ecocardiografía de estrés con dobutamina. Estas investigaciones revisten una gran importancia, ya que el tratamiento con nitratos podría aumentar dicho gradiente causando mayor deterioro, mientras que el tratamiento con bloqueadores beta, volumen, o estimulantes alfa-adrenérgicos sería beneficioso al reducirlo67,70.
Figura 2. Ecocardiograma transtorácico realizado en un plano apical de cuatro cámaras donde se aprecia la geometría del tracto de salida de ventrículo izquierdo (TSVI) con movimiento anterior sistólico de la válvula mitral (parte superior), insuficiencia mitral significativa y gradiente elevado en el TSVI (parte inferior).
Otras etiologías actualmente en investigación son la genética, existiendo por una parte una agrupación entre personas de la misma familia, y por otra una especial respuesta al estrés que se encuentra mediada genéticamente71.
TRATAMIENTO
Las implicaciones pronósticas y terapéuticas del SDAT difieren del IAM y conllevan diferente manejo clínico. Con su rápido reconocimiento se puede evitar la administración fútil de agentes fibrinolíticos y la realización de cateterismo en la fase aguda. El tratamiento con bloqueadores beta o con agonistas alfa-adrenérgicos, añadidos a inhibidores de la enzima conversora de angiotensina (IECA) son de gran utilidad para disminuir o anular el gradiente dinámico que se genera en el TSVI durante la fase aguda. Así mismo, su empleo durante la fase crónica, y posiblemente de modo indefinido, ha demostrado ser muy útil para prevenir las recurrencias4,7,65,72.
CONCLUSIONES
La cardiomiopatía de Takotsubo es un síndrome de reciente descripción caracterizado por la discinesia apical del ventrículo izquierdo de carácter transitorio, que tiene lugar con mayor frecuencia en mujeres que se encuentran alrededor de la menopausia. Su presentación clínica, ECG y enzimática simula un síndrome coronario agudo, aunque la diferencia con el mismo radica en la ausencia de estenosis en las arterias coronarias, lo que le confiere un buen pronóstico.
Su manejo clínico y la prevención de las recidivas son difíciles, ya que este síndrome plantea todavía muchas incógnitas en cuanto a su fisiopatología. Varios son los mecanismos propuestos y es posible que todos participen en la génesis del SDAT, aunque es la descarga de catecolaminas el mecanismo inicial que lo desencadena. Parecen necesarias ulteriores investigaciones para lograr el conocimiento del mismo. El empleo de los criterios diagnósticos basados en su presentación clínica facilita su sospecha y rápido reconocimiento para diferenciarlo del IAM, evitando la administración de tratamiento fibrinolítico (con su riesgo de complicaciones hemorrágicas) y de nitratos (con probable empeoramiento de la disfunción al provocar un aumento del gradiente dinámico). En la actualidad el empleo de bloqueadores beta ha demostrado ser un tratamiento eficaz tanto en la fase aguda como a largo plazo.
Declaración de conflicto de intereses
Los autores han declarado no tener ningún conflicto de intereses.
Correspondencia: Dra. B. Obón Azuara.
Servicio de Medicina Intensiva.
Hospital Clínico Universitario.
Avda. San Juan Bosco, 15.
50009 Zaragoza. España.
Correo electrónico: blankaobona@yahoo.es
Manuscrito aceptado el 1-VI-2006.