INTRODUCCION
El contrapulsador aórtico es un dispositivo intravascular en forma de catéter con luz central que permite medir la presión intraaórtica y que tiene un balón de entre 30 y 50 ml, que se coloca en la aorta descendente y que comúnmente se infla con helio de forma sincronizada con el ciclo cardíaco, bien con la onda de pulso en la incisura dícrota o, bien con el QRS del electrocardiograma. Esto permite el incremento de la presión diastólica y media en la aorta torácica, con la consiguiente mejoría de la perfusión coronaria, un mejor aporte de oxígeno miocárdico y, posteriormente, mediante la disminución de la poscarga al desinflarse en la fase de contracción isovolumétrica del ventrículo izquierdo (VI) y una mejor función sistólica del VI, efectos que se han descrito en las últimas décadas1-5.
Es conocida la utilidad de su uso preoperatorio en enfermos que precisarán una intervención o un procedimiento invasivo cardiovascular, y clásicamente se ha utilizado en el ámbito de los centros hospitalarios con cirugía cardíaca. Apenas existen referencias de su uso en hospitales de segundo nivel sin este tipo de servicios; sin embargo, los enfermos cardiológicos complicados se encuentran en todos los ámbitos de asistencia sanitaria y cuando están en situación de alto riesgo o presentan una complicación inesperada son numerosos los trámites y pasos que hay que dar para su adecuada ubicación en un centro de referencia; además, el traslado a veces se tiene que realizar en situación precaria con gran soporte terapéutico. Esto nos llevó a aumentar nuestra cartera de servicios con la contrapulsación aórtica, y ante los resultados, que estimamos satisfactorios, comunicamos los primeros 9 casos recogidos en los primeros 6 meses de uso de la técnica.
MÉTODO
Se trata de un análisis retrospectivo sobre los enfermos que precisaron contrapulsación aórtica durante los primeros 6 meses de este año. El objetivo fue comprobar que esta técnica puede estar al alcance de centros sin cirugía cardíaca, en los que el número de enfermos con cardiopatías y enfermedad coronaria es elevado, y así las complicaciones que presenten pueden ser tratadas con todos los medios disponibles. Se ha pretendido demostrar la viabilidad del uso de la contrapulsación aórtica en nuestro ámbito de trabajo y demostrar que el traslado de estos enfermos se realiza así en mejores condiciones y con mejores resultados respecto a como se llevaba a cabo previamente. Los pacientes incluidos en este período son los que reunían los criterios incluidos en las guías publicadas por el American College of Cardiology/American Heart Association Task Force on Practice Guidelines6 se resumen en:
Clase I
1. Shock cardiogénico, edema pulmonar y otras situaciones de fallo cardíaco que no responden a la apropiada administración de líquidos, a la terapia farmacológica o ambas, en pacientes con fallo cardíaco potencialmente reversible o como puente a un trasplante cardíaco.
2. Fallo cardíaco agudo acompañado de isquemia rebelde en preparación para cateterismo cardíaco o intervención definitiva.
3. Fallo cardíaco agudo complicado con regurgitación mitral o rotura del septo ventricular para obtener una estabilización hemodinámica que posibilite un diagnóstico, una intervención definitiva o ambos.
Clase II
Fallo cardíaco crónico progresivo si es necesario para proporcionar un tratamiento adecuado, tiempo para considerar opciones terapéuticas e intervención definitiva.
Incluimos, además, a pacientes con enfermedad crítica de tronco de la coronaria izquierda con isquemia rebelde a tratamiento médico completo y/o shock cardiogénico coincidente con los episodios de isquemia (estos episodios de disfunción cardíaca no están catalogados como shock cardiogénico y eran candidatos a cirugía cardíaca solicitando, si la situación de urgencia lo permitía, el consentimiento informado escrito al paciente). Se utilizó la consola Contrapulsador Transact H-8000 de Arrow con balones de 40 ml de helio, con la técnica de Seldinger por arteria femoral con introductor de 9,5F, siguiendo el protocolo habitual para su colocación7 con comprobación por radioscopia y posterior radiografía de tórax. Su posición óptima queda en la aorta descendente por debajo del inicio de la subclavia izquierda, comenzando con estimulación sincronizada con el QRS o con la onda de pulso en aquellos en los que se detectaban artefactos del trazado del electrocardiograma. Comenzamos con frecuencias de inflado de balón en cada latido (1:1) que son las que manteníamos durante el proceso de traslado y hasta la resolución de la situación clínica de los pacientes. En los casos que no fueron intervenidos y que presentaron una resolución de la causa que propició su colocación, iniciamos una retirada del soporte hemodinámico del dispositivo de forma protocolizada, reduciendo la frecuencia de inflado paulatinamente en función de la respuesta obtenida hasta una relación de 1:4, y antes de retirarlo, a 1:8 para comprobar que se podía realizar la retirada. A quienes se debía derivar a otros centros, se les trasladó en UCI móvil, con una consola que contaba con una batería de 2 h de autonomía además de poder conectarse a la red del vehículo; por otro lado, se suplementó la dotación de material de una bombona de helio de reserva por si se necesitara su cambio durante el traslado. Se registraron los datos y el resultado final de los casos a los que se trató con este tipo de dispositivo.
RESULTADOS
Comunicamos 9 casos tratados de forma consecutiva desde que comenzamos con esta modalidad de soporte hemodinámico: siete de ellos eran varones y dos mujeres, con una edad media de 58 años (tabla 1). De nuestros pacientes, sólo uno tuvo complicaciones no atribuibles en exclusiva a la colocación del dispositivo, aunque sí pudo influir negativamente en su desarrollo. En todos los pacientes (salvo los dos que fallecieron en la unidad) se registró una estabilización de la clínica con desaparición de los síntomas, mejora del edema pulmonar y desaparición de la inestabilidad eléctrica; esta mejoría fue llamativa e inmediata a los pocos minutos de su colocación y del inicio de la contrapulsación aórtica. Del total de nueve, 2 pacientes no precisaron cirugía cardíaca, y los otros cinco se trasladaron a un centro de cirugía cardíaca sin ninguna incidencia reseñable durante el traslado y pudieron ser intervenidos quirúrgicamente. La estancia media en la unidad, con independencia de la duración de la contrapulsación, fue de 59 h, con un mínimo de 1,2 h y un máximo de 6 días. De todas formas, la contrapulsación no se prolongó en ningún caso más de 24 h continuas salvo una ocasión en que se prolongó hasta 33 h; en otro caso se retiró y se tuvo que reinstaurar 24 h más tarde.
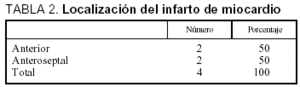
Entre los 4 casos cuyo motivo de ingreso fue el infarto de miocardio hay que reseñar que todos tenían afección de la cara anterior del VI (tabla 2) con una fracción de eyección media del 26%.
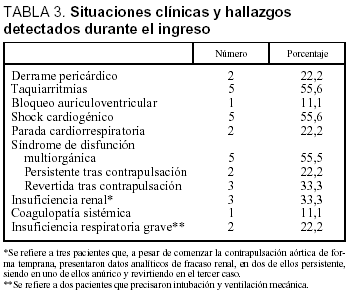
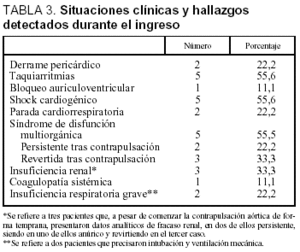
Analizando a los 9 pacientes, se registraron durante el ingreso las siguientes situaciones clínicas que acompañan a este tipo de enfermedades (tabla 3): shock cardiogénico (5/9) en los 4 pacientes con infarto de miocardio y en el quinto que ingresó con diagnóstico de miocarditis; taquiarritmias (5/9), e insuficiencia renal (3/9) (creatinina > 2 mg/dl), detectada en dos casos de forma persistente y en otro temporalmente, que en uno de ellos fue anúrica a pesar de comenzar la contrapulsación aórtica de forma temprana. En el resto de los pacientes con shock cardiogénico que tuvieron oliguria en el inicio del shock cardiogénico, ésta se corrigió con la contrapulsación aórtica, y la creatinina no alcanzó cifras significativas compatibles con deterioro significativo de la función renal. Los 2 pacientes con insuficiencia respiratoria grave fueron los dos que necesitaron intubación y ventilación mecánica, y ambos fallecieron en disfunción multiorgánica (uno de ellos de forma inmediata y el otro tras varios días de tratamiento, en el que se descartó finalmente la cirugía de revascularización y el trasplante debido a su situación general). Entre los procedimientos o técnicas que se aplicaron durante su estancia en la unidad (tabla 4) destacan la ecocardiografía (9/9) y la coronariografía (7/9).
DISCUSIÓN
Esta técnica de apoyo hemodinámico se utiliza de forma temporal en determinadas situaciones de inestabilidad cardiológica en que se precisa intervención cardíaca, y clásicamente están consideradas como indicaciones las que se señalan en las guías publicadas por el American College of Cardiology/American Heart Association Task Force on Practice Guidelines, descritas previamente en el apartado de "Método"6.
Se han sumado recientemente otras indicaciones para su uso, como la angina inestable con deterioro hemodinámico, la isquemia rebelde con evidencia de dolor precordial en reposo con cambios electrocardiográficos antes de la revascularización miocárdica o las taquiarritmias ventriculares malignas, cuando éstas son secundarias a isquemia en espera de la intervención o procedimiento definitivo8. Quedan otras indicaciones controvertidas en la bibliografía, pues se han señalado en estudios no aleatorizados o no concluyentes, como en el tratamiento de la isquemia residual y en la angioplastia primaria. Sin embargo, existe abundante experiencia en el tratamiento de la cardiopatía isquémica con o sin shock como complicación mecánica del infarto de miocardio, comprobando que con su uso mejora la situación hemodinámica9-11.
La mortalidad de los pacientes con shock cardiogénico clásicamente estaba cifrada en porcentajes superiores al 50-60%; sin embargo, cuando la enfermedad subyacente tiene una solución terapéutica quirúrgica y se inicia de forma temprana el tratamiento con balón de contrapulsación aórtica, los resultados en supervivencia mejoran notablemente12. En los pacientes con infarto de miocardio que desarrollan una complicación mecánica, como rotura septal de pared libre o disfunción aguda de la válvula mitral, tratados con urgencia mediante contrapulsación aórtica, lo que posibilita una posterior y urgente reparación quirúrgica, se reduce la mortalidad a menos del 55% (en el caso de la rotura septal, las cifras llegan al 20-27%)13. También ha mostrado utilidad en pacientes con infarto agudo de miocardio y angina inestable14-17 sin complicaciones mecánicas, así como de forma profiláctica en el preoperatorio de pacientes con enfermedad del tronco de la arteria coronaria izquierda4,18. Christenson et al llevaron a cabo un estudio prospectivo y aleatorizado en enfermos clasificados como de alto riesgo, incluso en pacientes sin deterioro hemodinámico19, con el uso preoperatorio del balón de contrapulsación, y concluyeron que es eficiente, pues mejora de forma significativa (con una p < 0,0001) cada uno de los siguientes ítems: índice cardíaco preoperatorio, mortalidad y morbilidad postoperatorias, estancia en la unidad de cuidados intensivos y estancia hospitalaria, así como consumo de fármacos. Estos mismos autores en otro análisis sobre 60 enfermos20, con fracción de eyección del ventrículo izquierdo menor del 30%, angina inestable, reoperación o estenosis del tronco de la coronaria izquierda mayor del 70%, detectaron un índice cardíaco postoperatorio significativamente superior en el grupo tratado de forma preoperatoria con balón (p < 0,001); la incidencia de bajo gasto cardíaco postoperatorio fue más baja en el grupo tratado (p < 0,001), y la estancia en la UCI y en el hospital, más corta (p < 0,001 y p = 0,002, respectivamente). Otro estudio prospectivo21, no aleatorizado, multicéntrico, sobre 457 pacientes sometidos a revascularización para enfermedad de tronco de la coronaria izquierda, pero en el que se excluyó a enfermos con fallo cardíaco, shock, isquemia rebelde o bypass previo, se comparó a los que habían recibido contrapulsación aórtica previa a la cirugía con los que no, y se encontraron mejores resultados en el grupo tratado con esta técnica, aunque los autores sugieren la necesidad de nuevos estudios aleatorizados con análisis multivariado para conocer el papel real de esta técnica en el enfermo con estenosis significativa y estable de tronco. Parece clara la utilidad del uso temprano del apoyo hemodinámico de este tipo de pacientes, pero estas situaciones no sólo se dan en hospitales de tercer nivel dotados de cirugía cardíaca, sino que suceden allí donde hay enfermos coronarios o con insuficiencia cardíaca.
Nuestra unidad es polivalente, está dotada de seis camas y en ella predominan los enfermos cardiovasculares, sobre todo con síndrome coronario agudo. Ingresan aproximadamente unos 230 casos/año con este diagnóstico, y durante el año 2001 se ha realizado coronariografía (40%) y cirugía cardíaca urgente durante la fase aguda del proceso con traslado a otro centro (10%), de los cuales la mitad cumplía indicaciones de inicio de contrapulsación aórtica no disponible ese año en nuestra unidad. El número de pacientes con necesidad de procedimientos de revascularización invasora percutánea o quirúrgica se incrementa cada día, a medida que los laboratorios de hemodinámica están disponibles para un mayor número de enfermos; además, con el envejecimiento de la población y el aumento de la supervivencia del enfermo coronario, éste a veces es candidato a varios de estos procedimientos. Así, no es infrecuente tratar a enfermos con antiguos infartos, revascularizaciones quirúrgicas previas o disfunciones miocárdicas sobreañadidas a trastornos crónicos. La dificultad con la que nos encontramos para derivar a los enfermos a centros dotados de este tipo de cirugía y la situación (muchas veces grave) en que son trasladados nos llevaron a incluir esta técnica en nuestra unidad, con la intención de proporcionar todos los medios necesarios a los pacientes que necesitan un procedimiento invasor urgente. Así, se proporciona apoyo hemodinámico en la mejor situación posible de forma temprana, de modo que durante ese período de espera los pacientes tengan todo el soporte hemodinámico disponible, sin que la situación geográfica suponga un factor discriminador en las oportunidades de encontrar la solución idónea en el tiempo adecuado.
Nuestra primera experiencia consiste en los primeros 9 casos tratados de forma consecutiva desde que comenzamos con esta modalidad de soporte hemodinámico. Los datos previos indican que es una técnica segura, con una incidencia de complicaciones baja (un 8% en otras series). De nuestros pacientes, sólo uno tuvo complicaciones atribuibles a la colocación del dispositivo: un varón de 59 años con shock cardiogénico tras un infarto de miocardio con disfunción multiorgánica y arteriopatía periférica generalizada, que presentó isquemia en las extremidades inferiores por hipoperfusión, más evidente en el miembro que tenía el dispositivo. El resto de los enfermos no presentó complicaciones atribuibles a la técnica.
De la totalidad de los 9 enfermos, dos fallecieron en la unidad por shock cardiogénico rebelde que derivó a fallo multiorgánico y muerte. Otros 2 pacientes no precisaron cirugía cardíaca y pudieron ser dados de alta a planta. Uno de ellos era un enfermo de 40 años con una miocarditis viral y disfunción sistólica grave que mejoró y, tras superar una situación crítica de shock en la que necesitó intenso tratamiento de soporte hemodinámico, fue mejorando hasta que se pudo retirar todo el apoyo y fue dado de alta a la planta. La otra paciente, de 60 años, tras un cuadro de angina de pecho con taquicardia ventricular sostenida y disfunción sistólica grave debida a un aneurisma anteroapical antiguo, al que se sumó la repercusión producida por el acontecimiento actual, necesitó revascularización percutánea por enfermedad coronaria con ACTP más stent en la arteria descendente anterior que tenía, además, contraindicaciones para cirugía cardíaca. Tras el procedimiento la situación fue mejorando paulatinamente y se logró retirar el apoyo inotrópico y mecánico. Días después fue dada de alta a la planta. Los otros 5 pacientes se trasladaron a un centro de cirugía cardíaca sin que durante el transporte se produjera ninguna incidencia reseñable. En este sentido, en función de la consola que se utilice, se tendrá una mayor maniobrabilidad para el transporte sanitario; de todas formas, se utilizan dispositivos cada vez más pequeños y versátiles. Estos 5 enfermos se pudieron intervenir quirúrgicamente en las siguientes horas de su llegada a los centros de destino, aunque uno de ellos (un paciente con enfermedad de tronco y antecedentes de radioterapia en el tórax por neoplasia) falleció en el período postoperatorio inmediato por fallo de bomba tras una larga intervención. El resto sobrevivió a la intervención quirúrgica.
Entre los 4 casos cuyo motivo de ingreso fue el infarto de miocardio, hay que reseñar que todos tenían afección de la cara anterior del ventrículo izquierdo, lo que está en consonancia con la mayor incidencia de insuficiencia cardíaca que globalmente acompaña al infarto anterior respecto a los de otras localizaciones. La fracción de eyección media detectada era de 26%, medida mediante ecocardiografía 2D por el método de Simpson. Además, estos pacientes tenían indicación de revascularización coronaria.
La estancia media en la unidad fue de 59 h. En este punto conviene destacar que la mayoría de los casos (5) presentaron la indicación de contrapulsación cuando llevaban pocas horas de ingreso y fueron derivados en las siguientes horas de su colocación, con un mínimo de 1,2 y un máximo de 21 h de estancia desde su ingreso hasta que se consiguió trasladarlos. Del total de enfermos, hubo cuatro que desarrollaron cuadro de shock cardiogénico o isquemia rebelde tras varios días de estancia, por lo que tuvieron una estancia global más prolongada; además, la actuación quirúrgica no siempre se podía acometer por la situación de fallo orgánico que desarrollaron algunos o por su estado general. Estos tuvieron que esperar hasta ver si existía una mejoría que posibilitara su tratamiento definitivo. Los procedimientos que recibieron son los habituales. Cabe destacar que sólo se pudo dilatar con ACTP y stent a una de las pacientes porque, como es lógico, la anatomía coronaria en casi todos los casos recomendaba una cirugía de revascularización más que un procedimiento percutáneo. Todos los pacientes tenían lesión de tres vasos o tronco de la coronaria izquierda, y en estos últimos se colocó el dispositivo por tener angina rebelde acompañada de deterioro hemodinámico con los episodios isquémicos, a pesar de tratamiento médico completo, aunque antes o después del cuadro anginoso rebelde no presentaran cuadro de shock.
En definitiva, la experiencia es muy positiva, y se puede concluir que la colocación es sencilla y el índice de complicaciones, siendo cuidadosos con el método de colocación y seguimiento del dispositivo, es bajo. Si la indicación es clara, las posibilidades de un mejor resultado quirúrgico son mayores; por otro lado, la colaboración de los equipos quirúrgicos es también mayor, pues existe una concienciación mayor del esfuerzo que se ha iniciado y de que los pacientes, al estar estabilizados con esta técnica, tienen mayores posibilidades de soportar el traslado y posteriormente el período perioperatorio. Los intentos a veces heroicos de trasladar a enfermos inestables con enfermedades de tronco críticas o, lo que es peor, pacientes con disfunción sistólica sostenidos con fármacos inotrópicos en condiciones clínicas de extrema gravedad tienen un resultado malo, y la experiencia negativa hace que posteriores enfermos con posibilidades tengan menos oportunidades. No olvidemos que hay muchos casos que tras la cirugía pueden tener un resultado final óptimo por trasplante cardíaco o por revascularización coronaria de pacientes con un componente reversible de la disfunción miocárdica, complicaciones mecánicas del infarto con roturas o disfunciones valvulares, etcétera. Seleccionando las indicaciones con responsabilidad podemos dar todas las oportunidades posibles a nuestros enfermos.