En estas semanas de crisis se está produciendo un fenómeno sin precedentes en el ámbito sanitario: además de la ingente bibliografía científica que las revistas especializadas se apresuran por divulgar, los profesionales estamos recibiendo continuamente diferentes protocolos de actuación procedentes de centros nacionales e internacionales, videotutoriales y opiniones de expertos que se han convertido en un material de incalculable valor si sabemos administrarlo. Compartir información médica tiene sus ventajas si su gestión se realiza de forma adecuada en esta epidemia. Las decisiones sanitarias han de ser racionales, rentables y respetuosas.
Racionales, porque han de estar sustentadas por la mejor evidencia científica, que viene determinada en orden decreciente por revisiones sistemáticas y metaanálisis, ensayos clínicos aleatorizados, estudios de cohortes, registros, estudios de casos-controles e informes de casos.
La emergencia de esta enfermedad ha provocado la puesta en marcha de numerosos ensayos clínicos diseñados de forma urgente y no siempre con el rigor metodológico deseado, dadas las circunstancias, pero cuyos resultados se esperan con gran expectación y premura. Al administrar determinados tratamientos no hemos sido del todo capaces de gestionar la evidencia científica por el temor a establecer estrategias terapéuticas subóptimas en enfermos graves. Cabe recordar que en Medicina hay experiencias que el paso del tiempo ha llegado a demostrar que menos es más, con iniciativas como Slow medicine en Italia, Smarter medicine en Suiza, Choosing wisely de ABIM en EE. UU. y Canadá y «Hacer y no hacer» en España1-3.
Los conocimientos actuales podrían aplicarse atendiendo a los enfermos críticos con infección por SARS-CoV-2 sin administrar ningún tratamiento antivírico y aplicando tratamiento de soporte respiratorio, hemodinámico y otros, en función del desarrollo de fracaso orgánico durante su ingreso en UCI. Estas medidas y la prevención de enfermedades infecciosas relacionadas con los cuidados sanitarios han de capitalizar el tratamiento de estos enfermos, en los que se prevé una estancia prolongada. Todo lo demás podemos catalogarlo como medidas de tratamiento concomitante de eficacia no probada y con riesgo de producir efectos indeseables derivados de sus interacciones medicamentosas y complicaciones secundarias. Podemos hacer extensiva esta premisa al uso de corticoides y AC monoclonales o antagonistas de receptores de interleucinas.
En la tabla 1 se enumeran los factores por los que no se justifica el tratamiento con antivíricos en la infección grave por SARS-CoV-2 en el paciente crítico.
Factores por los que no se justifica el tratamiento con antivíricos en la infección grave por SARS-CoV-2 en el paciente crítico
| Falta de estudios rigurosos que demuestren beneficios |
| Alta probabilidad de interacciones medicamentosas con tratamientos habituales en UCI |
| Extrapolación de resultados clínicos en pacientes en situación estable a pacientes críticos |
| Asunción de que la actividad antivírica frente a otros virus es eficaz contra SARS-CoV-2 |
| Actividad in vitro no necesariamente ha de ir acompañada de actividad in vivo |
| Equiparación errónea de los diferentes estadios de enfermedad para iniciar tratamiento |
Rentable hace referencia a la clásica relación coste/beneficio. Coste en un sentido amplio del término: hemos de entenderlo en esta crisis más orientado a la escasez de recursos y a una distribución más proporcionada de los tratamientos que a un concepto meramente monetario; estamos viviendo una competitividad de mercado que está generando desigualdades territoriales y, por qué no afirmarlo, también en la selección de pacientes. La pregunta no aclarada es: ¿cuáles son los pacientes que más se beneficiarían de recibir tratamiento antivírico y en qué estadios de la enfermedad sería más eficaz su administración? Manejar la incertidumbre protegiendo a los más vulnerables y a los que más se pueden beneficiar incluye distribuir estos recursos que hay que racionar seleccionando.
Respetuoso, porque la base científica necesita de fiabilidad y validación. Este último factor no es posible establecerlo en los tiempos actuales de crisis sanitaria por la pandemia, de ahí que las recomendaciones de tratamientos antivíricos sean de uso compasivo. Por tanto, el paciente debe ser informado y hay que dejar constancia de ello en la historia clínica. En esta pandemia la mayoría de los consentimientos informados se están obteniendo de forma extraordinaria por vía telefónica debido a las políticas de restricción de visitas establecidas en los hospitales. Es recomendable que, en cuanto el paciente recupere su capacidad de decidir, sea informado de las decisiones tomadas y se le haga partícipe, teniendo en cuenta su opinión, más aún en una situación de incertidumbre sobre los potenciales beneficios del tratamiento.
Tratamiento antivírico en la neumonía grave causada por SARS-CoV-2Diferentes fármacos antivíricos se han postulado en el tratamiento de la neumonía vírica por SARS-CoV-2. El posicionamiento de estos fármacos se ha fundamentado en su actividad frente a otras infecciones causadas por otros virus diferentes y en experiencias clínica extraídas de estudios observacionales.
Las experiencias clínicas con otros virus como influenza, ébola, MERS, SARS y otras infecciones víricas han motivado el uso de estos fármacos antivíricos en los casos de la COVID-19, tanto en pacientes críticos como en los que no ingresaron en UCI, con tasas de utilización de más de un 90%4.
Las series retrospectivas que comparan factores relacionados con la mortalidad no han observado diferencias relacionadas con el uso de antivíricos5.
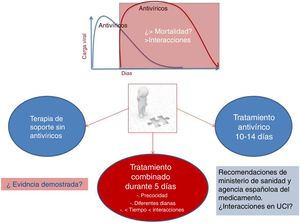
Se están administrando con la loable intención de disminuir la carga vírica y parece prudente considerar que los potenciales beneficios se producirían en las primeras fases de la enfermedad, que es cuando el virus presenta una mayor fase replicativa. Este hecho condiciona que los pacientes que ingresan en UCI procedentes de planta de hospitalización tras una estancia media de una semana estén empeorando más por la respuesta del organismo a la agresión que por un aumento de la carga vírica; esto hace que nos planteemos dudas sobre el beneficio de tratar ya en esta fase. Manejar en estos casos la evidencia científica en lugar del empirismo puede resultar una práctica clínica prudente, sobre todo por las interacciones y efectos secundarios demostrados con estos tratamientos, y no tanto por la hipotética falta de actividad frente al virus. En la figura 1 mostramos diferentes estrategias de tratamiento ante la falta de evidencias.
Evidencia científicaCuando se realiza una búsqueda en la web de la Organización Mundial de la Salud sobre los ensayos clínicos en marcha, actualmente están registrados más de 400, la mayoría de ellos en fase de reclutamiento o pendiente de iniciarlo. Los más recientemente publicados en revistas de alto impacto revelan resultados no concluyentes que condicionan la incertidumbre con que hemos de manejar esta parte del tratamiento6. Hacer un análisis reduccionista de ellos sin tener en cuenta las peculiaridades del paciente crítico nos puede conducir a errores, dado que la respuesta a los tratamientos es variable y que son múltiples los factores de confusión que influyen en el pronóstico del paciente crítico, tales como estado inmunitario previo, comorbilidades, intubación precoz, modo de ventilación mecánica, coinfecciones bacterianas, infecciones relacionadas con la atención sanitaria y tratamientos concomitantes.
Mecanismo de acción de los antivíricosLa explicación fisiopatológica de cómo el SARS-CoV-2 utiliza sus espículas de glicoproteínas para unirse a los receptores ACE de la membrana celular7 e introducirse en las células para multiplicarse y aumentar la replicación vírica justifica los diferentes fármacos que se han recomendado en el tratamiento. Una ventaja que tienen estas distintas alternativas de tratamiento es que no son excluyentes, ya que actúan sobre diferentes dianas en las células, y su uso combinado se justifica con la presunción de que pudieran actuar de forma sinérgica. Se han empleado diferentes antivíricos en los primeros casos, sin poder deducir de las series de casos publicadas la superioridad de unos sobre otros. A continuación, y de forma breve, resumimos los que están siendo utilizados en España.
Cloroquina e hidroxicloroquina no son realmente antivíricos, pero los hemos incluido al ser de los más usados en España durante esta pandemia. Pertenecen al grupo de las 4-aminoquinolinas y forman parte del tratamiento preventivo de la malaria, actúan sobre la endocitosis y exocitosis de las partículas víricas y, por tanto, pueden inhibir la entrada del virus. Los beneficios de la hidroxicloroquina se basan en que es más eficaz, aparte de que se le atribuye actividad antiinflamatoria que, como sabemos, está exacerbada en los casos graves que desarrollan distrés respiratorio. En estudios in vitro se ha demostrado mayor potencia de los efectos de la hidroxicloroquina8,9.
Otra diana de acción la ofrecen lopinavir/ritonavir. Como inhibidores de la proteasa, su efecto es impedir que la proteína se fragmente. Ha demostrado en modelos animales y en estudios in vitro su eficacia ante virus de la misma familia, como el SARS y MERS10; sin embargo, hay autores que cuestionan su capacidad de disminuir la carga vírica en el pulmón cuando hay una respuesta inflamatoria aumentada. Este hecho nos lleva a cuestionar su efectividad en los pacientes críticos con ventilación mecánica11. Se está administrando de forma combinada con interferón: en el ensayo clínico MIRACLE se demostró sinergia cuando se usan conjuntamente12. La principal debilidad es que hay poca experiencia clínica y que se han descrito numerosas interacciones y efectos secundarios.
Remdesivir. Lamentablemente, el fármaco que a priori se postula, a nuestro entender, como más atractivo para el uso en pacientes críticos está siendo el que menos acceso ha tenido en las UCI españolas. Su mecanismo de acción como inhibidor de la transcriptasa inversa inhibiendo la ARN-dependiente-ARN polimerasa le confiere actividad tanto para coronavirus humano como en modelos animales. En la actualidad hay en marcha distintos ensayos clínicos que aportarán luz sobre su eficacia frente a este virus en los casos más graves. La posibilidad de ser administrado por vía intravenosa aumenta la garantía de que alcance niveles plasmáticos sin depender, como ocurre en pacientes críticos con ventilación mecánica, de la absorción en el tubo digestivo que, en ocasiones, es errática en las presentaciones para sonda nasogástrica.
Comparative therapeutic efficacy of remdesivir and combination lopinavir, ritonavir, and interferon beta against MERS-CoV. Nat Commun. 2020 Jan 10;11:222. https://doi.org/10.1038/s41467-019-13940-613. Las experiencias clínicas documentadas como uso compasivo son esperanzadoras, aunque hemos de discutir los resultados documentados por Grein et al., considerando que no hubo un grupo control, que excluyó a pacientes con vasoactivos o fracaso renal y que no expresan en sus datos la gravedad medida por SOFA o APACHE para evaluar qué tipo de pacientes trataron. Además, el tratamiento se inició entre 9 y 15 días tras el inicio de síntomas y, según sabemos, los pacientes que superan dicha fase sin fracaso respiratorio suelen evolucionar favorablemente14. En la tabla 2 se exponen las potenciales ventajas y limitaciones del uso de remdesivir en pacientes críticos.
Ventajas y limitaciones de remdesivir en el tratamiento de neumonía grave por SARS-CoV-2
| Disminución eficaz in vitro de la carga vírica |
| Administración intravenosa en pacientes en ventilación mecánica, evitando uso por sonda nasogástrica |
| Concentración adecuada en pulmón |
| Pocas interacciones |
| Restricción de su uso en UCI durante la pandemia por SARS-CoV-2 |
| Falta de estudios bien diseñados en enfermos críticos |
La mayoría de los estudios sobre la eficacia de los antivíricos se basan en infecciones por otros virus diferentes al SARS-CoV-2 y se han testado en estadios iniciales, que difieren del momento en que están ingresando los casos graves en las UCI. Los estudios sobre la eficacia se refieren más a la disminución de carga vírica que a factores relacionados con el pronóstico real en términos de evolución clínica, mortalidad y mejora del fracaso orgánico.
La falta de selección de pacientes que pueden beneficiarse de los tratamientos disponibles ha condicionado que el acceso a determinados antivíricos se haya visto limitado e insistimos en la importancia que las interacciones de estos fármacos pueden tener en los enfermos críticos, cuya base indiscutible del tratamiento es el soporte de los fracasos orgánicos que, principalmente, está siendo el respiratorio.
La posibilidad de actuar en distintas dianas apoya la recomendación de combinar varios tratamientos y esperar de ello un efecto sinérgico. Parece razonable que, si se trata, se haga en las etapas iniciales de la enfermedad, que es cuando cobra sentido disminuir la carga vírica. Sin embargo, no parece justificado prolongar la duración del tratamiento. Sí es muy recomendable hacer un seguimiento estrecho de las interacciones y efectos secundarios y, en caso de detectarlos, suspender el tratamiento ante la incertidumbre de su potencial beneficio.
El reto actual será no solo determinar qué agentes son eficaces contra el virus sino, más bien, determinar en qué momento de la enfermedad puede ser efectiva cada medida propuesta.
Los límites formales de las agencias reguladoras de los ensayos clínicos pivotales han conllevado que, clásicamente, los enfermos de UCI sean excluidos y, por tanto, es arriesgado extrapolar los datos provenientes de otros tipos de pacientes. La práctica clínica correcta, y por consiguiente ética, solo adquiere legitimidad social si ha sido previamente demostrada a través de la investigación clínica. Maximizar los potenciales beneficios clínicos ha de buscarse disminuyendo al máximo los posibles daños de los tratamientos no probados.
FinanciaciónEstudio no financiado.
Conflicto de interesesLos autores declaran que no hay conflicto de intereses.