Artículo: Abraham E, Laterre PF, Garbino J, Pingleton S, Butler T, Dugernier T, et al., for the Lenercept Study Group. Lenercept (p55 tumor necrosis factor receptor fusion protein) in severe sepsis and early septic shock: a randomized, double-blind, placebo-controlled, multicenter phase III trial with 1,342 patients. Crit Care Med 2001;29:503-10.
Antecedentes: se supone que el exceso de TNF contribuye al fracaso orgánico y a la mortalidad asociados a la sepsis.
Los receptores solubles del TNF se unen al TNF circulante previniendo la activación de sus células diana. En modelos experimentales de sepsis, lenercept neutraliza el TNF y reduce la mortalidad.
Un ensayo clínico en fase II sugiere que el lenercept puede reducir la mortalidad un 36%, en términos relativos, en el grupo de pacientes con sepsis grave y shock séptico de presentación reciente.
Objetivo: estimar la eficacia del lenercept en reducir la mortalidad de los pacientes con sepsis grave.
Diseño: ensayo clínico con asignación aleatoria.
Lugar: 108 centros de Europa, Estados Unidos y Canadá.
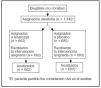
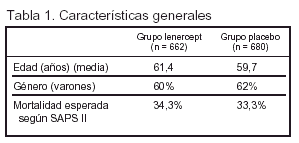
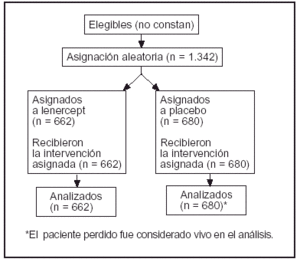
Pacientes (tabla 1 y fig. 1)
Figura 1
Criterios de inclusión: signos objetivos de infección, y al menos tres de los siguientes signos de sepsis: fiebre, taquicardia, taquipnea o leucocitosis, y al menos dos de los siguientes signos de hipoperfusión o de disfunción orgánica: acidosis, hipoxemia, trombocitopenia o coagulopatía u oliguria sin otra causa aparente, en las 12 horas anteriores a entrar en el estudio.
Criterios de exclusión: 1. Hipotensión con necesidad de fármacos vasoactivos durante > 4 h en las 24 h anteriores a la administración de lenercept. 2. Esperanza de vida < 3 meses. 3. Orden de no resucitación. 4. Infección por VIH. 5. Hemorragia no controlada. 6. Shock cardiogénico. 7. Rechazo de un órgano trasplantado. 8. Neutropenia secundaria a quimioterapia. 9. Tratamiento con hidrocortisona a dosis > 0,5 mg/kg/día. 10. Insuficiencia renal crónica en diálisis. 11. Pancreatitis. 12. Enfermedad hepática significativa.
Intervenciones que se comparan:
Grupo tratamiento: lenercept, 0,125 mg/kg de peso infundido durante 5-7 min.
Grupo control: placebo.
Asignación aleatoria: sí. No se explica en el texto si la asignación se mantuvo oculta.
Enmascaramiento: sí.
Desenlaces principales: mortalidad a los 28 días.
Análisis por intención de tratar: sí.
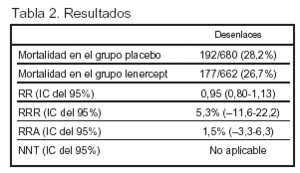
Resultados principales (tablas 2 y 3)
No se menciona la distribución por grupos del tipo de infección, ni de la adecuación del tratamiento antibiótico, ni de la incidencia de shock (globalmente, 27%).
Información sobre costes: no consta.
Financiación del estudio: en parte por F. Hoffmann-LaRoche, Ltd.
Conclusiones de los autores: el lenercept no presenta efecto significativo sobre la mortalidad en la población de estudio.
Conclusiones de los revisores: las conclusiones están de acuerdo con los resultados del estudio.
La población de estudio presenta una mortalidad en el grupo placebo en el rango bajo de la descrita en la sepsis grave, debida posiblemente a la exclusión de pacientes con necesidad de fármacos vasoactivos durante más de 4 h.