La mortalidad de los pacientes asmáticos ha disminuido de modo sustancial, principalmente por el avance en los tratamientos farmacológicos. Sin embargo, en algunos casos, a pesar del tratamiento médico óptimo, es necesario el soporte ventilatorio invasivo. El riesgo de barotrauma, que puede conllevar consecuencias fatales, está directamente relacionado con la hiperinsuflación pulmonar por atrapamiento aéreo y el aumento de la presión meseta (Pmes), siendo necesarios tiempos espiratorios prolongados e incluso desconexiones del respirador para disminuir la PEEP intrínseca1 El riesgo de muerte en pacientes con asma grave que precisan ventilación mecánica invasiva es del 6,5-10,3%2.
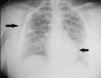
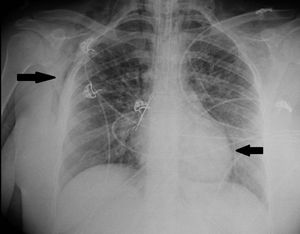
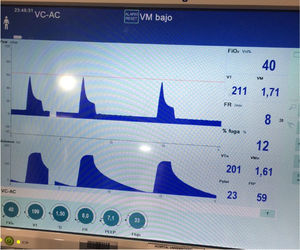
Presentamos el caso de una mujer de 21 años, fumadora de tabaco y de cannabis, con antecedente de asma intermitente extrínseco desde la infancia, que ingresó en la unidad de cuidados intensivos de nuestro hospital por una crisis asmática grave, que no había cedido tras tratamiento farmacológico máximo necesitando el apoyo de ventilación mecánica (VM) no invasiva. En situación de agotamiento muscular con acidosis respiratoria (pH 7,29, paCO2 63,2mmHg) precisó conexión a VM invasiva desde las primeras 3horas de ingreso. Durante los primeros días de estancia necesitó sedorrelajación profunda con midazolam, fentanest y cisatracurio y la administración de dosis muy elevadas de broncodilatadores inhalados (salbutamol 5mg/hora, ipratropio 0,5mg/hora, adrenalina 1mg/2horas), esteroides intravenosos (6-metilprednisolona 80mg/8horas) y fármacos de rescate intravenosos como la ketamina 60mg/kg/min en perfusión continua, sulfato de magnesio 12g/24horas y teofilina 0,8mg/kg/hora. Pese a ello, persistía una obstrucción grave al flujo aéreo, con atrapamiento aéreo a pesar de una ventilación protectora con hipercapnia permisiva: con volumen tidal (Vt) 440ml, relación inspiración-espiración 1:4, flujo 36l/min, PEEP 7mbar, FiO20,5, se generaba una presión pico 55-60mbar, Pmes35mbar, compliance de 23ml/mbar, PEEP total 16mbar. Tras 72horas de ingreso la paciente comenzó a presentar datos de barotrauma (neumopericardio, enfisema intersticial y subcutáneo [fig. 1], asociado a una acidosis respiratoria grave progresiva, con pH7,14 y paCO2 124mmHg. Decidimos implantar una membrana de oxigenación extracorpórea veno-venosa (ECMO VV) femoroyugular con el fin de poder realizar una ventilación ultraprotectora y reposo pulmonar (rest lung). Durante los siguientes días persistió la obstrucción respiratoria (fig. 2) y la pésima distensibilidad pulmonar (Vt<4ml/kg, relación inspiración-espiración 1:4, compliance 28ml/mbar, PEEP intrínseca 9mbar), precisando aún dosis altas de fármacos, la realización de lavados broncoalveolares mediante fibrobroncoscopia y maniobras de vaciado pulmonar. Tras 5 días en ECMO el cuadro obstructivo cedió, permitiendo modificar lentamente los parámetros ventilatorios, y destetar de la asistencia respiratoria extracorpórea al séptimo día. La evolución posterior fue lenta pero favorable, siendo dada de alta tras 25 días de ingreso. Como complicaciones asociadas presentó una infección respiratoria por S. aureus meticilín sensible y una miopatía del paciente crítico.
La ECMO VV constituye un mecanismo de soporte respiratorio temporal en el tratamiento de la insuficiencia respiratoria refractaria a las medidas convencionales, mejora la oxigenación, reduce el CO2 y permite reducir el riesgo de lesión pulmonar asociada a la VM mediante una ventilación protectora (Vt entre 4-6ml/kg) o ultraprotectora (Vt<4ml/kg)3.
El uso de la ECMO VV podría mejorar el pronóstico de grupos de pacientes con insuficiencia respiratoria aguda hipoxémica grave, como el síndrome de distrés respiratorio del adulto (SDRA), aunque aún se sigue considerando un tratamiento de rescate sin evidencia científica suficiente4.
Hay poca experiencia en su uso en casos de estatus asmáticos casi fatales en adultos, salvo publicaciones de casos y series5,6. La Extracorporeal Life Support Organization describió la evolución de los pacientes con estatus asmático que recibieron tratamiento de soporte con ECMO de su registro internacional desde 1986 hasta 20067. De los 1.257 pacientes que precisaron soporte respiratorio, tan solo 24 casos fueron por asma grave, implantándose la ECMO con una media de pH de 7,17mmHg (DE 0,16) y una media de paCO2 de 119,7mmHg (DE 58,1). Esta es la serie más amplia publicada, presentando una supervivencia del 83,3%. Sin embargo, a pesar de los buenos resultados, las complicaciones asociadas a la asistencia no fueron banales, describiéndose en un 37,5% sangrados relacionados con las cánulas o hemorragias pulmonares, infecciones (8,3%), complicaciones relacionadas con el circuito (41,4%) e incluso hemorragias intracraneales y muerte encefálica (12,5%). Di Lascio et al., en su reciente serie, incluyen 16 pacientes adultos con asma casi fatal durante 5 años que recibieron soporte con ECMO8. En esta serie, previa implantación de la ECMO, el pH medio fue de 6,89 (DE 0,014) y el paCO2 medio de 111mmHg (DE: 4,24), y recibieron lavados broncoalveolares con fibrobroncoscopio diariamente. Todos los pacientes sobrevivieron y ninguno presentó ninguna complicación relevante.
Recientemente se han desarrollado dispositivos específicos para la eliminación extracorpórea de CO2, menos complejos técnicamente que las ECMO, que podrían ser de utilidad en casos de necesidad de realizar rest lung9. Se ha planteado su uso en el SDRA y en la agudización de la EPOC, pero en el estatus asmático existe aún poca experiencia10.
Si analizamos nuestro caso y las series publicadas en el estatus asmático, por su naturaleza reversible, el soporte pulmonar con asistencia extracorpórea podría considerarse como una opción en el tratamiento precoz, sobre todo cuando se presenta en su vertiente más agresiva o casi fatal. Sin embargo, no están establecidos los criterios clínicos o gasométricos específicos para la implantación de la ECMO cuando es refractario al tratamiento convencional, como sucede en enfermedades como el SDRA. Por otro lado, las complicaciones asociadas a la ECMO son frecuentes y hay que valorar detenidamente los riesgos y los beneficios en cada caso, sin poder predecir el momento en el que el broncoespasmo va a ceder.
En nuestra paciente la decisión de implantar la asistencia se tomó cuando observamos datos incipientes de barotrauma, a pesar de mantener una hipercapnia permisiva moderada. Aun así fueron necesarios 5 días en ECMO con Vt<4ml/kg hasta que cedió el broncoespasmo. El riesgo que hubiese tenido que asumir con un tratamiento ventilatorio más convencional afortunadamente nunca lo sabremos.