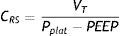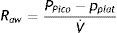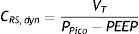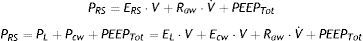La monitorización durante la ventilación controlada permite la determinación de diferentes parámetros de mecánica respiratoria. La interpretación adecuada de estos datos puede ser de utilidad para conocer el estado de los diferentes componentes del sistema respiratorio del paciente, así como para guiar los ajustes del ventilador. A lo largo de esta revisión se describen los conceptos básicos de mecánica respiratoria, su interpretación y su potencial para el ajuste fino de los parámetros de ventilación mecánica.
Monitoring during mechanical ventilation allows the measurement of different parameters of respiratory mechanics. Accurate interpretation of these data can be useful for characterizing the situation of the different components of the respiratory system, and for guiding ventilator settings. In this review, we describe the basic concepts of respiratory mechanics, their interpretation, and their potential use in fine-tuning mechanical ventilation.
Los pacientes críticos precisan ventilación mecánica invasiva (VM) en un alto porcentaje de casos, siendo esta una medida muchas veces imprescindible para la supervivencia del enfermo, aunque no inocua ni exenta de riesgos. La creciente preocupación por la denominada lesión pulmonar asociada a la ventilación mecánica (VALI) ha dirigido los esfuerzos al desarrollo de estrategias de ventilación que disminuyan en lo posible dicha lesión, evitando sus consecuencias tanto a nivel pulmonar como sistémico1.
Aunque la respuesta a la ventilación es en último término de naturaleza biológica, el factor desencadenante es mecánico2. La aplicación de un volumen de gas en el sistema respiratorio resulta en un juego de presiones y flujos que será más o menos complejo en función de los componentes que entren en juego. De esta manera, el resultado dependerá de si la ventilación es activa o no, de las características de la vía aérea y del parénquima pulmonar, así como de las propiedades de la pared torácica y de la activación de la musculatura respiratoria. Por tanto, la monitorización del paciente ventilado es la resultante final de las interacciones entre todos los elementos anteriormente descritos.
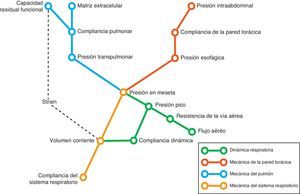
De manera recíproca, podemos intentar estimar el estado de cada uno de los elementos intervinientes en la mecánica respiratoria a partir del resultado final, que es el que obtenemos mediante la monitorización. Del mismo modo que para despejar varias incógnitas necesitamos múltiples ecuaciones, para conocer el estado de cada una de las piezas de este puzle necesitaremos diferentes variables, en ocasiones medidas en diferentes condiciones. La figura 1 presenta un esquema de algunas de estas variables y sus relaciones más evidentes.
Al final será necesario un análisis de diferentes resultados que convierta los datos obtenidos en conocimiento relevante para el manejo del enfermo. El objetivo de esta revisión pasa por describir los principales elementos de la mecánica ventilatoria y sus interacciones, con el fin de sentar las bases necesarias para la interpretación de dichos datos.
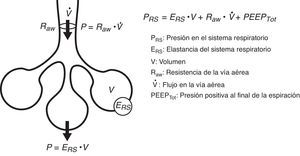
Ecuación del movimientoSe entiende por ecuación del movimiento a la relación entre la derivada temporal de una o varias variables y el estado físico del sistema al que pertenecen. Aplicado al tema que nos ocupa, se define la ecuación del movimiento del sistema respiratorio a la relación entre la presión en el sistema y los valores de volumen, flujo y flujo convectivo3. Esta ecuación y sus componentes se presentan en la figura 2. Lo que en definitiva representa esta ecuación es que la presión en cada momento en el sistema respiratorio tiene un componente elástico, necesario para la distensión del parénquima pulmonar, un componente resistivo, necesario para hacer avanzar el flujo de aire contra las resistencias de la vía aérea, y un componente inercial, debido a los cambios en el parénquima pulmonar causados por la aceleración del volumen. Se admite que para frecuencias respiratorias inferiores a 1Hz (60 resp/min) el componente debido a la inercia del sistema es despreciable, por lo que se suele desestimar4.
A partir de la ecuación del movimiento podemos dilucidar las condiciones que se tienen que dar para realizar un estudio adecuado de la mecánica respiratoria. Para facilitar la interpretación de los datos, el paciente no debe realizar ningún esfuerzo respiratorio, con lo que la Pmus equivale a 0. Si obtenemos una medida de presión en condiciones de flujo 0 (denominadas condiciones estáticas), el componente resistivo de la presión se anula. En esta situación podemos calcular la compliancia del sistema respiratorio, tal y como se detallará más adelante. Por eso es necesario realizar pausas inspiratorias y espiratorias, que hacen que el flujo en la vía aérea sea 0, para medir algunos de los parámetros mecánicos. Del mismo modo, pueden obtenerse medidas en condiciones de flujos inspiratorios muy bajos (menores de 9 l/min), que hacen que el componente resistivo de la presión sea despreciable5. En este caso se habla de condiciones cuasiestáticas. Por último, se habla de condiciones dinámicas cuando existe un flujo de aire no nulo en la vía aérea. Un mismo parámetro como la compliancia puede tener significados muy diferentes en función de las condiciones en las que se haya obtenido (estáticas o dinámicas).
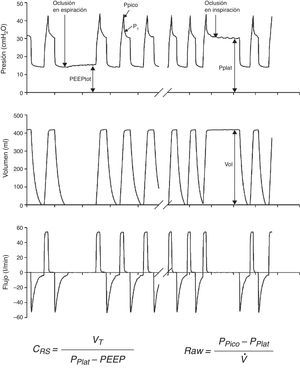
Mediciones en condiciones estáticasSi partimos de un modo ventilatorio controlado por volumen y obtenemos la curva tiempo-presión, podemos observar una caída de la presión inmediatamente después del cierre de la válvula inspiratoria. Durante este tiempo de pausa inspiratoria, antes de que la válvula espiratoria se abra, el flujo se detiene permitiendo que el volumen de aire entregado se mantenga y distribuya homogéneamente, en virtud del equilibrio alcanzado por las fuerzas viscoelásticas del pulmón. La presión alcanzada entonces, en condiciones estáticas, se define como presión meseta o plateau (Pplat) y es un reflejo de la presión de retracción elástica del sistema respiratorio. Cuando se alcanza el equilibrio en las presiones de la vía aérea del enfermo, la Pplat equivale a la presión alveolar (PA) (fig. 3).
Desarrollando más este concepto, la compliancia del sistema respiratorio (CRS) se puede definir como la relación entre presión y volumen, calculada habitualmente con la fórmula:
mientras que la elastancia se define como el inverso de la compliancia (esto es, presión por unidad de volumen).La medición de la PEEP total se realiza también en condiciones de flujo 0, al final de la espiración, realizando una pausa antes del comienzo del siguiente ciclo. Si bien su determinación se realiza de una manera sencilla, la interpretación del valor obtenido debe hacerse teniendo en cuenta las posibles situaciones que pueden originarla. Así, en aquellos pacientes en los que existe una espiración activa, se generará un gradiente de presión entre los alvéolos y el aire atmosférico; existe por tanto una presión positiva al final de la espiración intrínseca, pero que no supone un insuficiente vaciamiento del volumen tidal sino un aumento de la presión de retracción de la caja torácica en virtud del esfuerzo muscular. Por lo tanto, es necesaria la ausencia de esfuerzos espiratorios para una correcta medición de este parámetro.
La compliancia es una variable no lineal inherente al propio sistema respiratorio que se va modificando a medida que cambian tanto las condiciones del parénquima pulmonar como las de la caja torácica. Así, la presencia de atelectasias o de un SDRA causan una merma en la compliancia total del sistema respiratorio sin que la naturaleza elástica del pulmón sano remanente se vea afectada, poniendo en evidencia la dependencia que tiene la compliancia del volumen ventilable6. Sin embargo, el cálculo de la compliancia de acuerdo con esta fórmula se limita a un estado concreto del sistema respiratorio. Un estudio más detallado de las propiedades elásticas del sistema pasa por determinar la compliancia a distintos niveles de la curva (por ejemplo, a diferentes niveles de PEEP). Por último, el trazado de curvas presión-volumen supone una caracterización más completa de las propiedades mecánicas del sistema respiratorio, de tal manera que la compliancia es la pendiente de esa curva en cada punto. En la práctica clínica, la medición de las curvas estáticas presión-volumen resulta como mínimo laboriosa y entraña mayor o menor riesgo para el enfermo dependiendo del método utilizado. El lector interesado puede acudir a recientes revisiones sobre esta forma de monitorización en particular7,8.
Mediciones en condiciones dinámicasVolviendo a la ecuación del movimiento del sistema respiratorio, otra variable susceptible de ser monitorizada es la resistencia que se opone al flujo de aire. Puede calcularse como el cociente entre la diferencia de presión inicial (vía aérea proximal) y final (alvéolos) del circuito y el flujo de aire circulante.
Si bien el tejido pulmonar y las estructuras de la caja torácica ofrecen cierto grado de resistencia, la que ejercen las vías aéreas supone casi el total de las fuerzas opuestas al flujo. La resistencia de la vía aérea tiene relación con el volumen pulmonar en tanto en cuanto disminuye a medida que el pulmón se insufla y las vías aéreas tienden a abrirse9. Por lo tanto la resistencia es generalmente menor durante la inspiración, puesto que durante la espiración la tendencia es la opuesta.
Cuando el flujo es laminar, con velocidades bajas, la resistencia de la vía aérea varía de manera directamente proporcional a la viscosidad del gas y a la longitud de la vía aérea e inversamente proporcional a la cuarta potencia del radio de la vía aérea. De esta forma, si el radio de la vía aérea se redujera a la mitad, el flujo de aire circulante tendría que oponerse a una resistencia 16 veces mayor (ley de Poiseuille). En condiciones normales, el área de sección transversal total de la vía aérea aumenta de manera exponencial a medida que avanzamos en las sucesivas generaciones del árbol traqueobronquial. Es el radio de la vía aérea el principal determinante de la resistencia, dado que la longitud de la vía y la viscosidad del gas no se modifican en principio. En el enfermo ventilado mecánicamente hay que tener en cuenta la resistencia generada por el tubo endotraqueal.
La compliancia dinámica10 se define como la relación entre volumen corriente y presión máxima alcanzada en el sistema respiratorio, de acuerdo con la fórmula:
Este parámetro valora en conjunto el impacto de la caja torácica, el parénquima pulmonar y la resistencia de la vía aérea. Sus valores oscilan entre 10 y 20% menos que la compliancia estática, estando influidos por la edad y el peso11.
Mecánica de la pared torácicaLa pared torácica y el parénquima pulmonar funcionan, desde un punto de vista mecánico, como un sistema en serie. Es decir, las presiones generadas por ambos subsistemas se suman, contribuyendo a la presión final resultante. De esta manera, la ecuación del movimiento presentada anteriormente puede transformarse en otra que contemple la contribución de cada compartimento a la presión final:
donde PL es la presión transpulmonar, Pcw es la presión esofágica, EL la elastancia pulmonar, V el volumen pulmonar, Ecw la elastancia de la pared torácica, V˙ el flujo en la vía aérea y PEEPTot la presión positiva total al final de la espiración. En general se admite que la pared torácica no contribuye de manera significativa a generar una presión resistiva en el sistema respiratorio.Para la monitorización de la mecánica de la pared torácica es necesaria la medición de la presión pleural. El principal método de medida de esta presión es mediante la colocación de un catéter esofágico12. El tercio distal del esófago se encuentra en relación de vecindad con la cavidad pleural, y se asume que las presiones que se registran en este punto son equivalentes. Sin embargo, la validez de esta asunción está sometida a debate permanente. El registro de presiones en esta zona está sometido al artefacto generado por el corazón. Por otra parte, resulta difícil dar un valor absoluto de presión pleural, ya que existe un gradiente de presiones a lo largo de todo el tórax que influye en la distensión regional del parénquima pulmonar. A pesar de estas limitaciones, se considera que los cambios (valores relativos) en la presión esofágica se correlacionan de manera adecuada con los cambios en la presión pleural13. Por último, aunque se ha documentado una correlación aceptable entre la compliancia de la pared torácica y la presión intraabdominal14, la validez de esta correlación ha sido puesta en duda recientemente15.
Con este registro de presiones en un paciente ventilado puede calcularse la presión transpulmonar como la diferencia entre la presión en la vía aérea y la presión esofágica. Esta presión transpulmonar es la auténtica presión de distensión del parénquima pulmonar, por lo que parecería razonable su uso para el ajuste de la ventilación mecánica16,17. Utilizando los valores de presión transpulmonar y presión esofágica pueden calcularse la compliancia del parénquima pulmonar y de la pared torácica (como el cociente entre el volumen corriente y cada una de las presiones). Dado que una misma presión en la vía aérea puede resultar en presiones transpulmonares diferentes en función de las características mecánicas de la pared torácica, puede resultar de interés la monitorización de esta última para determinar el estrés real al que está sometido el parénquima pulmonar18. Por otro lado, la presencia de presiones transpulmonares negativas al final de la espiración es indicativa de una tendencia al colapso, predominantemente en las zonas dependientes del pulmón. Algunos investigadores han sugerido que los valores de PEEP deberían elevarse hasta hacer ligeramente positiva esta presión transpulmonar teleespiratoria19.
Estimación de la deformación del parénquima pulmonarEl desarrollo de la mecánica respiratoria en el paciente ventilado radica en el interés de utilizar los diferentes parámetros de mecánica respiratoria como guía para ajustar la ventilación mecánica y, especialmente, para disminuir la lesión asociada a la ventilación. Sin embargo, como ya se ha visto, la interpretación de cada dato debe hacerse en un contexto determinado y múltiples factores pueden influir en cada determinación. A modo de ejemplo, un valor aislado de presión en meseta puede tener un significado muy diferente en función de la compliancia de la pared abdominal, del esfuerzo inspiratorio del paciente o de la PEEP aplicada.
El refinamiento de los paradigmas de la lesión asociada a la ventilación mecánica ha llevado a la identificación de nuevos mecanismos de lesión y sus parámetros de monitorización correspondientes. En este sentido, los beneficios derivados del empleo de la PEEP en conjunción con la reducción paulatina del volumen corriente hace plantearse que es la deformación del parénquima pulmonar, y no solo la aplicación de una presión o un volumen, la causa del daño tisular20. Este concepto de que el estrés estático (presiones y volúmenes en ausencia de deformación) es mejor tolerado que el dinámico (con deformación del tejido) surge de modelos experimentales en cultivos celulares y animales21,22, y se abre camino hacia la práctica clínica. Los parámetros fisiológicos que permiten cuantificar la deformación tisular y su coste son el estrés y el strain23.
El estrés es la fuerza necesaria para deformar un cuerpo. En el caso que nos ocupa, para inflar el pulmón con el volumen corriente. De todos los conceptos anteriormente descritos se desprende que el equivalente al estrés es la presión transpulmonar.
El strain (mantenemos el término en inglés por su mayor difusión en la literatura) es la magnitud de esa deformación, expresada como fracción de la situación inicial. Aplicado a la mecánica respiratoria, la magnitud de la deformación es el volumen corriente. Sin embargo, hay cierta controversia respecto a cuál debe ser la situación inicial. En su propuesta original, el grupo de Gattinoni utiliza la capacidad residual funcional23. Esto es, el volumen de gas en el pulmón al final de una espiración a presión atmosférica. Otros autores han utilizado el volumen teleespiratorio (end-expiratory lung volume [EELV], volumen pulmonar al final de una espiración en presencia de PEEP)24,25. La diferencia entre ambas mediciones viene dada por los umbrales de seguridad y el ajuste de los cálculos en presencia de PEEP (tabla 1). En el primer caso, el aumento del volumen pulmonar se contabiliza como «deformación», y por tanto se sumaría al volumen corriente. En el segundo caso, este volumen se suma a la capacidad residual funcional. Dicho de otra manera, la adición de PEEP aumenta el strain si se computa usando la primera fórmula, mientras que lo disminuye si se utiliza la segunda. En realidad, hay que entender que la aplicación de PEEP produce tanto un reclutamiento de zonas previamente no aireadas (con lo que disminuiría el strain, ya que aumentaría el parénquima pulmonar disponible para la ventilación) como un aumento del volumen de zonas ya aireadas (con lo que aumentaría el strain). Por tanto, para un adecuado cálculo del cambio del strain en respuesta a la PEEP vuelve a ser necesaria la medición del volumen reclutado. El tema del reclutamiento alveolar excede los propósitos de este trabajo, por lo que el lector puede acudir a varias revisiones sobre el tema26,27.
Implicaciones clínicasLos objetivos principales de la monitorización de la mecánica son el diagnóstico del estado de la función respiratoria y la guía para el ajuste de la ventilación. No hay ninguna técnica diagnóstica que mejore por sí sola el pronóstico de los pacientes si no se acompaña de un tratamiento eficaz de lo que se diagnostica. Por lo tanto, para que redunde en un beneficio para los pacientes, la información obtenida mediante la monitorización, tras ser interpretada, debe convertirse en conocimiento que resulte en una mejora del tratamiento.
En lo que se refiere a las posibilidades diagnósticas, el análisis de los registros procedentes del ventilador permiten la detección de atrapamiento aéreo y auto-PEEP, la presencia de secreciones en el tubo endotraqueal o las alteraciones en la interacción entre el paciente y el ventilador, tal y como se ha descrito en una reciente monografía28.
Pero el auge de la mecánica respiratoria en el paciente ventilado se debe de manera muy especial a su potencial como guía para el ajuste de la ventilación mecánica. El desarrollo del paradigma de la lesión inducida/asociada al ventilador ha hecho que un objetivo básico en los pacientes sea la prevención de la misma. En este sentido, una medida estándar en la actualidad es la limitación de las presiones en meseta, especialmente en los pacientes con distrés respiratorio agudo29. Como marcador de la presión alveolar, las presiones en meseta deben mantenerse dentro de unos límites de seguridad para evitar la lesión por sobredistensión. En la actualidad se recomienda evitar unos valores superiores a 28-32cmH2O30.
Sin embargo, como ya se ha discutido, la presión en meseta puede estar elevada por una compliancia de la pared torácica anormalmente disminuida, y es la presión transpulmonar la auténtica fuerza de distensión alveolar. El empleo de esta presión como guía para el ajuste de la ventilación se asoció a buenos resultados clínicos a pesar de presiones en meseta elevadas19. Aunque no existen recomendaciones firmes sobre el empleo de la presión transpulmonar (que conlleva la monitorización de la presión esofágica, con las dificultades y limitaciones ya comentadas), parece razonable plantearse estas aproximaciones en pacientes con cuadros graves de insuficiencia respiratoria16.
Por último, existen multitud de estudios en la literatura proponiendo un ajuste de la PEEP de acuerdo con las características mecánicas del sistema respiratorio. Ya en el año 1976, el trabajo pionero de Suter correlacionó una PEEP ajustada según el punto de mejor compliancia estática con el mejor transporte de oxígeno en pacientes con distrés respiratorio agudo31. En un ensayo clínico reciente, el ajuste de la PEEP de acuerdo con la mejor compliancia se asoció a una mejor oxigenación, una menor incidencia de fallos orgánicos y una tendencia a menor mortalidad32.
Con aproximaciones similares, varios grupos han utilizado las medidas de compliancia dinámica. La PEEP que resulta en un mayor valor de compliancia dinámica se ha asociado en diferentes estudios a la prevención del colapso alveolar tras el reclutamiento33 y a una ventilación óptima34.
También se han empleado diferentes puntos de inflexión de la curva presión-volumen como guía para el ajuste de la PEEP35,36. Sin embargo, los escasos ensayos clínicos37,38 que han utilizado estas estrategias han tenido como grupo control pacientes ventilados con volúmenes altos, con lo que resulta imposible dilucidar si los efectos beneficiosos se deben al ajuste fino de la PEEP o simplemente a la protección por volúmenes corrientes bajos.
ConclusionesLa aplicación de ventilación mecánica supone una buena oportunidad parar la realización de estudios de mecánica respiratoria. A través de diferentes técnicas, maniobras y cálculos podemos determinar el estado del sistema respiratorio del paciente ventilado y aplicar tratamientos en consecuencia. Sin embargo, las medidas tienen sus limitaciones y los posibles tratamientos tienen efectos adversos. Hasta la fecha no se dispone de ninguna evidencia sólida de que una determinada medida de mecánica respiratoria ofrezca una guía clara para el ajuste del tratamiento. Por tanto, aunque la mecánica puede ayudarnos a entender qué ocurre en el sistema respiratorio de un paciente ventilado, no se puede proponer con rotundidad una guía para el ajuste del ventilador basada en estas medidas. La mecánica ventilatoria debe ser interpretada por el clínico como una ayuda en el contexto global del paciente.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.