Determinar la capacidad de predicción del índice de shock y del índice de shock modificado para hemorragia masiva tras sufrir un trauma grave.
DiseñoCohorte retrospectiva.
ÁmbitoAtención inicial hospitalaria al paciente con enfermedad traumática grave en una unidad de cuidados intensivos de trauma de un hospital terciario.
SujetosPacientes mayores de 14 años con trauma grave (injury severity score [ISS] >15), admitidos de forma consecutiva desde enero de 2014 hasta diciembre de 2015.
VariablesSe estudiaron sensibilidad (Se), especificidad (Sp), valores predictivos positivo y negativo (VP+ y VP–), razones de verosimilitud positiva y negativa (RV+ y RV–), curvas ROC (receiver operating characteristics) y el área bajo las mismas (AUROC) para predicción de hemorragia masiva.
ResultadosSe incluyeron 287 pacientes, el 76,31% (219) fueron varones, con una edad media de 43,36 (±17,71) e ISS de 26 (rango intercuartil [RIC]: 21-34). La frecuencia global de hemorragia masiva fue de 8,71% (25). Para el índice de shock se obtuvo: AUROC de 0,89 (intervalo de confianza [IC] 95%: 0,84-0,94), con un punto de corte óptimo en 1,11, Se del 91,3% (IC 95%: 73,2-97,58) y Sp del 79,69% (IC 95%: 74,34-84,16). Para el índice de shock modificado se obtuvo: AUROC de 0,90 (IC 95%: 0,86-0,95), con un punto de corte óptimo en 1,46, Se del 95,65% (IC 95%: 79,01-99,23) y Sp del 75,78% (IC 95%: 70,18-80,62).
ConclusionesEl índice de shock y el índice de shock modificado son buenos predictores de hemorragia masiva y de fácil aplicación durante la atención inicial del trauma grave.
To determine the predictive value of the Shock Index and Modified Shock Index in patients with massive bleeding due to severe trauma.
DesignRetrospective cohort.
SettingSevere trauma patient's initial attention at the intensive care unit of a tertiary hospital.
SubjectsPatients older than 14 years that were admitted to the hospital with severe trauma (Injury Severity Score >15) form January 2014 to December 2015.
VariablesWe studied the sensitivity (Se), specificity (Sp), positive and negative predictive value (PV+ and PV–), positive and negative likelihood ratio (LR+ and LR–), ROC curves (Receiver Operating Characteristics) and the area under the same (AUROC) for prediction of massive hemorrhage.
Results287 patients were included, 76.31% (219) were male, mean age was 43,36 (±17.71) years and ISS was 26 (interquartile range [IQR]: 21-34). The overall frequency of massive bleeding was 8.71% (25). For Shock Index: AUROC was 0.89 (95% confidence intervals [CI] 0.84 to 0.94), with an optimal cutoff at 1.11, Se was 91.3% (95% CI: 73.2 to 97.58) and Sp was 79.69% (95% CI: 74.34 to 84.16). For the Modified Shock Index: AUROC was 0.90 (95% CI: 0.86 to 0.95), with an optimal cutoff at 1.46, Se was 95.65% (95% CI: 79.01 to 99.23) and Sp was 75.78% (95% CI: 70.18 to 80.62).
ConclusionShock Index and Modified Shock Index are good predictors of massive bleeding and could be easily incorporated to the initial workup of patients with severe trauma.
El shock hemorrágico es la principal causa de muerte prevenible tras sufrir un trauma grave. Su identificación precoz sigue siendo difícil a nivel extrahospitalario y hospitalario, lo que causa un infratriaje y una transferencia inapropiada1,2.
El diagnóstico precoz del shock hemorrágico es un sine qua non para mejorar los resultados tras sufrir un trauma y con ello el control del sangrado. Una predicción precoz y precisa del shock hemorrágico permite la preparación adecuada del equipo de atención inicial y la activación precoz del protocolo de hemorragia masiva (PHM)3-5.
Estudios retrospectivos analizan diferentes índices de predicción, valorando su capacidad diagnóstica para hemorragia masiva (HM). Estos índices son complicados de realizar; para su determinación precisan de resultados de laboratorio y pruebas de imagen que consumen mucho tiempo y son difíciles de realizar a nivel extrahospitalario6.
Por otro lado, parámetros clínicos simples como la frecuencia cardiaca o la presión arterial han demostrado ser inexactos para predecir HM7-9.
El índice de shock (IS), definido como la frecuencia cardiaca dividida por la presión arterial sistólica, y el índice de shock modificado (ISM), definido como la frecuencia cardiaca dividida por la presión arterial media, son 2 índices que por su simplicidad y fácil aplicabilidad han sido motivo de estudio por diferentes autores.
Distintos estudios han demostrado que tras sufrir un trauma grave, un IS elevado se asocia con una elevada mortalidad10-12 y con la gravedad de la lesión13. El IS también se ha utilizado como predictor de días de ventilación mecánica y de estancia hospitalaria14, así como de la probabilidad de ingreso en una unidad de críticos15. Finalmente, existen estudios que relacionan el IS con la necesidad de transfusión sanguínea y la necesidad de una intervención hemostática16. Sin embargo, se sabe menos sobre su capacidad diagnóstica de HM.
El objetivo de nuestro estudio es determinar la capacidad de predicción del IS y del ISM para HM y determinar el punto de corte óptimo en pacientes que han sufrido un trauma grave.
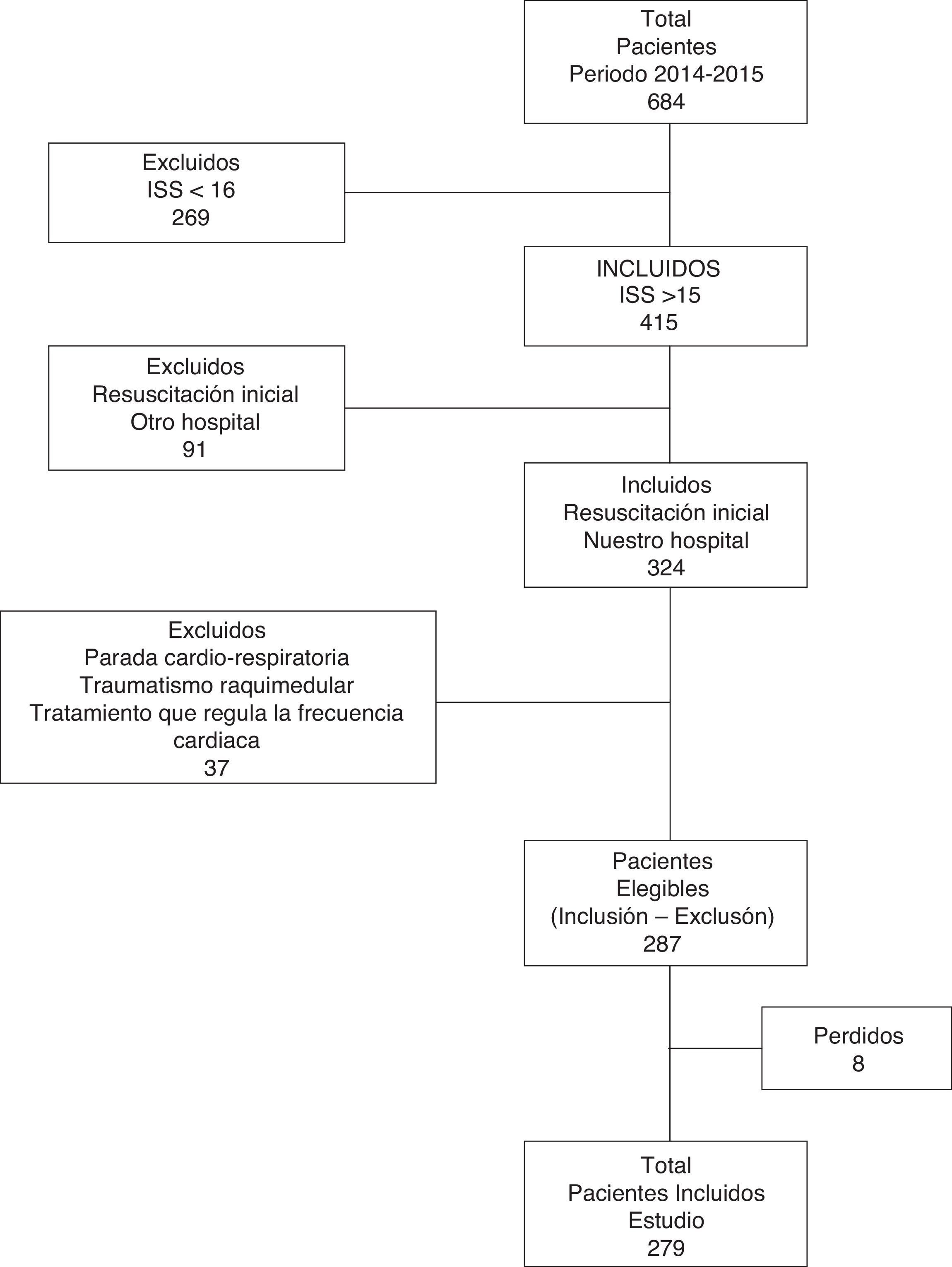
Diseño y métodosEstudio de cohortes retrospectiva (se incluyen todos los pacientes de forma consecutiva), realizado en una UCI de trauma y emergencias de un hospital terciario. Se incluyen pacientes mayores de 14 años con trauma grave (injury severity score [ISS] >15), a quienes realizamos la atención inicial a su llegada al hospital, admitidos desde enero de 2014 hasta diciembre de 2015 (se han excluido pacientes con parada cardiorrespiratoria en la atención extrahospitalaria, traumatismo raquimedular, uso de medicación que regula la frecuencia cardiaca y reanimación inicial realizada en otro centro). La atención inicial al trauma la realiza un equipo de atención especializado, constituido por 2 médicos de intensivos (adjunto y residente), 2 enfermeras, un auxiliar y 2 celadores. También integran el equipo diferentes especialidades consultoras relacionadas con la asistencia al paciente traumático. La atención se realiza según los esquemas del Advanced Trauma Life Support (ATLS). El hospital cuenta con un PHM aprobado por la comisión de transfusiones y la dirección del hospital.
La recogida de variables se realizó con enmascaramiento del observador. Se recogieron: variables demográficas (edad y sexo); variables fisiológicas (se recoge la primera frecuencia cardiaca, presiones arteriales sistólica y diastólica tras su llegada al hospital —box de reanimación inicial de UCI—); variables analíticas (gasometría arterial-pH, exceso de bases [EB], láctico, y variables pronósticas (revised trauma score [RTS], ISS). Se realizó una consulta del registro de transfusión de nuestra unidad, de donde se obtuvo el número de concentrados de hematíes transfundidos en las primeras 24h de cada paciente. Se definió HM a la administración de 10 o más concentrados de hematíes en las primeras 24h de ingreso tras el trauma. Posteriormente se realizó el cálculo matemático para determinar el IS y el ISM. El IS fue definido como la frecuencia cardiaca dividida por la presión arterial sistólica, y el ISM fue definido como la frecuencia cardiaca dividida por la presión arterial media; no se realizó la determinación del ISM en los pacientes sin presión arterial diastólica. Finalmente, se revisó el informe médico de alta, para valorar la estancia hospitalaria y la mortalidad.
Para el análisis de variables cualitativas se utilizó como medida de frecuencia la proporción. Para las variables cuantitativas se utilizó la media (±desviación estándar) y la mediana (rango intercuartil [RIC]). Para estimar la relación entre 2 variables categóricas se utilizaron las pruebas de χ2 y exacta de Fisher. Para la comparación entre 2 medias se utilizó la prueba t de Student (previo supuesto de normalidad —prueba de Kolmogorov-Smirnov— y homogeneidad de varianzas —prueba de Levene—); si se vulneran los supuestos se aplica la prueba T de Wilcoxom (nivel de significación 0,05).
Para cada índice se calcularon la sensibilidad, especificidad, valor predictivo positivo (VP+), valor predictivo negativo (VP–), razón de verosimilitud positiva (RV+) y razón de verosimilitud negativa (RV–). Se obtuvieron las curvas receiver operating characteristics (ROC) y se calculó el área bajo la curva (AUROC) con sus respectivos intervalos de confianza al 95%. Todos los análisis se realizaron con el paquete estadístico SPSS® para Windows (versión 19.0).
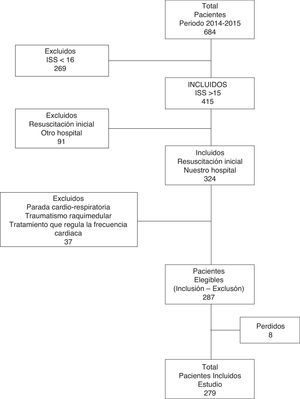
ResultadosSe estudiaron 287 pacientes (fig. 1). El 76,31% (219) fueron hombres, con una edad media de 43,36 (±17,71) años y un ISS de 26 (RIC: 21-34). El trauma cerrado fue del 91,6% (con la precipitación como mecanismo más frecuente). La frecuencia global de HM fue del 8,71% (25), los días de estancia en UCI de 3,74 (RIC: 1,81-11,55) y la mortalidad, del 15,33% (44).
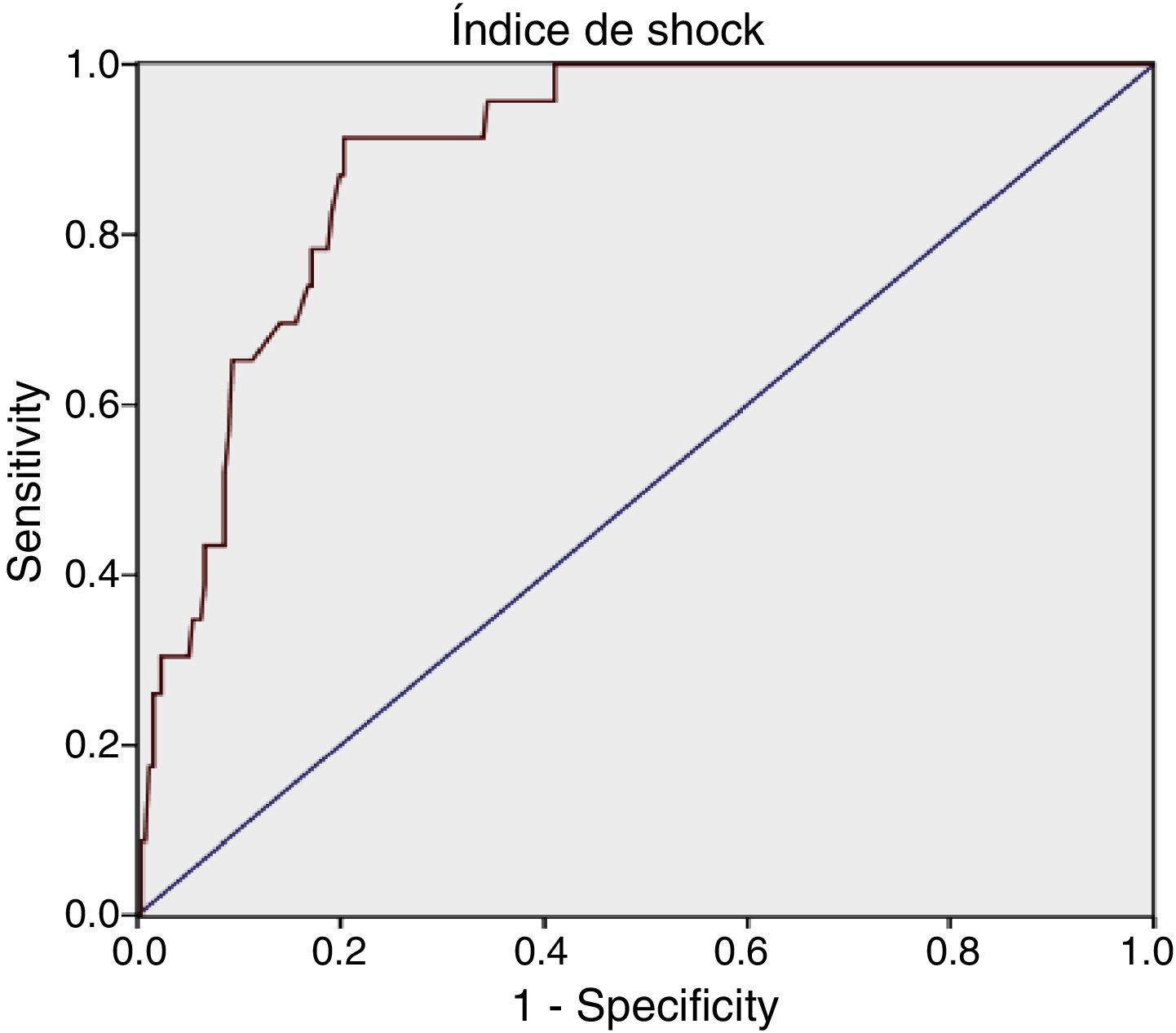
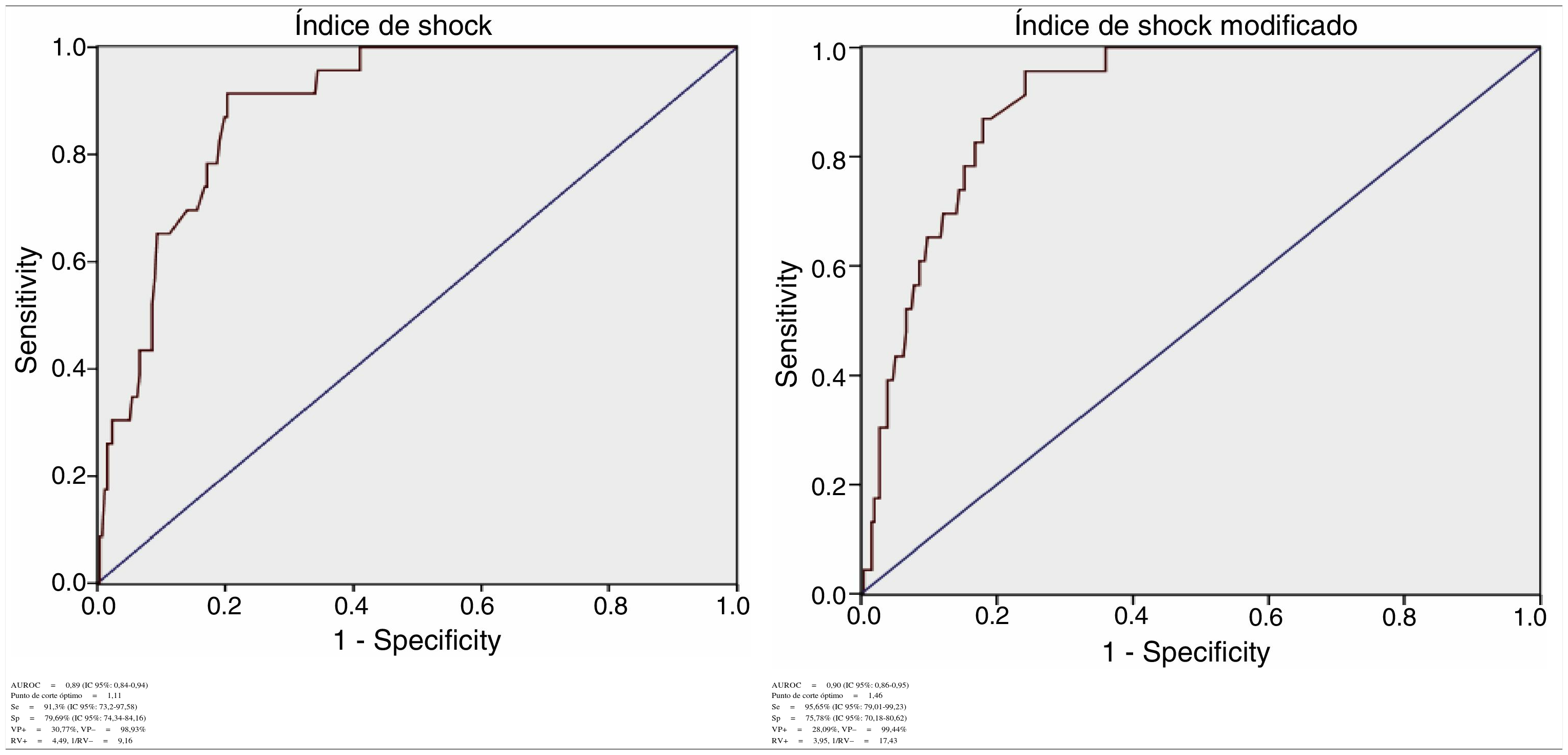
Para el IS se obtuvo: AUROC de 0,89 (IC 95%: 0,84-0,94), con un punto de corte óptimo en 1,11, sensibilidad del 91,3% (IC 95%: 73,2-97,58) y especificidad del 79,69% (IC 95%: 74,34-84,16).
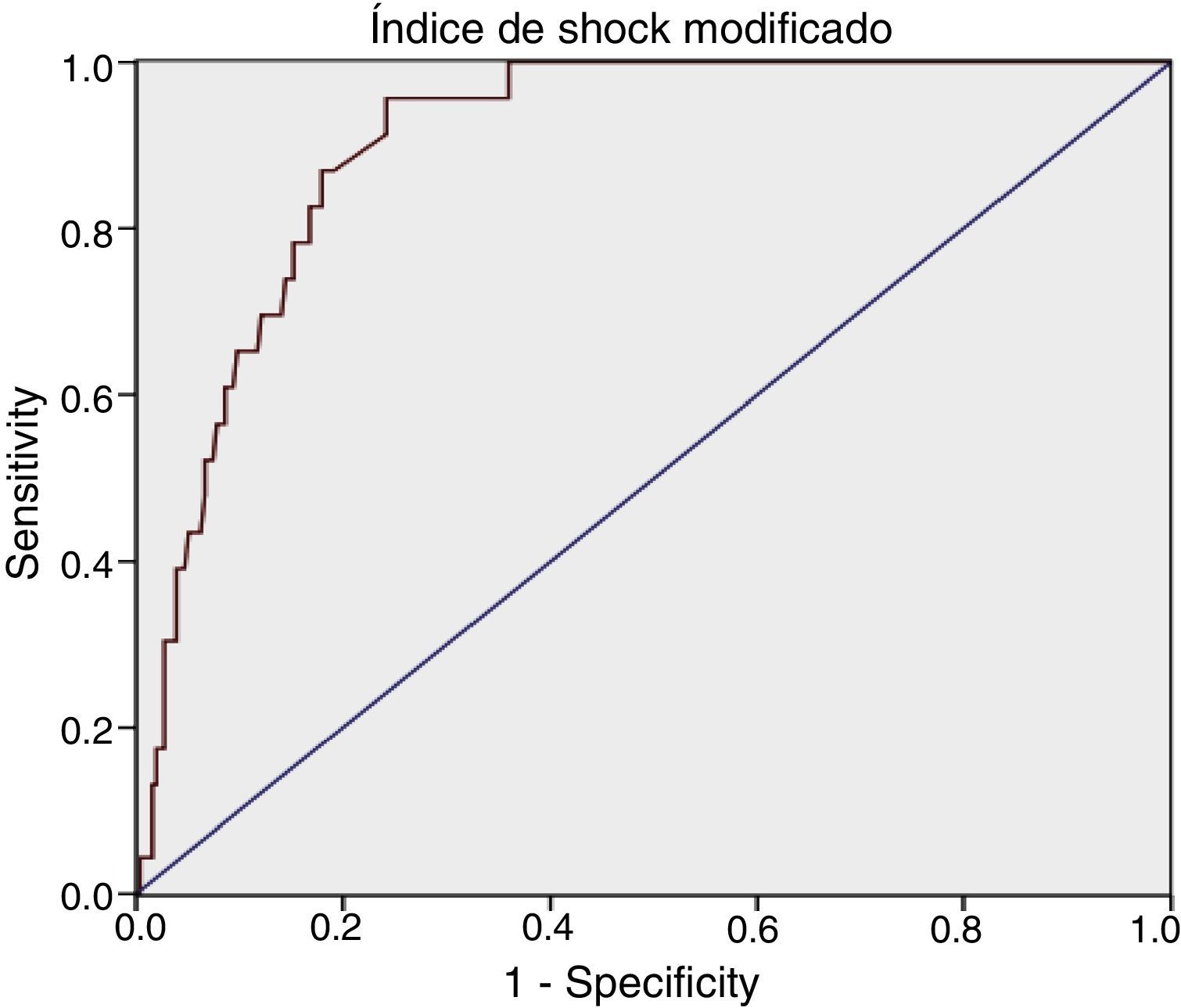
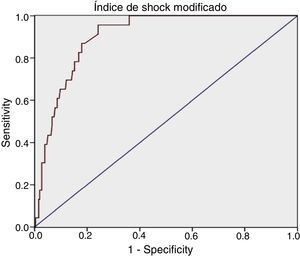
Para el ISM se obtuvo: AUROC de 0,90 (IC 95%: 0,86-0,95), con un punto de corte óptimo en 1,46, sensibilidad del 95,65% (IC 95%: 79,01-99,23) y especificidad del 75,78% (IC 95%: 70,18-80,62) (tabla 1).
Determinación diagnóstica del índice de shock e índice de shock modificado
| AUROC=0,89 (IC 95%: 0,84-0,94) Punto de corte óptimo=1,11 | AUROC=0,90 (IC 95%: 0,86-0,95) Punto de corte óptimo=1,46 |
| Se=91,3% (IC 95%: 73,2-97,58) | Se=95,65% (IC 95%: 79,01-99,23) |
| Sp=79,69% (IC 95%: 74,34-84,16) | Sp=75,78% (IC 95%: 70,18-80,62) |
| VP+=30,77%, VP–=98,93% | VP+=28,09%, VP–=99,44% |
| RV+=4,49, 1/RV–=9,16 | RV+=3,95, 1/RV–=17,43 |
AUROC: área bajo las curvas ROC; IC: intervalo de confianza; RV+: razón de verosimilitud positiva; RV–: razón de verosimilitud negativa; Se: sensibilidad; Sp: especificidad; VP+: valor predictivo positivo; VP–: valor predictivo negativo.
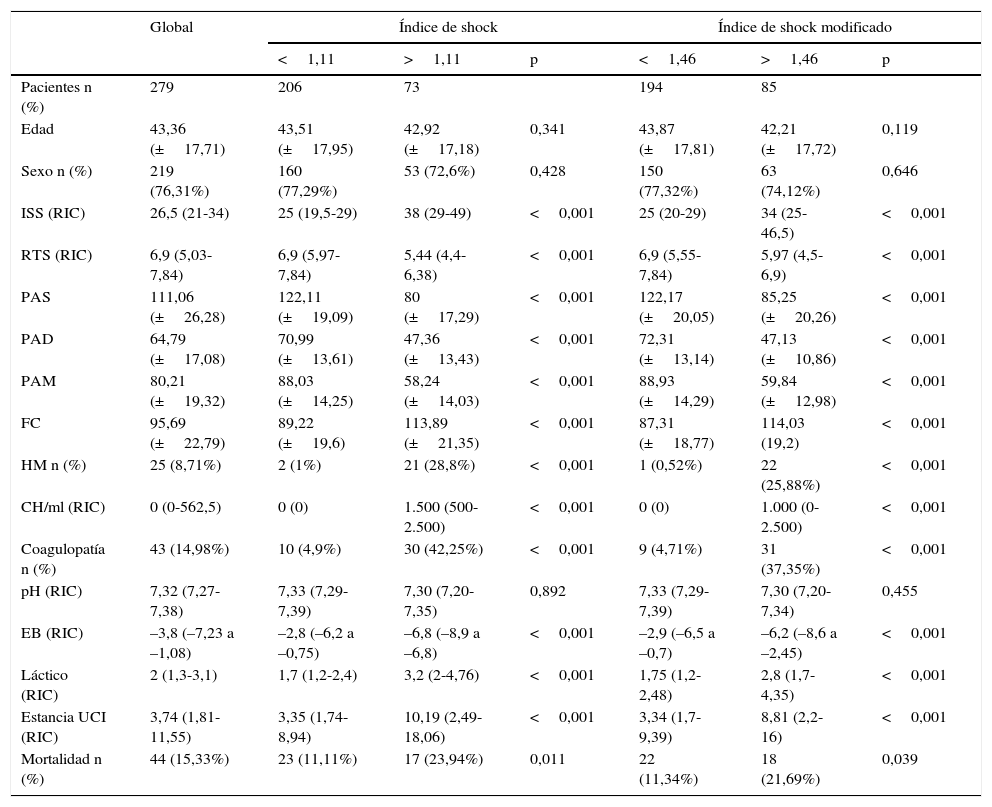
Se realizó un análisis a posteriori con los puntos de corte establecidos y se contrastaron diferentes variables obteniendo diferencias significativas para HM, gravedad de la lesión (ISS), coagulopatía, estancia en UCI y mortalidad (tabla 2).
Características de los pacientes según el índice de shock y el índice de shock modificado
| Global | Índice de shock | Índice de shock modificado | |||||
|---|---|---|---|---|---|---|---|
| <1,11 | >1,11 | p | <1,46 | >1,46 | p | ||
| Pacientes n (%) | 279 | 206 | 73 | 194 | 85 | ||
| Edad | 43,36 (±17,71) | 43,51 (±17,95) | 42,92 (±17,18) | 0,341 | 43,87 (±17,81) | 42,21 (±17,72) | 0,119 |
| Sexo n (%) | 219 (76,31%) | 160 (77,29%) | 53 (72,6%) | 0,428 | 150 (77,32%) | 63 (74,12%) | 0,646 |
| ISS (RIC) | 26,5 (21-34) | 25 (19,5-29) | 38 (29-49) | <0,001 | 25 (20-29) | 34 (25-46,5) | <0,001 |
| RTS (RIC) | 6,9 (5,03-7,84) | 6,9 (5,97-7,84) | 5,44 (4,4-6,38) | <0,001 | 6,9 (5,55-7,84) | 5,97 (4,5-6,9) | <0,001 |
| PAS | 111,06 (±26,28) | 122,11 (±19,09) | 80 (±17,29) | <0,001 | 122,17 (±20,05) | 85,25 (±20,26) | <0,001 |
| PAD | 64,79 (±17,08) | 70,99 (±13,61) | 47,36 (±13,43) | <0,001 | 72,31 (±13,14) | 47,13 (±10,86) | <0,001 |
| PAM | 80,21 (±19,32) | 88,03 (±14,25) | 58,24 (±14,03) | <0,001 | 88,93 (±14,29) | 59,84 (±12,98) | <0,001 |
| FC | 95,69 (±22,79) | 89,22 (±19,6) | 113,89 (±21,35) | <0,001 | 87,31 (±18,77) | 114,03 (19,2) | <0,001 |
| HM n (%) | 25 (8,71%) | 2 (1%) | 21 (28,8%) | <0,001 | 1 (0,52%) | 22 (25,88%) | <0,001 |
| CH/ml (RIC) | 0 (0-562,5) | 0 (0) | 1.500 (500-2.500) | <0,001 | 0 (0) | 1.000 (0-2.500) | <0,001 |
| Coagulopatía n (%) | 43 (14,98%) | 10 (4,9%) | 30 (42,25%) | <0,001 | 9 (4,71%) | 31 (37,35%) | <0,001 |
| pH (RIC) | 7,32 (7,27-7,38) | 7,33 (7,29-7,39) | 7,30 (7,20-7,35) | 0,892 | 7,33 (7,29-7,39) | 7,30 (7,20-7,34) | 0,455 |
| EB (RIC) | –3,8 (–7,23 a –1,08) | –2,8 (–6,2 a –0,75) | –6,8 (–8,9 a –6,8) | <0,001 | –2,9 (–6,5 a –0,7) | –6,2 (–8,6 a –2,45) | <0,001 |
| Láctico (RIC) | 2 (1,3-3,1) | 1,7 (1,2-2,4) | 3,2 (2-4,76) | <0,001 | 1,75 (1,2-2,48) | 2,8 (1,7-4,35) | <0,001 |
| Estancia UCI (RIC) | 3,74 (1,81-11,55) | 3,35 (1,74-8,94) | 10,19 (2,49-18,06) | <0,001 | 3,34 (1,7-9,39) | 8,81 (2,2-16) | <0,001 |
| Mortalidad n (%) | 44 (15,33%) | 23 (11,11%) | 17 (23,94%) | 0,011 | 22 (11,34%) | 18 (21,69%) | 0,039 |
CH: concentrados de hematíes; EB: exceso de bases; FC: frecuencia cardiaca; HM: hemorragia masiva; ISS: injury severity score; PAD: presión arterial diastólica; PAM: presión arterial media; PAS: presión arterial sistólica; RIC: rango intercuartil; RTS: revised trauma score; UCI: unidad de cuidados intensivos.
El shock hemorrágico es el tipo de shock que con mayor frecuencia presentan los pacientes que han sufrido una lesión traumática grave e identificarlo precozmente es fundamental para el pronóstico del paciente.
Nuestro estudio demuestra que ambos índices tienen una buena capacidad de predicción de HM y nuestros resultados son comparables a otros estudios que demuestran que el IS y el ISM podrían ser útiles en la identificación del shock hemorrágico tanto a nivel extrahospitalario como hospitalario.
A nivel extrahospitalario, Mitra et al. utilizan un punto de corte ≥1 del IS para predicción de HM (HM definida como al menos 5 concentrados de hematíes en 4h); con ello obtienen una sensibilidad del 47,9% y una especificidad del 90,5%17. Vandromme et al. observan en pacientes atendidos a nivel extrahospitalario un incremento significativo del riesgo de HM (HM definida como al menos 10 concentrados en 24h) para los pacientes con un IS >0,918.
A nivel hospitalario, Mutschler et al. determinan que un IS entre 1-1,4 y >1,4, 31% y 57% de los pacientes requieren al menos 10 concentrados de hematíes en las primeras 24h respectivamente19. Hagiwara et al. describen que en los pacientes con HM (HM definida como al menos 4 concentrados de hematíes en 24h) la media del IS fue de 1,05 (±0,58) y de 0,64 (±0,21) en los pacientes sin HM20.
Existen muchos factores que pueden modificar el IS y el ISM; por ejemplo, a nivel extrahospitalario la presencia de dolor y ansiedad pueden ser causa de taquicardia y con ello aumentar los valores de los índices, o la medición de la presión arterial con sistemas manuales o automáticos. Se sabe que la toma de la presión arterial con sistemas automáticos aumenta la presión arterial y con ello disminuir los valores de dichos índices. También debemos tener en cuenta la influencia del tratamiento a nivel extrahospitalario; Hagiwara et al. describen que pacientes con sangrado y que recibieron al menos 1l de sueroterapia a nivel extrahospitalario tenían un IS más alto (1,1±0,6 vs. 1,05±0,58)20. Por otro lado, existe diferencia cuando la estimación de los índices se realiza de forma puntual o por medidas repetidas; Chen et al. realizan un estudio en el cual concluyen que la determinación del IS a lo largo de un periodo de tiempo tiene una mayor predicción para HM21.
El IS y el ISM no solo han sido estudiados para la predicción de HM, índices elevados se han relacionado con una mayor mortalidad, gravedad de lesión (ISS) y días de estancia en UCI. Cannon et al. determinan que los pacientes con un IS de 0,9 y que han sufrido un trauma grave tienen tasas de mortalidad más altas10. McNab et al. observan la tendencia del IS durante el traslado del paciente a un centro hospitalario, y describen que un aumento ≥0,3 se asocia a un aumento de la mortalidad (27,6% vs. 5,8%) y se correlaciona con una mayor estancia hospitalaria14. Nuestro estudio encontró también diferencias en la gravedad de la lesión (ISS), coagulopatía, estancia en UCI y mortalidad.
El presente estudio tiene muchas limitaciones, entre ellas el ser un estudio que recoge las variables de forma retrospectiva, aunque la mayoría de estudios realizados hasta la fecha son estudios retrospectivos, tal y como demuestran Olaussen et al. en una revisión realizada por su grupo, según la cual, de los 351 estudios obtenidos en la búsqueda, solo 5 cumplían sus criterios de inclusión para valorar el IS como predictor de sangrado crítico22.
Otra limitación fundamental es la falta de una definición universal de HM. La definición de 10 concentrados en 24h introduce sesgos por excluir los pacientes con muerte temprana, excluir a los pacientes con sangrado activo y control posterior del sangrado (arteriografía y/o quirófano) que no llegaron a recibir 10 concentrados e incluir los pacientes sin necesidad de una transfusión aguda23. Nuestro grupo realizó un subanálisis de los pacientes que recibieron entre 4 y 10 concentrados en las primeras 24h: 39 pacientes tenían un probable foco de sangrado activo (necesidad de 4 a 10 concentrados en 24h) de los cuales el 84,7% (33) presentaban inestabilidad hemodinámica, el 53,8% (21) precisaron de cirugía y/o arteriografía para el control de sangrado y 7 fallecieron por shock hemorrágico refractario sin llegar a recibir 10 concentrados de hematíes. Debido a ello, al igual que Haguiwara et al.20 y Olaussen et al.22 consideramos necesario revisar los criterios de diagnóstico de HM y buscar una definición con una mayor sensibilidad para la identificación de la enfermedad (al menos 4 concentrados en 24h o al menos 5 concentrados en 4h)23,24.
ConclusionesEl IS y el ISM son buenos predictores de HM y de fácil aplicación durante la atención inicial del trauma grave. Nuestro punto de corte para el IS es de 1,11 y para el ISM es de 1,46.
AutoríaLuis Juan Terceros-Almanza: búsqueda bibliográfica. Base de datos. Recogida de datos. Análisis estadístico. Redacción del artículo. Carlos García-Fuentes: búsqueda Bibliográfica. Base de datos. Recogida de datos. Análisis estadístico. Redacción del artículo. Susana Bermejo-Aznárez: redacción del artículo. Isidro Javier Prieto del Portillo: recogida de datos. Carolina Mudarra-Reche: recogida de datos. Ignacio Sáez-de la Fuente: recogida de datos. Mario Chico-Fernández: redacción del artículo.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
AgradecimientosA la Unidad de Trauma y Emergencias del Servicio de Medicina Intensiva del Hospital Universitario 12 de Octubre.