Los virus linfotrópicos–T, tipo i (HTLV-I) y tipo ii (HTLV-II) fueron los primeros retrovirus identificados en los seres humanos. El virus HTLV-I es el agente causal de la paraparesia espástica tropical o mielopatía asociada al HTLV-I (enfermedad neurológica degenerativa), de la leucemia de células T del adulto y otras enfermedades como la leucemia linfoide crónica de células B, uveítis, artritis y dermatitis1,2, mientras que el HTLV-II no ha sido vinculado claramente a ninguna enfermedad, aunque tradicionalmente el análisis microbiológico de despistaje incluye siempre el HTLV I/II. La mayoría de los pacientes seropositivos para HTLV-I no desarrollan sintomatología clínica, pero una carga viral elevada o la depresión inmunitaria por coinfección con VIH o tratamiento con fármacos inmunosupresores, favorecen el desarrollo de la enfermedad. Estos virus son endémicos en determinadas zonas geográficas como Japón, África subsahariana, el Caribe, América central y del sur, donde se calcula que entre el 6%-37% de los adultos sanos de 40 años son seropositivos. La transmisión se realiza por contacto sexual, vía parenteral y también de madre a hijo, a través de la lactancia materna. Para considerar que un área geográfica es endémica, algunos autores proponen que la prevalencia de HTLV-I en algunas poblaciones debe ser entre 1-5%3.
La transmisión de HTLV-I por transfusiones sanguíneas se ha documentado en múltiples estudios, por lo que el despistaje de anticuerpos contra los virus HTLV I/II es obligatorio en los bancos de sangre de muchos países4. En España y otros países, en la actualidad solamente se realiza la detección de anticuerpos frente al HTLV-I en aquellos donantes de sangre y de órganos que presentan factores de riesgo5. La trasmisión del HTLV por trasplante de órganos sólidos procedentes de donantes infectados ha sido ampliamente documentada6,7. En el año 2003 se describieron los 3 primeros casos en España de trasmisión HTLV-I por el trasplante de un hígado y 2 riñones procedentes del mismo donante infectado8–11, presentando todos los receptores una paraparesia espástica tropical que les condicionó paraplejia o muy alta discapacidad.
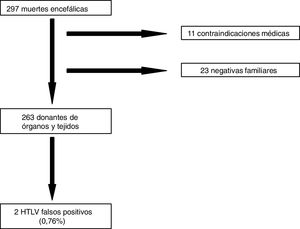
Considerando la gran trascendencia de la trasmisión de esta infección a través del trasplante de órganos sólidos, nos planteamos estudiar la prevalencia de anticuerpos para los virus linfotrópicos HTLV I/II, en potenciales donantes de órganos en Asturias. Para ello, analizamos todas las muertes encefálicas ingresadas en la unidad de cuidados intensivos desde el año 2014 al 2018, ambos inclusive. Se recogieron datos epidemiológicos y resultados de la serología para los virus HTLV I/II en los potenciales donantes de órganos, una vez excluidas contraindicaciones médicas y negativas a la donación. Los factores de riesgo de infección por HTLV I/II que se analizaron fueron la zona geográfica de nacimiento/domicilio habitual, la adicción a drogas por vía parenteral y las prácticas sexuales de riesgo. La detección de anticuerpos se realizó mediante técnica de quimioluminiscencia (CLIA), utilizando el sistema automatizado Liaison XL (Liaison® XL murex recHTLV-I/II, DiaSorin) capaz de detectar anticuerpos anti-HTLV-I y anti-HTLV-II simultáneamente, pero sin discriminar entre anticuerpos al HTLV-I y al HTLV-II. Las muestras positivas por CLIA se confirmaron con un segundo ELISA y posteriormente se enviaron al Instituto de Salud Carlos III para su confirmación por Western Blot. El tiempo de realización de la técnica CLIA fue de una hora y el coste del reactivo, de 3€, no suponiendo su realización un retraso en la logística del proceso de donación. Se analizaron un total de 297 muertes encefálicas, de las cuales se descartaron 11 por contraindicación médica y 23 por negativa a la donación (fig. 1). De las 263 muertes encefálicas que fueron donantes de órganos, 139 (52,9%) eran varones y 124 (47,1%) mujeres, con una edad media de 62,4 años y una estancia media desde el ingreso hasta la extracción de órganos de 4,73 días. De estos donantes se extrajeron 841 órganos, siendo trasplantados 610. Con respecto a la nacionalidad, solamente 9 donantes (3,4%) eran extranjeros, de los cuales 4 (1,5%) procedían de zonas de riesgo (Colombia, Cuba, República Dominicana y Perú). Con respecto a otros factores de riesgo, solamente uno (0,4%) presentaba relaciones sexuales de riesgo. Dos potenciales donantes (0,76%) fueron positivos para CLIA para HTLV I/II, uno de ellos con un valor límite de 1,3 unidades arbitrarias (límite superior de la normalidad: 1,0), considerado un falso positivo. El otro tenía un CLIA de 4,0 unidades arbitrarias, siendo descartado como donante. El Western Blot fue negativo en ambos casos, confirmando que se trataba de resultados falsos positivos, lo que representa el 0,76% de las determinaciones. Estos resultados condicionaron la pérdida de un donante. A la vista de nuestro estudio, concluimos que la seroprevalencia para HTLV I/II en potenciales donantes de órganos en Asturias es baja, pero el progresivo incremento de los flujos migratorios, la dificultad de obtener en la historia clínica algunos factores de riesgo y la tasa de portadores asintomáticos de HTLV-I que desconocen su estado de portador podrían incrementar el riesgo de trasmitir el HTLV mediante el trasplante de órganos. Por otra parte, los pacientes trasplantados con tratamiento inmunosupresor tienen una alta probabilidad de desarrollar enfermedad asociada al HTLV-I, que conlleva una alta mortalidad y una importante discapacidad. Por este motivo, con la finalidad de mejorar la calidad y la seguridad de los órganos trasplantados, en la próxima revisión del Documento de Consenso del Grupo de Estudio de la Infección en el Trasplante y la Organización Nacional de Trasplantes sobre criterios de selección del donante respecto a la transmisión de infecciones12,13, se recomendará la realización de cribado universal de HTLV-I con serología en todos los donantes de órganos.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.