El shock cardiogénico poscardiotomía representa la situación clínica más grave del síndrome de bajo gasto poscirugía cardiaca. Aunque infrecuente, su fisiopatología específica y compleja y su elevada morbimortalidad lo convierten en una entidad especialmente relevante en el contexto de la medicina intensiva. El diagnóstico requiere un elevado índice de sospecha clínica y monitorización multimodal, con un papel fundamental para la ecocardiografía y el catéter de arteria pulmonar. Su manejo debe ser precoz, escalonado y dinámico, multisistémico, multidisciplinar, basado en resolver potenciales complicaciones mecánicas y optimizar los determinantes del gasto cardiaco mediante aporte de volumen o tratamiento deplectivo, fármacos inotrópicos y vasopresores/vasodilatadores y, en ausencia de respuesta, soporte circulatorio mecánico precoz. El objetivo de este artículo es presentar una revisión narrativa y una actualización de la fisiopatología, el diagnóstico y el manejo clínico del shock poscardiotomía. Además, se proponen pautas de actuación que faciliten el manejo clínico diario.
Postcardiotomy cardiogenic shock represents the most serious expression of low cardiac output syndrome after cardiac surgery. Although infrequent, it is a relevant condition due to its specific and complex pathophysiology and important morbidity-mortality. The diagnosis requires a high index of suspicion and multimodal hemodynamic monitoring, where echocardiography and the pulmonary arterial catheter play a main role. Early and multidisciplinary management should focus on the management of postoperative or mechanical complications and the optimization of determinants of cardiac output through fluid therapy or diuretic treatments, inotropic drugs and vasopressors/vasodilators and, in the absence of a response, early mechanical circulatory support. The aim of this paper is to review and update the pathophysiology, diagnosis and management of postcardiotomy cardiogenic shock.
El shock cardiogénico poscardiotomía (SCP) representa la expresión clínica más grave del síndrome de bajo gasto poscirugía cardiaca (SBGC). Corresponde a la situación hemodinámica en la que el gasto cardiaco (GC) es insuficiente para satisfacer la demanda metabólica tisular. Se manifiesta como la imposibilidad de separar del bypass cardiopulmonar al enfermo que se está interviniendo, o bien como shock persistente tras la cirugía, a pesar de fármacos vasoactivos y/o balón de contrapulsación intraaórtico (BCIAo). Se define por la disminución del GC que conduce a hipoperfusión e hipotensión, esto es, un índice cardiaco<2,0l/min/m2, una tensión arterial sistólica<90mmHg (o necesidad de vasopresores para conseguir una tensión arterial sistólica≥90mmHg), una presión en el capilar pulmonar>16-18mmHg y oliguria1,2. Hasta el 40% de los pacientes postoperados con shock, a los que se les realiza una ecocardiografía, presentan datos de disfunción ventricular derecha.
Esta situación clínica, relativamente infrecuente (hasta el 6% de los postoperados), es muy relevante por su elevada morbimortalidad (incluso mayor que en otros tipos de shock cardiogénico3) y porque se asocia a un aumento del consumo de recursos4,5. De hecho, un gran porcentaje de enfermos requieren dispositivos de soporte circulatorio mecánico (SCM) para mantener la perfusión orgánica mientras se recupera la función contráctil y del resto de los órganos6. No obstante, a pesar de los avances tecnológicos, las cifras de mortalidad no muestran una clara mejoría6. Para mejorar los resultados es necesario un abordaje multidisciplinar con personal experto que permita identificar y tratar el cuadro de forma precoz y el uso adecuado de los sistemas de SCM. Este abordaje permitiría rescatar, con buen pronóstico a medio-largo plazo, a pacientes que, de otra manera, no sobrevivirían7.
Íntimamente relacionado, y asociado con el SCP, encontramos el síndrome vasopléjico tras cirugía cardiaca. Hasta la mitad de estos pacientes pueden desarrollar vasoplejía (bajas resistencias vasculares sistémicas) con una fisiopatología similar al shock séptico, presentando shock distributivo hasta el 5% de los mismos8. Es indispensable el reconocimiento precoz y la instauración de vasopresores para garantizar la perfusión orgánica.
En la presente revisión se estudian los conceptos fisiopatológicos relacionados con este cuadro clínico y se proponen pautas de actuación que ayuden al lector a reconocer y tratar adecuadamente esta difícil y compleja situación.
FisiopatologíaEn la cirugía cardiaca podemos observar 3 principales mecanismos fisiopatológicos asociados: el daño quirúrgico local, la lesión por isquemia-reperfusión (LIR) y la propia circulación extracorpórea (CEC)9.
Simplificando la fisiopatología de la LIR, para facilitar el entendimiento podemos definir 3 puntos clave: la entrada masiva de Ca++ en la célula con disregulación de los mecanismos homeostáticos de equilibrio iónico celular, el uso inadecuado del oxígeno reperfundido con formación de radicales libres (estrés oxidativo) y la disfunción del poro de permeabilidad transitoria mitocondrial e inactivación de la fosforilación oxidativa. La cardioplejía administrada durante la cirugía protege, mediante la conservación de energía tras inducir una rápida parada diastólica, ralentizando la tasa metabólica y contrarrestando los efectos deletéreos de la LIR mediante agentes protectores específicos9. Esta miocardioprotección depende de factores intrínsecos (hipertrofia, reserva funcional, etc.)10 y de la capacidad de la cardioplejía para mantener inactivos los canales iónicos que provocan consumo de energía11. El disbalance entre los mecanismos lesivos y protectores provocará aturdimiento miocárdico postoperatorio y, en su grado máximo, shock cardiogénico secundario.
Además, la CEC desencadena una respuesta inflamatoria donde intervienen distintos sistemas: contacto, coagulación, fibrinólisis y mecanismos humorales y celulares tardíos12,13. La interrelación de estos sistemas potencia las consecuencias de la LIR, facilitando la disfunción orgánica (material suplementario). En la figura 1Edel material suplementario se presenta, de forma esquemática, la etiopatogenia del shock vasodilatador.
Algoritmo de monitorización y abordaje.
a Monitorización hemodinámica básica: presión arterial invasiva, electrocardiograma continuo, temperatura, balance hídrico, saturación venosa mixta o central, analítica, gasometría y presión venosa central.
b Adaptado de Habicher et al.16.
c Adaptado de Busse et al.8.
d El azul de metileno no se recomienda en pacientes con déficit de 6-glucosafosfato deshidrogenasa, inhibidores selectivos de la recaptación de la serotonina, inhibidores selectivos de la recaptación de noradrenalina-serotonina, inhibidores de la monoaminooxidasa.
CAP: catéter de arteria pulmonar; DRA: daño renal agudo; EC: ecocardiografía; FC: frecuencia cardiaca; GEDVI: volumen telediastólico global del ventrículo izquierdo; IC: índice cardiaco; PCP: presión en el capilar pulmonar; POAP: presión de oclusión arterial pulmonar; PVC: presión venosa central; RVS: resistencias vasculares sistémicas; SvcO2: saturación venosa central de oxígeno; SvO2: saturación venosa mixta de oxígeno; TAM: tensión arterial media; TAS: tensión arterial sistólica; TDVI: telediastólica de ventrículo izquierdo; TRRC: técnicas de reemplazo renal continuas; VCI: vena cava inferior; VD: ventrículo derecho; VI: ventrículo izquierdo; VSVI: volumen sistólico de ventrículo izquierdo.
La génesis del aturdimiento miocárdico y la vasoplejía comparten mecanismos comunes, siendo habitualmente un cuadro clínico mixto; sin embargo, estudios experimentales señalan que la recuperación endotelial es más tardía14.
Manejo inicial y monitorización hemodinámicaEl SCP requiere un manejo rápido, dinámico y escalonado centrado en detectar y resolver las posibles causas subyacentes o facilitadoras, para lo que se requiere una monitorización hemodinámica completa y precoz.
Tras el ingreso y la monitorización básica, se debe realizar una optimización inicial guiada por objetivos hemodinámicos y siguiendo las recomendaciones de las sociedades científicas15–17. Aquellos pacientes que persistan en situación clínica de shock requerirán monitorización invasiva y ecocardiográfica para valorar y profundizar en la etiología, seleccionar la mejor estrategia terapéutica y monitorizar la respuesta a las medidas implementadas18,19 (fig. 1). Para ello, 2 sistemas de monitorización serán clave en el SCP: la ecocardiografía y el catéter de arteria pulmonar (CAP).
La ecocardiografía tiene un papel esencial al proporcionar, de forma rápida y no invasiva, información anatómica y funcional17. En el SCP se debe realizar de forma precoz y por personal experto, permitiendo detectar complicaciones que supongan un compromiso vital (fig. 1), derrame pericárdico, valorar la función de ambos ventrículos, estimar las presiones de llenado, detectar datos de isquemia miocárdica o disfunción de los injertos aortocoronarios, si los hubiera, y estimar la presencia de datos de congestión, derrame o consolidaciones pulmonares, así como descartar neumotórax20.
Por su parte, el CAP permite un análisis hemodinámico detallado que aporta información relevante en el SCP, donde su utilidad es más evidente, siendo el dispositivo invasivo de elección en presencia de SCM21,22. El CAP permite obtener las presiones pulmonares y de llenado derechas e izquierdas, el GC, la SvO2 y la fracción de eyección y el volumen telediastólico del ventrículo derecho (estos 2 últimos parámetros solo se pueden obtener con un CAP con un termistor de respuesta rápida)23. Estudios recientes6,24 destacan su utilidad en la identificación de aquellos pacientes que requieren implantación precoz de SCM y aquellos que presentan fallo biventricular (lo que ayudará en la elección del dispositivo). Facilita, asimismo, la optimización de la volemia, el ajuste/retirada de los fármacos vasoactivos/inotropos, y contribuye a guiar el destete del SCM. Incluso se señala una mejoría pronóstica en aquellos pacientes con shock cardiogénico, especialmente cuando precisan SCM24.
En el SCP se producen modificaciones hemodinámicas significativas en cortos periodos de tiempo que requerirán una reevaluación estrecha del estatus volémico. Es tan importante identificar a aquellos pacientes que responderán a la administración de fluidos con un aumento del GC como a aquellos con presiones de llenado elevadas que requieran tratamiento deplectivo. Si hubiera parámetros de respuesta a volumen asociados a elevadas presiones de llenado o fracaso ventricular derecho, se realizará una valoración riesgo/beneficio ante la posibilidad de agravar el deterioro hemodinámico administrando fluidos.
En el SCP es habitual, especialmente si hay shock vasopléjico asociado, que, a pesar de alcanzar la euvolemia, se requiera iniciar/ajustar fármacos vasoactivos para lograr una adecuada presión de perfusión. Aunque las guías recomiendan una tensión arterial media≥65mmHg, este objetivo debe individualizarse según las cifras basales del paciente16,19 y el resto del perfil hemodinámico.
Asimismo, cualquier alteración en la frecuencia o ritmo cardiaco que suponga un compromiso hemodinámico significativo requerirá reversión inmediata mediante cardioversión eléctrica y/o sobreestimulación17, o revisión del marcapasos epicárdico y optimización de la frecuencia cardiaca.
En caso de disfunción ventricular izquierda, descartadas/tratadas las causas previamente descritas, es necesario analizar la contractilidad y la poscarga para valorar el inicio/ajuste de fármacos inotrópicos, vasoconstrictores o vasodilatadores17. Si persisten los datos de hipoperfusión o fracaso orgánico avanzado, se debe considerar el SCM precoz dado que su demora se ha relacionado con una mayor mortalidad6,22.
En presencia de disfunción ventricular derecha será necesario optimizar la función ventricular izquierda debido a su influencia en el GC derecho, asegurar una adecuada presión de perfusión ventricular y disminuir la poscarga del ventrículo derecho (VD) mediante vasodilatadores pulmonares (VDP). En ausencia de respuesta, se valorará el SCM17. Esto se desarrolla más adelante.
InotroposLa selección del inotropo en el SCP dependerá de las circunstancias clínicas del paciente y su evaluación hemodinámica. La elección de un fármaco específico es controvertida en ausencia de estudios aleatorizados multicéntricos con gran número de enfermos (debido a las múltiples dificultades que entraña su desarrollo) y está basada principalmente en la experiencia clínica y en recomendaciones y opinión de expertos. En un análisis de la Cochrane Library25 de 19 estudios con 2.385 pacientes con shock cardiogénico o SBGC (secundario a infarto, insuficiencia cardiaca o poscirugía cardiaca) se investigó la eficacia de diferentes inotropos: levosimendán vs. dobutamina, enoximona o placebo; enoximona vs. dobutamina, piroximona o adrenalina-nitroglicerina; adrenalina vs. noradrenalina o noradrenalina-dobutamina; dopexamina vs. dopamina; milrinona vs. dobutamina y dopamina-milrinona vs. dopamina-dobutamina. La revisión concluye que la evidencia existente no permite respaldar el uso de un inotropo específico o terapia combinada vasodilatadora que disminuya la mortalidad en pacientes con shock cardiogénico o SBGC, lo que obliga a diseñar estudios de alta calidad que faciliten esta elección.
Las catecolaminas tienen efectos inotrópicos y cronotrópicos positivos. La dobutamina y la adrenalina mejoran el volumen/latido y la frecuencia cardiaca, disminuyendo moderadamente la presión en el capilar pulmonar y la presión telediastólica del ventrículo izquierdo (VI). La milrinona, inhibidor de la fosfodiesterasa 3, aumenta el volumen/latido y la frecuencia cardiaca, con disminución de la presión en el capilar pulmonar y resistencias vasculares sistémicas y pulmonares. Levosimendán es un fármaco inodilatador, sensibilizador al calcio, que también aumenta el volumen/latido y disminuye las resistencias vasculares. Este fármaco, probablemente por ser el más actual, ha sido sometido a mayor número de trabajos y consecuentes revisiones y metaanálisis, dando lugar a una controversia que aún se mantiene activa. En pacientes con SBGC puede tener indicación, como inodilatador, en el postoperatorio precoz; en el caso del SCP necesitará asociar un vasoconstrictor.
Con base en la experiencia acumulada y en ausencia de estudios concluyentes, el inotrópico de primera línea suele ser la dobutamina. En caso de pobre respuesta y/o tratamiento crónico con betabloqueantes, si la tensión arterial media>60mmHg se puede considerar la milrinona o el levosimendán. En presencia de hipotensión, puede ser necesario un vasoconstrictor como la noradrenalina. Generalmente, la adrenalina, como inotropo o vasoconstrictor, se utiliza como segunda línea.
VasopresoresLos vasopresores pueden clasificarse según sus acciones adrenérgicas o no adrenérgicas. Entre los adrenérgicos el más utilizado es la noradrenalina, seguido de dopamina y adrenalina26. Diversas guías clínicas recomiendan la noradrenalina como fármaco de primera elección en el shock vasodilatador27 y en el cardiogénico, si fuera necesario un vasopresor, combinado con dobutamina28. No existe evidencia firme para elegir el vasopresor y la mayoría de los estudios se han realizado en el shock séptico; sin embargo, podemos afirmar que la dopamina incrementa el riesgo de arritmias y posiblemente la mortalidad en comparación con la noradrenalina29. La noradrenalina tiene numerosas ventajas: a) potencia comparable con adrenalina y fenilefrina; b) no actúa sobre receptores β2 (pudiendo servir el lactato como guía de reanimación); c) no incrementa el consumo miocárdico de oxígeno; d) preserva el acoplamiento ventrículo-arterial, al contrario que la adrenalina, y e) mejora el GC al aumentar el volumen telediastólico (movilización del volumen de reserva esplácnico) y su acción β1. No obstante, todas las catecolaminas favorecen el estrés oxidativo e interaccionan con el metabolismo celular y la respuesta inflamatoria, lo que ha llevado al desarrollo del concepto de «descatecolaminización», cuyo objetivo es disminuir la exposición a estos fármacos.
Otros vasopresores no adrenérgicosVasopresina y su análogo terlipresina (profármaco activado por peptidasas endoteliales en lisina-vasopresina) actúan sobre los receptores V1a disminuyendo la producción de óxido nítrico e incrementando la concentración de Ca++ intracelular. Se han realizado ensayos utilizando la vasopresina profilácticamente (0,03U/min), iniciada antes de la entrada en bomba, con disminución de los requerimientos de catecolaminas y menor shock vasodilatador postoperatorio30.
En el estudio VANCS (<0,04U/min) los pacientes postoperados de cirugía cardiaca que recibieron vasopresina presentaron menos complicaciones graves que aquellos con noradrenalina31. En el estudio VASST (shock séptico) la vasopresina permitió disminuir la dosis de noradrenalina, pero no encontraron diferencias de mortalidad32.
La terlipresina presenta resultados similares, con predominio sobre el receptor V1, permitiendo la descatecolaminización33, aunque no hay datos concluyentes sobre el mejor método de administración (bolos o infusión).
El azul de metileno inhibe la óxido nítrico sintetasa y la guanilato ciclasa, ambas involucradas en la fisiopatología del shock vasodilatador. Utilizado desde el intraoperatorio en pacientes que tomaban inhibidores de la enzima convertidora de la angiotensina hasta el día de la intervención, ha demostrado una menor incidencia de shock vasopléjico postoperatorio34. Suele utilizarse «fuera de indicación» en casos de refractariedad, habitualmente en bolos «lentos» para evitar episodios de hipertensión pulmonar. Algunos autores continúan con una perfusión, tras el bolo inicial, evidenciando que un uso precoz presenta mayor beneficio que de rescate35.
La hidroxicobalamina (vitamina B12) es un potente inhibidor de la óxido nítrico sintetasa y liga el sulfuro de hidrógeno, importante vasodilatador endógeno que interactúa con los canales de K-ATP dependientes. Su utilización por primera vez en cirugía cardiaca fue como alternativa al azul de metileno, en un paciente que tomaba inhibidores de la serotonina, con buenos resultados hemodinámicos36. Posteriormente se han comunicado series de casos de shock refractario, como terapia adyuvante, con resultados prometedores37, incluidos pacientes con dispositivos de SCM38. No se conoce bien cuándo se produce el efecto pico ni su inicio de acción, existiendo cierta variabilidad interindividual37. En la mayor serie de casos publicada, la combinación de hidroxicobalamina y azul de metileno consiguió un alto porcentaje de respuesta hemodinámica precoz en pacientes con noradrenalina y vasopresina concomitantes39.
Los corticoides reducen la respuesta inflamatoria (inhibición de interleucinas, citocinas y endotoxinas), pese a lo cual no se ha observado una disminución de la mortalidad en cirugía cardiaca40. Actualmente el uso de la hidrocortisona como agente descatecolaminérgico se sustenta en los resultados del estudio CORTICUS en el shock séptico41 y en el hecho de que se ha observado supresión del eje hipotálamo-pituitario-adrenal en la CEC42.
La angiotensina II tiene un doble mecanismo de acción: estimula la glándula suprarrenal favoreciendo la liberación de aldosterona y cortisol y actúa sobre el sistema nervioso simpático y el músculo liso provocando vasoconstricción al liberar calcio intracelular43. El estudio ATHOS-3 demostró su capacidad para mejorar la tensión arterial media tras 3h de infusión en pacientes con shock vasodilatador refractario (69,9 vs. 23,4%; p<0,0001; OR 7,95; IC 95% 4,76-13,3). De los pacientes incluidos 7 requerían ECMO y solo un 6% eran postoperatorios44. En el ámbito de la cirugía cardiaca existen series de casos en los que se observa un efecto beneficioso en la reducción de las dosis de noradrenalina45.
En cuanto a la vitamina C y la tiamina, estudios recientes evidencian que, en pacientes críticos, puede existir un déficit de esta vitamina que podría relacionarse con hipotensión46. La vitamina C es un cofactor para la síntesis de aminas endógenas47, puede sensibilizar los receptores de catecolaminas, reducir el óxido nítrico y disminuir la liberación de histamina. En una serie de casos se describe como la adición de vitamina C pudo disminuir los requerimientos de noradrenalina en el postoperatorio de cirugía cardiaca46. Sin embargo, 2 ensayos en pacientes sépticos, VICTAS (vitamina C, tiamina e hidrocortisona)48 y VITAMINS (vitamina C, hidrocortisona y tiamina vs. hidrocortisona)49, no demostraron beneficios de la triple terapia vs. placebo o hidrocortisona sola en la reducción de la necesidad de aminas o tiempo de ventilación mecánica.
Con respecto a los inhibidores de las prostaglandinas, potencialmente la producción de prostaglandinas durante la respuesta inflamatoria podría ser partícipe de la vasoplejía asociada. En un ensayo donde 18 pacientes recibieron flurbiprofeno se observó un mejor perfil hemodinámico postoperatorio que en el grupo control sin afectación de la función renal50.
La evidencia existente sobre fármacos vasopresores adyuvantes se sustenta en gran medida en pacientes sépticos. En cirugía cardiaca, después de la noradrenalina, la vasopresina es la que tiene mayor evidencia. Deberemos tener en cuenta la fisiopatología del shock vasodilatador, el momento de administración y los posibles efectos adversos a la hora de elegir un fármaco adyuvante a la terapia tradicional.
La tabla 1 detalla las características y dosis de los inotropos y vasopresores más usados en clínica.
Características de los fármacos inotropos y vasopresores
| Fármaco | Receptores/lugar de acción | Dosis recomendada | Mecanismo de acción | Efectos secundarios |
|---|---|---|---|---|
| Dobutamina | Agonista β1, β2 | 1-20μg/kg/min | Activación adenilciclasa, aumento niveles de AMPc intracelular. ↑ Ca++ intracelular. ↑ Contractilidad | Arritmias |
| Milrinona | Inhibidor PDE3 | 0,3-1μg/kg/min | Inhibe enzima PDE3, aumento AMPc intracelular. ↑ Ca++ intracelular. ↑ Contractilidad. | Hipotensión arterial, arritmia, trombocitopenia |
| Levosimendán | Sensibilizador al calcio | 0,05-0,2μg/kg/min | Potencia la sensibilidad al Ca de proteínas contráctiles y abre los canales de K sensibles al ATP en músculo liso vascular. Inodilatador | Hipotensión arterial, arritmia |
| Noradrenalina | Agonista α1, α2, β1 | 0,01-1μg/kg/min | ↑ Ca++ intracelular. Vasoconstricción | Dosis elevadas: isquemia intestinal, miocárdica, periférica |
| Adrenalina | Agonista α1, α2, β1, β2 | 0,01-0,5μg/kg/min | ↑ Ca++ intracelular. Vasoconstricción | Dosis elevadas: isquemia intestinal, miocárdica, periférica. Elevación ácido láctico |
| Vasopresina | V1-V2 | <0,04U/min | V1 ↑ Ca++ intracelular (sensibiliza efecto catecolaminas)↓ Síntesis ONModula canales K+-ATP dependientesVasoconstricción | Dosis elevadas: isquemia intestinal, miocárdica, periféricaReceptores V2: edema, vasodilatación, trombosis microvascular (estimula liberación factor Von Willebrand) |
| Terlipresina | V1a-V2Más selectivo sobre receptores V1 | 0,5-1mg bolos/6-8h | ||
| Hidrocortisona | Receptor cortisol intracelular | 50mg/6h | Sensibiliza efecto de catecolaminas, actividad mineralocorticoide. Disminuye respuesta inflamatoria | Insomnio, náuseas, miopatía esteroidea a grandes dosis, riesgo de favorecer infecciones a dosis elevadas |
| Azul de metileno | Inhibición guanilato ciclasa y ONSI | 1-3mg/kg bolo0,5mg/kg/h durante 6-12h | ↓ C-GMP. Vasoconstricción | Hemólisis en déficit de 6-GPDH. Síndrome serotoninérgico si ISRS, ISRNS o IMAO. Hipertensión pulmonar. Inhibición parcial de la heparinaa |
| Hidroxicobalamina | Inhibición ONSIQuelante sulfuro de hidrógeno | 5g en 5min | Modula canales K+-ATP dependientes | Cromaturia, náuseas, cefalea, hipopotasemia en anemia megaloblástica |
| Angiotensina | AT-R1AT-R2 | 10-40ng/kg/min | AT-R1 estimula SNS: ↑ Ca++ intracelular. Favorece liberación de cortisol y vasopresina. VasoconstricciónAT-R2 vasodilatación | Fenómenos tromboembólicos, hipertensión pulmonar |
AMPc: adenosín monofosfato clíclico; ATP: adenosín trifosfato; Ca++: calcio iónico; C-GMP: monofosfato guanosina cíclico; IMAO: inhibidores de la monoamino oxidasa; ISRNS: inhibidores selectivos de la recaptación de serotonina-noradrenalina; ISRS: inhibidores selectivos de la recaptación serotonina; ON: óxido nítrico; ONSI: óxido nítrico sintetasa inducible; PDE3: fosfodiesterasa 3; SNS: sistema nervioso simpático; 6-GPDH: glucosa-6-fosfato deshidrogenasa.
a Sloand EM, Kessler CM, McIntosh CL, Klein HG. Methylene blue for neutralization of heparin. Thromb Res. 1989;54:677-86.
Los escenarios clínicos en los que más frecuentemente aparece fracaso del VD son: la enfermedad coronaria con lesión de la coronaria derecha; valvulopatías, especialmente la mitral; trasplante cardiaco; cardiopatía congénita; tromboendarterectomía pulmonar y pacientes con asistencia ventricular izquierda.
El SCP secundario al fracaso de VD condiciona una elevada morbimortalidad. El manejo es similar al de cualquier paciente con SBGC y SCP51. Entre las peculiaridades terapéuticas del fracaso de VD (tabla 2) se incluye la disminución de la poscarga ventricular derecha para mejorar el acoplamiento ventrículo-arterial, lo que favorece el llenado del VI y disminuye el desplazamiento del septo interventricular hacia la cavidad izquierda, mejorando el GC. Además, se deben corregir las situaciones que producen un aumento de las resistencias vasculares pulmonares como la hipoxemia, la hipercapnia y la acidosis52.
Manejo del shock cardiogénico poscardiotomía/fracaso ventricular derecho
| Optimización de precarga |
| – Volumen si sangrado o pérdida de fluidos. Valoración constante de la respuesta a volumen |
| – Si PAD elevada/sobrecarga hídrica: diuréticos o técnicas de reemplazo renal |
| Optimización ritmo y frecuencia cardiaca |
| – Conservar ritmo sinusal si es posible, tratamiento de las taquiarritmias |
| – Si bloqueo auriculoventricular, uso de marcapasos |
| Optimización del acople ventrículo-arterial |
| – Inotropos o inodilatadores+vasodilatadores pulmonares iv vs. inhalados (según situación hemodinámica y respiratoria) (ver tabla 1E del material suplementario: vasodilatadores) |
| – Si fracaso: considerar soporte mecánico (puente recuperación vs. trasplante) |
| Optimización de la presión de perfusión |
| – Uso de agentes vasoactivos: noradrenalina, vasopresina |
| Optimización respiratoria |
| – Ajustar PEEP. Evitar atelectasias e hiperinflación |
| – Valorar el uso de vasodilatadores pulmonares para mejorar la insuficiencia respiratoria |
| – Evitar: hipercapnia, hipoxemia y acidosis metabólica |
| Situación refractaria |
| – Shock persistente/HTP asistencia mecánica: ECMO VA |
| – Principal problema insuficiencia respiratoria: ECMO VV |
Para disminuir la poscarga del VD podemos utilizar VDP locales (vía inhalada o nebulizada) o sistémicos (vía oral/enteral o intravenosa) (tabla 1E del material suplementario)53. El tipo de fármaco elegido estará determinado por el contexto clínico del paciente54,55. El uso de VDP intravenosos se asocia a hipotensión arterial sistémica, al no existir VDP selectivos puros, lo que provoca mala tolerancia clínica en pacientes con necesidad de vasopresores. Por ello, la vía inhalada es de elección en estos pacientes51,56, evitando, en gran parte, los efectos sistémicos deletéreos. Como VDP inhalados se utilizan fundamentalmente el óxido nítrico inhalado (NOi), la milrinona, las prostaglandinas y el iloprost. El NOi es el más utilizado en esta indicación. Presenta como ventaja una vida media corta y, como inconvenientes, la necesidad de administración continua, su contraindicación una vez el paciente es destetado de la ventilación mecánica, la necesidad de monitorización de NO2 y el posible efecto rebote57. Como alternativa, las prostaciclinas inhaladas son ampliamente utilizadas en algunos centros por su efecto similar al NOi58. El epoprostenol inhalado obtiene efectos hemodinámicos muy similares al NOi y también presenta una vida media corta59. En este contexto, las prostaciclinas inhaladas como el iloprost presentan un perfil farmacocinético más favorable, con una vida media que permite su administración cada 3-4h y se puede utilizar tanto en pacientes en ventilación mecánica como en espontánea. En términos hemodinámicos es, al menos, igual de eficaz que el NOi y el epoprostenol, consiguiendo disminuir las presiones arteriales pulmonares y mejorando la eyección del VD y el índice cardiaco de forma más prolongada60,61. A nivel clínico, ha demostrado mejorar la tensión arterial sistémica y disminuir el tiempo de ventilación mecánica invasiva en pacientes con fracaso de VD en el postoperatorio inmediato de trasplante cardiaco. En las posibles complicaciones no encontraron diferencias en el sangrado ni hemorragias relacionadas con la antiagregación plaquetaria, ni complicaciones relacionadas con la nebulización59.
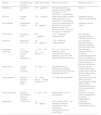
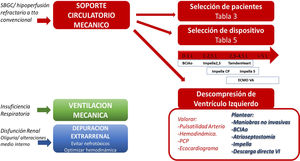
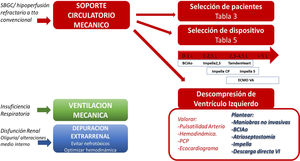
Soporte circulatorio mecánicoSe estima que entre el 0,3 y el 3,6% de los pacientes operados de cirugía cardiaca presentan un SCP refractario a fármacos vasoactivos (y en muchos casos al BCIAo) que requiere SCM extracorpóreo como tratamiento de rescate5,62,63. Estos pacientes, sin el soporte, tienen un pronóstico potencialmente fatal, mientras que con SCM la supervivencia esperable, aunque diferente según las series publicadas, puede alcanzar el 40%63. La adecuada selección del paciente, el momento de inicio de la terapia, la formación y experiencia del equipo multidisciplinar, junto con la capacidad de reconocimiento de la futilidad, son factores clave para obtener buenos resultados clínicos. En la tabla 3 se detallan las indicaciones según las recientes recomendaciones de varias sociedades científicas. La figura 2 muestra el soporte mecánico que puede ser necesario en el SCP.
Indicaciones y recomendaciones sobre asistencias circulatorias mecánicas en el shock poscardiotomía
| Recomendaciones | Clase | Nivel |
|---|---|---|
| Se recomienda que el soporte en el SCP se inicie antes de la instauración de la disfunción multiorgánica o el metabolismo anaeróbico (lactato<4mmol/l) en pacientes con posibilidad de recuperación miocárdica sin sangrado incontrolable que requiera cirugía | I | B |
| Cuando la probabilidad de recuperación de la función miocárdica es baja, solo se recomienda soporte mecánico en pacientes potencialmente elegibles para trasplante cardiaco o soporte mecánico de largo plazo | I | C |
| Se recomienda el uso precoz de SCM tras cirugía cardiaca en los pacientes con BCIAo y tratamiento médico óptimo, con fracaso del destete del bypass extracorpóreo o en situación hemodinámica muy comprometida | I | B |
| Antes de iniciar SCM se deben valorar las comorbilidades importantes, edad avanzada, niveles de lactato y función renal, ya que son factores de riesgo asociados a mortalidad | IIa | B |
| El tipo y modo de SCM debe basarse en la situación hemodinámica y las características del paciente: fracaso uni o biventricular, fracaso derecho y/o izquierdo, fracaso circulatorio pre/intra/postoperatorio, disfunción ventricular aguda o crónica, shock cardiogénico o parada cardiaca | IIa | C |
| Se debe considerar la ECMO con canulación periférica en pacientes con SCP, en presencia de disfunción ventricular izquierda o biventricular | IIa | B |
| En la ECMO periférica con canulación femoral, debe considerarse colocar una cánula de perfusión distal para disminuir el riesgo de isquemia del miembro | IIa | B |
| La configuración Oxy-RVAD se debe considerar en el fracaso aislado del VD refractario | IIb | C |
| En presencia de isquemia en el miembro, a pesar de la perfusión anterógrada, se debe considerar el acceso de la femoral contralateral, la arteria axilar o el acceso central | IIa | C |
| La canulación de la arteria axilar/subclavia o la canulación aórtica central se debe considerar como alternativa a la canulación femoral, sobre todo para soportes prolongados | IIb | C |
| La canulación directa a través del ápex del VI debe considerarse para drenaje del VI y para la conversión a asistencia ventricular VI-like (ápex VI-arteria subclavia) | IIb | C |
| Las configuraciones híbridas/alternativas (VVA, VAV u otras, incluyendo dispositivos adicionales) se deben considerar en pacientes con ECMO VV o VA con fracaso cardiaco, síndrome de Arlequín (hipoxemia diferencial), fracaso respiratorio, hipoxemia refractaria, drenaje venoso insuficiente y/o estasis VI | IIb | C |
| En determinadas situaciones hemodinámicas, o alteraciones estructurales cardiacas, se debe considerar el uso asociado de otros dispositivos: BCIAo, dispositivos transaórticos o transeptales | IIa | C |
| Puede considerarse el implante de un BCIAo en casos de disfunción ventricular moderada durante el destete del bypass antes de iniciar SCM. O en presencia de insuficiencia cardiaca aguda tras salida de bypass, antes de iniciar SCM | IIb | C |
| No se recomienda el implante del BCIAo en los casos de disfunción severa de VI o disfunción biventricular como primera opción en los casos de imposibilidad de destete de bypass o insuficiencia cardiaca aguda posterior al destete del bypass | III | C |
| Puede considerarse asociar el BCIAo a un dispositivo SCM en pacientes con escasa o ausencia de apertura de la válvula aórtica al iniciar el SCM con el flujo elegido | IIb | C |
| El uso de un dispositivo microaxial transvalvular (percutáneo o axilar) puede considerarse en el SCP como primera opción o concomitante con un SCM en presencia de una disfunción aislada del VI. O en pacientes con escasa o ausencia de apertura de la válvula aórtica al iniciar el SCM con el flujo elegido | IIb | C |
| El uso de dispositivos de asistencia ventricular a corto plazo en pacientes con SCP (disfunción aislada de VD) puede considerarse como opción terapéutica primaria | IIb | C |
| En presencia de signos de distensión de VI y estasis, cierre de la válvula aórtica y edema pulmonar, se recomienda el uso de acciones conservadoras (manipulación del flujo de ECMO, vasodilatadores, uso de PEEP), incluyendo el BCIAo para facilitar la descarga del VI. En los casos que no responden a las medidas previas, se recomienda el uso de otros dispositivos para descargar el VI (por ejemplo, transaórticos) | I | B |
| En presencia de signos de distensión de VI y estasis, cierre de la válvula aórtica y edema pulmonar, puede considerarse la septostomía de descarga | IIb | C |
Niveles de evidencia: A: datos derivados de múltiples ensayos clínicos randomizados o metaanálisis, B: datos derivados de un único ensayo clínico randomizado o estudios no randomizados grandes. C: Consenso de opinión de expertos y/o pequeños estudios, estudios retrospectivos o registros.
Clases de recomendación: I: evidencia y/o acuerdo general de que un tratamiento es beneficioso, útil y efectivo. Está recomendado/indicado. II: no hay acuerdo general en la evidencia o hay divergencia de opinión acerca de la utilidad/eficacia de un tratamiento o procedimiento (IIa: el peso de la evidencia/opinión está a favor de la utilidad/eficacia. El tratamiento «debería» ser considerado; IIb: Utilidad/eficacia menos establecida por la evidencia/opinión. El tratamiento «puede»ser considerado). III: acuerdo general de que un tratamiento/procedimiento no es útil/efectivo e incluso a veces puede ser dañino.
Fuente: Weman et al.9.
Soporte mecánico multisistémico en el shock cardiogénico poscardiotomía (SCP). El SCP debe considerarse como una afectación multisistémica, que nos obliga a realizar soporte de múltiples órganos. Además de la ventilación mecánica y terapias de depuración extrarrenal, en los pacientes con SCP refractario hay que plantear, de manera precoz, la necesidad de SMC. La selección de pacientes se realizará según los datos aportados en la tabla 3. La selección del dispositivo (tabla 1E) se realizará ajustando a la situación clínica concreta del enfermo, la necesidad de soporte uni o ventricular, afectación pulmonar, mayor o menor cantidad de flujo para conseguir adecuada perfusión orgánica, etc. En los casos en que se desarrolle congestión pulmonar, dilatación ventricular izquierda y/o pérdida de pulsatilidad arterial, hay que plantear la descompresión ventricular izquierda, bien con maniobras poco invasivas (ajuste de flujos del soporte mecánico, de fármacos vasoactivos y diuréticos), bien con maniobras que consigan mayor descarga, como el BCIAo, la atrioseptostomía, la aspiración arterial pulmonar, el dispositivo Impella® (o similares) o la descarga directa del ventrículo izquierdo.
El momento del implante no está bien definido, pero debemos considerar siempre un implante precoz, bien durante el acto quirúrgico en enfermos que no se pueden destetar de la CEC, bien en las primeras horas del postoperatorio si persiste el shock, ya que su retraso conlleva peores resultados64.
En líneas generales, los dispositivos de SCM cuentan con un acceso de drenaje, un circuito con una bomba centrífuga, un acceso de retorno y, opcionalmente, un oxigenador intercalado. Dependiendo de la configuración, se puede proporcionar soporte uni o biventricular. Pueden ser de canulación periférica o central y dar soporte oxigenatorio, además de circulatorio. También existen dispositivos de soporte axial que se van a situar de forma transvalvular, ya sea en cavidades izquierdas o derechas. La tabla 4 muestra las principales características, ventajas e inconvenientes de los dispositivos más frecuentemente usados.
Características de los sistemas de soporte circulatorio mecánico
| Percutáneo | Quirúrgico | ||||||
|---|---|---|---|---|---|---|---|
| BCIAo | Tandem Heart | Impella® 2,5/5,0/LD/CP/RP | ECMO VA periférica | ECMO central | VAD centrífuga | VAD neumática | |
| Mecanismo | Contrapulsación intraaórtica | Flujo continuo centrífugo | Flujo continuo axial | Flujo continuo centrífugo | Flujo continuo centrífugo | Flujo continuo centrífugo | Flujo neumático pulsátil |
| Soporte | VI | VI/VD según configuración | VI (RP → VD) | VI+VD, oxigenación | VI+VD, oxigenación | VI/VD/BiV | VI/VD/BiV |
| Efecto VI | ↓ Poscarga y trabajo del VI. ↑ GC 0,5lpm | ↓ Poscarga VI. ProtekDuo®: soporte VD | Descarga VI | ↑ Poscarga VI (axilar<femoral) | Descarga VA y ↓ trabajo | Descarga VA y ↓ trabajo | Descarga VA y ↓ trabajo |
| Flujo máximo | - | Hasta 5lpm | Impella® 2,5 → 1,8lpm; CP → 4,3 (3,8); 5,0/LD → 5lpm (4,3 reales) | Diámetro cánulas dependiente (5lpm aprox) | Diámetro cánulas dependiente (5-8lpm aprox) | 9lpm | 7lpm |
| Duración | Días | 14 días | 2,5/CP: 4 días; 5,0/LP: 6 días; RP: 14 días | 30 días | 30 días | 30 días | 80 días (media) |
| Ventajas | Inserción rápida, a pie de cama | Estabilidad flujos | Perfil hemodinámico. Implante sencillo | Inserción rápida, a pie de cama, oxigenación | Estabilidad flujo. Perfil hemodinámico | Estabilidad flujo. Perfil hemodinámico. ± oxigenador | Soporte durable. Perfil hemodinámico |
| Complicaciones | Embolismo, daño vascular, trombocitopenia | Requiere septostomía, CIA post, migración cánula, taponamiento | Migración, lesión VAo/ventrículo, taponamiento, hemólisis, TV, embolia, isquemia | Trombosis VI, EAP, síndrome de Arlequín, hemorragia, isquemia miembro | Hemorragia, embolia | Hemorragia, embolia | Hemorragia, ACV |
| Contraindicado | IAo moderada-severa, disección aórtica, vasculopatía | IAo moderada-severa, disección aórtica, vasculopatía | Trombo ventricular, RVAo mecánica, EAo<0,6cm, IAo moderada-severa, CIA/CIV, HVI moderada-severa | IAo moderada-severa, disección aórtica, vasculopatía, hemorragia incontrolable | Disección aórtica, hemorragia incontrolable | Imposibilidad anticoagulación | Imposibilidad anticoagulación |
ACV: accidente cerebrovascular; BiV: biventricular; CIA/CIV: comunicación interauricular/interventricular; EAo: estenosis aórtica; EAP: edema agudo de pulmón; ECMO: oxigenación por membrana extracorpórea; HVI: hipertrofia de ventrículo izquierdo; IAo: insuficiencia aórtica; RVAo: recambio valvular aórtico; TV: taquicardia ventricular; VA: veno-arterial; VAD: dispositivo de asistencia ventricular; VAo: válvula aórtica; VD: ventrículo derecho; VI: ventrículo izquierdo.
Hasta el momento, no existen estudios que comparen, de forma controlada, los dispositivos de SCM y muestren diferencias significativas en cuanto a resultados y mortalidad, por lo que la decisión debe individualizarse teniendo en cuenta factores como si el fracaso es uni o biventricular, si hay insuficiencia respiratoria concomitante, el grado y la severidad del shock, las posibilidades de recuperación (o incluso opciones de trasplante) y la experiencia y disponibilidad de los equipos65.
Existe controversia en cuanto a la posible superioridad de la canulación central frente a la periférica65. La central favorece un soporte hemodinámico, con flujo anterógrado en la aorta, descargando de forma efectiva el ventrículo, y el drenaje directo de la aurícula permite generar mayores flujos de soporte. En cambio, la periférica permite el cierre esternal, disminuyendo las complicaciones hemorrágicas e infecciosas. La evidencia científica está basada, fundamentalmente, en series retrospectivas. En el estudio retrospectivo con mayor número de pacientes y metaanálisis ulterior no hubo diferencias en la mortalidad; en cambio, sí mostró menos sangrado, transfusiones y fracaso renal con necesidad de técnicas de reemplazo renal (TRR) en el grupo de canulación periférica64,65. En contraposición, un estudio y metaanálisis posterior sí observó una mejor supervivencia en los pacientes soportados con ECMO-VA periférico66. Las complicaciones, sobre todo en la canulación arterial, son de carácter isquémico en el miembro afectado y hemorrágico. Existen alternativas de retorno, como la arteria axilar-subclavia, que retorna un flujo anterógrado y, por tanto, aumenta menos la poscarga que el acceso femoral sin tener que realizar esternotomía67. La canulación de la arteria pulmonar se puede utilizar para retorno en una asistencia derecha o como drenaje para drenar cavidades derechas e izquierdas68.
Cuando se utiliza la ECMO-VA periférica, una complicación relativamente frecuente es el aumento de la poscarga del VI generada por el flujo retrógrado del sistema, que conlleva que la función miocárdica nativa no sea capaz de generar volumen sistólico e, incluso, la falta de apertura de la válvula aórtica. Ello genera congestión pulmonar y aumento de la presión intraventricular, disminuyendo las posibilidades de recuperación de la función miocárdica. En la fase inicial de distensión ventricular debemos realizar un manejo conservador basado en la disminución del flujo del SCM, el uso de inotrópicos y vasodilatadores. Estas medidas, solas o asociadas a implante de BCIAo, pueden ser suficientes. En caso contrario, o si se produce congestión pulmonar severa, se debe plantear drenaje directo de las cavidades izquierdas mediante un sistema transaórtico, un catéter interauricular, o con un drenaje directo de cavidades izquierdas colocado de forma quirúrgica69.
A pesar de que la ECMO-VA es el tipo de soporte más usado en el SCP (especialmente la periférica con accesos femorales)70, existen soportes alternativos y/o complementarios (tabla 5). El BCIAo sigue siendo, con frecuencia, el primer soporte instaurado debido a su fácil implantación, bajo porcentaje de complicaciones y eficacia71,72. La familia de Impella® genera un soporte univentricular efectivo. La experiencia en el SCP es escasa, pero en pacientes seleccionados sin insuficiencia respiratoria grave y situación no urgente puede ser una opción adecuada. El uso de asistencia ventricular de corta duración puede ser apropiado en primera instancia, en casos seleccionados, para dar soporte uni/biventricular y, si fuera necesario, con oxigenador intercalado.
Disfunción renal aguda asociada a SCP (material suplementario)La aparición de disfunción renal aguda en cirugía cardiaca se asocia a una mortalidad de un 22% y cuando precisa TRR, de hasta un 65%. De los supervivientes, aproximadamente un 10% no recuperan la función renal y dependen de la hemodiálisis posteriormente73. En pacientes con SCP, la disfunción renal aguda puede ser grave y persistir durante semanas o meses74. En el momento actual, tras numerosos ensayos y metaanálisis75–80, no hay evidencia firme que apoye que el inicio precoz de las TRR disminuya la mortalidad. Una estrategia conservadora para iniciar TRR poscirugía cardiaca, con objetivos bien definidos, es un enfoque aceptable que permitirá a muchos pacientes recuperar la función renal sin las potenciales complicaciones de estas.
En definitiva, podemos concluir que el SCP es una entidad muy relevante en el contexto de la medicina intensiva y los cuidados críticos, con una elevada morbimortalidad. Su adecuado conocimiento y un tratamiento rápido y ordenado, basado en la monitorización completa y en la experiencia, con uso de SCM precoz, si es preciso, puede mejorar su evolución y pronóstico. Se aportan pautas de actuación que pueden ser de utilidad para el clínico que debe manejar este tipo de pacientes en su práctica diaria.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.