Contribuir a la validación de la escala de Braden en el paciente ingresado en la UCI mediante un análisis de su fiabilidad y validez predictiva.
DiseñoAnalítico, observacional, longitudinal y prospectivo.
ÁmbitoUnidad de Cuidados Intensivos del Hospital Virgen del Rocío (Sevilla).
PacientesSe incluyeron los pacientes de 18años o más que permanecieron ingresados en la unidad durante más de 24h. Fueron excluidos los pacientes que presentaron úlceras por presión al ingreso. En total, 335 pacientes fueron incluidos durante dos períodos de estudio de un mes de duración cada uno de ellos.
IntervencionesNinguna.
Variables de interés principalesComo variable principal se consideró la aparición de UPP en estadios deli aliv. Para el resto de variables se tomaron 3 categorías: demográficas, clínicas y de pronóstico.
ResultadosLa incidencia de pacientes que desarrollaron úlceras por presión fue del 8,1%. Un 40,6% han sido de estadioi y un 59,4% de estadioii, destacando el sacro como localización más frecuente. El valor del coeficiente alfa de Cronbach en las valoraciones consideradas ha indicado una fiabilidad de buena a moderada. En las 3 valoraciones realizadas un punto de corte de 12 se presentó como óptimo en la valoración del primer y segundo días de ingreso. En relación a la valoración del día con puntuación mínima, el punto de corte óptimo fue 10.
ConclusionesLa escala de Braden muestra una insuficiente validez predictiva y pobre precisión tanto para un punto de corte de 18 como de 16, que son los aceptados en los distintos escenarios clínicos.
Contribution to validation of the Braden scale in patients admitted to the ICU, based on an analysis of its reliability and predictive validity.
DesignAn analytical, observational, longitudinal prospective study was carried out.
SettingIntensive Care Unit, Hospital Virgen del Rocío, Seville (Spain).
PatientsPatients aged 18years or older and admitted for over 24hours to the ICU were included. Patients with pressure ulcers upon admission were excluded. A total of 335 patients were enrolled in two study periods of one month each.
InterventionsNone.
Variables of interestThe presence of gradei-iv pressure ulcers was regarded as the main or dependent variable. Three categories were considered (demographic, clinical and prognostic) for the remaining variables.
ResultsThe incidence of patients who developed pressure ulcers was 8.1%. The proportion of gradei andii pressure ulcer was 40.6% and 59.4% respectively, highlighting the sacrum as the most frequently affected location. Cronbach's alpha coefficient in the assessments considered indicated good to moderate reliability. In the three evaluations made, a cutoff point of 12 was presented as optimal in the assessment of the first and second days of admission. In relation to the assessment of the day with minimum score, the optimal cutoff point was 10.
ConclusionsThe Braden scale shows insufficient predictive validity and poor precision for cutoff points of both 18 and 16, which are those accepted in the different clinical scenarios.
Los pacientes que ingresan en las unidades de cuidados intensivos (UCI) suelen presentar fallo de uno o más órganos o sistemas e incluso fracaso multiorgánico, y frecuentemente necesitan medidas de soporte vital como ventilación mecánica, sedación continua, fármacos vasoactivos, además de múltiples tipos de dispositivos como catéteres, drenajes, sondas e inmovilizaciones. Estas medidas perjudican significativamente uno de los mecanismos más importantes para el mantenimiento de la integridad cutánea, la movilidad, haciendo a los pacientes altamente vulnerables al desarrollo de úlceras por presión (UPP)1-2. Por ello, aunque las UPP representan un problema de salud que afecta a todos los niveles asistenciales, adquiere una especial relevancia en las UCI, donde encontramos niveles de incidencia que oscilan ampliamente entre el 3,3 y el 52,9%3-4. Aunque se admite que su aparición no es un factor causal de mortalidad durante un ingreso hospitalario, se asocia a esta y a otras complicaciones en la recuperación: incremento del riesgo de infección, malnutrición intrahospitalaria, y aumento de la estancia, de la carga de trabajo de enfermería y del coste sanitario5.
Identificar a los pacientes en riesgo es esencial para la adecuada implementación de programas de prevención y para la adecuada utilización de los recursos. Se han desarrollado y validado diferentes escalas de valoración de riesgo con la finalidad de ayudar a los profesionales sanitarios a identificar los riesgos individuales para la aparición de UPP6.
Una escala de valoración de riesgo debería ser lo suficientemente competente para diferenciar pacientes que estén en riesgo de desarrollo de UPP y pacientes que no lo estén. Se recomienda el uso de herramientas para valoración del riesgo validadas, pero no se ha determinado qué herramienta es la que mejor se adapta a un entorno de cuidados concreto7.
En la actualidad solo 7 escalas han sido validadas para su utilización en la UCI. Tres de ellas son escalas específicas del paciente crítico (Cubbin-Jackson, Norton Mod. Bienstein y Jackson-Cubbin) y 4 son generalistas (Norton, Waterlow, Braden y Braden Mod Song-Choi)8.
Pero sin duda el esfuerzo más importante para realizar un análisis sobre los factores de riesgo ha sido desarrollado por Barbara Braden y Nancy Bergstrom, que fueron las primeras autoras —y únicas hasta ahora— en desarrollar un mapa conceptual sobre el desarrollo de las UPP. La escala de Braden fue desarrollada en 1985 en Estados Unidos, en el contexto de un proyecto de investigación en centros sociosanitarios, como intento de dar respuesta a algunas de las limitaciones de la escala de Norton, realizando su escala a través de un esquema conceptual en el que reseñaron, ordenaron y relacionaron los conocimientos existentes sobre UPP9-10. La escala de Braden consta de 6 subescalas: percepción sensorial, exposición de la piel a la humedad, actividad física, movilidad, nutrición y peligro de lesiones cutáneas por fuerzas de fricción y/o cizalla. Es una escala negativa, es decir, que a menor puntuación el riesgo es más elevado, con un rango que oscila entre los 6 y los 23 puntos. Se consideran pacientes de riesgo los que obtienen puntuaciones iguales o inferiores a 18, y se clasifican como: pacientes de muy alto riesgo (puntuación ≤9), de alto riesgo (puntuaciones entre 10 y 12), de riesgo moderado (puntuaciones entre 13 y 14) y de bajo riesgo (puntuaciones entre 15 y 18)11.
En su estudio inicial, Bergstrom et al.10 reportaron una sensibilidad del 83% y una especificidad del 64% para un punto de corte de 16. Quince años más tarde, los mismos autores recomendaron el punto de corte de 18 como más apropiado al poder incluir a pacientes más ancianos y a los fisiológicamente más inestables tanto caucásicos como afroamericanos12. Pero este punto de corte óptimo puede no ser el más adecuado en todos los entornos clínicos debido a las distintas características de los pacientes y a los factores de riesgo a los que puedan verse sometidos. El objetivo de este estudio ha sido contribuir a la validación de la escala de Braden en el paciente ingresado en una UCI mediante un análisis de su fiabilidad y su validez predictiva.
Material y métodoSe ha realizado un estudio con un diseño analítico, observacional, longitudinal y prospectivo. La población de estudio han sido los pacientes ingresados en una UCI de adultos ubicada en un hospital de tercer nivel y general. Esta UCI cuenta con 72 camas, de las cuales 10 corresponden a una unidad de cuidados intermedios. La recogida de datos se ha llevado a cabo en 2 fases. La primera fase, con una duración de 31días, comenzó el 9 de febrero de 2015 y concluyó el 12 de marzo de 2015. La segunda fase, con una duración de 32días, comenzó el 30 de mayo de 2015 y finalizó el 30 de junio de 2015. Se incluyeron en el estudio los pacientes de 18años o más que permanecieron ingresados en la unidad durante más de 24h. Fueron excluidos los pacientes que presentaron UPP al ingreso y los ingresados en la unidad de cuidados intermedios. Los pacientes que requirieron reingreso fueron considerados un nuevo caso. El seguimiento de los pacientes se mantuvo hasta el momento de la aparición de la primera UPP o hasta el momento del alta o defunción. En el caso de aparición de una UPP se continuó monitorizando a los pacientes por si desarrollaban una nueva UPP y para valoración de la evolución de las UPP ya desarrolladas.
Con relación al tamaño muestral, para conseguir una precisión del 3% en la estimación de una proporción mediante un intervalo de confianza asintótico normal con corrección para poblaciones finitas al 95% bilateral, asumiendo que la proporción de incidencia esperada de UPP en la población general sea un 8%, ya que ha sido la incidencia media de los 5 últimos años, y que el tamaño total de la población en esta UCI con estancia mayor de 24horas sea de 1.800 pacientes al año, sería necesario incluir 268 unidades experimentales en el estudio. Teniendo en cuenta que el porcentaje esperado de abandonos sea del 15%, se consideró necesario reclutar 316 unidades experimentales en el estudio.
Procedimiento de recogida de datosLos datos fueron recogidos diariamente por 5 enfermeras investigadoras mediante observación directa. En el momento en que se desarrollaba una UPP, era recogida en la historia del paciente junto con los datos relacionados con la misma (fecha de aparición, estadio, localización y evolución). Se ha utilizado el sistema de clasificación y estadificación de UPP en 4 estadios que recomienda el National Pressure Ulcer Advisory Panel (NPUAP) y el European Pressure Ulcer Advisory Panel (EPUAP)13. Para verificar el grado de las UPP se contó con la opinión de una segunda enfermera investigadora con la finalidad de establecer el diagnóstico final. Para la valoración del riesgo de aparición de UPP se utilizó la escala de Braden. Si la puntuación obtenida era >18 el paciente se consideró sin riesgo para el desarrollo de UPP, entre 15-18 se consideró con riesgo leve, entre 13-14 con riesgo moderado, entre 10-12 con riesgo alto y ≤9 con riesgo muy alto. En función de este riesgo, se aplicaron las medidas preventivas incluidas en el protocolo de prevención de UPP de esta UCI. Cada paciente fue valorado diariamente hasta la finalización de su periodo de seguimiento. En una primera fase se consideraron para los análisis de fiabilidad y validez: la puntuación en las primeras 24h de ingreso, la puntuación del segundo día de ingreso y el valor mínimo de la puntuación obtenida a lo largo de la estancia del paciente en la UCI. En una segunda fase se repitieron los análisis de fiabilidad y validez excluyendo las UPP en estadioi.
Variables e instrumentosComo variable principal o dependiente se consideró la aparición de UPP durante el periodo de ingreso en estadios o categorías deli aliv y en cualquier localización corporal. No se consideraron las categorías adicionales para Estados Unidos.
Para el resto de variables se tomaron 3 categorías:
- 1.
Demográficas: edad y sexo.
- 2.
Clínicas: duración de la estancia en UCI, procedencia del paciente, si fue reingreso, comorbilidades, diagnóstico de ingreso, carga de trabajo de enfermería medida con la escala Nursing Activities Scores (NAS), complicaciones y variables de resultado (limitación del esfuerzo terapéutico [LET], fallecimiento).
- 3.
Variables de pronóstico: puntuación diaria de riesgo de desarrollo de UPP mediante la escala Braden y puntuación de la escala SAPS 3 al ingreso como índice de gravedad.
El proyecto se ha desarrollado siguiendo las recomendaciones recogidas en la declaración de Helsinki sobre principios éticos para las investigaciones médicas en seres humanos.
Todos los registros y cuestionarios fueron preservados por el investigador principal. La identificación de los pacientes solo estuvo consignada por el número de caso que se le hubiese adjudicado, cumpliendo de esa forma la legislación española sobre la protección de datos (Ley Orgánica 15/1999 de 13 de diciembre).
Se solicitó la autorización del Comité de Ética de Investigación Biomédica de Andalucía para la realización del presente estudio de investigación que no consideró necesaria la solicitud de consentimiento informado debido a la no realización de ningún tipo de intervención.
Análisis estadísticoSe realizó un análisis exploratorio de los datos para identificar valores extremos y caracterizar diferencias entre subgrupos de individuos, así como alteraciones en la forma de las variables cuantitativas, determinando si se violaban los supuestos estadísticos. Posteriormente se procedió a realizar el análisis descriptivo de la muestra. Las variables numéricas se expresaron como medias y desviaciones estándar las que se ajustaban a una distribución normal, y como medianas y cuartiles las que no lo hacían, mientras que las variables cualitativas se expresaron con frecuencias absolutas y porcentajes.
La incidencia fue calculada como incidencia acumulada. La tasa de incidencia o densidad de incidencia se calculó como la relación entre el número de UPP desarrolladas a lo largo de la estancia en la UCI y la suma de los períodos de estancia en la UCI de cada uno de los individuos a lo largo del período de estudio por cada 1.000días de estancia.
Se realizó análisis inferencial bivariado para comparar variables de tipo cuantitativo/numérico entre pacientes que desarrollaron UPP y los que no lo hicieron. Se utilizó la prueba no paramétrica U de Mann-Whitney, pues no se pudo aceptar el supuesto de normalidad en las variables cuantitativas. Análogamente, para estudiar la relación entre variables de tipo cualitativo en los 2 grupos se empleó el test chi-cuadrado o el test exacto de Fisher. Se han complementado los resultados con los intervalos de confianza al 95%.
Con el objetivo de comprobar la fiabilidad de los ítems que conforman la escala de Braden se analizó la consistencia interna de esta escala en la muestra de estudio mediante el coeficiente alfa de Cronbach. El coeficiente de correlación de Spearman (rs) se ha utilizado para determinar las subescalas que han presentado una mayor correlación con el riesgo total obtenido en la escala Braden y el coeficiente de determinación (rs2) para conocer qué porcentaje de la variabilidad de la escala de Braden se explicó por cada una de las subescalas.
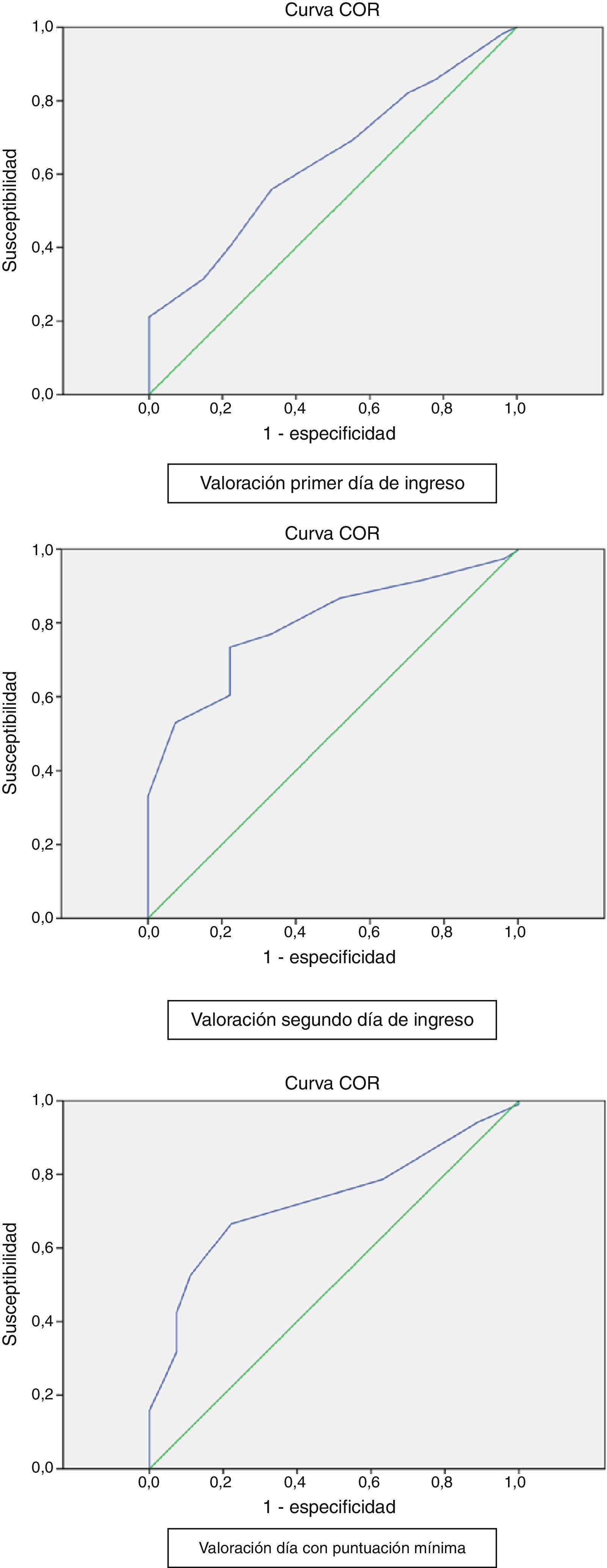
Para el análisis de la validez de la escala se midieron la sensibilidad, la especificidad, la eficacia o exactitud, el valor predictivo positivo, el valor predictivo negativo y el cociente de probabilidades (likelihood ratio). Se generó la curva receiver operating characteristics (ROC) y se calculó el área bajo la curva (AUC).
El análisis de los datos se realizó con el paquete estadístico IBM SPSS 20.0 para Windows.
ResultadosLa muestra total de estudio ha sido de 335 pacientes. No se incluyeron 154 pacientes por ingresos menores de 24h y un paciente por ser menor de edad. Se excluyeron 15pacientes por presentar UPP en el momento de su ingreso. La edad media de nuestra muestra de estudio ha sido de 59,76años (DE±14,30). En cuanto al sexo, un 61,5% eran varones. La estancia en la UCI ha presentado una mediana de 4 (p25=2,0; p75=4,0) días.
Del total de 335 pacientes incluidos, 27 desarrollaron UPP. Por tanto, la incidencia de pacientes que desarrollaron UPP ha sido de un 8,1%. Tres de estos pacientes desarrollaron 2UPP y uno de ellos desarrolló 3UPP. Por tanto, el número total de UPP desarrolladas ha sido de 32. Expresada la incidencia como tasa de incidencia de pacientes que desarrollaron UPP, el resultado ha sido de 11,72 por 1.000días de estancia, con un IC95% de 7,88-16,82.
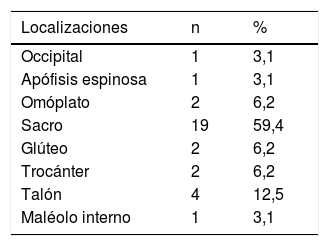
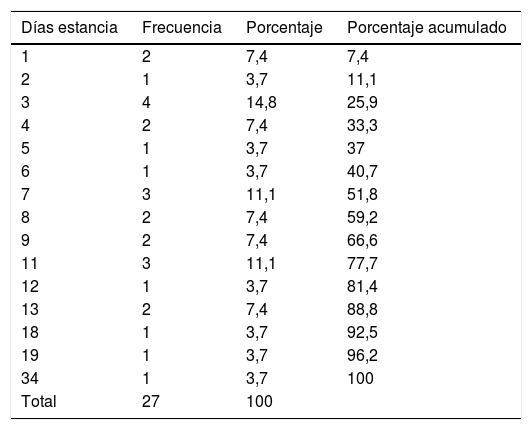
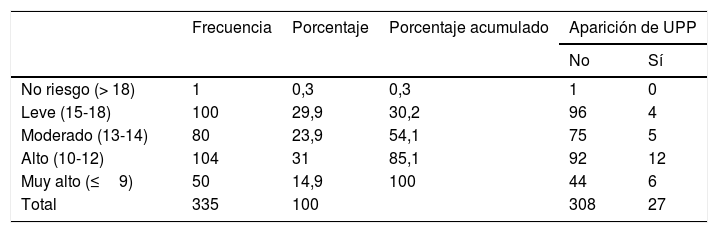
En cuanto a su estadio, 13 (40,6%) UPP han sido de estadioi y 19 (59,4%) UPP de estadioii. No ha aparecido ninguna UPP en estadiosiii oiv. Las UPP desarrolladas presentaron múltiples localizaciones, que se detallan en la tabla 1, destacando el sacro como localización más frecuente (n=19; 59,4%). Con relación al tiempo de aparición en días de UPP, presentó una mediana de 7 días (p25=3,5; p75=11) con un mínimo de 1día y un máximo de 34días. El 88,9% de las UPP aparecieron en los primeros 14días de ingreso. La distribución en frecuencias y porcentajes queda recogida en la tabla 2. Solo un paciente fue clasificado como sin riesgo de desarrollo de UPP en la valoración realizada en las primeras 24h, como queda recogido en la tabla 3. En la valoración del segundo día de ingreso, de los 27 pacientes que desarrollaron UPP, 6 fueron clasificados con riesgo leve, 14 con riesgo alto y 7 con riesgo muy alto. En la valoración llevada a cabo en el día de puntuación mínima un paciente fue clasificado con riesgo leve, uno con riesgo moderado, 15 con riesgo alto y 10 con riesgo muy alto.
Tiempo de aparición de las úlceras por presión
| Días estancia | Frecuencia | Porcentaje | Porcentaje acumulado |
|---|---|---|---|
| 1 | 2 | 7,4 | 7,4 |
| 2 | 1 | 3,7 | 11,1 |
| 3 | 4 | 14,8 | 25,9 |
| 4 | 2 | 7,4 | 33,3 |
| 5 | 1 | 3,7 | 37 |
| 6 | 1 | 3,7 | 40,7 |
| 7 | 3 | 11,1 | 51,8 |
| 8 | 2 | 7,4 | 59,2 |
| 9 | 2 | 7,4 | 66,6 |
| 11 | 3 | 11,1 | 77,7 |
| 12 | 1 | 3,7 | 81,4 |
| 13 | 2 | 7,4 | 88,8 |
| 18 | 1 | 3,7 | 92,5 |
| 19 | 1 | 3,7 | 96,2 |
| 34 | 1 | 3,7 | 100 |
| Total | 27 | 100 |
Categorización del riesgo de aparición de úlceras por presión (UPP) el primer día de ingreso y desarrollo de UPP
| Frecuencia | Porcentaje | Porcentaje acumulado | Aparición de UPP | ||
|---|---|---|---|---|---|
| No | Sí | ||||
| No riesgo (> 18) | 1 | 0,3 | 0,3 | 1 | 0 |
| Leve (15-18) | 100 | 29,9 | 30,2 | 96 | 4 |
| Moderado (13-14) | 80 | 23,9 | 54,1 | 75 | 5 |
| Alto (10-12) | 104 | 31 | 85,1 | 92 | 12 |
| Muy alto (≤9) | 50 | 14,9 | 100 | 44 | 6 |
| Total | 335 | 100 | 308 | 27 | |
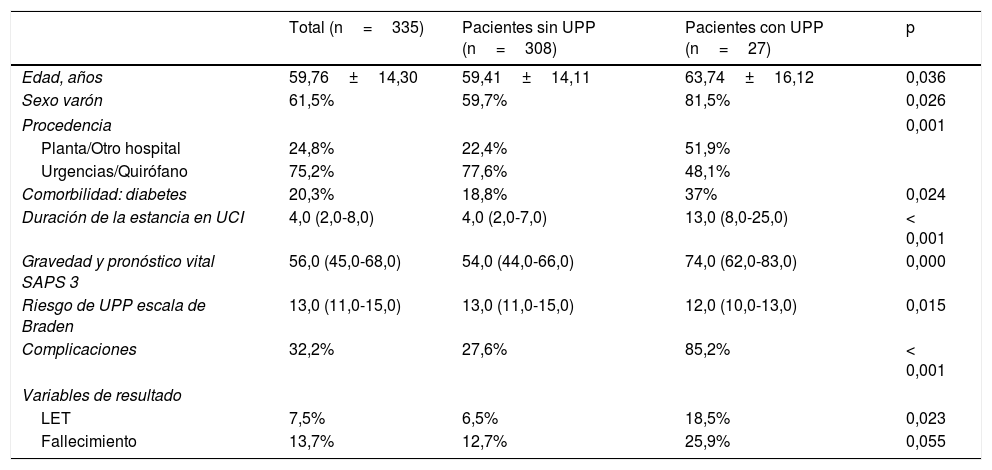
Las variables independientes analizadas mediante análisis univariante que se presentaron como significativamente asociadas al desarrollo de UPP se muestran en la tabla 4.
Comparación de variables en pacientes que desarrollaron úlceras por presión (UPP) y no desarrollaron UPP
| Total (n=335) | Pacientes sin UPP (n=308) | Pacientes con UPP (n=27) | p | |
|---|---|---|---|---|
| Edad, años | 59,76±14,30 | 59,41±14,11 | 63,74±16,12 | 0,036 |
| Sexo varón | 61,5% | 59,7% | 81,5% | 0,026 |
| Procedencia | 0,001 | |||
| Planta/Otro hospital | 24,8% | 22,4% | 51,9% | |
| Urgencias/Quirófano | 75,2% | 77,6% | 48,1% | |
| Comorbilidad: diabetes | 20,3% | 18,8% | 37% | 0,024 |
| Duración de la estancia en UCI | 4,0 (2,0-8,0) | 4,0 (2,0-7,0) | 13,0 (8,0-25,0) | < 0,001 |
| Gravedad y pronóstico vital SAPS 3 | 56,0 (45,0-68,0) | 54,0 (44,0-66,0) | 74,0 (62,0-83,0) | 0,000 |
| Riesgo de UPP escala de Braden | 13,0 (11,0-15,0) | 13,0 (11,0-15,0) | 12,0 (10,0-13,0) | 0,015 |
| Complicaciones | 32,2% | 27,6% | 85,2% | < 0,001 |
| Variables de resultado | ||||
| LET | 7,5% | 6,5% | 18,5% | 0,023 |
| Fallecimiento | 13,7% | 12,7% | 25,9% | 0,055 |
Con el objetivo de comprobar la fiabilidad de los ítems que conforman la escala de Braden, estudiamos la consistencia interna de esta escala en nuestra muestra de pacientes mediante el coeficiente alfa de Cronbach14,15, que sirvió para cuantificar el grado de correlación parcial de los ítems, es decir, el grado en el que los ítems del constructo estaban relacionados. El valor del coeficiente alfa de Cronbach en la valoración en las primeras 24h fue de 0,443, indicando una relación moderada entre los ítems. En la valoración del segundo día de ingreso fue de 0,722, indicando una buena fiabilidad con una relación fuerte entre los ítems, y en la valoración en el día de puntuación mínima fue de 0,561, indicando una fiabilidad moderada. En una segunda fase, excluyendo las UPP en estadioi, el valor del coeficiente alfa de Cronbach en la valoración en las primeras 24h fue de 0,425, indicando una relación moderada entre los ítems. En la valoración del segundo día de ingreso fue de 0,690, indicando una buena fiabilidad con una relación fuerte entre los ítems, y en la valoración en el día de puntuación mínima fue de 0,543, indicando una fiabilidad moderada.
Las subescalas que presentaron una mayor correlación con el riesgo total obtenido en la escala Braden —dicho de otra forma, a qué subescalas se debió mayoritariamente el riesgo observado en nuestra muestra— fueron la percepción sensorial, la movilidad y la fricción/deslizamiento en las 3 valoraciones realizadas tanto considerando todos los estadios como excluyendo las UPP en estadioi. Para su cálculo hemos utilizado el coeficiente de correlación de Spearman (rs).
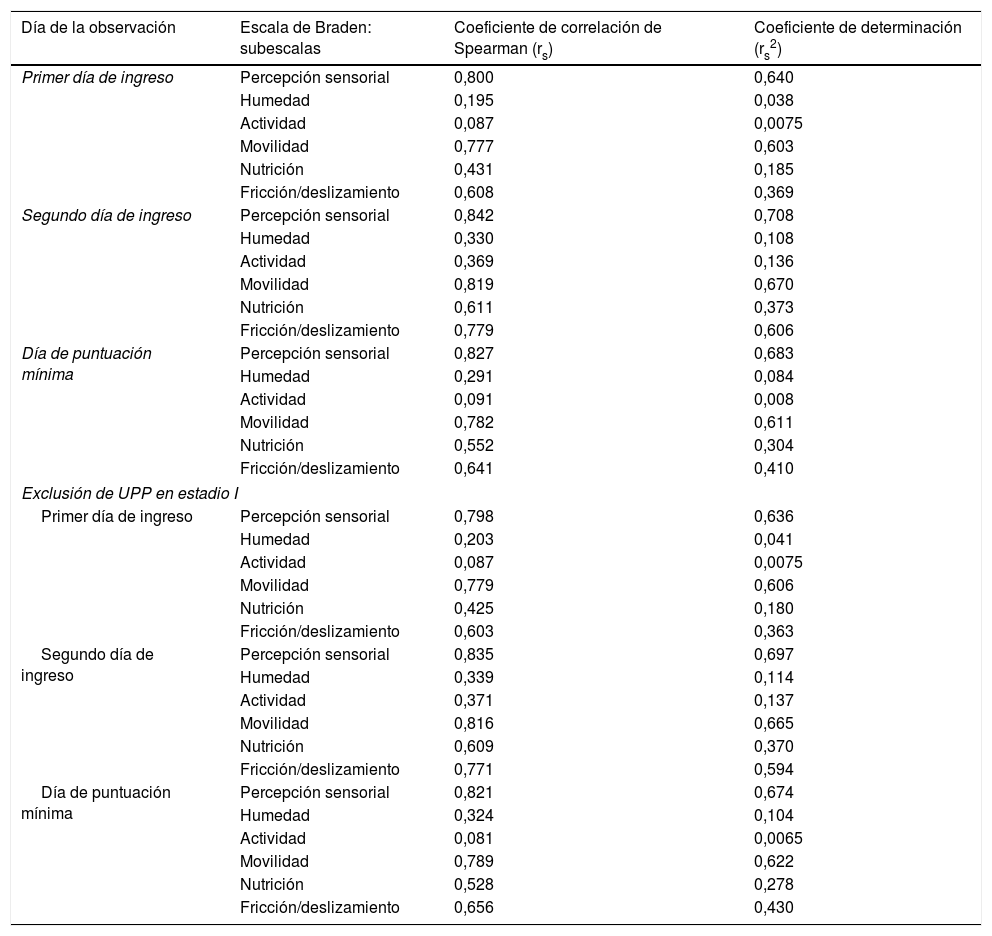
Mediante el coeficiente de determinación (rs2) se calculó qué porcentaje de la variabilidad de la escala de Braden se explicaba por cada una de las subescalas (en la tabla 5 se muestran tanto los coeficientes de correlación como los de determinación según día de observación). En la valoración del primer día de ingreso, un 64% de la variabilidad de la escala de Braden se explicó por la percepción sensorial, un 60,3% por la movilidad y un 36,9% por la fricción/deslizamiento. En la valoración del segundo día de ingreso, un 70,8% de la variabilidad de la escala de Braden se explicó por la percepción sensorial, un 67% por la movilidad y un 37,3% por la fricción/deslizamiento. En cuanto a la valoración correspondiente al día de puntuación mínima, un 68,3% de la variabilidad de la escala de Braden se explicó por la percepción sensorial, un 61,1% por la movilidad y un 41% por la fricción/deslizamiento. Valores muy similares resultaron al excluir las UPP en estadioi.
Coeficientes de correlación y determinación escala de Braden según el día de la observación
| Día de la observación | Escala de Braden: subescalas | Coeficiente de correlación de Spearman (rs) | Coeficiente de determinación (rs2) |
|---|---|---|---|
| Primer día de ingreso | Percepción sensorial | 0,800 | 0,640 |
| Humedad | 0,195 | 0,038 | |
| Actividad | 0,087 | 0,0075 | |
| Movilidad | 0,777 | 0,603 | |
| Nutrición | 0,431 | 0,185 | |
| Fricción/deslizamiento | 0,608 | 0,369 | |
| Segundo día de ingreso | Percepción sensorial | 0,842 | 0,708 |
| Humedad | 0,330 | 0,108 | |
| Actividad | 0,369 | 0,136 | |
| Movilidad | 0,819 | 0,670 | |
| Nutrición | 0,611 | 0,373 | |
| Fricción/deslizamiento | 0,779 | 0,606 | |
| Día de puntuación mínima | Percepción sensorial | 0,827 | 0,683 |
| Humedad | 0,291 | 0,084 | |
| Actividad | 0,091 | 0,008 | |
| Movilidad | 0,782 | 0,611 | |
| Nutrición | 0,552 | 0,304 | |
| Fricción/deslizamiento | 0,641 | 0,410 | |
| Exclusión de UPP en estadio I | |||
| Primer día de ingreso | Percepción sensorial | 0,798 | 0,636 |
| Humedad | 0,203 | 0,041 | |
| Actividad | 0,087 | 0,0075 | |
| Movilidad | 0,779 | 0,606 | |
| Nutrición | 0,425 | 0,180 | |
| Fricción/deslizamiento | 0,603 | 0,363 | |
| Segundo día de ingreso | Percepción sensorial | 0,835 | 0,697 |
| Humedad | 0,339 | 0,114 | |
| Actividad | 0,371 | 0,137 | |
| Movilidad | 0,816 | 0,665 | |
| Nutrición | 0,609 | 0,370 | |
| Fricción/deslizamiento | 0,771 | 0,594 | |
| Día de puntuación mínima | Percepción sensorial | 0,821 | 0,674 |
| Humedad | 0,324 | 0,104 | |
| Actividad | 0,081 | 0,0065 | |
| Movilidad | 0,789 | 0,622 | |
| Nutrición | 0,528 | 0,278 | |
| Fricción/deslizamiento | 0,656 | 0,430 | |
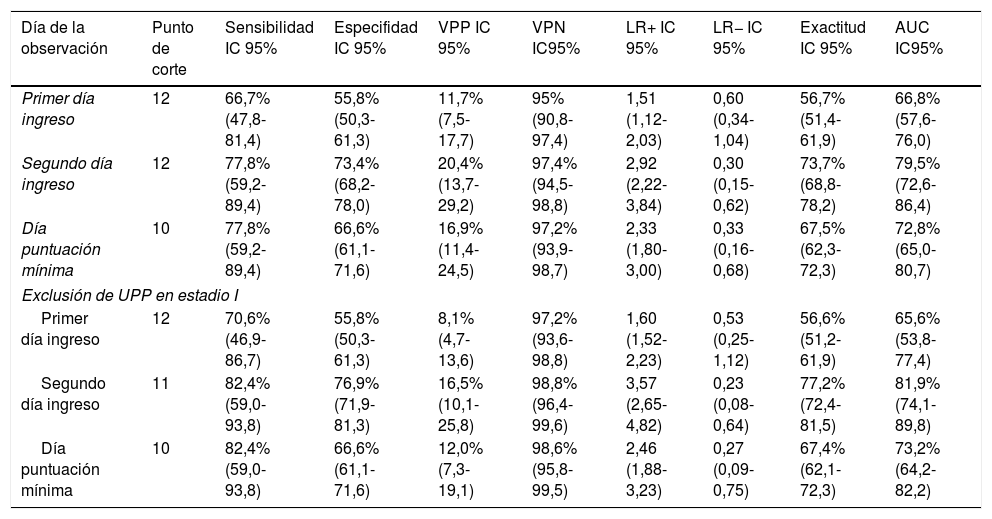
Con relación a los parámetros de validez y capacidad predictiva (tabla 6), un punto de corte de 12 se presentó como óptimo, por presentar el mejor balance entre sensibilidad y especificidad en la valoración del primer y segundo días de ingreso, presentando una sensibilidad del 66,7% y una especificidad del 55,8% en el caso del primer día, y una sensibilidad del 77,8% y una especificidad del 73,4% en el caso del segundo día. En relación a la valoración del día con puntuación mínima, el punto de corte óptimo fue 10 con una sensibilidad de 77,8% y especificidad de 66,6%. Al excluir las UPP en estadio i, un punto de corte de 12 se presentó como óptimo, por presentar el mejor balance entre sensibilidad y especificidad, en la valoración del primer día de ingreso presentando una sensibilidad de 70,6% y una especificidad de 55,8%. Un punto de corte de 11 se presentó como óptimo en el caso del segundo día de ingreso con una sensibilidad de 82,4% y especificidad de 76,9%. Con relación a la valoración del día con puntuación mínima, el punto de corte óptimo fue 10, con una sensibilidad del 82,4% y una especificidad del 66,6%.
Validez predictiva de la escala Braden según tipo de valoración
| Día de la observación | Punto de corte | Sensibilidad IC 95% | Especifidad IC 95% | VPP IC 95% | VPN IC95% | LR+ IC 95% | LR− IC 95% | Exactitud IC 95% | AUC IC95% |
|---|---|---|---|---|---|---|---|---|---|
| Primer día ingreso | 12 | 66,7% (47,8-81,4) | 55,8% (50,3-61,3) | 11,7% (7,5-17,7) | 95% (90,8-97,4) | 1,51 (1,12-2,03) | 0,60 (0,34-1,04) | 56,7% (51,4-61,9) | 66,8% (57,6-76,0) |
| Segundo día ingreso | 12 | 77,8% (59,2-89,4) | 73,4% (68,2-78,0) | 20,4% (13,7-29,2) | 97,4% (94,5-98,8) | 2,92 (2,22-3,84) | 0,30 (0,15-0,62) | 73,7% (68,8-78,2) | 79,5% (72,6-86,4) |
| Día puntuación mínima | 10 | 77,8% (59,2-89,4) | 66,6% (61,1-71,6) | 16,9% (11,4-24,5) | 97,2% (93,9-98,7) | 2,33 (1,80-3,00) | 0,33 (0,16-0,68) | 67,5% (62,3-72,3) | 72,8% (65,0-80,7) |
| Exclusión de UPP en estadio I | |||||||||
| Primer día ingreso | 12 | 70,6% (46,9-86,7) | 55,8% (50,3-61,3) | 8,1% (4,7-13,6) | 97,2% (93,6-98,8) | 1,60 (1,52-2,23) | 0,53 (0,25-1,12) | 56,6% (51,2-61,9) | 65,6% (53,8-77,4) |
| Segundo día ingreso | 11 | 82,4% (59,0-93,8) | 76,9% (71,9-81,3) | 16,5% (10,1-25,8) | 98,8% (96,4-99,6) | 3,57 (2,65-4,82) | 0,23 (0,08-0,64) | 77,2% (72,4-81,5) | 81,9% (74,1-89,8) |
| Día puntuación mínima | 10 | 82,4% (59,0-93,8) | 66,6% (61,1-71,6) | 12,0% (7,3-19,1) | 98,6% (95,8-99,5) | 2,46 (1,88-3,23) | 0,27 (0,09-0,75) | 67,4% (62,1-72,3) | 73,2% (64,2-82,2) |
AUC: área bajo la curva ROC; IC 95: intervalo de confianza del 95%; LR+: likelihood ratio positivo; LR−: likelihood ratio negativo; VPN: valor predictivo negativo; VPP: valor predictivo positivo.
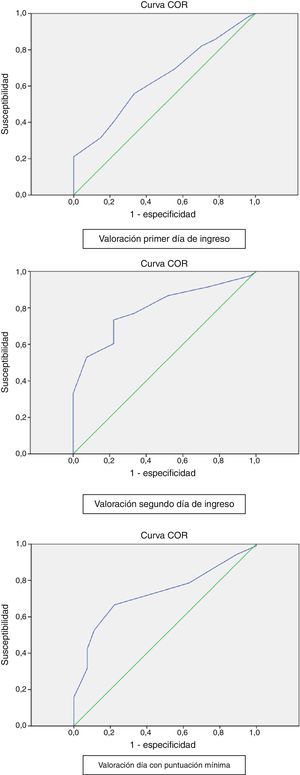
En la figura 1 se representan las diferentes áreas bajo la curva ROC. El análisis del AUC mostró una moderada capacidad discriminatoria (66,8%) en la valoración del primer día de ingreso y en la del día con puntuación mínima (72,8%) y una buena capacidad discriminatoria (79,5%) para la valoración del segundo día de ingreso. Valores muy similares resultaron al excluir las UPP en estadioi.
DiscusiónTeniendo en consideración que la incidencia reportada en el entorno de esta UCI fue del 8,1%, podemos afirmar que es inferior a los valores hallados por otros autores en similares entornos clínicos. Solo el estudio de Tescher et al.3 reportó una incidencia inferior, del 3,3%. Pero hemos de tener en cuenta que en este estudio no se incluyeron las UPP en estadioi, dado su potencial carácter reversible, y que se incluyeron pacientes ingresados en 10UCI y en 7 unidades de cuidados intermedios. En nuestro estudio, un 40,6% fueron UPP en estadioi, y además no fueron incluidos los pacientes ingresados en la unidad de cuidados intermedios. Estos resultados podrían deberse a que la formación y la sensibilización del personal de enfermería a la hora de declarar tanto el riesgo como la aparición de UPP es elevada, en la medida que en la unidad está implantado un protocolo de actuación para la prevención de UPP, consistente en la realización de una valoración sistemática del riesgo de aparición de UPP usando la escala de Braden, lo que permite a las enfermeras establecer de forma precoz una serie de medidas preventivas acordes al nivel de riesgo detectado. Estas medidas son las recomendadas por la GNEAUPP en sus directrices generales sobre el tratamiento de las UPP16. Brunet y Kurcgant17 publicaron la incidencia de UPP antes y después de la implementación de un protocolo de prevención. Este protocolo se estableció con el objetivo de identificar los pacientes en riesgo para el desarrollo de UPP e instituir intervenciones preventivas que quedaban claramente recogidas en el protocolo. Consiguieron una reducción de la incidencia importante: del 41,02% antes de la implementación, al 23,1%.
En el presente estudio, de los 27 pacientes que presentaron UPP, 23 (85,1%) desarrollaron una UPP, 3 (11,1%) desarrollaron 2 UPP y uno (3,7%) desarrolló 3 UPP. En todos los estudios revisados, la mayoría de pacientes desarrollaron solo una UPP. En el estudio de Campanili et al.18, el 100% de los pacientes solo desarrolló una UPP. Datos similares a los de nuestro estudio se publicaron en el artículo de Tayyib et al.19, con el 81,8% de pacientes que presentaron una UPP, el 12,1% que presentaron 2UPP y el 6,1% que presentaron 3UPP. La primera localización en frecuencia fue la zona sacra, con un 59,4%. En el estudio de Oliveira et al.4 la aparición de UPP en la zona sacra fue del 65,8%, en el estudio de Catalá et al.20 fue del 61% y en el de Matos et al.21, del 60%. Destacar el estudio de Roca-Biosca et al.22, en el que las UPP en la cara (oreja, nariz y boca) provocadas por dispositivos y las UPP en sacro (isquion, nalgas y sacro) presentaron la misma frecuencia, el 31,6%.
Actualmente trabajamos en las UCI con instrumentos para la valoración del riesgo de aparición de UPP, que no se han desarrollado específicamente para estos entornos y por tanto pueden no ser adecuados, ya que no tienen en cuenta factores de riesgo que son prácticamente exclusivos de estas áreas23. Con relación a la valoración del riesgo de aparición de UPP mediante la escala de Braden en nuestro entorno, el 99,7% de los pacientes fue clasificado con riesgo para desarrollar UPP en las primeras 24h de su admisión en la unidad. De ellos, el 29,9% presentaron riesgo leve, riesgo moderado el 23,9%, riesgo alto el 31% y riesgo muy alto el 14,9%. Un total de 307 pacientes (91,6%) fue considerado como en riesgo pero no desarrollaron UPP. Todos los pacientes que desarrollaron UPP fueron clasificados como pacientes de riesgo. En la investigación de Slowikowski y Funk24 casi el 60% de los pacientes fueron clasificados con alto riesgo o muy alto riesgo de desarrollo de UPP, el 29,8% con riesgo moderado, el 10% con bajo riesgo y solo 2 pacientes (0,5%) fueron clasificados como sin riesgo. Por tanto, el 99,5% de los pacientes fueron clasificados como en riesgo de desarrollar UPP. En el estudio de Cremasco et al.25 el 98,7% de los pacientes fueron clasificados desde su ingreso con riesgo para desarrollar UPP, y en el de Brunet y Kurcgant17, del total de la muestra, el 99,1% de los pacientes fueron clasificados con riesgo para el desarrollo de UPP.
A la luz de estos estudios podemos concluir que entre el 75 y el 90% de los pacientes fueron clasificados como en riesgo para el desarrollo de UPP pero permaneció libre de ellas. Cuando utilizamos la escala de Braden se sobre-predice el riesgo de aparición de UPP, y por ello es difícil sacar cualquier conclusión sobre la capacidad de esta escala como predictora. Si utilizando esta escala prácticamente un 100% de los pacientes, en el entorno de UCI, se clasifican en riesgo, es posible que se implementen medidas preventivas potencialmente innecesarias que redunden en excesivos costes para los sistemas de salud y en usos ineficientes del tiempo de los profesionales. Pero por otro lado también podríamos pensar que, debido a que las medidas preventivas se implementan en los pacientes en riesgo porque los profesionales son conocedores de su importancia, no todos los pacientes en riesgo llegaron a desarrollar las UPP.
En nuestro estudio, los ítems o subescalas Braden que mostraron una mayor correlación con el riesgo total Braden —dicho de otra forma, a qué ítems o subescalas se debe mayoritariamente el riesgo observado en nuestra muestra— fueron la percepción sensorial, la movilidad y la fricción/deslizamiento. No apareció diferencia significativa en relación con la subescala actividad entre los pacientes que desarrollaron UPP y los que quedaron libres de ellas. Este resultado es consistente con los obtenidos en estudios previos en el entorno de cuidados intensivos. La mayoría de los pacientes en este entorno se encuentran confinados a la cama y presentan pocas variaciones en sus niveles de actividad. En el estudio de Cox26, de las 6 subescalas, solo la movilidad y la fricción/cizalla se comportaron como predictores significativos de UPP. Aunque la evidencia nos confirma que la puntuación obtenida en la escala Braden actúa como predictora de UPP en el entorno del paciente crítico, las investigaciones realizadas sobre la contribución de las puntuaciones de las subescalas han sido limitadas y los resultados obtenidos poco concluyentes.
En nuestro estudio, la escala de Braden del primer día de ingreso presentó una muy alta sensibilidad para un punto de corte de 18 (100%), aunque la especificidad fue muy baja (0,3%), al igual que el valor predictivo positivo (8,1%). Para un punto de corte de 16, la sensibilidad fue del 100%, la especificidad del 7,8% y el valor predictivo positivo del 8,7%. Similares resultados se obtuvieron en la valoración del segundo día de ingreso y en la del día con puntuación mínima. Estos valores, para ambos puntos de corte, sugieren una proporción elevada de falsos positivos. Un punto de corte de 12 mostró el mejor balance entre sensibilidad y especificidad, valor predictivo positivo y valor predictivo negativo en las valoraciones del primer y segundo días de ingreso. En el estudio realizado por Hyun et al.27 en el entorno de 3UCI —dos médicas y una quirúrgica—, el punto de corte óptimo se situó en 13, resultado similar al obtenido en nuestra investigación. Serpa et al.28 también identificaron un punto de corte óptimo de 12 en la valoración del primer día de ingreso y de 13 en valoraciones subsiguientes.
El análisis del AUC mostró una moderada capacidad discriminatoria (66,8%) en la valoración del primer día de ingreso y en la del día con puntuación mínima (72,8%), y una buena capacidad discriminatoria (79,5%) para la valoración del segundo día de ingreso. En el caso del estudio mencionado con anterioridad (Hyun et al.27), el AUC fue de 67,2% para un punto de corte de 13, y en la investigación de Serpa et al.28 el AUC se estableció en un 77,8% en la valoración del primer día y en un 77,9% en la del tercer día.
ConclusionesLa incidencia de pacientes que desarrollaron UPP ha sido del 8,1%. Expresada como tasa de incidencia, el resultado ha sido de 11,72 por 1.000días de estancia. El 40,6% han sido de estadioi y el 59,4% de estadioii, destacando el sacro como localización más frecuente. Con relación a la fiabilidad, en la valoración del segundo día de ingreso el valor del coeficiente alfa de Cronbach fue de 0,722, indicando una buena fiabilidad, aunque solo se presentó como moderada en el resto de valoraciones. En el presente estudio, un punto de corte de 12 con una AUC del 79,5% en la valoración del segundo día de ingreso mostró el mejor valor predictivo en nuestro entorno de atención al paciente crítico. Al excluir las UPP de estadioi, un punto de corte de 11 con una AUC del 81,9% en la valoración del segundo día de ingreso mostró el mejor valor predictivo. Podemos concluir que la escala de Braden en nuestra investigación muestra una insuficiente validez predictiva y pobre precisión, discriminando a los pacientes en riesgo de desarrollo de UPP tanto para un punto de corte de 18 como para un punto de corte de 16, que son los aceptados en los distintos escenarios clínicos.
AutoríaMarta Lima Serrano ha realizado el análisis estadístico y la interpretación de los datos, ha revisado el manuscrito críticamente y aprobado la versión final del manuscrito para su publicación.
M. Isabel González Méndez ha diseñado el estudio, ha supervisado la correcta realización del estudio, ha redactado el manuscrito y ha aprobado la versión final del manuscrito para su publicación.
Inmaculada Alonso Araujo ha participado en la adquisición de datos, ha revisado el manuscrito críticamente y ha aprobado la versión final del manuscrito para su publicación.
Catalina Martín Castaño ha participado en la adquisición de datos, ha revisado el manuscrito críticamente y ha aprobado la versión final del manuscrito para su publicación.
Joaquín Salvador Lima Rodríguez ha participado en el diseño de la investigación y en la interpretación de datos, ha revisado el manuscrito críticamente y ha aprobado la versión final del manuscrito para su publicación.
FinanciaciónTodos los autores declaran no haber recibido financiación económica alguna para la realización de la investigación ni para la preparación del artículo.
Conflicto de interesesNinguno. Todos los autores declaran no tener relación ni financiera ni personal con otras personas u organizaciones que pudieran influir en su trabajo de manera inadecuada.